人教版化学九上同步精讲课件 课题4.4.2化合价(14张ppt)
文档属性
| 名称 | 人教版化学九上同步精讲课件 课题4.4.2化合价(14张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 174.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-07 00:00:00 | ||
图片预览




文档简介
化合价
一、激趣导入
实验测知,化合物均有固定的组成,即形成化合物的元素有固定的原子个数比。
物质
HCl
H2O
NaCl
Fe2O3
原子个数比
1∶1
2∶1
1∶1
2∶3
【结论】物质不同,原子个数比可能不同。
二、考点剖析
(一)知识讲解
1、化合价
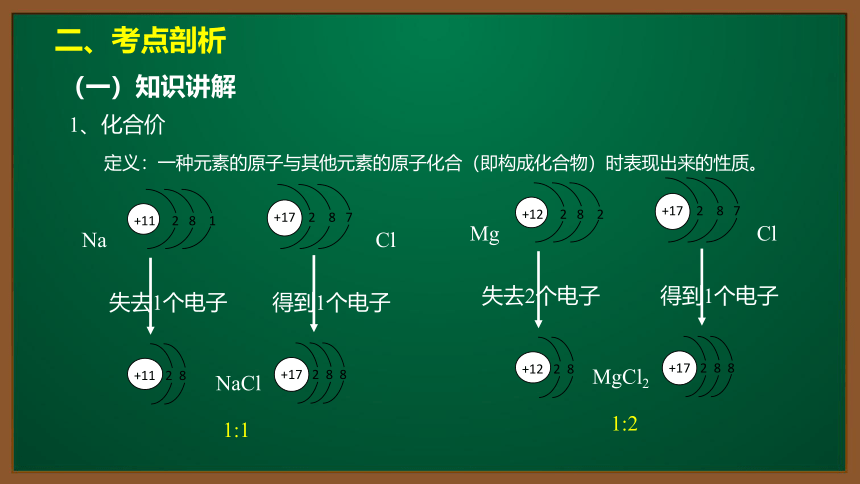
定义:一种元素的原子与其他元素的原子化合(即构成化合物)时表现出来的性质。
+11 2 8 1
+17 2 8 7
+11 2 8
+17 2 8 8
Na
Cl
失去1个电子
得到1个电子
NaCl
1:1
+12 2 8 2
+17 2 8 7
+12 2 8
+17 2 8 8
Mg
Cl
失去2个电子
得到1个电子
MgCl2
1:2
二、考点剖析
(一)知识讲解
1、化合价
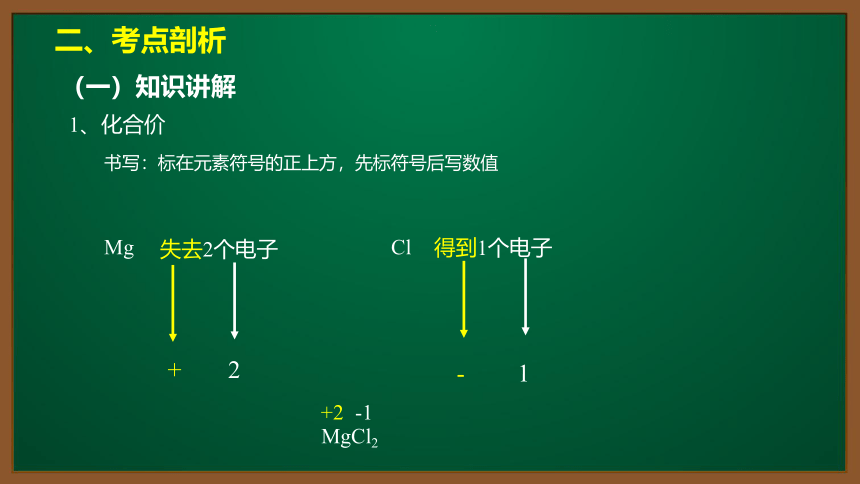
书写:标在元素符号的正上方,先标符号后写数值
Mg
Cl
失去2个电子
得到1个电子
+
2
-
1
MgCl2
+2
-1
二、考点剖析
(一)知识讲解
1、化合价
规则:在化合物中各元素正负化合价的代数和为零。
MgCl2
+2
-1
(+2)╳1+(-1) ╳ 2=0
单质中,元素的化合价为零。
二、考点剖析
(一)知识讲解
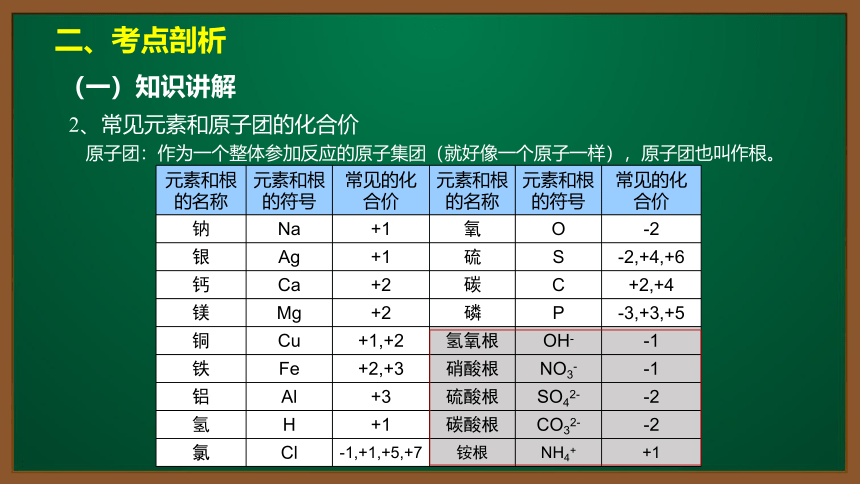
2、常见元素和原子团的化合价
元素和根的名称
元素和根的符号
常见的化合价
元素和根的名称
元素和根的符号
常见的化合价
钠
Na
+1
氧
O
-2
银
Ag
+1
硫
S
-2,+4,+6
钙
Ca
+2
碳
C
+2,+4
镁
Mg
+2
磷
P
-3,+3,+5
铜
Cu
+1,+2
氢氧根
OH-
-1
铁
Fe
+2,+3
硝酸根
NO3-
-1
铝
Al
+3
硫酸根
SO42-
-2
氢
H
+1
碳酸根
CO32-
-2
氯
Cl
-1,+1,+5,+7
铵根
NH4+
+1
原子团:作为一个整体参加反应的原子集团(就好像一个原子一样),原子团也叫作根。
二、考点剖析
(一)知识讲解
2、常见元素和原子团的化合价
部分元素的化合价口诀:
一价钾钠氯氢银,二价氧钙钡镁锌,
二三铁、二四碳,二四六硫铝正三,
铜汞二价最常见,单质零价永不变!
二、考点剖析
(一)知识讲解
3、化合价与离子符号的区别与联系:
①区别:
化合价用+2、+1、-2、-1……表示,标在元素符号正上方(“1”不省略);
离子符号用2+、+、2-、-……表示,标在元素符号的右上角(“1”省略)。
②联系:同种元素的化合价和其离子所带的电荷,通常数值相等、正负相同。
Mg
+2
Mg
2+
化合价
离子符号
二、考点剖析
(一)知识讲解
4、根据化合价书写化学式
【例】已知某种磷的氧化物中磷为+5价,氧为-2价,写出这种磷的氧化物的化学式。
步骤:
①写出组成化合物的两种元素的符号,正价的写在左边,负价的写在右边。
②写出两种元素正、负化合价
③交叉化合价,用最简整数比表示
P O
2
5
【口诀】一排序,二标价,三约简,四交叉,五检查。
+5 -2
二、考点剖析
(一)知识讲解
5、根据化学式计算某元素的化合价
【例】已知:O为-2价,求Fe2O3中铁元素的化合价。
计算依据:化合物中,正、负化合价代数和为0。
解:设Fe的化合价为x
2x+(-2)╳3=0
x=+3
答:Fe2O3中铁元素的化合价为+3。
硒元素具有抗衰老、抑制癌细胞生长的功能。在硒的一种化合物硒酸钠(Na2SeO4)中,硒元素的化合价是( )
A.-3 B.+6 C.+4 D.+7
B
二、考点剖析
(二) 典例分析
解:设硒元素的化合价是x,
根据在化合物中正负化合价代数和为零,可得:
(+1)×2+x+(-2)×4=0
x=+6价。
二、考点剖析
(三) 技巧点拨
1、牢记常见元素及原子团的化合价。
2、掌握利用化合价书写化合物化学式的方法。
3、掌握利用化学式计算某元素化合价的方法。
三、归纳小结
化合价
定义
规则
根据化合价书写化学式
根据化学式计算某元素的化合价
书写
常见元素和原子团的化合价
谢谢观看
一、激趣导入
实验测知,化合物均有固定的组成,即形成化合物的元素有固定的原子个数比。
物质
HCl
H2O
NaCl
Fe2O3
原子个数比
1∶1
2∶1
1∶1
2∶3
【结论】物质不同,原子个数比可能不同。
二、考点剖析
(一)知识讲解
1、化合价
定义:一种元素的原子与其他元素的原子化合(即构成化合物)时表现出来的性质。
+11 2 8 1
+17 2 8 7
+11 2 8
+17 2 8 8
Na
Cl
失去1个电子
得到1个电子
NaCl
1:1
+12 2 8 2
+17 2 8 7
+12 2 8
+17 2 8 8
Mg
Cl
失去2个电子
得到1个电子
MgCl2
1:2
二、考点剖析
(一)知识讲解
1、化合价
书写:标在元素符号的正上方,先标符号后写数值
Mg
Cl
失去2个电子
得到1个电子
+
2
-
1
MgCl2
+2
-1
二、考点剖析
(一)知识讲解
1、化合价
规则:在化合物中各元素正负化合价的代数和为零。
MgCl2
+2
-1
(+2)╳1+(-1) ╳ 2=0
单质中,元素的化合价为零。
二、考点剖析
(一)知识讲解
2、常见元素和原子团的化合价
元素和根的名称
元素和根的符号
常见的化合价
元素和根的名称
元素和根的符号
常见的化合价
钠
Na
+1
氧
O
-2
银
Ag
+1
硫
S
-2,+4,+6
钙
Ca
+2
碳
C
+2,+4
镁
Mg
+2
磷
P
-3,+3,+5
铜
Cu
+1,+2
氢氧根
OH-
-1
铁
Fe
+2,+3
硝酸根
NO3-
-1
铝
Al
+3
硫酸根
SO42-
-2
氢
H
+1
碳酸根
CO32-
-2
氯
Cl
-1,+1,+5,+7
铵根
NH4+
+1
原子团:作为一个整体参加反应的原子集团(就好像一个原子一样),原子团也叫作根。
二、考点剖析
(一)知识讲解
2、常见元素和原子团的化合价
部分元素的化合价口诀:
一价钾钠氯氢银,二价氧钙钡镁锌,
二三铁、二四碳,二四六硫铝正三,
铜汞二价最常见,单质零价永不变!
二、考点剖析
(一)知识讲解
3、化合价与离子符号的区别与联系:
①区别:
化合价用+2、+1、-2、-1……表示,标在元素符号正上方(“1”不省略);
离子符号用2+、+、2-、-……表示,标在元素符号的右上角(“1”省略)。
②联系:同种元素的化合价和其离子所带的电荷,通常数值相等、正负相同。
Mg
+2
Mg
2+
化合价
离子符号
二、考点剖析
(一)知识讲解
4、根据化合价书写化学式
【例】已知某种磷的氧化物中磷为+5价,氧为-2价,写出这种磷的氧化物的化学式。
步骤:
①写出组成化合物的两种元素的符号,正价的写在左边,负价的写在右边。
②写出两种元素正、负化合价
③交叉化合价,用最简整数比表示
P O
2
5
【口诀】一排序,二标价,三约简,四交叉,五检查。
+5 -2
二、考点剖析
(一)知识讲解
5、根据化学式计算某元素的化合价
【例】已知:O为-2价,求Fe2O3中铁元素的化合价。
计算依据:化合物中,正、负化合价代数和为0。
解:设Fe的化合价为x
2x+(-2)╳3=0
x=+3
答:Fe2O3中铁元素的化合价为+3。
硒元素具有抗衰老、抑制癌细胞生长的功能。在硒的一种化合物硒酸钠(Na2SeO4)中,硒元素的化合价是( )
A.-3 B.+6 C.+4 D.+7
B
二、考点剖析
(二) 典例分析
解:设硒元素的化合价是x,
根据在化合物中正负化合价代数和为零,可得:
(+1)×2+x+(-2)×4=0
x=+6价。
二、考点剖析
(三) 技巧点拨
1、牢记常见元素及原子团的化合价。
2、掌握利用化合价书写化合物化学式的方法。
3、掌握利用化学式计算某元素化合价的方法。
三、归纳小结
化合价
定义
规则
根据化合价书写化学式
根据化学式计算某元素的化合价
书写
常见元素和原子团的化合价
谢谢观看
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
