1.4 常见的碱(除杂)(第8课时)课件(共17PPT)
文档属性
| 名称 | 1.4 常见的碱(除杂)(第8课时)课件(共17PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 686.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-07-08 00:00:00 | ||
图片预览






文档简介
SO42-:
Cl-:
CO32-:
OH-:
H+:
NH4+ :
思考:下列常见离子与哪些离子不共存?
Ba2+
Ag+
H+(气体和水)、Ca2+、Ba2+、 Mg2+ 、 Al3+、 Mn2+、 Zn2+、Fe2+、 Fe3+、Cu2+、 Ag+
H+(水)、 NH4+ (气体)、 Mg2+ 、 Al3+、 Mn2+、 Zn2+、Fe2+、 Fe3+、 Cu2+、 Ag+
CO32- OH-
OH-(盐内容)
1、KCl中混有少量MnO2
加足量水溶解,过滤得到滤液,蒸发结晶得到氯化钾固体
2、MnO2中混有少量KCl
加足量水溶解,过滤得到固体,清水洗涤、烘干得到二氧化锰固体
适用于固液分离(即可溶物与不溶物)
3、KNO3中混有NaCl
加足量水溶解,配成某温度下的饱和溶液,降温结晶析出KNO3固体
适用于S随T变化影响不同的两种可溶物
4、蒸馏水中混有少量酒精
加热混合液体(温度控制在78℃—100 ℃之间),酒精汽化为气体,遇冷液化为液态酒精,剩下的为蒸馏水
适用于沸点不同的两种液体
以上用到的分离混合物的方法的共同点是什么?
利用物质的物理性质分离混合物——物理方法
1、下列各组物质,可用过滤法来分离的是( );
可用结晶法分离的是( )。
A、硝酸钠和氯化钠 B、锌粉和铜粉
C、果汁和果渣 D、酒精和水
C
A
NaCl(Na2CO3)
NaOH(Na2CO3)
NaCl(NaOH)
适量HCl
适量HCl
适量Ca(OH)2,过滤
除去下列物质中所含的少量杂质(括号内的为杂质)
气体
沉淀
水
新的杂质
2、你刚才用到的方法属于什么变化?
3、你在利用这些方法时,所选试剂只与 反应,生成 、 或 ,而不混入 。
利用物质的化学性质分离混合物——化学方法
杂质
一、物质的除杂原则:
不增(不引入新杂质)
不减(不与原物质反应)
易分(生成不同状态的物质,如沉淀、气体、水)
揪其根本(可从离子、原子角度去判断杂质)
沾亲带故(试剂中部分离子与原物质相同)
心法口诀
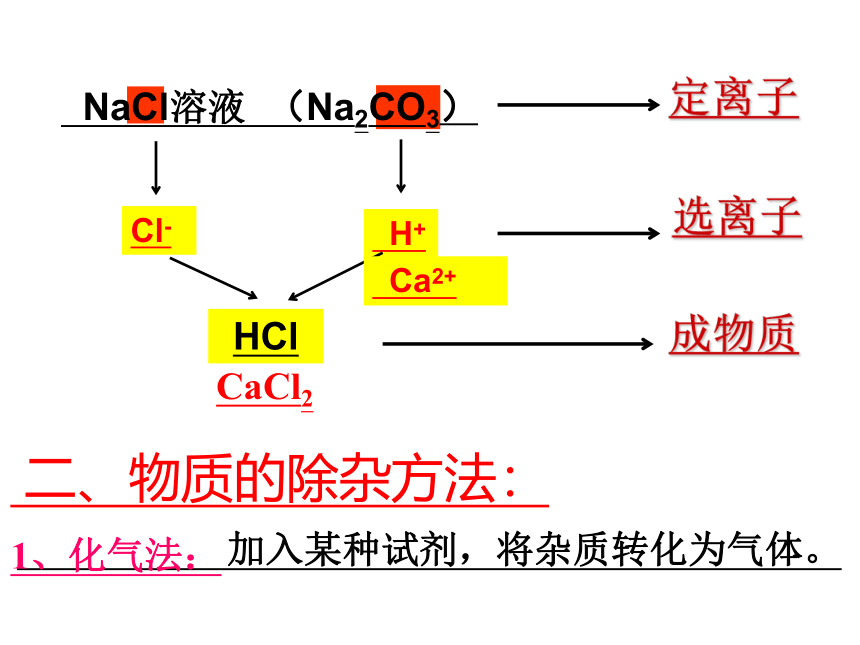
NaCl溶液 (Na2CO3)
H+
Cl-
HCl
定离子
选离子
成物质
Ca2+
CaCl2
加入某种试剂,将杂质转化为气体。
1、化气法:
二、物质的除杂方法:
适量的BaCl2溶液
NaCl(Na2SO4)
NaCl溶液(NaOH)
适量的CuCl2、FeCl3、MgCl2溶液
Na2SO4溶液(CuSO4)
适量的NaOH溶液
NaCl溶液(Fe2(SO4)3)
适量的Ba(OH)2溶液
NaCl溶液(CaCl2)
适量的Na2CO3 溶液
2、沉淀法:加入某种试剂,将杂质转化为沉淀,
然后过滤出去。
Cu(CuO)
练习4:除去铜粉中的混有的少量铁粉
Cu(Fe)
适量的或过量的HCl溶液或H2SO4溶液
练习5:除去氧化铜中混有的少量铜 CuO(Cu)
CaO(CaCO3)
高温
3、溶解法:用酸将杂质转化为液体除去。
4、加热法:通过加热将杂质转化为原物质或除去。
练习6: CO(CO2)
NaOH溶液
浓H2SO4 、 NaOH固体、生石灰、碱石灰等
O2(H2O)
5、吸收法:常用于除去气体中的杂质。
6、置换法:用活泼金属置换出盐中不活泼金属。
NaNO3(Na2SO4)__________; Na2SO4(CuSO4)_______;
NaCl(Na2CO3)__________; NaOH[Ca(OH)2]_________;
CaCl2(HCl)________; NaNO3(AgNO3)__________;
Ba(NO3)2
NaOH
HCl或CaCl2
Na2CO3
CaCO3
NaCl
NaCl(CuSO4)_________; H2(HCl)________;
Cu(Fe)___________; CO(CO2)________;
CO2(H2O)___________;
Ba(OH)2
NaOH
HCl
NaOH
浓H2SO4
小试牛刀
三、试剂用量和操作方法
除去下列物质中所含的少量杂质(括号内的为杂质),所用试剂及主要实验操作不正确的一组是( )
项目
物质
所用试剂及主要实验操作
A
CO(CO2)
通过装有足量NaOH溶液的洗气瓶后,干燥
B
Cu粉(Fe粉)
加入足量的稀盐酸,充分反应后,过滤、洗涤、干燥
C
NaCl溶液(CaCl2)
加入适量Na2CO3溶液,充分反应后,过滤
D
CaCl2固体(CaCO3)
充分加热
D
除杂试剂取用量:
一般除杂试剂取用的量为___________,
适量
判断:下列除杂所加试剂的用量是否正确
1、NaCl溶液(CaCl2)加入过量的Na2CO3溶液
2、NaCl固体 (Na2CO3)加入过量的稀盐酸蒸发结晶
3、CaCl2溶液(HCl) 加入过量的CaCO3
×
√
√
如果取用过量的试剂,后续操作中能以简单方法将过量的试剂除去,要不影响除杂目的。
练习7:下列除杂设计,所选试剂和操作方法均正确的是( )
选项
物质
所选试剂
操作方法
A
HCl气体(H2O)
固体氢氧化钠
通过装有过量试剂的干燥管,收集
B
CaCl2溶液(HCl)
碳酸钙粉末
加过量试剂,充分反应,
过滤
C
KNO3溶液(CuSO4)
Ba(OH)2溶液
加过量试剂,充分反应,
过滤
D
CaCO3固体(CaCl2)
足量水
溶解、过滤、蒸发结晶
B
练习8:化工生产中需要对原料提纯,以利于提高产品质量。经测定某氯化钠样品中混有硫酸钠,为了除杂质并制得纯净的氯化钠固体,在实验室研究中某学生设计方案如下:
回答下列问题。
(1) 操作②能否用硝酸钡溶液?说明理由:
(2)进行步骤②后,如何判断硫酸钠已除尽,方法是
(3)此设计方案不严密,请补充缺少的实验步骤
不能,虽然能够除去硫酸钠,但带入新的杂质硝酸钠
取步骤②后的上层清液于试管中,滴加氯化钡溶液,无明显现象,说明硫酸钠已经除尽
过滤后加入足量稀盐酸
练习9:由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须加入过量的NaOH、BaCl2、Na2CO3将粗盐进行精制。流程如下图。
(1)下列设计的三种溶液的加入顺序中,不能达目的是( )。
A.NaOH、Na2CO3、BaCl2 B.NaOH、BaCl2、Na2CO3
C. BaCl2、NaOH、Na2CO3
(2)加入过量Na2CO3溶液除了能除去粗盐中的CaCl2,还有一个作用是_______________。
(3)通过操作Ⅲ所得滤液中溶质___________________________。
除去多余的BaCl2
NaCl NaOH Na2CO3
A
练习10、除去下列各组物质中杂质,所用试剂和方法不正确的是( )
物质 杂质 除杂质所用试剂和方法
A、 Na2CO3 NaOH 通入适量二氧化碳
B、 CO 气体 CO2 通过灼热氧化铜
C、 HNO3溶液 HCl 过量的AgNO3溶液,过滤
D、 CuCl2溶液 Cu(OH)2 加入适量稀盐酸
BC
Cl-:
CO32-:
OH-:
H+:
NH4+ :
思考:下列常见离子与哪些离子不共存?
Ba2+
Ag+
H+(气体和水)、Ca2+、Ba2+、 Mg2+ 、 Al3+、 Mn2+、 Zn2+、Fe2+、 Fe3+、Cu2+、 Ag+
H+(水)、 NH4+ (气体)、 Mg2+ 、 Al3+、 Mn2+、 Zn2+、Fe2+、 Fe3+、 Cu2+、 Ag+
CO32- OH-
OH-(盐内容)
1、KCl中混有少量MnO2
加足量水溶解,过滤得到滤液,蒸发结晶得到氯化钾固体
2、MnO2中混有少量KCl
加足量水溶解,过滤得到固体,清水洗涤、烘干得到二氧化锰固体
适用于固液分离(即可溶物与不溶物)
3、KNO3中混有NaCl
加足量水溶解,配成某温度下的饱和溶液,降温结晶析出KNO3固体
适用于S随T变化影响不同的两种可溶物
4、蒸馏水中混有少量酒精
加热混合液体(温度控制在78℃—100 ℃之间),酒精汽化为气体,遇冷液化为液态酒精,剩下的为蒸馏水
适用于沸点不同的两种液体
以上用到的分离混合物的方法的共同点是什么?
利用物质的物理性质分离混合物——物理方法
1、下列各组物质,可用过滤法来分离的是( );
可用结晶法分离的是( )。
A、硝酸钠和氯化钠 B、锌粉和铜粉
C、果汁和果渣 D、酒精和水
C
A
NaCl(Na2CO3)
NaOH(Na2CO3)
NaCl(NaOH)
适量HCl
适量HCl
适量Ca(OH)2,过滤
除去下列物质中所含的少量杂质(括号内的为杂质)
气体
沉淀
水
新的杂质
2、你刚才用到的方法属于什么变化?
3、你在利用这些方法时,所选试剂只与 反应,生成 、 或 ,而不混入 。
利用物质的化学性质分离混合物——化学方法
杂质
一、物质的除杂原则:
不增(不引入新杂质)
不减(不与原物质反应)
易分(生成不同状态的物质,如沉淀、气体、水)
揪其根本(可从离子、原子角度去判断杂质)
沾亲带故(试剂中部分离子与原物质相同)
心法口诀
NaCl溶液 (Na2CO3)
H+
Cl-
HCl
定离子
选离子
成物质
Ca2+
CaCl2
加入某种试剂,将杂质转化为气体。
1、化气法:
二、物质的除杂方法:
适量的BaCl2溶液
NaCl(Na2SO4)
NaCl溶液(NaOH)
适量的CuCl2、FeCl3、MgCl2溶液
Na2SO4溶液(CuSO4)
适量的NaOH溶液
NaCl溶液(Fe2(SO4)3)
适量的Ba(OH)2溶液
NaCl溶液(CaCl2)
适量的Na2CO3 溶液
2、沉淀法:加入某种试剂,将杂质转化为沉淀,
然后过滤出去。
Cu(CuO)
练习4:除去铜粉中的混有的少量铁粉
Cu(Fe)
适量的或过量的HCl溶液或H2SO4溶液
练习5:除去氧化铜中混有的少量铜 CuO(Cu)
CaO(CaCO3)
高温
3、溶解法:用酸将杂质转化为液体除去。
4、加热法:通过加热将杂质转化为原物质或除去。
练习6: CO(CO2)
NaOH溶液
浓H2SO4 、 NaOH固体、生石灰、碱石灰等
O2(H2O)
5、吸收法:常用于除去气体中的杂质。
6、置换法:用活泼金属置换出盐中不活泼金属。
NaNO3(Na2SO4)__________; Na2SO4(CuSO4)_______;
NaCl(Na2CO3)__________; NaOH[Ca(OH)2]_________;
CaCl2(HCl)________; NaNO3(AgNO3)__________;
Ba(NO3)2
NaOH
HCl或CaCl2
Na2CO3
CaCO3
NaCl
NaCl(CuSO4)_________; H2(HCl)________;
Cu(Fe)___________; CO(CO2)________;
CO2(H2O)___________;
Ba(OH)2
NaOH
HCl
NaOH
浓H2SO4
小试牛刀
三、试剂用量和操作方法
除去下列物质中所含的少量杂质(括号内的为杂质),所用试剂及主要实验操作不正确的一组是( )
项目
物质
所用试剂及主要实验操作
A
CO(CO2)
通过装有足量NaOH溶液的洗气瓶后,干燥
B
Cu粉(Fe粉)
加入足量的稀盐酸,充分反应后,过滤、洗涤、干燥
C
NaCl溶液(CaCl2)
加入适量Na2CO3溶液,充分反应后,过滤
D
CaCl2固体(CaCO3)
充分加热
D
除杂试剂取用量:
一般除杂试剂取用的量为___________,
适量
判断:下列除杂所加试剂的用量是否正确
1、NaCl溶液(CaCl2)加入过量的Na2CO3溶液
2、NaCl固体 (Na2CO3)加入过量的稀盐酸蒸发结晶
3、CaCl2溶液(HCl) 加入过量的CaCO3
×
√
√
如果取用过量的试剂,后续操作中能以简单方法将过量的试剂除去,要不影响除杂目的。
练习7:下列除杂设计,所选试剂和操作方法均正确的是( )
选项
物质
所选试剂
操作方法
A
HCl气体(H2O)
固体氢氧化钠
通过装有过量试剂的干燥管,收集
B
CaCl2溶液(HCl)
碳酸钙粉末
加过量试剂,充分反应,
过滤
C
KNO3溶液(CuSO4)
Ba(OH)2溶液
加过量试剂,充分反应,
过滤
D
CaCO3固体(CaCl2)
足量水
溶解、过滤、蒸发结晶
B
练习8:化工生产中需要对原料提纯,以利于提高产品质量。经测定某氯化钠样品中混有硫酸钠,为了除杂质并制得纯净的氯化钠固体,在实验室研究中某学生设计方案如下:
回答下列问题。
(1) 操作②能否用硝酸钡溶液?说明理由:
(2)进行步骤②后,如何判断硫酸钠已除尽,方法是
(3)此设计方案不严密,请补充缺少的实验步骤
不能,虽然能够除去硫酸钠,但带入新的杂质硝酸钠
取步骤②后的上层清液于试管中,滴加氯化钡溶液,无明显现象,说明硫酸钠已经除尽
过滤后加入足量稀盐酸
练习9:由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须加入过量的NaOH、BaCl2、Na2CO3将粗盐进行精制。流程如下图。
(1)下列设计的三种溶液的加入顺序中,不能达目的是( )。
A.NaOH、Na2CO3、BaCl2 B.NaOH、BaCl2、Na2CO3
C. BaCl2、NaOH、Na2CO3
(2)加入过量Na2CO3溶液除了能除去粗盐中的CaCl2,还有一个作用是_______________。
(3)通过操作Ⅲ所得滤液中溶质___________________________。
除去多余的BaCl2
NaCl NaOH Na2CO3
A
练习10、除去下列各组物质中杂质,所用试剂和方法不正确的是( )
物质 杂质 除杂质所用试剂和方法
A、 Na2CO3 NaOH 通入适量二氧化碳
B、 CO 气体 CO2 通过灼热氧化铜
C、 HNO3溶液 HCl 过量的AgNO3溶液,过滤
D、 CuCl2溶液 Cu(OH)2 加入适量稀盐酸
BC
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
