1.6 几种重要的盐 第5课时 课件(共13张PPT)
文档属性
| 名称 | 1.6 几种重要的盐 第5课时 课件(共13张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 150.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-07-08 00:00:00 | ||
图片预览



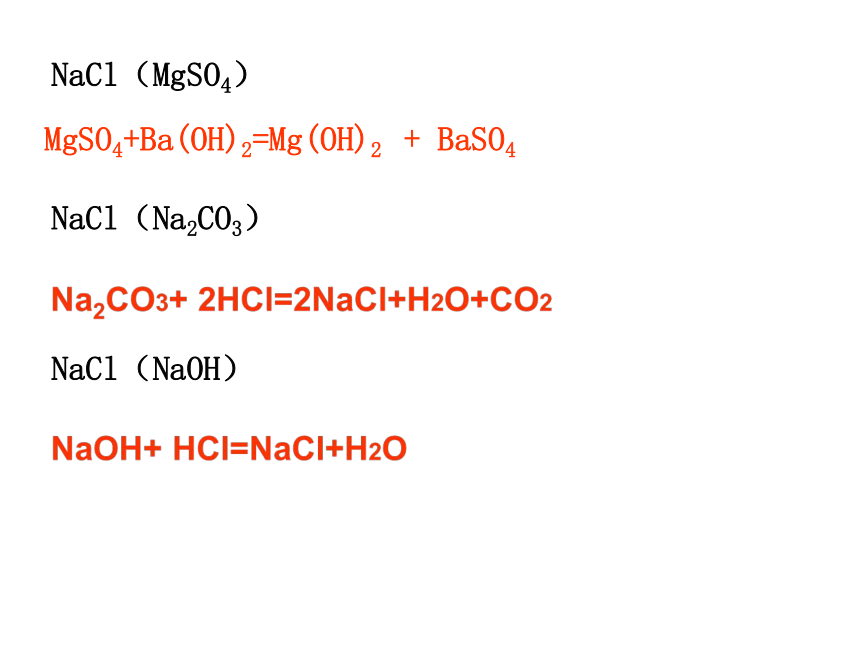


文档简介
1.6几种重要的盐
第五课时
根据所学酸和碱的化学性质,你能写出获得氯化钠的途径有多少?
动手写一写
经海水蒸发结晶而来的粗盐主要成分为NaCl,常含有一些杂质,请选择适量的试剂将食盐中的以下杂质除去,写出反应的方程式
NaCl(Na2SO4)
Na2SO4+BaCl2=2NaCl+BaSO4
NaCl(CaCl2)
CaCl2+Na2CO3=2NaCl+CaCO3
NaCl(MgCl2)
MgCl2+2NaOH=2NaCl+Mg(OH)2
NaCl(MgSO4)
MgSO4+Ba(OH)2=Mg(OH)2 + BaSO4
NaCl(Na2CO3)
NaCl(NaOH)
设计流程
经海水蒸发结晶而来的粗盐主要成分为NaCl,常含有泥沙、MgCl2、CaCl2等杂质,如何提纯粗盐?
→
?
NaCl(泥沙、MgCl2、CaCl2)
过滤
NaOH
Na2CO3
2、为了保证完全除去杂质,所加试剂用量?
1、选择合适的试剂和除杂方法
NaOH、Na2CO3、过滤
过量
3、如何除去过量的NaOH、 Na2CO3
加入适量稀盐酸:除去过量的NaOH和Na2CO3
4、过滤操作什么时候进行?
加盐酸之前过滤
样品
加水溶解
粗盐溶液
过量
NaOH溶液
过滤
沉淀
滤液NaCl、 NaOH、 Na2CO3
NaCl(CaCl2、MgCl2、泥沙)
设计流程图
过量
Na2CO3溶液
NaCl、 NaOH、 Na2CO3、泥沙、Mg(OH)2、CaCO3
适量稀盐酸
NaCl溶液
蒸发结晶
精盐
如果粗盐中含有泥沙、MgCl2、Na2SO4、CaCl2等杂质,如何提纯粗盐?
Ba2+
BaCl2
过量
1、如何除去过量的BaCl2?
碳酸钠
2、NaOH溶液、Na2CO3溶液、BaCl2溶液添加顺序如何?
NaOH溶液、BaCl2溶液、Na2CO3溶液
BaCl2溶液、Na2CO3溶液、NaOH溶液
BaCl2溶液、NaOH溶液、Na2CO3溶液
总结粗盐提纯的注意点
1、为了确保完全除去杂质,药品应加过量
2、过滤应在加入适量稀盐酸之前
3、氯化钡溶液加入应在碳酸钠溶液之前
练1.为了除去粗盐中的CaCl2、MgSO4及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量的NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量的BaCl2溶液。正确的操作顺序是 ( )
A.①④②⑤③ B.④①②⑤③
C.②⑤④③① D.⑤②④①③
练2、某食盐样品中含有少量沙土、氯化钙和氯化镁。以下是除去食盐样品中沙土、氯化钙和氯化镁的实验流程:
根据流程图回答:
(1)操作Ⅰ的名称是???? ?,加入的试剂A是???? ??,沉淀是?????? ????;
(2)写出NaOH与杂质反应的化学方程式:????????????? ???????????????;
(3)加入试剂B的目的是????????????????????????????????????;
(4)蒸发结晶时用到玻璃棒的作用是?????????????????????????? ??????????。
练3、某氯化钠样品中含有硫酸钠、氯化镁、氯化钙等杂质,设计如下过程除去杂质:
步骤Ⅰ:加足量的水溶解.
步骤Ⅱ:依次加入过量的氯化钡溶液、过量的氢氧化钠溶液、过量的X溶液,充分反应后过滤.
步骤Ⅲ:加入足量的稀盐酸.
根据上述过程回答下列问题:
(1)步骤Ⅰ需要用到的玻璃仪器是______和______.
(2)步骤Ⅱ中加入氯化钡溶液时,发生反应的化学方程式是______;物质X是______溶液.
(3)步骤Ⅱ得到的固体中主要含有的物质是______.步骤Ⅱ中可以用过量的______溶液(填一种物质)代替氯化钡和氢氧化钠两种溶液,也可以达到相同实验目的.
(4)步骤Ⅲ加入足量稀盐酸的目的是______;步骤Ⅳ的实验操作名称是______.
第五课时
根据所学酸和碱的化学性质,你能写出获得氯化钠的途径有多少?
动手写一写
经海水蒸发结晶而来的粗盐主要成分为NaCl,常含有一些杂质,请选择适量的试剂将食盐中的以下杂质除去,写出反应的方程式
NaCl(Na2SO4)
Na2SO4+BaCl2=2NaCl+BaSO4
NaCl(CaCl2)
CaCl2+Na2CO3=2NaCl+CaCO3
NaCl(MgCl2)
MgCl2+2NaOH=2NaCl+Mg(OH)2
NaCl(MgSO4)
MgSO4+Ba(OH)2=Mg(OH)2 + BaSO4
NaCl(Na2CO3)
NaCl(NaOH)
设计流程
经海水蒸发结晶而来的粗盐主要成分为NaCl,常含有泥沙、MgCl2、CaCl2等杂质,如何提纯粗盐?
→
?
NaCl(泥沙、MgCl2、CaCl2)
过滤
NaOH
Na2CO3
2、为了保证完全除去杂质,所加试剂用量?
1、选择合适的试剂和除杂方法
NaOH、Na2CO3、过滤
过量
3、如何除去过量的NaOH、 Na2CO3
加入适量稀盐酸:除去过量的NaOH和Na2CO3
4、过滤操作什么时候进行?
加盐酸之前过滤
样品
加水溶解
粗盐溶液
过量
NaOH溶液
过滤
沉淀
滤液NaCl、 NaOH、 Na2CO3
NaCl(CaCl2、MgCl2、泥沙)
设计流程图
过量
Na2CO3溶液
NaCl、 NaOH、 Na2CO3、泥沙、Mg(OH)2、CaCO3
适量稀盐酸
NaCl溶液
蒸发结晶
精盐
如果粗盐中含有泥沙、MgCl2、Na2SO4、CaCl2等杂质,如何提纯粗盐?
Ba2+
BaCl2
过量
1、如何除去过量的BaCl2?
碳酸钠
2、NaOH溶液、Na2CO3溶液、BaCl2溶液添加顺序如何?
NaOH溶液、BaCl2溶液、Na2CO3溶液
BaCl2溶液、Na2CO3溶液、NaOH溶液
BaCl2溶液、NaOH溶液、Na2CO3溶液
总结粗盐提纯的注意点
1、为了确保完全除去杂质,药品应加过量
2、过滤应在加入适量稀盐酸之前
3、氯化钡溶液加入应在碳酸钠溶液之前
练1.为了除去粗盐中的CaCl2、MgSO4及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量的NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量的BaCl2溶液。正确的操作顺序是 ( )
A.①④②⑤③ B.④①②⑤③
C.②⑤④③① D.⑤②④①③
练2、某食盐样品中含有少量沙土、氯化钙和氯化镁。以下是除去食盐样品中沙土、氯化钙和氯化镁的实验流程:
根据流程图回答:
(1)操作Ⅰ的名称是???? ?,加入的试剂A是???? ??,沉淀是?????? ????;
(2)写出NaOH与杂质反应的化学方程式:????????????? ???????????????;
(3)加入试剂B的目的是????????????????????????????????????;
(4)蒸发结晶时用到玻璃棒的作用是?????????????????????????? ??????????。
练3、某氯化钠样品中含有硫酸钠、氯化镁、氯化钙等杂质,设计如下过程除去杂质:
步骤Ⅰ:加足量的水溶解.
步骤Ⅱ:依次加入过量的氯化钡溶液、过量的氢氧化钠溶液、过量的X溶液,充分反应后过滤.
步骤Ⅲ:加入足量的稀盐酸.
根据上述过程回答下列问题:
(1)步骤Ⅰ需要用到的玻璃仪器是______和______.
(2)步骤Ⅱ中加入氯化钡溶液时,发生反应的化学方程式是______;物质X是______溶液.
(3)步骤Ⅱ得到的固体中主要含有的物质是______.步骤Ⅱ中可以用过量的______溶液(填一种物质)代替氯化钡和氢氧化钠两种溶液,也可以达到相同实验目的.
(4)步骤Ⅲ加入足量稀盐酸的目的是______;步骤Ⅳ的实验操作名称是______.
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
