人教版化学九下同步精讲课件 11.1.1氯化钠、碳酸钠、碳酸氢钠和碳酸钙(14张ppt)
文档属性
| 名称 | 人教版化学九下同步精讲课件 11.1.1氯化钠、碳酸钠、碳酸氢钠和碳酸钙(14张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 223.8KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-08 00:00:00 | ||
图片预览






文档简介
常见的盐
生活的食盐有什么用途?生活中常见的盐还有哪些?
一、激趣导入
二、考点剖析
(一)知识讲解
1、常见的盐
NaCl 氯化钠 食盐
Na2CO3 碳酸钠 纯碱、苏打
NaHCO3 碳酸氢钠 小苏打
CaCO3 碳酸钙 大理石 、石灰石的主要成分
KMnO4 高锰酸钾
CuSO4 硫酸铜
由金属离子(或NH4+离子)和酸根离子构成的化合物叫做盐。
(纯碱不是碱,是盐)
二、考点剖析
(一)知识讲解
2、氯化钠
俗称食盐,化学式NaCl。
外观是白色晶体状,味咸。易溶于水。
主要用途
⑴生活:作调味品(调味剂)、腌渍蔬菜等
⑵医疗:配制生理盐水(0.9%),维持人的正常生理活动
⑶农业:选种。
⑷工业:制取碳酸钠、氢氧化钠、氯气和盐酸等。
(5)作融雪剂:公路上的积雪也可以用氯化钠来消除。
二、考点剖析
(一)知识讲解
2、氯化钠
氯化钠在自然界的分布很广,海水、盐湖、盐井、盐矿中都蕴藏着大量的食盐。
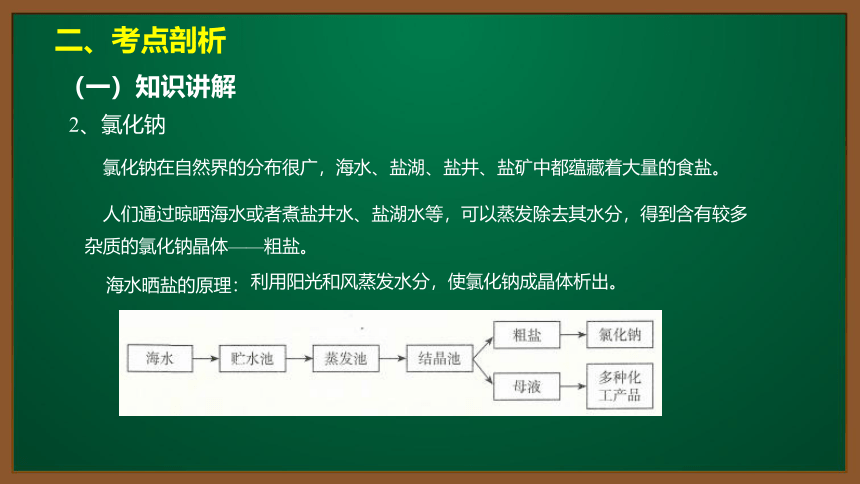
人们通过晾晒海水或者煮盐井水、盐湖水等,可以蒸发除去其水分,得到含有较多杂质的氯化钠晶体——粗盐。
利用阳光和风蒸发水分,使氯化钠成晶体析出。
海水晒盐的原理:
二、考点剖析
(一)知识讲解
3、碳酸钠、碳酸氢钠和碳酸钙
名称
碳酸钠
碳酸氢钠
碳酸钙
俗名
物理
性质
主要
用途
苏打、纯碱
小苏打
大理石、石灰石的主要成分
易溶于水的白色粉末
易溶于水的白色粉末
难溶于水的白色固体
用于生产玻璃、造纸、纺织、洗涤剂
发酵粉的主要成分、治疗胃酸过多的药剂
可作补钙剂。石灰石、大理石作建筑材料、也用于实验室制取二氧化碳
二、考点剖析
(一)知识讲解
4、碳酸钠的化学性质
1)碳酸钠的水溶液呈碱性;
2)碳酸钠可与酸反应;
向碳酸钠中加入盐酸,并将气体通入澄清的石灰水
现象
分析
产生大量气泡,澄清石灰水变浑浊
有二氧化碳生成
Na2CO3+2HCl=2NaCl+ CO2 ↑ +H2O
NaHCO3+HCl=NaCl+ CO2 ↑ +H2O
(碳酸氢钠的水溶液也呈碱性)
碳酸氢钠可与酸反应;
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
向碳酸钠溶液中加入澄清石灰水
现象
分析
出现白色沉淀
二者发生反应,生成一种难溶物
二、考点剖析
(一)知识讲解
4、碳酸钠的化学性质
3)碳酸钠与氢氧化钙反应;
Na2CO3+CaCl2=CaCO3↓+2NaCl
向碳酸钠溶液中加入氯化钙溶液
现象
分析
出现白色沉淀
二者发生反应,生成一种难溶物
二、考点剖析
(一)知识讲解
4、碳酸钠的化学性质
4)碳酸钠与某些盐溶液反应;
二、考点剖析
(一)知识讲解
5、碳酸盐的鉴别
碳酸钠、碳酸钙等物质都是含碳酸根的盐;均可与酸反应生成二氧化碳气体。
所用试剂为稀盐酸和澄清石灰水。
实验操作
实验现象
实验结论
向少量样品中加入稀盐酸,将产生的气体通入澄清石灰水。
有无色气体生成,澄清石灰水变浑浊。
该样品是碳酸盐。
碳酸钠俗称“纯碱”.有关它的表述不正确的是( )
A.“纯碱”其实不是碱,它属于盐类
B.可用纯碱代替洗涤灵洗涤餐具表面的油污
C.用纯碱可除去面团发酵产生的酸
D.“冬天捞碱”可说明纯碱的溶解度随温度的变化不大
D
二、考点剖析
(二) 典例分析
二、考点剖析
(三) 技巧点拨
1、理解和熟记常见的盐的俗称、主要性质及用途。
2、正确掌握碳酸盐的鉴别方法。
三、归纳小结
常见的盐
常见的盐
碳酸钠的化学性质
水溶液呈碱性
可与酸、氢氧化钙等物质反应
碳酸盐的鉴别
氯化钠
碳酸钠、碳酸氢钠和碳酸钙
谢谢观看
生活的食盐有什么用途?生活中常见的盐还有哪些?
一、激趣导入
二、考点剖析
(一)知识讲解
1、常见的盐
NaCl 氯化钠 食盐
Na2CO3 碳酸钠 纯碱、苏打
NaHCO3 碳酸氢钠 小苏打
CaCO3 碳酸钙 大理石 、石灰石的主要成分
KMnO4 高锰酸钾
CuSO4 硫酸铜
由金属离子(或NH4+离子)和酸根离子构成的化合物叫做盐。
(纯碱不是碱,是盐)
二、考点剖析
(一)知识讲解
2、氯化钠
俗称食盐,化学式NaCl。
外观是白色晶体状,味咸。易溶于水。
主要用途
⑴生活:作调味品(调味剂)、腌渍蔬菜等
⑵医疗:配制生理盐水(0.9%),维持人的正常生理活动
⑶农业:选种。
⑷工业:制取碳酸钠、氢氧化钠、氯气和盐酸等。
(5)作融雪剂:公路上的积雪也可以用氯化钠来消除。
二、考点剖析
(一)知识讲解
2、氯化钠
氯化钠在自然界的分布很广,海水、盐湖、盐井、盐矿中都蕴藏着大量的食盐。
人们通过晾晒海水或者煮盐井水、盐湖水等,可以蒸发除去其水分,得到含有较多杂质的氯化钠晶体——粗盐。
利用阳光和风蒸发水分,使氯化钠成晶体析出。
海水晒盐的原理:
二、考点剖析
(一)知识讲解
3、碳酸钠、碳酸氢钠和碳酸钙
名称
碳酸钠
碳酸氢钠
碳酸钙
俗名
物理
性质
主要
用途
苏打、纯碱
小苏打
大理石、石灰石的主要成分
易溶于水的白色粉末
易溶于水的白色粉末
难溶于水的白色固体
用于生产玻璃、造纸、纺织、洗涤剂
发酵粉的主要成分、治疗胃酸过多的药剂
可作补钙剂。石灰石、大理石作建筑材料、也用于实验室制取二氧化碳
二、考点剖析
(一)知识讲解
4、碳酸钠的化学性质
1)碳酸钠的水溶液呈碱性;
2)碳酸钠可与酸反应;
向碳酸钠中加入盐酸,并将气体通入澄清的石灰水
现象
分析
产生大量气泡,澄清石灰水变浑浊
有二氧化碳生成
Na2CO3+2HCl=2NaCl+ CO2 ↑ +H2O
NaHCO3+HCl=NaCl+ CO2 ↑ +H2O
(碳酸氢钠的水溶液也呈碱性)
碳酸氢钠可与酸反应;
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
向碳酸钠溶液中加入澄清石灰水
现象
分析
出现白色沉淀
二者发生反应,生成一种难溶物
二、考点剖析
(一)知识讲解
4、碳酸钠的化学性质
3)碳酸钠与氢氧化钙反应;
Na2CO3+CaCl2=CaCO3↓+2NaCl
向碳酸钠溶液中加入氯化钙溶液
现象
分析
出现白色沉淀
二者发生反应,生成一种难溶物
二、考点剖析
(一)知识讲解
4、碳酸钠的化学性质
4)碳酸钠与某些盐溶液反应;
二、考点剖析
(一)知识讲解
5、碳酸盐的鉴别
碳酸钠、碳酸钙等物质都是含碳酸根的盐;均可与酸反应生成二氧化碳气体。
所用试剂为稀盐酸和澄清石灰水。
实验操作
实验现象
实验结论
向少量样品中加入稀盐酸,将产生的气体通入澄清石灰水。
有无色气体生成,澄清石灰水变浑浊。
该样品是碳酸盐。
碳酸钠俗称“纯碱”.有关它的表述不正确的是( )
A.“纯碱”其实不是碱,它属于盐类
B.可用纯碱代替洗涤灵洗涤餐具表面的油污
C.用纯碱可除去面团发酵产生的酸
D.“冬天捞碱”可说明纯碱的溶解度随温度的变化不大
D
二、考点剖析
(二) 典例分析
二、考点剖析
(三) 技巧点拨
1、理解和熟记常见的盐的俗称、主要性质及用途。
2、正确掌握碳酸盐的鉴别方法。
三、归纳小结
常见的盐
常见的盐
碳酸钠的化学性质
水溶液呈碱性
可与酸、氢氧化钙等物质反应
碳酸盐的鉴别
氯化钠
碳酸钠、碳酸氢钠和碳酸钙
谢谢观看
同课章节目录
