2020-2021学年高一化学人教版必修二第二章第二节第3课时发展中的化学电源课件-化学电源(20张ppt)
文档属性
| 名称 | 2020-2021学年高一化学人教版必修二第二章第二节第3课时发展中的化学电源课件-化学电源(20张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-09 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
第3课时
发展中的化学电源
第二节
化学能与电能
情景导入
你能说说生活中你熟悉的化学电源吗?
情景导入
碱性锌锰干电池
铅蓄电池
锂离子电池
纽扣电池
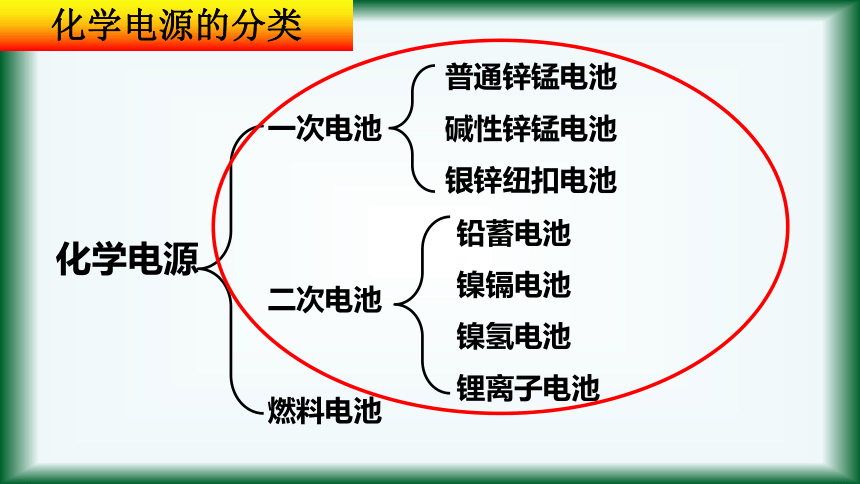
化学电源
一次电池
二次电池
燃料电池
普通锌锰电池
碱性锌锰电池
银锌纽扣电池
铅蓄电池
镍镉电池
镍氢电池
锂离子电池
化学电源的分类
【学习目标】
1、了解常见一次电池、二次电池的特点
2、掌握一次电池、二次电池电极反应式的书写方法
已知普通锌锰干电池的总反应为:
Zn
+2NH4Cl
=2NH3+ZnCl2
+H2,如何写出正负极反应?
负极:Zn
-
2e-
=
Zn2+
正极:2NH4+
+
2e-
=
2NH3
+
H2
负极:
Zn
正极:石墨
电解质:
MnO2
,
NH4Cl
淀粉糊
1、
MnO2
作用:吸收氢气
2、缺点:漏液、气鼓、失效
3、改进:外壳套上防腐金属筒或塑料桶
将NH4Cl
换成湿的KOH
典例示范1
重难突破一【一次电池】
已知碱性锌锰干电池的总反应为:
Zn
+
2MnO2
+
2H2O
=
2MnOOH
+
Zn(OH)2
如何写出正负极反应?
负极:Zn
+
2OH-
-
2e-
=
Zn(OH)2
正极:MnO2
+
H2O
+
e-
=
MnOOH
+
OH-
负极:
Zn
正极:MnO2
电解质:KOH溶液
典例示范2
已知银锌纽扣电池的总反应为:
Zn+
Ag2O
+
H2O
=
Zn(OH)2
+
2Ag,
如何写出正负极反应?
负极:Zn
+
2OH-
-
2e-
=
Zn(OH)2
正极:Ag2O
+
H2O
+
2e-
=
2Ag
+
2OH-
负极:
Zn
正极:
Ag2O
电解质:KOH溶液
问题思考1
总反应:Zn+
Ag2O
=
ZnO
+
2Ag
正极:Ag2O
+
H2O
+
2e-
=
2Ag
+
2OH-
负极:Zn
+
2OH-
-2e-
=
ZnO
+
H2O
补充:银锌纽扣电池的另一写法
二、二次电池
1、铅蓄电池
Pb为负极
,
PbO2为正极
电解液:
30%的H2SO4溶液
如何写出放电过程中的正负极反应?
Pb+PbO2+2H2SO4
2PbSO4
+
2H2O
放电
充电
负极:Pb
-
2e-
+
SO42-
=
PbSO4
正极:PbO2
+
2e-
+
SO42-
+
4H+
=
PbSO4
+
2H2O
重难突破二【二次电池】
问题思考2
已知铅蓄电池的总反应为:
铅蓄电池的放电原理为:
(1)放电结束后,电解液的酸性变化?
(2)当电路中转移0.2mol
电子时,正负极质量如何变化?
酸性减弱,pH变大
负极:Pb
-
2e-
+
SO42-
=
PbSO4
0.1
0.2
0.1
△m=
0.1
×96=9.6g
正极:PbO2
+
2e-
+
SO42-
+
4H+
=
PbSO4
+
2H2O
0.1
0.2
0.1
△m=
0.1
×64=6.4g
交流讨论
Pb+PbO2+2H2SO4
=
2PbSO4
+
2H2O
Cd
为负极
,
NiO(OH)
为正极
电解液:
KOH溶液
已知镍镉电池的总反应为:
如何写出放电过程中的正负极反应?
Cd+2NiO(OH)+2H2O
Cd(OH)2+2Ni(OH)2
放电
充电
负极:
Cd
+2OH--2e-=
Cd(OH)2
正极:
NiO(OH)
+
H2O
+
e-=
Ni(OH)2
+
OH-
镍镉电池
问题思考3
储氢合金为负极
,
NiO(OH)
为正极
电解液:
KOH溶液
已知镍氢电池的总反应为:
如何写出放电过程中的正负极反应?
H2+2NiO(OH)
2Ni(OH)2
放电
充电
负极:
H2
-2e-
+
2OH-
=
2H2O
正极:
NiO(OH)
+
H2O
+
e-=
Ni(OH)2
+
OH-
问题思考4
Li
为负极
,
LiMn2O4
为正极
电解液:聚合物
已知锂离子电池的总反应为:
如何写出放电过程中的正负极反应?
Li
+
LiMn2O4
Li2Mn2O4
放电
充电
负极:
Li
-e-=
Li
+
正极:
LiMn2O4
+
Li
+
+
e-=
Li2Mn2O4
锂电池
问题思考5
锂离子电池能否用水溶液做电解液?
不能,锂与水会反应
归纳小结
【电极反应书写】答题模板
总反应式
价升高
失电子
负极
正极
电极
反应
价降低
得电子
电极
反应
价变化
反应物生成物
反应物生成物
注意:若负极反应较为简单,也可先写出负极反应,再用总反应减去负极反应得到正极反应(复杂电池)
【归纳小结】
【开拓视野】
石墨烯基锂离子电池
2016年7月8日,世界首款石墨烯基
锂离子电池在京发布,该产品由上
海东旭光电的子公司上海碳源汇谷
推出,并命名为“烯王”。该产品
性能优良,可在零下30度到80度环
境下工作,电池循环寿命高达3500
次,充电效率是普通电池的24倍
1、手机充电5秒,就可使用长达半个月
2、汽车充电几分钟,就可以连续开行1000公里
3、中国石墨烯技术世界第一,领跑全球
1.电子表和电子计算器中所用的是钮扣式的微型银锌电池,其
电极分别为Ag2O和Zn,电解液为KOH溶液。工作时电池总反
应为:Ag2O+Zn+H2O
=2Ag+Zn(OH)2。
(1)工作时电流从________极流向________极;
(填“Ag2O”或“Zn”,下同)
(2)正极的电极反应式为:________________________________;
(3)工作时电池正极区的pH________;
(4)外电路中每通过0.2mol电子,锌的质量理论上减少_____g。
课堂检测
Ag2O
Zn
Ag2O
+
H2O
+
2e-
=
2Ag
+
2OH-
增大
6.5
负极:
正极:
总反应:
Al-3e-
+4OH-=
AlO2
-+2H2O
2Al
+
2OH-
+
2H2O
=
3H2↑
+
2AlO2
-
2H2O
+
2e-
=
H2↑
+
2OH-
2.
负极:
正极:
总反应:
Cu-2e-
=
Cu2+
Cu
+
4H+
+
2NO3-=Cu2+
+
2NO2↑
+
2H2O
2H+
+
NO3-
+
e-
=
NO2↑
+
H2O
3.
4.电动汽车以锂电池提供动力,锂电池技术已经成为
汽车研究的前沿科技。某锂电池的电池反应为:
xLi+Li3-xNiCoMnO6
Li3NiCoMnO6
放电
充电
写出放电过程中的正负极反应。
负极:
ⅹ
Li
-ⅹ
e-=
ⅹLi
+
正极:
Li3-xNiCoMnO6
+ⅹLi
+
+ⅹe-=
Li3NiCoMnO6
5.Li?SOCl2电池可用于心脏起搏器。该电池的电极材料分别
为锂和碳,电解液是LiAlCl4?SOCl2。电池总反应可表示为:
4Li+2SOCl2=4LiCl+S+SO2↑。
请回答下列问题:
(1)电池的负极材料为________,发生的电极反应为________________________;
(2)电池正极反应_________________________________;
(3)组装该电池必须在无水、无氧的条件下进行,原因是____________________________________________
Li
Li-e-=
Li+
2SOCl2+4e-=4Cl-+S+SO2↑
因为构成电池的主要成分Li能和氧气、水反应,
且SOCl2也与水反应
第3课时
发展中的化学电源
第二节
化学能与电能
情景导入
你能说说生活中你熟悉的化学电源吗?
情景导入
碱性锌锰干电池
铅蓄电池
锂离子电池
纽扣电池
化学电源
一次电池
二次电池
燃料电池
普通锌锰电池
碱性锌锰电池
银锌纽扣电池
铅蓄电池
镍镉电池
镍氢电池
锂离子电池
化学电源的分类
【学习目标】
1、了解常见一次电池、二次电池的特点
2、掌握一次电池、二次电池电极反应式的书写方法
已知普通锌锰干电池的总反应为:
Zn
+2NH4Cl
=2NH3+ZnCl2
+H2,如何写出正负极反应?
负极:Zn
-
2e-
=
Zn2+
正极:2NH4+
+
2e-
=
2NH3
+
H2
负极:
Zn
正极:石墨
电解质:
MnO2
,
NH4Cl
淀粉糊
1、
MnO2
作用:吸收氢气
2、缺点:漏液、气鼓、失效
3、改进:外壳套上防腐金属筒或塑料桶
将NH4Cl
换成湿的KOH
典例示范1
重难突破一【一次电池】
已知碱性锌锰干电池的总反应为:
Zn
+
2MnO2
+
2H2O
=
2MnOOH
+
Zn(OH)2
如何写出正负极反应?
负极:Zn
+
2OH-
-
2e-
=
Zn(OH)2
正极:MnO2
+
H2O
+
e-
=
MnOOH
+
OH-
负极:
Zn
正极:MnO2
电解质:KOH溶液
典例示范2
已知银锌纽扣电池的总反应为:
Zn+
Ag2O
+
H2O
=
Zn(OH)2
+
2Ag,
如何写出正负极反应?
负极:Zn
+
2OH-
-
2e-
=
Zn(OH)2
正极:Ag2O
+
H2O
+
2e-
=
2Ag
+
2OH-
负极:
Zn
正极:
Ag2O
电解质:KOH溶液
问题思考1
总反应:Zn+
Ag2O
=
ZnO
+
2Ag
正极:Ag2O
+
H2O
+
2e-
=
2Ag
+
2OH-
负极:Zn
+
2OH-
-2e-
=
ZnO
+
H2O
补充:银锌纽扣电池的另一写法
二、二次电池
1、铅蓄电池
Pb为负极
,
PbO2为正极
电解液:
30%的H2SO4溶液
如何写出放电过程中的正负极反应?
Pb+PbO2+2H2SO4
2PbSO4
+
2H2O
放电
充电
负极:Pb
-
2e-
+
SO42-
=
PbSO4
正极:PbO2
+
2e-
+
SO42-
+
4H+
=
PbSO4
+
2H2O
重难突破二【二次电池】
问题思考2
已知铅蓄电池的总反应为:
铅蓄电池的放电原理为:
(1)放电结束后,电解液的酸性变化?
(2)当电路中转移0.2mol
电子时,正负极质量如何变化?
酸性减弱,pH变大
负极:Pb
-
2e-
+
SO42-
=
PbSO4
0.1
0.2
0.1
△m=
0.1
×96=9.6g
正极:PbO2
+
2e-
+
SO42-
+
4H+
=
PbSO4
+
2H2O
0.1
0.2
0.1
△m=
0.1
×64=6.4g
交流讨论
Pb+PbO2+2H2SO4
=
2PbSO4
+
2H2O
Cd
为负极
,
NiO(OH)
为正极
电解液:
KOH溶液
已知镍镉电池的总反应为:
如何写出放电过程中的正负极反应?
Cd+2NiO(OH)+2H2O
Cd(OH)2+2Ni(OH)2
放电
充电
负极:
Cd
+2OH--2e-=
Cd(OH)2
正极:
NiO(OH)
+
H2O
+
e-=
Ni(OH)2
+
OH-
镍镉电池
问题思考3
储氢合金为负极
,
NiO(OH)
为正极
电解液:
KOH溶液
已知镍氢电池的总反应为:
如何写出放电过程中的正负极反应?
H2+2NiO(OH)
2Ni(OH)2
放电
充电
负极:
H2
-2e-
+
2OH-
=
2H2O
正极:
NiO(OH)
+
H2O
+
e-=
Ni(OH)2
+
OH-
问题思考4
Li
为负极
,
LiMn2O4
为正极
电解液:聚合物
已知锂离子电池的总反应为:
如何写出放电过程中的正负极反应?
Li
+
LiMn2O4
Li2Mn2O4
放电
充电
负极:
Li
-e-=
Li
+
正极:
LiMn2O4
+
Li
+
+
e-=
Li2Mn2O4
锂电池
问题思考5
锂离子电池能否用水溶液做电解液?
不能,锂与水会反应
归纳小结
【电极反应书写】答题模板
总反应式
价升高
失电子
负极
正极
电极
反应
价降低
得电子
电极
反应
价变化
反应物生成物
反应物生成物
注意:若负极反应较为简单,也可先写出负极反应,再用总反应减去负极反应得到正极反应(复杂电池)
【归纳小结】
【开拓视野】
石墨烯基锂离子电池
2016年7月8日,世界首款石墨烯基
锂离子电池在京发布,该产品由上
海东旭光电的子公司上海碳源汇谷
推出,并命名为“烯王”。该产品
性能优良,可在零下30度到80度环
境下工作,电池循环寿命高达3500
次,充电效率是普通电池的24倍
1、手机充电5秒,就可使用长达半个月
2、汽车充电几分钟,就可以连续开行1000公里
3、中国石墨烯技术世界第一,领跑全球
1.电子表和电子计算器中所用的是钮扣式的微型银锌电池,其
电极分别为Ag2O和Zn,电解液为KOH溶液。工作时电池总反
应为:Ag2O+Zn+H2O
=2Ag+Zn(OH)2。
(1)工作时电流从________极流向________极;
(填“Ag2O”或“Zn”,下同)
(2)正极的电极反应式为:________________________________;
(3)工作时电池正极区的pH________;
(4)外电路中每通过0.2mol电子,锌的质量理论上减少_____g。
课堂检测
Ag2O
Zn
Ag2O
+
H2O
+
2e-
=
2Ag
+
2OH-
增大
6.5
负极:
正极:
总反应:
Al-3e-
+4OH-=
AlO2
-+2H2O
2Al
+
2OH-
+
2H2O
=
3H2↑
+
2AlO2
-
2H2O
+
2e-
=
H2↑
+
2OH-
2.
负极:
正极:
总反应:
Cu-2e-
=
Cu2+
Cu
+
4H+
+
2NO3-=Cu2+
+
2NO2↑
+
2H2O
2H+
+
NO3-
+
e-
=
NO2↑
+
H2O
3.
4.电动汽车以锂电池提供动力,锂电池技术已经成为
汽车研究的前沿科技。某锂电池的电池反应为:
xLi+Li3-xNiCoMnO6
Li3NiCoMnO6
放电
充电
写出放电过程中的正负极反应。
负极:
ⅹ
Li
-ⅹ
e-=
ⅹLi
+
正极:
Li3-xNiCoMnO6
+ⅹLi
+
+ⅹe-=
Li3NiCoMnO6
5.Li?SOCl2电池可用于心脏起搏器。该电池的电极材料分别
为锂和碳,电解液是LiAlCl4?SOCl2。电池总反应可表示为:
4Li+2SOCl2=4LiCl+S+SO2↑。
请回答下列问题:
(1)电池的负极材料为________,发生的电极反应为________________________;
(2)电池正极反应_________________________________;
(3)组装该电池必须在无水、无氧的条件下进行,原因是____________________________________________
Li
Li-e-=
Li+
2SOCl2+4e-=4Cl-+S+SO2↑
因为构成电池的主要成分Li能和氧气、水反应,
且SOCl2也与水反应
