2.4 物质的分类 课件(共17张PPT)
文档属性
| 名称 | 2.4 物质的分类 课件(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-07-09 00:00:00 | ||
图片预览






文档简介
二、物质分类的意义
医院、实验室、超市、菜场、衣服摆放等
一、生活中应该分类法的例子
分类能够提高我们工作、学习的效率,使我们更快、更便捷地达到目的。
三、怎样分类
选择分类依据
仔细观察和研究
四、哪些分类依据
物质的物理性质、化学性质
氯化钠
高锰酸钾
氧化镁
氯气
氧气
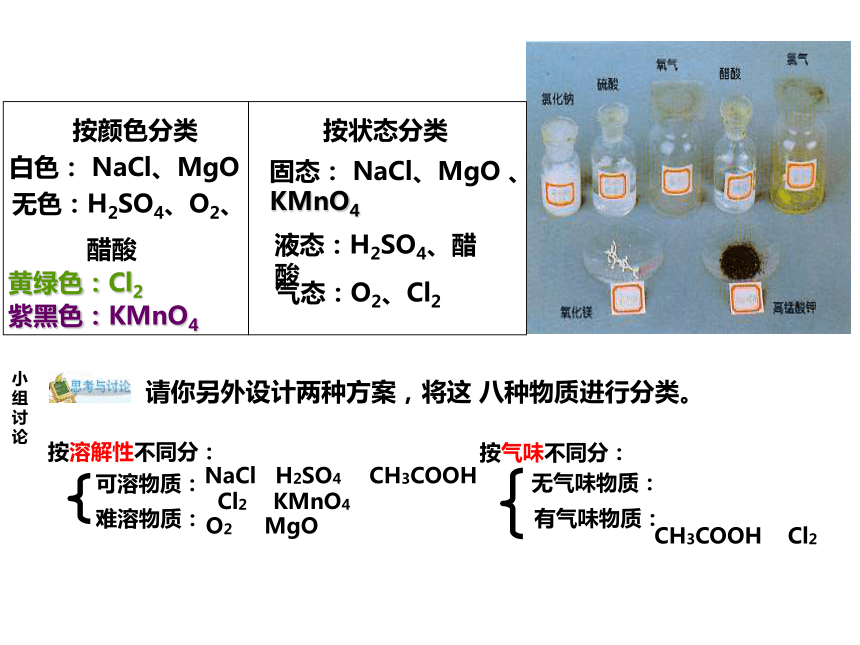
一、观察图中所示的物质,并按它们的颜色和状态进行分类。
按颜色分类
按状态分类
固态: NaCl、MgO 、KMnO4
无色:H2SO4、O2、
醋酸
黄绿色:Cl2
紫黑色:KMnO4
白色: NaCl、MgO
液态:H2SO4、醋酸
气态:O2、Cl2
请你另外设计两种方案,将这 八种物质进行分类。
小组讨论
可溶物质:
难溶物质:
NaCl H2SO4 CH3COOH Cl2 KMnO4
O2 MgO
按气味不同分:
有气味物质:
无气味物质:
CH3COOH Cl2
按溶解性不同分:
1、从物质的物理性质角度分类
对学过的常见物质进行分类:
(1) 按颜色分
(2) 按状态分
(3) 按……分
2、从物质的化学性质角度分类
归纳:纯净物之间的物理性质各不相同。如:颜色、状态、气味、硬度、密度、溶解性等,利用物理性质的不同可对纯净物进行分类。
归纳:纯净物的化学性质也各不相同。如:可燃性、助燃性、还原性、氧化性等等,利用这些不同也可对纯净物进行分类。
每只烧杯里装了什么物质?
如图所示,7只烧杯中分别装有蔗糖、食盐、冰醋酸、无水硫酸铜粉末、色拉油、高锰酸钾、碳酸钠溶液中的某一种物质。能否区分所装的物质各是什么?
【提出问题】
【设计方案】
根据已知物质和未知物质的特性,如状态、颜色、气味、溶解性、可燃性等,运用实验的方法,通过对比可以对物质进行分门别类。
【方案一】
已知物质的特性
待区分物质的特性
名
称
糖
食盐
冰醋酸
硫酸铜
色拉油
高锰酸钾固体
碳酸钠溶液
1
2
3
4
5
6
7
状态
颜色
气味
溶于水
加热熔化
......
将实验结果记录在表格中
固
固
液
固
液
固
液
白
白
无
白
黄
紫黑
无
无
无
无
无
无
有
无
溶
溶
溶
溶
蓝色
溶
紫色
不
溶
易
熔
难
熔
难
熔
难
熔
【方案二】
看状态
固态
液态
看颜色
紫黑色
高锰酸钾
白色
加水
变蓝色
无水硫酸铜粉末
溶解
加热
迅速熔化
蔗糖
难熔化
食盐
看颜色
黄色
色拉油
无色
闻气味
有酸味
无气味
冰醋酸
碳酸钠溶液
【方案三】
看状态
固态
液态
看颜色
紫黑色
高锰酸钾
白色
加水
变蓝色
无水硫酸铜粉末
溶解
加
AgNO3
无现象
蔗糖
变浑浊
食盐
看颜色
黄色
色拉油
无色
加酚酞
无现象
变红色
冰醋酸
碳酸钠溶液
(滴加
稀盐酸)
(有气泡)
【进行实验】
按照实验方案一、二、三进行实验,根据不同物质性质不同,实验现象不同加以区别。
【实验结论】
⑴不溶于水、淡黄色液体:
色拉油
⑵紫黑色固体、形成紫红色溶液:
高锰酸钾
⑶白色固体、形成蓝色溶液:
无水硫酸铜粉末
⑷无色溶液:
蔗糖、食盐、冰醋酸、碳酸钠
①闻气味:
有酸味的是
②滴加盐酸:
有气体生成的是
③滴加AgNO3溶液:
有白色沉淀生成的是
④无任何现象的是:
蔗糖
冰醋酸
碳酸钠
食盐
组成结构
性质
用途
物质的性质、用途与其组成有什么联系?
决定
决定
科学家常常根据组成来给物质分类。
1.物质
分类
纯净物
混合物
空气、溶液
分类标准
( )
物质种类多少
氧气、水、氯酸钾
纯净物
混合物
宏观
微观
特征
联系
纯净物
混合物
若干种相混提纯
只有一种物质组成
由两种或两种以上物质组成
由同种分子构成
由不同种分子构成
有固定熔点、沸点级密度
无固定熔点、沸点
可有化学式表示
不能用化学式表示
二、根据纯净物的组成、用途不同,可对纯净物进行分类。
(1)单质:
由一种元素组成的纯净物。
A.特征:
①同种元素组成
②是纯净物
B.判别:
①先确定是不是纯净物
②是否由一种元素组成
C.分类:
金属
非金属
按性质不同
D.注意点:
纯净物根据元素种类多少的不同,可分为单质和化合物两大类。
由同种元素组成的物质,可能是单质,也可能是混合物。如:O2和O3
(2)化合物:
由两种或两种以上元素组成的纯净物。
如:H2O、P2O5、硫酸、烧碱食盐、纯碱等
A.特征:
①不同种元素组成
②是纯净物
B.判别依据:
①先确定是不是纯净物
②是否由不同种元素组成
a.氧化物:
由两种元素组成,其中一种是氧元素的化合物。
如:H2O、P2O5、Fe2O3、CuO等
A.特征:
①两种元素组成的化合物
②必含氧元素
B.判别依据:
①先确定是不是属于化合物
②是否由“二元一氧”组成
C.分类:
金属氧化物
非金属氧化物
按元素组成
CuO Fe2O3 CaO MgO等
CO2 CO H2O SO2等
①化合物由组成的元素的种类不同可分为氧化物、酸、碱、盐
C.分类:
②根据物质组成中是否含有碳元素分为有机物和无机物
a.有机物:含碳的化合物(碳的氧化物、碳酸盐、碳酸除外)
b.无机物:一般指由碳以外的其他元素组成的化合物。
化学性质:
①具可燃性,燃烧时生成CO2和H2O。
②加热时易炭化:加热或不完全燃烧时有黑色的炭生成。
少数含碳的化合物如CO、CO2、H2CO3、碳酸盐属于无机化合物
b.酸:电离时产生的阳离子全部是氢离子的化合物。
c.碱:电离时产生的阴离子全部是氢氧根离子的化合物。
d.盐:由酸根离子和金属离子或铵根离子组成的化合物。
小结
物质
单质
化合物
纯净物
混合物
空气、溶液
金属单质:
非金属单质:
(稀有气体)
Fe
O2
Ne
无 机
化合物:
有机化合物:
CuO
CH4
氧化物:
酸:
H2SO4
碱:
NaOH
盐:
KNO3
金 属
氧化物:
非金属
氧化物:
SO2
(1)纯净的空气;(2)液态氧;(3)硫磺;(4)矿泉水;
(5)干冰;(6)胆矾晶体;(7)高锰酸钾彻底加热分解的固体残留物;(8)碘酒;(9)浓硫酸;(10)乙醇;(11)铜;(12)氧化钙
其中属于混合物的有____________;属于纯净物的有_____________________。
单质有_________;化合物有______;金属有______;非金属有______。氧化物有______。
1、利用物质的组成分类
练习:
1、4、7、8、9
2、3、5、6、10、11、12
2、3、11
5、6、10、12
11
2、3
5、12、
医院、实验室、超市、菜场、衣服摆放等
一、生活中应该分类法的例子
分类能够提高我们工作、学习的效率,使我们更快、更便捷地达到目的。
三、怎样分类
选择分类依据
仔细观察和研究
四、哪些分类依据
物质的物理性质、化学性质
氯化钠
高锰酸钾
氧化镁
氯气
氧气
一、观察图中所示的物质,并按它们的颜色和状态进行分类。
按颜色分类
按状态分类
固态: NaCl、MgO 、KMnO4
无色:H2SO4、O2、
醋酸
黄绿色:Cl2
紫黑色:KMnO4
白色: NaCl、MgO
液态:H2SO4、醋酸
气态:O2、Cl2
请你另外设计两种方案,将这 八种物质进行分类。
小组讨论
可溶物质:
难溶物质:
NaCl H2SO4 CH3COOH Cl2 KMnO4
O2 MgO
按气味不同分:
有气味物质:
无气味物质:
CH3COOH Cl2
按溶解性不同分:
1、从物质的物理性质角度分类
对学过的常见物质进行分类:
(1) 按颜色分
(2) 按状态分
(3) 按……分
2、从物质的化学性质角度分类
归纳:纯净物之间的物理性质各不相同。如:颜色、状态、气味、硬度、密度、溶解性等,利用物理性质的不同可对纯净物进行分类。
归纳:纯净物的化学性质也各不相同。如:可燃性、助燃性、还原性、氧化性等等,利用这些不同也可对纯净物进行分类。
每只烧杯里装了什么物质?
如图所示,7只烧杯中分别装有蔗糖、食盐、冰醋酸、无水硫酸铜粉末、色拉油、高锰酸钾、碳酸钠溶液中的某一种物质。能否区分所装的物质各是什么?
【提出问题】
【设计方案】
根据已知物质和未知物质的特性,如状态、颜色、气味、溶解性、可燃性等,运用实验的方法,通过对比可以对物质进行分门别类。
【方案一】
已知物质的特性
待区分物质的特性
名
称
糖
食盐
冰醋酸
硫酸铜
色拉油
高锰酸钾固体
碳酸钠溶液
1
2
3
4
5
6
7
状态
颜色
气味
溶于水
加热熔化
......
将实验结果记录在表格中
固
固
液
固
液
固
液
白
白
无
白
黄
紫黑
无
无
无
无
无
无
有
无
溶
溶
溶
溶
蓝色
溶
紫色
不
溶
易
熔
难
熔
难
熔
难
熔
【方案二】
看状态
固态
液态
看颜色
紫黑色
高锰酸钾
白色
加水
变蓝色
无水硫酸铜粉末
溶解
加热
迅速熔化
蔗糖
难熔化
食盐
看颜色
黄色
色拉油
无色
闻气味
有酸味
无气味
冰醋酸
碳酸钠溶液
【方案三】
看状态
固态
液态
看颜色
紫黑色
高锰酸钾
白色
加水
变蓝色
无水硫酸铜粉末
溶解
加
AgNO3
无现象
蔗糖
变浑浊
食盐
看颜色
黄色
色拉油
无色
加酚酞
无现象
变红色
冰醋酸
碳酸钠溶液
(滴加
稀盐酸)
(有气泡)
【进行实验】
按照实验方案一、二、三进行实验,根据不同物质性质不同,实验现象不同加以区别。
【实验结论】
⑴不溶于水、淡黄色液体:
色拉油
⑵紫黑色固体、形成紫红色溶液:
高锰酸钾
⑶白色固体、形成蓝色溶液:
无水硫酸铜粉末
⑷无色溶液:
蔗糖、食盐、冰醋酸、碳酸钠
①闻气味:
有酸味的是
②滴加盐酸:
有气体生成的是
③滴加AgNO3溶液:
有白色沉淀生成的是
④无任何现象的是:
蔗糖
冰醋酸
碳酸钠
食盐
组成结构
性质
用途
物质的性质、用途与其组成有什么联系?
决定
决定
科学家常常根据组成来给物质分类。
1.物质
分类
纯净物
混合物
空气、溶液
分类标准
( )
物质种类多少
氧气、水、氯酸钾
纯净物
混合物
宏观
微观
特征
联系
纯净物
混合物
若干种相混提纯
只有一种物质组成
由两种或两种以上物质组成
由同种分子构成
由不同种分子构成
有固定熔点、沸点级密度
无固定熔点、沸点
可有化学式表示
不能用化学式表示
二、根据纯净物的组成、用途不同,可对纯净物进行分类。
(1)单质:
由一种元素组成的纯净物。
A.特征:
①同种元素组成
②是纯净物
B.判别:
①先确定是不是纯净物
②是否由一种元素组成
C.分类:
金属
非金属
按性质不同
D.注意点:
纯净物根据元素种类多少的不同,可分为单质和化合物两大类。
由同种元素组成的物质,可能是单质,也可能是混合物。如:O2和O3
(2)化合物:
由两种或两种以上元素组成的纯净物。
如:H2O、P2O5、硫酸、烧碱食盐、纯碱等
A.特征:
①不同种元素组成
②是纯净物
B.判别依据:
①先确定是不是纯净物
②是否由不同种元素组成
a.氧化物:
由两种元素组成,其中一种是氧元素的化合物。
如:H2O、P2O5、Fe2O3、CuO等
A.特征:
①两种元素组成的化合物
②必含氧元素
B.判别依据:
①先确定是不是属于化合物
②是否由“二元一氧”组成
C.分类:
金属氧化物
非金属氧化物
按元素组成
CuO Fe2O3 CaO MgO等
CO2 CO H2O SO2等
①化合物由组成的元素的种类不同可分为氧化物、酸、碱、盐
C.分类:
②根据物质组成中是否含有碳元素分为有机物和无机物
a.有机物:含碳的化合物(碳的氧化物、碳酸盐、碳酸除外)
b.无机物:一般指由碳以外的其他元素组成的化合物。
化学性质:
①具可燃性,燃烧时生成CO2和H2O。
②加热时易炭化:加热或不完全燃烧时有黑色的炭生成。
少数含碳的化合物如CO、CO2、H2CO3、碳酸盐属于无机化合物
b.酸:电离时产生的阳离子全部是氢离子的化合物。
c.碱:电离时产生的阴离子全部是氢氧根离子的化合物。
d.盐:由酸根离子和金属离子或铵根离子组成的化合物。
小结
物质
单质
化合物
纯净物
混合物
空气、溶液
金属单质:
非金属单质:
(稀有气体)
Fe
O2
Ne
无 机
化合物:
有机化合物:
CuO
CH4
氧化物:
酸:
H2SO4
碱:
NaOH
盐:
KNO3
金 属
氧化物:
非金属
氧化物:
SO2
(1)纯净的空气;(2)液态氧;(3)硫磺;(4)矿泉水;
(5)干冰;(6)胆矾晶体;(7)高锰酸钾彻底加热分解的固体残留物;(8)碘酒;(9)浓硫酸;(10)乙醇;(11)铜;(12)氧化钙
其中属于混合物的有____________;属于纯净物的有_____________________。
单质有_________;化合物有______;金属有______;非金属有______。氧化物有______。
1、利用物质的组成分类
练习:
1、4、7、8、9
2、3、5、6、10、11、12
2、3、11
5、6、10、12
11
2、3
5、12、
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
