第6讲-溶质的质量分数与溶液的配制(讲义+课后练习)---2021—2022学年浙教版八上科学暑期讲义(无答案)
文档属性
| 名称 | 第6讲-溶质的质量分数与溶液的配制(讲义+课后练习)---2021—2022学年浙教版八上科学暑期讲义(无答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-07-12 00:00:00 | ||
图片预览



文档简介
center159385第6讲 : 溶质的质量分数与溶液的配制
构成物质的奥秘
第6讲 : 溶质的质量分数与溶液的配制
构成物质的奥秘
学习目标
学习目标
1.理解溶液中溶质的质量分数的含义,能进行简单的计算;
2.学会配制一定溶质质量分数的溶液;
3.学会浓溶液稀释和稀溶液浓缩的有关方法。
170497557785模块一:溶质的质量分数
模块一:溶质的质量分数
知识讲解
知识讲解
知识检测
知识检测
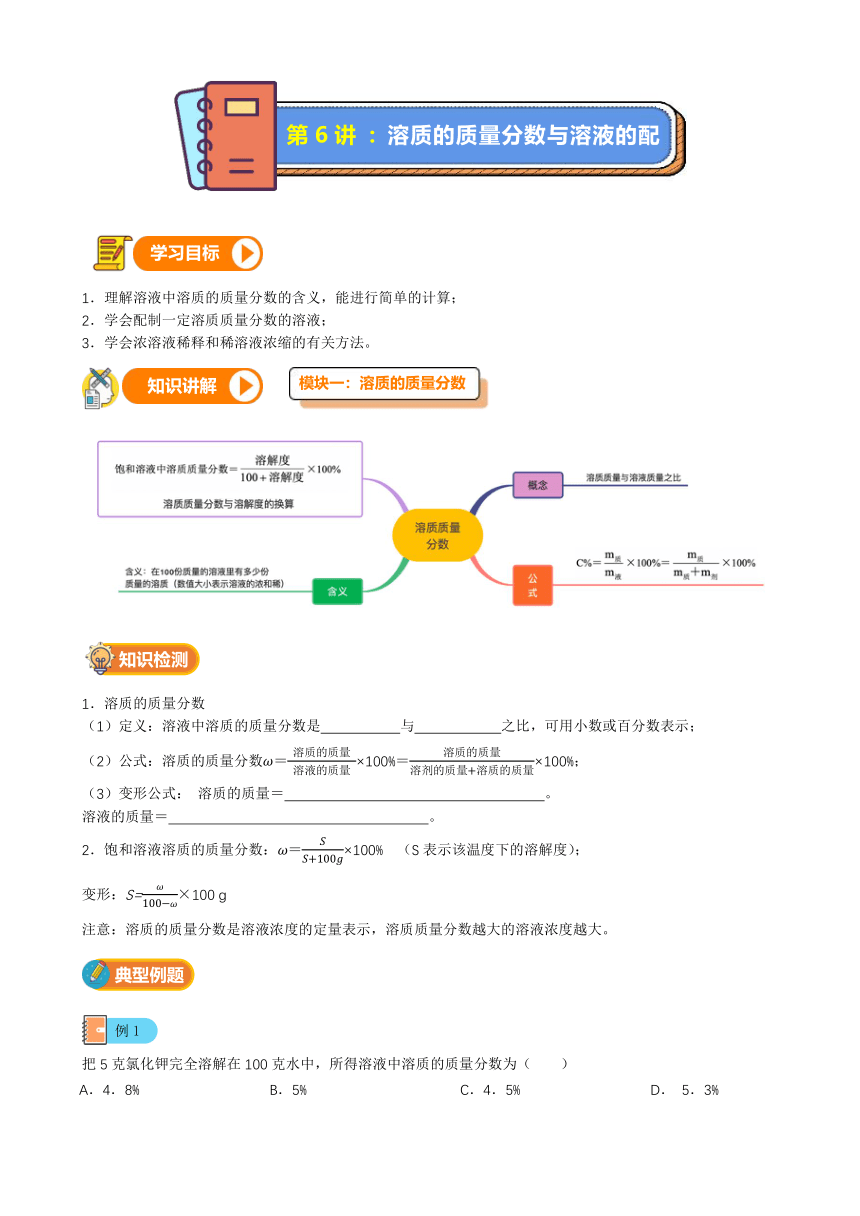
1.溶质的质量分数
(1)定义:溶液中溶质的质量分数是 与 之比,可用小数或百分数表示;
(2)公式:溶质的质量分数ω= 溶质的质量 溶液的质量×100%=溶质的质量溶剂的质量+溶质的质量×100%;
(3)变形公式: 溶质的质量= 。
溶液的质量= 。
2.饱和溶液溶质的质量分数:ω=SS+100g×100% (S表示该温度下的溶解度);
变形:S=ω100?ω×100 g
注意:溶质的质量分数是溶液浓度的定量表示,溶质质量分数越大的溶液浓度越大。
典型例题
典型例题
例1
例1
把5克氯化钾完全溶解在100克水中,所得溶液中溶质的质量分数为( )
A.4.8%
B.5%
C.4.5%
D. 5.3%
例2
例2
氯化钠在20℃时的溶解度为36g,该温度下,氯化钠溶液中溶质的质量分数不可能为( )
A.20%
B.26.5%
C.25%
D.30%
例3
例3
溶质的质量分数为10%的氢氧化钠溶液,对其意义理解不正确的是( )
A.100g水中溶解有10g氢氧化钠
B.10g溶液中含有1g氢氧化钠
C.溶液中溶质质量与溶剂质量的比为1:9
D.把5g氢氧化钠固体溶解在45g水中,可制成10%的氢氧化钠溶液
例4
例4
将20℃时一定质量的饱和硝酸钾溶液,分别进行如下实验后,所得结论正确的是( )
A.升温至30℃时,溶液中溶质的质量分数不变
B.保持温度不变,蒸发10g水后,硝酸钾的溶解度增大
C.保持温度不变,蒸发10g水后,溶液中溶质的质量分数减小
D.保持温度不变,加入10g硝酸钾后,溶液中溶质的质量分数增大
例5
例5
20℃时,将等质量的a、b两种不含结晶水的固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后,现象如图甲;然后升温到50℃时现象如图乙;a、b两种物质的溶解度曲线如图丙。由这一过程可知( )
365315538735A.图甲中a溶液溶质质量分数比b溶液大
B.图乙中a、b溶液一定都是饱和溶液
C.图丙中表示a的溶解度曲线是M
D.30℃时a、b溶液溶质质量分数不相等
例6
例6
配制500mL的质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),需要氢氧化钠和水的质量各是多少?
变式训练
变式训练
练1
练1
向100克20%的氯化铵饱和溶液中加入10克氯化铵固体,则下列说法正确的是( )
A.溶液质量增加
B.溶质的质量增大
C.溶质质量分数增大
D.以上说法都错
练2
练2
20%的氯化钠溶液中,溶质、溶剂、溶液之间的质量关系不正确的是( )
A.m质:m液=1:5
B.C.m质:m剂=1:4
C.B.m质:m液=1:6
D.m剂:m液=4:5
练3
练3
将一杯不饱和的食盐溶液恒温蒸发直至有大量食盐晶体析出,下列曲线能正确反映食盐的溶质质量分数随蒸发掉的水的质量m而变化的是( )
A. B. C. D.
练4
练4
如表是固体甲和乙在不同温度时的溶解度。下列说法中正确的是( )
温度/℃
0
20
40
100
甲溶解度/克
0.173
0.165
0.121
0.076
乙溶解度/克
13.3
31.6
63.9
246
A.20℃时甲物质的饱和溶液升高温度会变为不饱和溶液
B.100℃时乙物质的饱和溶液冷却到室温会析出晶体,但溶液仍饱和
C.20℃时,甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数
D.20℃时,100克乙物质加入100克水中,所得溶液的溶质质量分数等于50%
练5
练5
欲使50g质量分数为10%的NaCl溶液变为20%,操作最简便的方法是( )
A.加入5g?NaCl
B.加入6.25g?NaCl
C.蒸发22.5?g水
D.蒸发25?g水
练6
练6
某同学取四份50克水后,分别加入一定质量的硝酸钾固体配制成t℃的溶液,充分搅拌后,滤去未溶解的固体,将相关数据记录如下表:
操作序号
1
2
3
4
加入硝酸钾的质量/克
40
50
60
70
溶液的质量/克
90
100
105
105
根据以上数据,计算t℃时硝酸钾饱和溶液的溶质质量分数。
175831524130模块二:溶液的配制
模块二:溶液的配制
知识讲解
知识讲解
知识检测
知识检测
1.溶液的配制
(1)器材:天平、量筒、烧杯、玻璃棒、药匙、胶头滴管;
(2)步骤:①计算:计算溶剂和溶质的质量或体积;
②称量和量取:固体用 称取;液体用 量取;
③溶解:将用量筒量取的水,倒入盛有氯化钠的烧杯里,用玻璃棒搅拌,玻璃棒的作用是 ;
④装瓶并贴上标签。
2.溶液的溶质质量分数的误差的影响因素
(1)溶质的原因:如果药品中含有杂质,则导致配制的溶液中溶质的质量分数 ;如果称量时药品和砝码位置颠倒,若未使用游码,则对溶液中溶质的质量分数 ;若使用了游码,则所配制溶液中溶质的质量分数 ;
(2)溶剂的原因:主要是量取溶剂过程中读数的方法导致的,仰视读数导致量取的溶剂量 ;俯视读数导致量取的溶剂量 ;
(3)配制时的原因:烧杯提前用水润洗,导致实际溶剂量 ;药品倒入烧杯中时不慎撒出,导致溶质量 等;
(4)装入试剂瓶时的原因:试剂瓶用水润洗,导致溶剂量 。
3.溶液的稀释与浓缩
(1)依据:溶液稀释前后, 质量不变;
(2)注意:两种溶液混合时, 可以相加,但 不能相加;
(3)溶液稀释问题的计算
①原则:稀释前后,溶液中溶质的质量不变;
将溶液稀释的方法是在浓溶液中加入溶剂水,由于加入的水属于溶剂,所以溶剂的质量和溶液(溶质+溶剂)的质量增加,但溶质的质量不变,据此可以解决稀释溶液时的相关问题。
②计算公式: 或m浓·a%=(m浓+m水)·b%
扩展: a%(浓)= b%(稀)
注意:V水=m水ρ水=m稀?m浓ρ水
的数值 ,均为 。
典型例题
典型例题
例1
例1
用氯化钠固体配制一定质量分数的氯化钠溶液,不需要用到的仪器是( )
A.烧杯
B.量筒
C.托盘天平
D.蒸发皿
例2
例2
实验室要配制50g 3%的食盐水,其中操作方法不正确的是( )
A.计算所需氯化钠的质量为1.5g,水的体积为48.5mL
B.移动游码至1.5克,然后在左盘添加氯化钠至天平平衡
C.用50mL量筒量取48.5mL水,将称好的氯化钠倒入量筒中
D.用玻璃棒搅拌,使氯化钠完全溶解
例3
例3
配制一定质量分数的食盐溶液时,会引起溶质质量分数偏小的操作是( )
A.称量食盐时,天平的指针向左倾斜
B.称量食盐时所加的码砝上有一些铁锈
C.用量筒取水时仰视读数
D.将已配制好的氯化钠溶液装入试剂瓶时,有少量溶液洒在瓶外
例4
例4
化学兴趣小组要在实验室中配制一定溶质质量分数的氯化钠溶液。
甲图中缺少一种必须用到的玻璃仪器是______(填写名称),其作用是_________。
(2)在用量筒量取蒸馏水时,读数时视线应该与_______保持水平。
(3)准确称量氯化钠18g,量取蒸馏水的体积如乙图所示,完全溶解后所得溶液中溶质质量分数是______(水的密度为1g?cm-3)。
(4)若他们在量取溶剂时,俯视量筒读数,会导致所配的溶液溶质质量分数______(填“增大”“减少”或“不变”)
例5
例5
把m克质量分数为a%的NaCl溶液加水稀释,下列图象中正确描述溶液中溶质质量与加水质量关系的是( )
A. B. C. D.
例6
例6
已知10%稀硫酸的密度为 1.07g/cm3,98%浓硫酸的密度为1.84g/cm3
(1)配制1070克10%的稀硫酸溶液需纯硫酸______克?
(2)配制1000毫升10%的稀硫酸溶液需98%浓硫酸______克?(保留一位小数)
(3)实验室需配制1000毫升10%的稀硫酸溶液,则需98%浓硫酸多少毫升?(保留一位小数)
变式训练
变式训练
练1
练1
实验室配制氯化钠溶液的操作中,正确的是( )
A. B. C. D.
练2
练2
如图为配制50g溶质质量分数为10%的氯化钠溶液的操作过程,下列有关操作与目的分析均正确的是( )
A.用剩的食盐放回原试剂瓶避免浪费
B.天平调平后在左、右托盘中各垫一张相同的纸保证称取的食盐质量更准确
C.用50mL量筒替代天平量取所需的水更加简便
D.溶解时用玻璃棒搅拌增加食盐的溶解能力
练3
练3
在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是( )
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处
C.将量筒中的水倒入烧杯时,量筒中有少量水残余
D.将配好的氯化钠溶液转移到细口瓶中时,不慎洒出部分溶液
练4
练4
实验室要配制50g 5%的氢氧化钠溶液.现有①托盘天平 ②量筒(10mL、50mL、100mL)③药匙,根据要求填空:
(1)完成本实验还需要的主要玻璃仪器是______。
(2)具体操作步骤可概括为________。
(3)本实验需氢氧化钠质量为______g,需水______mL,取水时应选用______mL的量筒。
练5
练5
一份溶质质量分数为2%的氯化钠溶液蒸发掉20克水,其溶质质量分数为10%,则原溶液中溶质的质量是( )
A.0.5g
B.1g
C.2.5g
D.4g
练6
练6
如图是某试剂瓶标签上的内容。
(1)要把10g这种浓硫酸稀释为20%的硫酸,需要水的质量为______g。
(2)取10mL该硫酸可配制成9.8%的硫酸______g。
(3)要配置100g质量分数为10%的稀硫酸需要这种浓硫酸的质量是______。
构成物质的奥秘
第6讲 : 溶质的质量分数与溶液的配制
构成物质的奥秘
学习目标
学习目标
1.理解溶液中溶质的质量分数的含义,能进行简单的计算;
2.学会配制一定溶质质量分数的溶液;
3.学会浓溶液稀释和稀溶液浓缩的有关方法。
170497557785模块一:溶质的质量分数
模块一:溶质的质量分数
知识讲解
知识讲解
知识检测
知识检测
1.溶质的质量分数
(1)定义:溶液中溶质的质量分数是 与 之比,可用小数或百分数表示;
(2)公式:溶质的质量分数ω= 溶质的质量 溶液的质量×100%=溶质的质量溶剂的质量+溶质的质量×100%;
(3)变形公式: 溶质的质量= 。
溶液的质量= 。
2.饱和溶液溶质的质量分数:ω=SS+100g×100% (S表示该温度下的溶解度);
变形:S=ω100?ω×100 g
注意:溶质的质量分数是溶液浓度的定量表示,溶质质量分数越大的溶液浓度越大。
典型例题
典型例题
例1
例1
把5克氯化钾完全溶解在100克水中,所得溶液中溶质的质量分数为( )
A.4.8%
B.5%
C.4.5%
D. 5.3%
例2
例2
氯化钠在20℃时的溶解度为36g,该温度下,氯化钠溶液中溶质的质量分数不可能为( )
A.20%
B.26.5%
C.25%
D.30%
例3
例3
溶质的质量分数为10%的氢氧化钠溶液,对其意义理解不正确的是( )
A.100g水中溶解有10g氢氧化钠
B.10g溶液中含有1g氢氧化钠
C.溶液中溶质质量与溶剂质量的比为1:9
D.把5g氢氧化钠固体溶解在45g水中,可制成10%的氢氧化钠溶液
例4
例4
将20℃时一定质量的饱和硝酸钾溶液,分别进行如下实验后,所得结论正确的是( )
A.升温至30℃时,溶液中溶质的质量分数不变
B.保持温度不变,蒸发10g水后,硝酸钾的溶解度增大
C.保持温度不变,蒸发10g水后,溶液中溶质的质量分数减小
D.保持温度不变,加入10g硝酸钾后,溶液中溶质的质量分数增大
例5
例5
20℃时,将等质量的a、b两种不含结晶水的固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后,现象如图甲;然后升温到50℃时现象如图乙;a、b两种物质的溶解度曲线如图丙。由这一过程可知( )
365315538735A.图甲中a溶液溶质质量分数比b溶液大
B.图乙中a、b溶液一定都是饱和溶液
C.图丙中表示a的溶解度曲线是M
D.30℃时a、b溶液溶质质量分数不相等
例6
例6
配制500mL的质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),需要氢氧化钠和水的质量各是多少?
变式训练
变式训练
练1
练1
向100克20%的氯化铵饱和溶液中加入10克氯化铵固体,则下列说法正确的是( )
A.溶液质量增加
B.溶质的质量增大
C.溶质质量分数增大
D.以上说法都错
练2
练2
20%的氯化钠溶液中,溶质、溶剂、溶液之间的质量关系不正确的是( )
A.m质:m液=1:5
B.C.m质:m剂=1:4
C.B.m质:m液=1:6
D.m剂:m液=4:5
练3
练3
将一杯不饱和的食盐溶液恒温蒸发直至有大量食盐晶体析出,下列曲线能正确反映食盐的溶质质量分数随蒸发掉的水的质量m而变化的是( )
A. B. C. D.
练4
练4
如表是固体甲和乙在不同温度时的溶解度。下列说法中正确的是( )
温度/℃
0
20
40
100
甲溶解度/克
0.173
0.165
0.121
0.076
乙溶解度/克
13.3
31.6
63.9
246
A.20℃时甲物质的饱和溶液升高温度会变为不饱和溶液
B.100℃时乙物质的饱和溶液冷却到室温会析出晶体,但溶液仍饱和
C.20℃时,甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数
D.20℃时,100克乙物质加入100克水中,所得溶液的溶质质量分数等于50%
练5
练5
欲使50g质量分数为10%的NaCl溶液变为20%,操作最简便的方法是( )
A.加入5g?NaCl
B.加入6.25g?NaCl
C.蒸发22.5?g水
D.蒸发25?g水
练6
练6
某同学取四份50克水后,分别加入一定质量的硝酸钾固体配制成t℃的溶液,充分搅拌后,滤去未溶解的固体,将相关数据记录如下表:
操作序号
1
2
3
4
加入硝酸钾的质量/克
40
50
60
70
溶液的质量/克
90
100
105
105
根据以上数据,计算t℃时硝酸钾饱和溶液的溶质质量分数。
175831524130模块二:溶液的配制
模块二:溶液的配制
知识讲解
知识讲解
知识检测
知识检测
1.溶液的配制
(1)器材:天平、量筒、烧杯、玻璃棒、药匙、胶头滴管;
(2)步骤:①计算:计算溶剂和溶质的质量或体积;
②称量和量取:固体用 称取;液体用 量取;
③溶解:将用量筒量取的水,倒入盛有氯化钠的烧杯里,用玻璃棒搅拌,玻璃棒的作用是 ;
④装瓶并贴上标签。
2.溶液的溶质质量分数的误差的影响因素
(1)溶质的原因:如果药品中含有杂质,则导致配制的溶液中溶质的质量分数 ;如果称量时药品和砝码位置颠倒,若未使用游码,则对溶液中溶质的质量分数 ;若使用了游码,则所配制溶液中溶质的质量分数 ;
(2)溶剂的原因:主要是量取溶剂过程中读数的方法导致的,仰视读数导致量取的溶剂量 ;俯视读数导致量取的溶剂量 ;
(3)配制时的原因:烧杯提前用水润洗,导致实际溶剂量 ;药品倒入烧杯中时不慎撒出,导致溶质量 等;
(4)装入试剂瓶时的原因:试剂瓶用水润洗,导致溶剂量 。
3.溶液的稀释与浓缩
(1)依据:溶液稀释前后, 质量不变;
(2)注意:两种溶液混合时, 可以相加,但 不能相加;
(3)溶液稀释问题的计算
①原则:稀释前后,溶液中溶质的质量不变;
将溶液稀释的方法是在浓溶液中加入溶剂水,由于加入的水属于溶剂,所以溶剂的质量和溶液(溶质+溶剂)的质量增加,但溶质的质量不变,据此可以解决稀释溶液时的相关问题。
②计算公式: 或m浓·a%=(m浓+m水)·b%
扩展: a%(浓)= b%(稀)
注意:V水=m水ρ水=m稀?m浓ρ水
的数值 ,均为 。
典型例题
典型例题
例1
例1
用氯化钠固体配制一定质量分数的氯化钠溶液,不需要用到的仪器是( )
A.烧杯
B.量筒
C.托盘天平
D.蒸发皿
例2
例2
实验室要配制50g 3%的食盐水,其中操作方法不正确的是( )
A.计算所需氯化钠的质量为1.5g,水的体积为48.5mL
B.移动游码至1.5克,然后在左盘添加氯化钠至天平平衡
C.用50mL量筒量取48.5mL水,将称好的氯化钠倒入量筒中
D.用玻璃棒搅拌,使氯化钠完全溶解
例3
例3
配制一定质量分数的食盐溶液时,会引起溶质质量分数偏小的操作是( )
A.称量食盐时,天平的指针向左倾斜
B.称量食盐时所加的码砝上有一些铁锈
C.用量筒取水时仰视读数
D.将已配制好的氯化钠溶液装入试剂瓶时,有少量溶液洒在瓶外
例4
例4
化学兴趣小组要在实验室中配制一定溶质质量分数的氯化钠溶液。
甲图中缺少一种必须用到的玻璃仪器是______(填写名称),其作用是_________。
(2)在用量筒量取蒸馏水时,读数时视线应该与_______保持水平。
(3)准确称量氯化钠18g,量取蒸馏水的体积如乙图所示,完全溶解后所得溶液中溶质质量分数是______(水的密度为1g?cm-3)。
(4)若他们在量取溶剂时,俯视量筒读数,会导致所配的溶液溶质质量分数______(填“增大”“减少”或“不变”)
例5
例5
把m克质量分数为a%的NaCl溶液加水稀释,下列图象中正确描述溶液中溶质质量与加水质量关系的是( )
A. B. C. D.
例6
例6
已知10%稀硫酸的密度为 1.07g/cm3,98%浓硫酸的密度为1.84g/cm3
(1)配制1070克10%的稀硫酸溶液需纯硫酸______克?
(2)配制1000毫升10%的稀硫酸溶液需98%浓硫酸______克?(保留一位小数)
(3)实验室需配制1000毫升10%的稀硫酸溶液,则需98%浓硫酸多少毫升?(保留一位小数)
变式训练
变式训练
练1
练1
实验室配制氯化钠溶液的操作中,正确的是( )
A. B. C. D.
练2
练2
如图为配制50g溶质质量分数为10%的氯化钠溶液的操作过程,下列有关操作与目的分析均正确的是( )
A.用剩的食盐放回原试剂瓶避免浪费
B.天平调平后在左、右托盘中各垫一张相同的纸保证称取的食盐质量更准确
C.用50mL量筒替代天平量取所需的水更加简便
D.溶解时用玻璃棒搅拌增加食盐的溶解能力
练3
练3
在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是( )
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处
C.将量筒中的水倒入烧杯时,量筒中有少量水残余
D.将配好的氯化钠溶液转移到细口瓶中时,不慎洒出部分溶液
练4
练4
实验室要配制50g 5%的氢氧化钠溶液.现有①托盘天平 ②量筒(10mL、50mL、100mL)③药匙,根据要求填空:
(1)完成本实验还需要的主要玻璃仪器是______。
(2)具体操作步骤可概括为________。
(3)本实验需氢氧化钠质量为______g,需水______mL,取水时应选用______mL的量筒。
练5
练5
一份溶质质量分数为2%的氯化钠溶液蒸发掉20克水,其溶质质量分数为10%,则原溶液中溶质的质量是( )
A.0.5g
B.1g
C.2.5g
D.4g
练6
练6
如图是某试剂瓶标签上的内容。
(1)要把10g这种浓硫酸稀释为20%的硫酸,需要水的质量为______g。
(2)取10mL该硫酸可配制成9.8%的硫酸______g。
(3)要配置100g质量分数为10%的稀硫酸需要这种浓硫酸的质量是______。
同课章节目录
