第八课时提纯鉴别检验
图片预览






文档简介
(共18张PPT)
专题复习之 物质的鉴别和提纯
物质鉴别方法:
(一)用化学方法
证明被鉴物质 方法 现象
酸
碱
含Cl-的物质
含SO42-的物质
含CO32-的物质
H2
CO
CO2
O2
H2O
1 滴加石蕊试液 1试剂变红
2 加Zn、Fe等金属 2产生可燃性气体
滴加酚酞试液 试液变红
滴加AgNO3、HNO3 白色沉淀
滴加BaCl2、HNO3 白色沉淀
滴加盐酸产生气体通入Ca(OH)2 白色沉淀
火焰上方罩干燥小烧杯 有水珠出现
点燃、产生的气体与石灰水反应 白色沉淀
澄清石灰水 变浑浊
带火星木条 复燃
白色无水硫酸铜粉末 变蓝色
一、物质的鉴别
物质的鉴别,简单地说就是区别物质,即根据其物理性质或化学性质的不同而加以辨别的过程. 区别的依据是通过加入试剂后产生的现象:逸出气体、产生沉淀、发生颜色变化等来判断。
取少量加试剂,由现象定结果
例如鉴别两瓶无色的NaCl 和 Na2CO3溶液
(1)取少量溶液(固体取少许配成溶液)于试管中;(2)加入少量的试剂
(3)观察实验现象
(4)判断、得出结论
解题步骤
常见的题型:
1.任选试剂的鉴别
没有任何条件限制地选择试剂,区别一组物质,但一般要求所用试剂最少,反应步骤最简。
任取所需要的试剂,根据化学实验现象区别:
氯化钠、硝酸钠、碳酸钠3种无色溶液。
2.限用一种试剂的鉴别
要求只用一种试剂来实现所给物质的区别,即在加入一种试剂后,各鉴别对象表现的现象各异,根据现象的差异加以区别。
例1、用一种试剂区别以下三种初中化学常见的黑 色固体:炭粉、铁粉、氧化铜。
例2、用一种试剂鉴别以下三种溶液:
NaCl 、AgNO3、Na2CO3,这种试剂
是 。
3.不用外加试剂的鉴别
要求不用任何外加试剂区别所给一组物质,区别的原理是利用组内物质的一般特性,辨认出有特殊性质的物质,再用已鉴别出的物质来区别余下的其它物质,
从物质的物理性质寻找突破口
例1、不用其他试剂,用最简单的方法鉴别下列五种物质的溶液:
①NaOH②Al2(SO4)3③FeCl3④Ba(NO3)2⑤KCl,则正确的鉴别顺
序是( )A②④③①⑤ B ③①②④⑤ C ①③②④⑤ D③②④①⑤
观颜色
闻气味
例2、NH3·H2O K2SO4 MgCl2 Na2CO3四种溶液
从物质间反应的次数与现象来判断
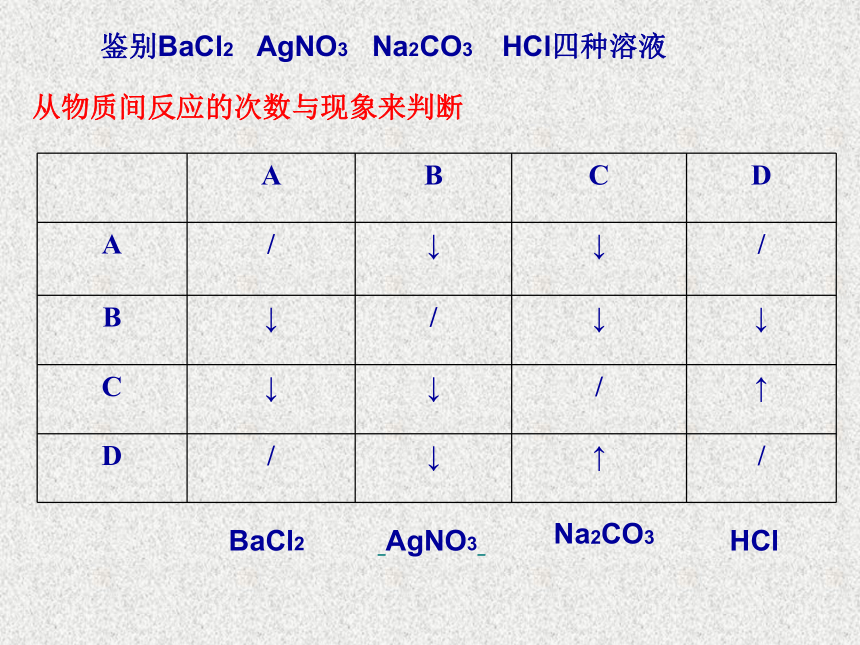
鉴别BaCl2 AgNO3 Na2CO3 HCl四种溶液
B
A B C D
A / ↓ ↓ /
B ↓ / ↓ ↓
C ↓ ↓ / ↑
D / ↓ ↑ /
鉴别BaCl2 AgNO3 Na2CO3 HCl四种溶液
从物质间反应的次数与现象来判断
BaCl2
AgNO3
Na2CO3
HCl
小结:
1、根据物理性质来鉴别:如颜色、气味、溶解性、密度等
2、用酸碱指示剂、PH试纸来鉴别——区别酸性和碱性溶液
3、用酸、碱、盐、来鉴别——通过所发生化学反应的现象:如
变色、放出气体、生成沉淀等来区别
4、用燃烧的木条来鉴别
二、物质的提纯
根据物质和杂质的性质,采用物理或化学方法把混合物中杂质分离除去,从而保留一种较为纯净的成分,这一过程叫做物质的提纯,又叫除杂。
提纯的基本原则是:
除杂不能加杂
提纯的方法:
物理方法
化学方法
练一练
1:如何除去食盐中混有泥沙(粗盐提纯)。
如何除去NaCl中混有的CuO 。
溶解、过滤法 :适用于可溶于水的固体和难溶于水的固
体的提纯
2、如何除去KNO3中混有少量的NaCl 。
结晶法(冷却热饱和溶液法):适用于多种可溶于水的固体而它们的溶解度受温度影响程度不同
3、若CO中混有少量CO2气体,欲除去CO2,将混合气体通过
溶液。
4、若制取的H2中混有少量HCl气体和水蒸气,应先将
气体通过 ,再通过 即可。
吸收法:混合气体中的杂质被某种溶剂或溶液吸收,而要提纯的气体不能被吸收时,可用此方法。
NaOH
NaOH溶液
浓硫酸
5、如何除去氧化钙中含有的碳酸钙?
除去NaCl溶液中混有的少量Na2CO3 ,应选择的试剂为:
化气法: 通过加热或加入试剂把混合物中杂质发生化学变化,
变成气体而除去。
稀盐酸
6、除去下列括号内的杂质应选什么试剂:
⑴、NaCl(CaCl2 )
(2)KCl( K2SO4 )
(3)KNO3(KCl )
沉淀法:往混合溶液中加入某种试剂,使其中的杂质通过化学
反应以沉淀形式析出,然后经过滤除去沉淀,得到净化后的溶液。
Na2CO3 溶液
AgNO3 溶液
BaCl2 溶液
7、除去CO2中少量CO,最好采取的方法:
转化法:通过适当的方法,把混合物中杂质转化,使混合物
转化为纯净物,这种方法是最为有效的除杂方法。
8、如何除去ZnSO4溶液中含有少量CuSO4杂质。
置换法:将混合物中的杂质与适量试剂通过发生置换反应而除去。
9、如何除去银粉中的少量锌粉。
溶解法:用试剂与杂质反应溶解而除掉
通过灼热的氧化铜
锌粉
高温煅烧
小结:
1、搞清楚杂质是什么,要保护什么,然后选除杂试剂
2、当杂质与被提纯的物质有部分相同时,通常将其转化
为被提纯的物质
3、除去Cl- 一般用Ag+转化为Ag Cl沉淀;
除去 SO42- 一般用Ba 2+转化为BaSO4沉淀;
除去CO32-一般用H+(酸)转化为CO2气体、加热转化为
CO2气体或转化为沉淀。
1、氢氧化钠固体已放在表面皿中一段时间了,请你证明该固体是否已变质 简述实验步骤和现象,并写出相关的化学方程式.
练一练
2、假银圆大多是锌的某些合金,请用不同的物质类别进行区分
(写出2种)
3、为了除去粗盐中的Ca2+、Mg2+、SO2-入泥沙。可将粗盐溶于
水。然后进行下列五项操作。
①过滤 ②过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3
溶液⑤加过量BaCl2溶液,
其中正确的操作顺序是( )
A ⑤②④①③ B④①②⑤③ C ②⑤④①③ D ①④②⑤③
4、不用其他试剂,用最简单的方法鉴别下列五种物质的溶液:
①NaOH ②Al2(SO4)3 ③FeCl3 ④Ba(NO3)2 ⑤KCl,
则正确的鉴别顺序是( )
A②④③①⑤ B ③①②④⑤ C ①③②④⑤ D③②④①⑤
5、下列混合物可以用溶解、过滤、蒸发操作来分离的是:( ) A.CaCO3 CaO B.NaCl KNO3
C.NaNO3 BaSO4 D.KCl KClO3
6、只用一种物质就能将稀硫酸、水、澄清石灰水三种无色液体鉴
别出来,可供选用的物质是:①PH试纸、②酚酞试液、③稀盐酸、
④碳酸钠溶液、⑤石蕊试液,其中能用于鉴别的是( )
A、①④⑤ B、①②⑤ C、①②③ D、③④⑤
7、只用一种试剂,一次将氯化镁、氯化钡、氢氧化钾三种溶液区别开来。则这种试剂的化学式是
8、实验室有失去标签的盐酸、碳酸钠、硫酸、氢氧化钾和硝酸钾
五种溶液。为把他们区别开来,所加试剂及先后顺序合理的一组是
A、氯化钡溶液、稀硝酸、石蕊试液
B、稀硝酸、石蕊试液、硝酸银溶液
C、石蕊试液、稀硝酸、硝酸银溶液
D、稀硝酸、酚酞试液、硝酸银溶液
9、用稀盐酸和锌粒的反应制取氢气时,常混有HCl、水蒸气等杂质,
为证明并除去杂质,制得纯净、干燥的氢气,根据下图回答:
(1)应选择的发生装置和净化装置是_____。
(2)连接选择的装置各管口的顺序是(填字母):
( )接( ),( )接( ),( )接( )。
(3)证明并除去混有的氯化氢的实验现象是__ _,
依据的化学方程式是__ _ _。
(4)证明混有并除去水蒸气的实验现象是__ _,
依据的化学方程式是________ _。
思考:丙和乙能否交换位置,浓硫酸是否可以不用?
常见离子的检验方法
离子 检验试剂 主要实验现象
H+
OH-
Cl-
SO42-
CO32-
NH4+
Cu2+
Fe3+
紫色石蕊试液
红色
无色酚酞试液
红色
AgNO3溶液及稀HNO3
白色沉淀(不溶于酸)
Ba(NO3)2溶液及HCl
白色沉淀(不溶于酸)
HCl溶液及Ca(OH)2溶液
气体生成并有浑浊现象
NaOH溶液(碱溶液)
湿润的红色石蕊试纸
加热产生使湿润的红色石蕊试纸变蓝的气体
NaOH溶液(碱溶液)
蓝色(絮状)沉淀
NaOH溶液(碱溶液)
红褐(絮状)色沉淀
专题复习之 物质的鉴别和提纯
物质鉴别方法:
(一)用化学方法
证明被鉴物质 方法 现象
酸
碱
含Cl-的物质
含SO42-的物质
含CO32-的物质
H2
CO
CO2
O2
H2O
1 滴加石蕊试液 1试剂变红
2 加Zn、Fe等金属 2产生可燃性气体
滴加酚酞试液 试液变红
滴加AgNO3、HNO3 白色沉淀
滴加BaCl2、HNO3 白色沉淀
滴加盐酸产生气体通入Ca(OH)2 白色沉淀
火焰上方罩干燥小烧杯 有水珠出现
点燃、产生的气体与石灰水反应 白色沉淀
澄清石灰水 变浑浊
带火星木条 复燃
白色无水硫酸铜粉末 变蓝色
一、物质的鉴别
物质的鉴别,简单地说就是区别物质,即根据其物理性质或化学性质的不同而加以辨别的过程. 区别的依据是通过加入试剂后产生的现象:逸出气体、产生沉淀、发生颜色变化等来判断。
取少量加试剂,由现象定结果
例如鉴别两瓶无色的NaCl 和 Na2CO3溶液
(1)取少量溶液(固体取少许配成溶液)于试管中;(2)加入少量的试剂
(3)观察实验现象
(4)判断、得出结论
解题步骤
常见的题型:
1.任选试剂的鉴别
没有任何条件限制地选择试剂,区别一组物质,但一般要求所用试剂最少,反应步骤最简。
任取所需要的试剂,根据化学实验现象区别:
氯化钠、硝酸钠、碳酸钠3种无色溶液。
2.限用一种试剂的鉴别
要求只用一种试剂来实现所给物质的区别,即在加入一种试剂后,各鉴别对象表现的现象各异,根据现象的差异加以区别。
例1、用一种试剂区别以下三种初中化学常见的黑 色固体:炭粉、铁粉、氧化铜。
例2、用一种试剂鉴别以下三种溶液:
NaCl 、AgNO3、Na2CO3,这种试剂
是 。
3.不用外加试剂的鉴别
要求不用任何外加试剂区别所给一组物质,区别的原理是利用组内物质的一般特性,辨认出有特殊性质的物质,再用已鉴别出的物质来区别余下的其它物质,
从物质的物理性质寻找突破口
例1、不用其他试剂,用最简单的方法鉴别下列五种物质的溶液:
①NaOH②Al2(SO4)3③FeCl3④Ba(NO3)2⑤KCl,则正确的鉴别顺
序是( )A②④③①⑤ B ③①②④⑤ C ①③②④⑤ D③②④①⑤
观颜色
闻气味
例2、NH3·H2O K2SO4 MgCl2 Na2CO3四种溶液
从物质间反应的次数与现象来判断
鉴别BaCl2 AgNO3 Na2CO3 HCl四种溶液
B
A B C D
A / ↓ ↓ /
B ↓ / ↓ ↓
C ↓ ↓ / ↑
D / ↓ ↑ /
鉴别BaCl2 AgNO3 Na2CO3 HCl四种溶液
从物质间反应的次数与现象来判断
BaCl2
AgNO3
Na2CO3
HCl
小结:
1、根据物理性质来鉴别:如颜色、气味、溶解性、密度等
2、用酸碱指示剂、PH试纸来鉴别——区别酸性和碱性溶液
3、用酸、碱、盐、来鉴别——通过所发生化学反应的现象:如
变色、放出气体、生成沉淀等来区别
4、用燃烧的木条来鉴别
二、物质的提纯
根据物质和杂质的性质,采用物理或化学方法把混合物中杂质分离除去,从而保留一种较为纯净的成分,这一过程叫做物质的提纯,又叫除杂。
提纯的基本原则是:
除杂不能加杂
提纯的方法:
物理方法
化学方法
练一练
1:如何除去食盐中混有泥沙(粗盐提纯)。
如何除去NaCl中混有的CuO 。
溶解、过滤法 :适用于可溶于水的固体和难溶于水的固
体的提纯
2、如何除去KNO3中混有少量的NaCl 。
结晶法(冷却热饱和溶液法):适用于多种可溶于水的固体而它们的溶解度受温度影响程度不同
3、若CO中混有少量CO2气体,欲除去CO2,将混合气体通过
溶液。
4、若制取的H2中混有少量HCl气体和水蒸气,应先将
气体通过 ,再通过 即可。
吸收法:混合气体中的杂质被某种溶剂或溶液吸收,而要提纯的气体不能被吸收时,可用此方法。
NaOH
NaOH溶液
浓硫酸
5、如何除去氧化钙中含有的碳酸钙?
除去NaCl溶液中混有的少量Na2CO3 ,应选择的试剂为:
化气法: 通过加热或加入试剂把混合物中杂质发生化学变化,
变成气体而除去。
稀盐酸
6、除去下列括号内的杂质应选什么试剂:
⑴、NaCl(CaCl2 )
(2)KCl( K2SO4 )
(3)KNO3(KCl )
沉淀法:往混合溶液中加入某种试剂,使其中的杂质通过化学
反应以沉淀形式析出,然后经过滤除去沉淀,得到净化后的溶液。
Na2CO3 溶液
AgNO3 溶液
BaCl2 溶液
7、除去CO2中少量CO,最好采取的方法:
转化法:通过适当的方法,把混合物中杂质转化,使混合物
转化为纯净物,这种方法是最为有效的除杂方法。
8、如何除去ZnSO4溶液中含有少量CuSO4杂质。
置换法:将混合物中的杂质与适量试剂通过发生置换反应而除去。
9、如何除去银粉中的少量锌粉。
溶解法:用试剂与杂质反应溶解而除掉
通过灼热的氧化铜
锌粉
高温煅烧
小结:
1、搞清楚杂质是什么,要保护什么,然后选除杂试剂
2、当杂质与被提纯的物质有部分相同时,通常将其转化
为被提纯的物质
3、除去Cl- 一般用Ag+转化为Ag Cl沉淀;
除去 SO42- 一般用Ba 2+转化为BaSO4沉淀;
除去CO32-一般用H+(酸)转化为CO2气体、加热转化为
CO2气体或转化为沉淀。
1、氢氧化钠固体已放在表面皿中一段时间了,请你证明该固体是否已变质 简述实验步骤和现象,并写出相关的化学方程式.
练一练
2、假银圆大多是锌的某些合金,请用不同的物质类别进行区分
(写出2种)
3、为了除去粗盐中的Ca2+、Mg2+、SO2-入泥沙。可将粗盐溶于
水。然后进行下列五项操作。
①过滤 ②过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3
溶液⑤加过量BaCl2溶液,
其中正确的操作顺序是( )
A ⑤②④①③ B④①②⑤③ C ②⑤④①③ D ①④②⑤③
4、不用其他试剂,用最简单的方法鉴别下列五种物质的溶液:
①NaOH ②Al2(SO4)3 ③FeCl3 ④Ba(NO3)2 ⑤KCl,
则正确的鉴别顺序是( )
A②④③①⑤ B ③①②④⑤ C ①③②④⑤ D③②④①⑤
5、下列混合物可以用溶解、过滤、蒸发操作来分离的是:( ) A.CaCO3 CaO B.NaCl KNO3
C.NaNO3 BaSO4 D.KCl KClO3
6、只用一种物质就能将稀硫酸、水、澄清石灰水三种无色液体鉴
别出来,可供选用的物质是:①PH试纸、②酚酞试液、③稀盐酸、
④碳酸钠溶液、⑤石蕊试液,其中能用于鉴别的是( )
A、①④⑤ B、①②⑤ C、①②③ D、③④⑤
7、只用一种试剂,一次将氯化镁、氯化钡、氢氧化钾三种溶液区别开来。则这种试剂的化学式是
8、实验室有失去标签的盐酸、碳酸钠、硫酸、氢氧化钾和硝酸钾
五种溶液。为把他们区别开来,所加试剂及先后顺序合理的一组是
A、氯化钡溶液、稀硝酸、石蕊试液
B、稀硝酸、石蕊试液、硝酸银溶液
C、石蕊试液、稀硝酸、硝酸银溶液
D、稀硝酸、酚酞试液、硝酸银溶液
9、用稀盐酸和锌粒的反应制取氢气时,常混有HCl、水蒸气等杂质,
为证明并除去杂质,制得纯净、干燥的氢气,根据下图回答:
(1)应选择的发生装置和净化装置是_____。
(2)连接选择的装置各管口的顺序是(填字母):
( )接( ),( )接( ),( )接( )。
(3)证明并除去混有的氯化氢的实验现象是__ _,
依据的化学方程式是__ _ _。
(4)证明混有并除去水蒸气的实验现象是__ _,
依据的化学方程式是________ _。
思考:丙和乙能否交换位置,浓硫酸是否可以不用?
常见离子的检验方法
离子 检验试剂 主要实验现象
H+
OH-
Cl-
SO42-
CO32-
NH4+
Cu2+
Fe3+
紫色石蕊试液
红色
无色酚酞试液
红色
AgNO3溶液及稀HNO3
白色沉淀(不溶于酸)
Ba(NO3)2溶液及HCl
白色沉淀(不溶于酸)
HCl溶液及Ca(OH)2溶液
气体生成并有浑浊现象
NaOH溶液(碱溶液)
湿润的红色石蕊试纸
加热产生使湿润的红色石蕊试纸变蓝的气体
NaOH溶液(碱溶液)
蓝色(絮状)沉淀
NaOH溶液(碱溶液)
红褐(絮状)色沉淀
