湖南省衡阳市八中11-12学年高二学业水平模拟考试(化学理)
文档属性
| 名称 | 湖南省衡阳市八中11-12学年高二学业水平模拟考试(化学理) |  | |
| 格式 | zip | ||
| 文件大小 | 181.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | |||
| 科目 | 化学 | ||
| 更新时间 | 2012-05-09 16:13:53 | ||
图片预览


文档简介
衡阳市八中高二学业水平模拟考试
化 学
命题人:王 超 审题人:贺熙德
时量:90分钟 满分:100分
可能用到的相对原子质量:H:1 C:12 N:14 O:16 S:32 Na:23 Fe:56 Cu:64 He:4 Cl:35.5
一、选择题(每小题只有一个选项符合题意,每小题2分,共25小题,共50分)
1.“绿色化学”要求从根本上减少乃至杜绝污染。下列对农作物收割后留下的秸杆的处理方
法中, 不符合“绿色化学”理念的是
A.就地焚烧 B.发酵后作为农家肥
C.加工成精饲料 D.制造沼气
2.下列物质分类的正确组合是
混合物 化合物 单质 盐
A 盐酸溶液 NaOH溶液 石墨 食盐
B 漂白粉 KNO3晶体 O3 纯碱(Na2CO3)
C 空气 澄清石灰水 铁 石灰石
D CuSO4·5H2O CaCl2 水银 CaO
3.有下列物质:①盐酸、②NaOH、③明矾、④FeCl3 ⑤肥皂。能在水处理中作混凝剂的是
A.①④⑤ B.③④⑤ C.③④ D.全部
4.下列物质中,有固定沸点的是
A.石油 B.汽油 C.聚乙烯 D.苯
5.下列说法正确的是
A.甲烷与空气混合物点燃会发生爆炸,在点燃甲烷前要检验气体的纯度
B.某物质完全燃烧后生成CO2和水,该物质一定含有碳、氢、氧三种元素
C.因为汽油中含有碳和氢气,所以燃烧后生成二氧化碳和水
D.CO和CO2都含有碳和氧两种元素,所以它们的化学性质相同
6.关于右图所示装置的说法中,不正确的是
A.锌片是该装置的负极,该电极反应为Zn—2e—=Zn2+
B.电子由锌片通过导线流向铜片21世纪教育网
C.该装置能将化学能转化为电能
D.铜片上发生氧化反应
7.5、某氯碱厂不慎有大量氯气逸出周围空间,此时,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子。最适宜采用的物质是
A.NaOH B.NaCl C .Na2CO3 D.NaBr
8. 合成氨工业上采用循环操作的主要是因为
A.加快反应速率 B.能提高NH3的平衡浓度 C.降低NH3的沸点 D.提高N2和H2的利用率
9.下列离子方程式的书写正确的是
A.铁和稀硫酸反应 2Fe + 6H+ == 2Fe3+ + 3H2↑
B.向硫酸钠溶液中滴加氯化钡溶液 Ba2+ + SO42― == BaSO4↓
C.氯水加入到溴化钾溶液中 Br―+ Cl2 == Br2 + Cl― 21世纪教育网
D.碳酸钙溶于稀盐酸 CO32― + 2H+ == H2O + CO2↑
10.除去SO2中的SO3,并得到纯净的SO2,最好使混合气体通过………
A、水 B、NaHSO3饱和溶液 C、NaHCO3饱和溶液 D、98.3%浓硫酸
11.下列各组离子的溶液中能大量共存的是
A、Ag+、Na+ 、Fe 2+ 、Cl - B、Ca2+、Na+ 、NO3-、Cl- 、
C、Mg2+、K+、0H- 、SO42- D、Ca2+、Na+ 、SO42-、Cl-
12.下列物质的制备,符合工业生产实际的是
A.将氯气通入澄清石灰水中制漂白粉
B.用离子交换膜法电解饱和食盐水制备烧碱、氢气和氯气21世纪教育网
C.将氢气和氯气混合后点燃,产物用水吸收制备盐酸
D.将SO2和O2的混合气加高压后,通过接触室,制备SO3
13. 下列物质中,属于酸性氧化物的是
A.NO2 B.N2O5 C.NO D.CO
14.现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ⑧单质溴和氯化钠的水溶液,分离以上各混合液的正确方法依次是
A . 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C . 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
15.用NA表示阿伏加德罗常数,下列叙述正确的是 [来源:21世纪教育网]
A.4.4gCO2 和N2O混合物所含原子数为0.3NA
B.一定温度下,6.72LCl2与11.2gFe粉反应转移电子数为0.3 NA
C.50mL18mol/L硫酸与足量的Cu粉反应产生10.08L气体
D.标准状况下,4g氦气中所含的原子数为0.5NA
16.下列变化,需要加入适当的氧化剂才能完成的是
A、CuO→Cu B、Cu(OH)2 →CuCl2
C、H2SO4 →CuSO4 D、SO2→ SO3
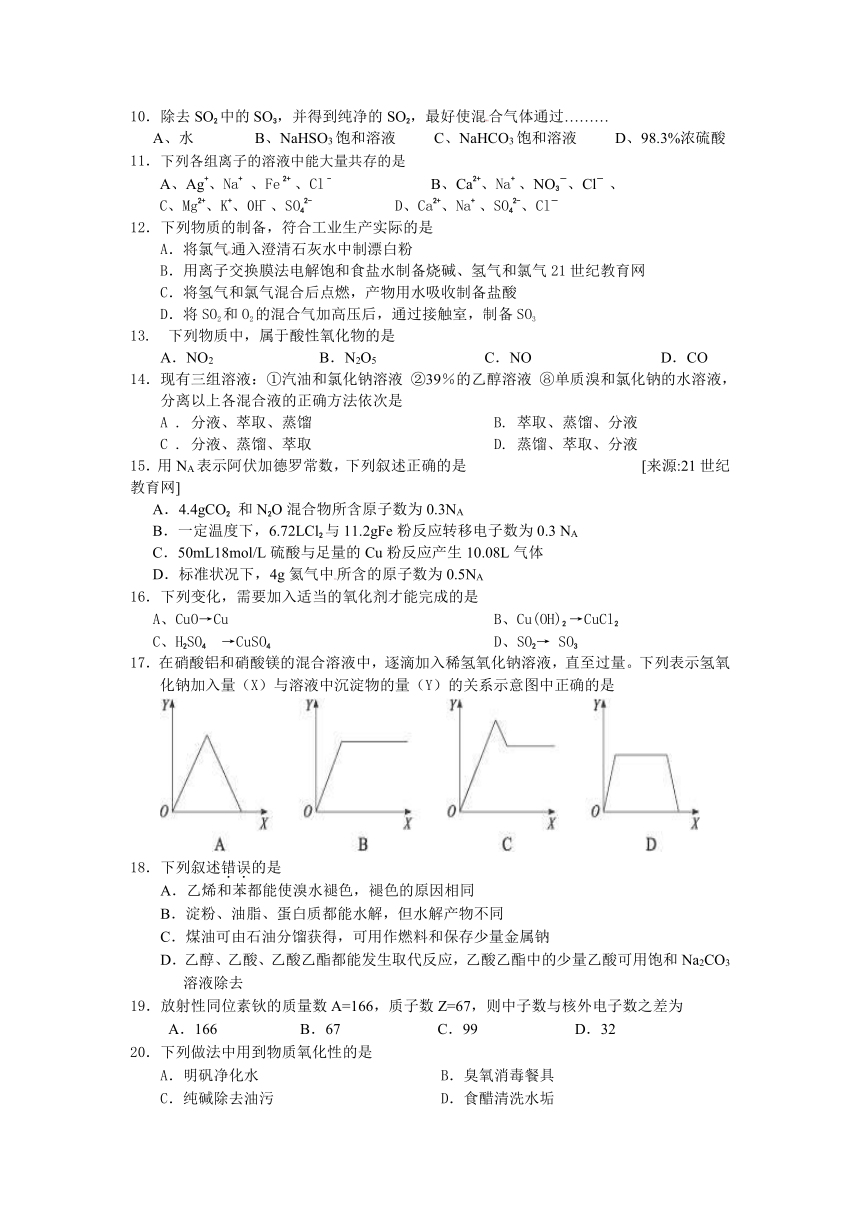
17.在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(X)与溶液中沉淀物的量(Y)的关系示意图中正确的是
18.下列叙述错误的是
A.乙烯和苯都能使溴水褪色,褪色的原因相同
B.淀粉、油脂、蛋白质都能水解,但水解产物不同
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
19.放射性同位素钬的质量数A=166,质子数Z=67,则中子数与核外电子数之差为
A.166 B.67 C.99 D.32
20.下列做法中用到物质氧化性的是
A.明矾净化水 B.臭氧消毒餐具
C.纯碱除去油污 D.食醋清洗水垢
21.将13.7g Na2CO3和NaHCO3的混合物充分加热,共收集到标准状况下的气体1.12L,则混合物中Na2CO3和NaHCO3的物质的量之比为
A.1︰1 B.1︰2 C.2︰1 D.3︰1
22.短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
甲 乙
丙21世纪教育网 丁 戊
A.原子半径: 丙<丁<戊 B.金属性:甲>丙
C.最外层电子数:甲>乙 D.氢氧化物碱性:丙>丁>戊
23.已知反应:X+Y=M+N为放热反应,对该反应的下列说法中正确的是
A.X的能量一定高于M
B. Y的能量一定高于N
C. X和Y的总能量一定高于M和N的总能量
D. 因为该反应为放热反应,故不必加热反应就可发生
24. 下列物质中,含有共价键的化合物是
A.Cl2 B.NaCl C.CaO D.HCl
25.向某溶液中滴加KSCN的溶液,无明显现象,再向其中滴加氯水,溶液变为血红色,则下列说法正确的是
A、原溶液中一定含有Fe3+离子 ,不含Fe2+ B、溶液中的Fe2+ 离子被氯气还原为Fe3+
C、原溶液中一定含有Fe2+ 离子 ,不含Fe3+ D、溶液中同时含Fe2+ 或Fe3+离子
二、填空题(每空2分,共34分)
26.(10分) 农村还有些家庭直接用河水或池塘水或井水龙头作为生活饮用水,一般是把水担回家倒入水缸,加明矾使水澄清,加漂白粉进行消毒,煮沸消除暂时硬度,明矾的化学式为 ,写出它溶于水后生成胶体的离子方程式: 。漂白粉的成分是 ,它在自然条件下能产生次氯酸,次氯酸的氧化性很强,能杀死病菌。写出漂白粉在空气中生成次氯酸的化学方程式: 。煮沸时形成水垢的成份
是 (填化学式)
27、(8分)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
C D21世纪教育网
A21世纪教育网 B E 21世纪教育网 F
(1)画出E的原子结构示意图 ;
(2)写出C的最高价氧化物的电子式 ;
(3)A最高价氧化物的水化物的化学式 。
(4)元素D和元素F的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式 。
28.(8分) ABCDE五种物质中含有同一种元素,其相互转化
关系如右图所示。C是空气污染物。
如果A是淡黄色固体单质:(以下均写化学式)
则C是 E是 。
写出:E→C的化学方程式
如果A是无色气体:
E→C的化学方程式为
29.(10分)以海水中常见物质A为原料可以发展很多种工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题:
(1)电解A溶液反应的离子方程式为 ;
(2)写出C与D制取消毒剂的化学方程式 ;
(3)若要使工业合成J反应的平衡向生成J的方向移动,可采取的措施有 [来源:21世纪教育网]
A.升高温度 B.增大压强 C.使用催化剂 D.液化分离J
(4)将F和J通入A的饱和溶液中的顺序为
A.先通入F后通入J B.先通入J后通入F
C.同时通入 D.没有先后顺序要求
(5)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数。
则计算样品中NaCl的质量分数的数学表达式为: 。
三、实验题(每空1分,共6分)
30.下列物质的转化或分离是用哪种方法实现的
A.溶解 B.裂解 C.分馏 D.裂化 E.干馏 F.蒸馏 G.电解 H.过滤 I.萃取 J.渗析 K.盐析
请将所选方法的字母代号填在横线上(每一项只填写一种最主要的方法,用字母填空)。
(1)把煤转化为焦炉气、煤焦油和焦炭等
(2)除去粗盐溶液中的泥沙
(3)从海水得到的无水MgCl2中提取金属镁
(4)从碘水中提取碘
(5)获得短链不饱和烃,如乙烯、丙烯、丁二烯等
(6)除去淀粉溶液中所含的食盐
四、计算题(8分)
31. 将饱和氯化钠溶液以惰性电极电解一段时间后停止电解,这时剩余的电解液体积为 200mL ,其溶液
PH为13,
(1)在标准状况下能收集到的气体体积为 L,
(2)此时转移的电子为 mol。
衡阳市八中高二学业水平模拟考试化学参考答案
一、选择题(每小题只有一个选项符合题意,每小题2分,共25小题,共50分)
1-5:ABCDA 6-10:DCDBD 11-15:BBBCA
16-20:DCADB 21-25:BDCDC
二、非选择题(50分)[来源:21世纪教育网]
26.(8分)KAl(SO4)2·12H2O Al3++3H2OAl(OH)3(胶体)+3H+
CaCl2、Ca(C1O)2 Ca(C1O)2+CO2+2H2O=CaCO3↓+2HClO
CaCO3、Mg(OH)2
27.(8分) (1) (2)
(3) NaOH (4) NH3+HCl = NH4Cl
28(8分) (1)SO2 H2SO4 Cu + 2H2SO4(浓)=== CuSO4 +SO2↑ +2H2O
(2) 3Cu + 8HNO3(稀)==3Cu(NO3)2+2NO ↑ +4H2O
29(10分)(1)2H2O+2Cl- Cl2↑+H2↑+2OH-
(2)Cl2 + NaOH==NaClO +NaCl +H2O
(3)B D (4)B (5)(1--)100%
30(8分)(1)E (2)H (3)G (4)I (5)B(6)J
31(8分)(1)0.448 (2)0.02
A
B
C
D
E
O2
O2
O2
H2O
Cu
H2
20090216
+16
2
8
6
加热
化 学
命题人:王 超 审题人:贺熙德
时量:90分钟 满分:100分
可能用到的相对原子质量:H:1 C:12 N:14 O:16 S:32 Na:23 Fe:56 Cu:64 He:4 Cl:35.5
一、选择题(每小题只有一个选项符合题意,每小题2分,共25小题,共50分)
1.“绿色化学”要求从根本上减少乃至杜绝污染。下列对农作物收割后留下的秸杆的处理方
法中, 不符合“绿色化学”理念的是
A.就地焚烧 B.发酵后作为农家肥
C.加工成精饲料 D.制造沼气
2.下列物质分类的正确组合是
混合物 化合物 单质 盐
A 盐酸溶液 NaOH溶液 石墨 食盐
B 漂白粉 KNO3晶体 O3 纯碱(Na2CO3)
C 空气 澄清石灰水 铁 石灰石
D CuSO4·5H2O CaCl2 水银 CaO
3.有下列物质:①盐酸、②NaOH、③明矾、④FeCl3 ⑤肥皂。能在水处理中作混凝剂的是
A.①④⑤ B.③④⑤ C.③④ D.全部
4.下列物质中,有固定沸点的是
A.石油 B.汽油 C.聚乙烯 D.苯
5.下列说法正确的是
A.甲烷与空气混合物点燃会发生爆炸,在点燃甲烷前要检验气体的纯度
B.某物质完全燃烧后生成CO2和水,该物质一定含有碳、氢、氧三种元素
C.因为汽油中含有碳和氢气,所以燃烧后生成二氧化碳和水
D.CO和CO2都含有碳和氧两种元素,所以它们的化学性质相同
6.关于右图所示装置的说法中,不正确的是
A.锌片是该装置的负极,该电极反应为Zn—2e—=Zn2+
B.电子由锌片通过导线流向铜片21世纪教育网
C.该装置能将化学能转化为电能
D.铜片上发生氧化反应
7.5、某氯碱厂不慎有大量氯气逸出周围空间,此时,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子。最适宜采用的物质是
A.NaOH B.NaCl C .Na2CO3 D.NaBr
8. 合成氨工业上采用循环操作的主要是因为
A.加快反应速率 B.能提高NH3的平衡浓度 C.降低NH3的沸点 D.提高N2和H2的利用率
9.下列离子方程式的书写正确的是
A.铁和稀硫酸反应 2Fe + 6H+ == 2Fe3+ + 3H2↑
B.向硫酸钠溶液中滴加氯化钡溶液 Ba2+ + SO42― == BaSO4↓
C.氯水加入到溴化钾溶液中 Br―+ Cl2 == Br2 + Cl― 21世纪教育网
D.碳酸钙溶于稀盐酸 CO32― + 2H+ == H2O + CO2↑
10.除去SO2中的SO3,并得到纯净的SO2,最好使混合气体通过………
A、水 B、NaHSO3饱和溶液 C、NaHCO3饱和溶液 D、98.3%浓硫酸
11.下列各组离子的溶液中能大量共存的是
A、Ag+、Na+ 、Fe 2+ 、Cl - B、Ca2+、Na+ 、NO3-、Cl- 、
C、Mg2+、K+、0H- 、SO42- D、Ca2+、Na+ 、SO42-、Cl-
12.下列物质的制备,符合工业生产实际的是
A.将氯气通入澄清石灰水中制漂白粉
B.用离子交换膜法电解饱和食盐水制备烧碱、氢气和氯气21世纪教育网
C.将氢气和氯气混合后点燃,产物用水吸收制备盐酸
D.将SO2和O2的混合气加高压后,通过接触室,制备SO3
13. 下列物质中,属于酸性氧化物的是
A.NO2 B.N2O5 C.NO D.CO
14.现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ⑧单质溴和氯化钠的水溶液,分离以上各混合液的正确方法依次是
A . 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C . 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
15.用NA表示阿伏加德罗常数,下列叙述正确的是 [来源:21世纪教育网]
A.4.4gCO2 和N2O混合物所含原子数为0.3NA
B.一定温度下,6.72LCl2与11.2gFe粉反应转移电子数为0.3 NA
C.50mL18mol/L硫酸与足量的Cu粉反应产生10.08L气体
D.标准状况下,4g氦气中所含的原子数为0.5NA
16.下列变化,需要加入适当的氧化剂才能完成的是
A、CuO→Cu B、Cu(OH)2 →CuCl2
C、H2SO4 →CuSO4 D、SO2→ SO3
17.在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(X)与溶液中沉淀物的量(Y)的关系示意图中正确的是
18.下列叙述错误的是
A.乙烯和苯都能使溴水褪色,褪色的原因相同
B.淀粉、油脂、蛋白质都能水解,但水解产物不同
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
19.放射性同位素钬的质量数A=166,质子数Z=67,则中子数与核外电子数之差为
A.166 B.67 C.99 D.32
20.下列做法中用到物质氧化性的是
A.明矾净化水 B.臭氧消毒餐具
C.纯碱除去油污 D.食醋清洗水垢
21.将13.7g Na2CO3和NaHCO3的混合物充分加热,共收集到标准状况下的气体1.12L,则混合物中Na2CO3和NaHCO3的物质的量之比为
A.1︰1 B.1︰2 C.2︰1 D.3︰1
22.短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
甲 乙
丙21世纪教育网 丁 戊
A.原子半径: 丙<丁<戊 B.金属性:甲>丙
C.最外层电子数:甲>乙 D.氢氧化物碱性:丙>丁>戊
23.已知反应:X+Y=M+N为放热反应,对该反应的下列说法中正确的是
A.X的能量一定高于M
B. Y的能量一定高于N
C. X和Y的总能量一定高于M和N的总能量
D. 因为该反应为放热反应,故不必加热反应就可发生
24. 下列物质中,含有共价键的化合物是
A.Cl2 B.NaCl C.CaO D.HCl
25.向某溶液中滴加KSCN的溶液,无明显现象,再向其中滴加氯水,溶液变为血红色,则下列说法正确的是
A、原溶液中一定含有Fe3+离子 ,不含Fe2+ B、溶液中的Fe2+ 离子被氯气还原为Fe3+
C、原溶液中一定含有Fe2+ 离子 ,不含Fe3+ D、溶液中同时含Fe2+ 或Fe3+离子
二、填空题(每空2分,共34分)
26.(10分) 农村还有些家庭直接用河水或池塘水或井水龙头作为生活饮用水,一般是把水担回家倒入水缸,加明矾使水澄清,加漂白粉进行消毒,煮沸消除暂时硬度,明矾的化学式为 ,写出它溶于水后生成胶体的离子方程式: 。漂白粉的成分是 ,它在自然条件下能产生次氯酸,次氯酸的氧化性很强,能杀死病菌。写出漂白粉在空气中生成次氯酸的化学方程式: 。煮沸时形成水垢的成份
是 (填化学式)
27、(8分)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
C D21世纪教育网
A21世纪教育网 B E 21世纪教育网 F
(1)画出E的原子结构示意图 ;
(2)写出C的最高价氧化物的电子式 ;
(3)A最高价氧化物的水化物的化学式 。
(4)元素D和元素F的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式 。
28.(8分) ABCDE五种物质中含有同一种元素,其相互转化
关系如右图所示。C是空气污染物。
如果A是淡黄色固体单质:(以下均写化学式)
则C是 E是 。
写出:E→C的化学方程式
如果A是无色气体:
E→C的化学方程式为
29.(10分)以海水中常见物质A为原料可以发展很多种工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题:
(1)电解A溶液反应的离子方程式为 ;
(2)写出C与D制取消毒剂的化学方程式 ;
(3)若要使工业合成J反应的平衡向生成J的方向移动,可采取的措施有 [来源:21世纪教育网]
A.升高温度 B.增大压强 C.使用催化剂 D.液化分离J
(4)将F和J通入A的饱和溶液中的顺序为
A.先通入F后通入J B.先通入J后通入F
C.同时通入 D.没有先后顺序要求
(5)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数。
则计算样品中NaCl的质量分数的数学表达式为: 。
三、实验题(每空1分,共6分)
30.下列物质的转化或分离是用哪种方法实现的
A.溶解 B.裂解 C.分馏 D.裂化 E.干馏 F.蒸馏 G.电解 H.过滤 I.萃取 J.渗析 K.盐析
请将所选方法的字母代号填在横线上(每一项只填写一种最主要的方法,用字母填空)。
(1)把煤转化为焦炉气、煤焦油和焦炭等
(2)除去粗盐溶液中的泥沙
(3)从海水得到的无水MgCl2中提取金属镁
(4)从碘水中提取碘
(5)获得短链不饱和烃,如乙烯、丙烯、丁二烯等
(6)除去淀粉溶液中所含的食盐
四、计算题(8分)
31. 将饱和氯化钠溶液以惰性电极电解一段时间后停止电解,这时剩余的电解液体积为 200mL ,其溶液
PH为13,
(1)在标准状况下能收集到的气体体积为 L,
(2)此时转移的电子为 mol。
衡阳市八中高二学业水平模拟考试化学参考答案
一、选择题(每小题只有一个选项符合题意,每小题2分,共25小题,共50分)
1-5:ABCDA 6-10:DCDBD 11-15:BBBCA
16-20:DCADB 21-25:BDCDC
二、非选择题(50分)[来源:21世纪教育网]
26.(8分)KAl(SO4)2·12H2O Al3++3H2OAl(OH)3(胶体)+3H+
CaCl2、Ca(C1O)2 Ca(C1O)2+CO2+2H2O=CaCO3↓+2HClO
CaCO3、Mg(OH)2
27.(8分) (1) (2)
(3) NaOH (4) NH3+HCl = NH4Cl
28(8分) (1)SO2 H2SO4 Cu + 2H2SO4(浓)=== CuSO4 +SO2↑ +2H2O
(2) 3Cu + 8HNO3(稀)==3Cu(NO3)2+2NO ↑ +4H2O
29(10分)(1)2H2O+2Cl- Cl2↑+H2↑+2OH-
(2)Cl2 + NaOH==NaClO +NaCl +H2O
(3)B D (4)B (5)(1--)100%
30(8分)(1)E (2)H (3)G (4)I (5)B(6)J
31(8分)(1)0.448 (2)0.02
A
B
C
D
E
O2
O2
O2
H2O
Cu
H2
20090216
+16
2
8
6
加热
同课章节目录
