第二节 来自石油和煤的两种基本化工原料
文档属性
| 名称 | 第二节 来自石油和煤的两种基本化工原料 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-05-15 00:00:00 | ||
图片预览











文档简介
(共45张PPT)
好好学习,天天向上!
七中实验校 王泽全
第三章 有机化合物
*
回忆:什么是 饱和烃(烷烃)
以及 烷烃的通式
烃分子中的碳原子之间只以 结合,剩余价键均与 原子结合,使每个碳原子的化合价都已达到“饱和”。这样的烃叫做饱和烃,也称为烷烃。
烷烃通式: 。
CnH2n+2 (n≥1整数)
单键
氢
*
煤和石油不仅是重要的燃料,还是重要的化工原料。
从石油中获得的乙烯、从石油和煤焦油中获得的苯,是两种重要的基本化工原料。
(1)通过收集生活中的乙烯材料,感受乙烯在生活中的广泛存在,感受乙烯在化学工业上应用价值。
(2)通过科学探究的方案进行实验,观察现象,分析结论,得出烯烃的概念。
(3)认识乙烯的分子结构模型,尝试书写乙烯的电子式、结构式、结构简式。
(4)知道乙烯能被KMnO4溶液氧化;乙烯的燃烧反应,会书写乙烯燃烧化学方程式;通过乙烯与溴的四氯化碳溶液反应,会书写加成反应的化学方程式;了解乙烯的加聚反应
第三章 有机化合物
第二节 来自石油和煤的两种基本化工原料
---乙烯
课时目标
重难点:乙烯的结构和性质
乙烯的用途:
塑料袋,薄膜等高分子材料
乳化剂,洗涤剂,防冻剂
燃料,塑料,增塑剂
植物生长调节剂,催熟剂
高分子材料
杀虫剂
无纺布 醋酸纤维 管材
乙烯被称为“石化工业之母”,乙烯的产量可以用来衡量一个国家的石油化工发展水平。2007年我国的乙烯产量超过1000万吨,稳居世界第二位 。
小资料
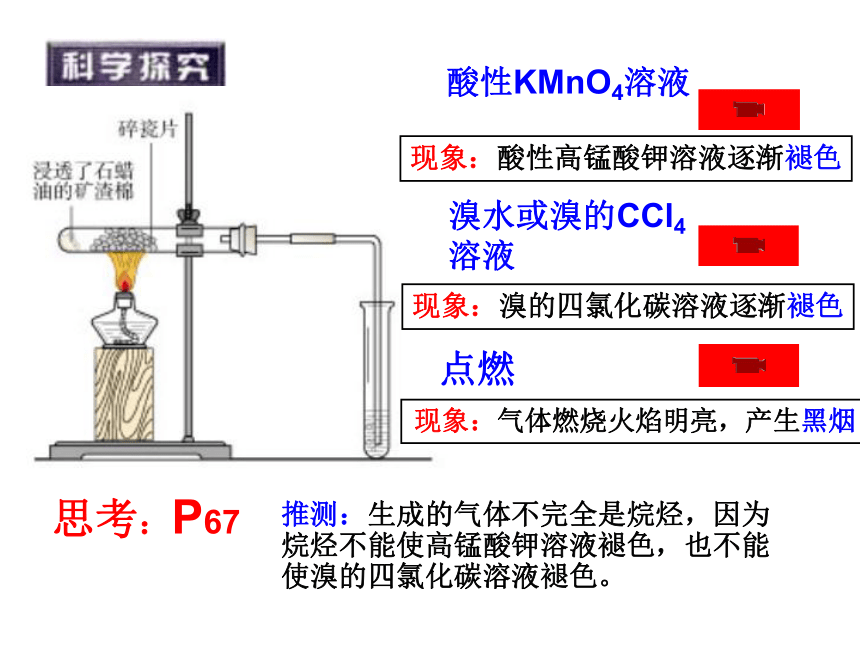
酸性KMnO4溶液
溴水或溴的CCl4溶液
点燃
现象:酸性高锰酸钾溶液逐渐褪色
现象:溴的四氯化碳溶液逐渐褪色
现象:气体燃烧火焰明亮,产生黑烟
思考:P67
推测:生成的气体不完全是烷烃,因为烷烃不能使高锰酸钾溶液褪色,也不能使溴的四氯化碳溶液褪色。
结论: 石蜡油分解的产物中有烯烃
定义:含有碳碳双键的烃
什么叫烯烃?
C
C
*
分子式 电子式 结构式 结构简式
一、乙烯的组成和结构:
C2H4
C=C
H
H
H
H
CH2 = CH2
平面型,键角120
C
:
C
:
:
:
H
H
H
H
:
:
空间构型:
*
乙烯是 色 气味的气体
溶于水;密度较空气 .
无
稍有
难
略小
二、乙烯的物理性质:
收集方法 : .
排水法
三、乙烯的化学性质:
1、氧化反应:
C2H4+3O2 → 2CO2+2H2O
点燃
(1)燃烧:
C
C
的性质!?
(2)被酸性高锰酸钾氧化
酸性高锰酸钾溶液褪色。
现象:
三、乙烯的化学性质:
用于鉴别乙烯和烷烃
用于鉴别乙烯和烷烃,但不用于除杂,如:除去甲烷中的乙烯,不能用高锰酸钾,因为乙烯被氧化成了CO2,会引入新杂质.
2 、加成反应
1,2-二溴乙烷
三、乙烯的化学性质:
C
H
H
C
H
H
Br Br
+
C
H
H
C
H
H
Br
Br
用于鉴别和除杂乙烯和烷烃
与高锰酸钾褪色原理一样吗?
有机物分子中的不饱和键(双键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应。
练一练:请写出乙烯与H2、HCl、Cl2、H2O 发生的加成反应的化学方程式。
2 、加成反应
三、乙烯的化学性质:
1,2-二溴乙烷
(无色液体)
CH2=CH2 + Br2
CH2BrCH2Br
乙烯与氢气加成
C
H
H
C
H
H
H
H
+
C
H
H
C
H
H
H
H
乙烷
催化剂
乙烯与氯化氢加成
C
H
H
C
H
H
H
Cl
+
C
H
H
C
H
H
H
Cl
一氯乙烷
催化剂
乙烯与氯气加成
C
H
H
C
H
H
Cl
Cl
+
C
H
H
C
H
H
Cl
Cl
催化剂
1,2-二氯乙烷
乙烯与水加成
C
H
H
C
H
H
H
OH
+
C
H
H
C
H
H
H
OH
乙醇
催化剂
乙烯分子之间相互加成可以聚合得到聚乙烯
n CH2=CH2
催化剂
四、用途: P68 最后一段 自学
分子式 CH4 (烷烃) C2H4 (烯烃)
通式
结构
燃烧
通入酸性KMnO4溶液
通入Br2水或Br2的CCl4溶液
含有C=C
烷烃只含碳碳单键
火焰明亮并伴有黑烟,生成CO2和H2O
淡蓝色火焰
生成CO2和H2O
不反应,无现象
不反应,无现象
褪色,发生加成反应
褪色,发生氧化反应
小结:
CnH2n
(n≥2整数)
CnH2n+2
(n≥1整数)
练1:
能用于鉴别甲烷和乙烯的试剂是 ( )
A. 溴水 B.酸性高锰酸钾溶液
C. NaOH溶液 D.四氯化碳溶液
AB
下列物质不可能是乙烯加成产物的是( )
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
制取一氯乙烷的最好方法是( )
A. 乙烷和氯气反应
B. 乙烯和氯气反应
C. 乙烯和氯化氢反应
D. 乙烯和氢气反应
B
C
练2:
练3:
Wan?
完≠玩
*
第三章 有机化合物
复 习
烷烃(甲烷) 烯烃(乙烯)
分子式
状态
碳碳键型
空间结构
取代反应
加成反应
燃烧反应
使溴水褪色
使KMnO4(H+)褪色
介绍另一种重要的化工原料 ----- 苯
(1)通过收集生活中苯的材料,感受苯在生活中的广泛存在,感受苯在化学工业上的应用价值。
(2)通过观察能描述苯的物理性质;
(3)比较苯的分子结构与烷烃、烯烃的结构的区别,能推测苯的化学性质;能够设计实验方案加以验证,从而得出结论。
(4)通过苯的燃烧反应,描述现象,书写化学方程式;通过苯与溴水的反应,知道苯可以发生取代反应,书写苯的溴化、硝化反应方程式;
(5)知道苯可以发生加成反应,书写苯与氢气的加成反应方程式。
第三章 有机化合物
第二节 来自石油和煤的两种基本化工原料
---苯
课时目标
重难点:苯的结构和性质
性质 颜色 气味 密度 熔沸点 毒性
苯
水
无色
特殊气味
比水小不溶于水
无色
无
熔点5.5℃沸点80.1 ℃
有毒
一、苯的物理性质:
苯的发现
苯是1825年由英国科学家法拉第(M. Faraday)首先发现的。
分子式:
1.根据分子式C6H6,它属于饱和烃还是不饱和
烃?
讨论:
2.根据饱和链烃的通式,苯分子中可能含有的
双键数目?
3.写出C6H6分子的可能链状结构简式。
(不饱和烃)
(4个)
二、苯的组成和结构:
C6H6
CH2=C=CH—CH=C=CH2
CH2 =C=C = C=CH—CH3
CH2 =C=C = CH—CH=CH2 等等 性质??
P69 学与问 实验3-1
1、向试管中加入少量苯,再加入溴水,震荡后,观察现象
2、向试管中加入少量苯,再加入酸性高锰酸钾溶液,震荡后,观察现象
现象1:不褪色,溶液分层,上层为橙红色(萃取)
现象2:不褪色,溶液分层。下层为紫红色
说明苯分子中不存在碳碳双键,是一种介于单键与双键之间的一种特殊键。
结论:
疑问:苯到底是怎样的结构呢?
凯库勒假设的苯分子的结构:1.苯分子中的6个碳原子形成平面六边形;2.苯环中的碳碳单键、双键交替排列。
现代科学方法测得的苯分子结构:
空间构型:平面正六边形
(凯库勒式)
C
C
C
C
C
C
H
H
H
H
H
H
x
x
x
x
和 是同种物质
2.结构式和结构简式:
1.分子式:C6H6
⑵碳碳键介于单键和双键之间的独特的键。(既不是碳碳单键也不是碳碳双键)
⑴平面正六边形;
⒊空间构型:
二、苯的组成和结构:
或
比例模型
1、氧化反应 (可燃性)
2C6H6+15O2
点燃
实验现象:火焰明亮并带有浓烟
三、苯的化学性质:
2、苯的取代反应
(1)溴代反应
溴苯(密度比水大的无色液体)
反应条件:液溴,催化剂 FeBr3
(2)硝化反应
硝酸分子中里的—NO2原子团叫做硝基,苯分子中的氢原子被—NO2所取代的反应,叫做硝化反应。
硝基苯
2、苯的取代反应
3、苯的加成反应 (难度大)
苯虽然不具有像烯烃一样经典的碳碳双键,但在特定的条件下,仍能发生加成反应。
在镍作催化剂的条件下,苯可以与氢气发生加成反应。
环己烷
镍
烷烃(甲烷) 烯烃(乙烯) 苯
分子式
状态
碳碳键型
空间结构
取代反应
加成反应
燃烧反应
使溴水褪色
使KMnO4(H+)褪色
复 习
能说明苯分子苯环的平面正六边形结构中,碳碳链不是单双键交替排布的事实是( )
A.苯的一元取代物没有同分异构体
B.苯的间位二元取代物只有一种
C.苯的邻位二元取代物只有一种
D.苯的对位二元取代物只有一种
练1
C
C11H15N
练2
有机物分子结构,可以用键线式表示,例如CH3CH=CHCH3可表示为: 人抽烟时,吸入肺部的众多有害物质中,除CO外还有一种称为尼古丁的有毒物质,它的结构简式用键线式表示为:
试写出尼古丁的分子式 。
N
练3
已知二氯苯的同分异构体有三种,从而可知四氯苯的同分异构体数目有 ( )
A、2 B、3 C、4 D、5
A
A
B
B
B
B
A是氯,B是氢......?种
A是氢,B是氯......?种
仍为3种
B
.3种
这种芳香烃的 2 氯取代物与______氯取代物一样多
6
洗涤剂,溶剂、消毒剂,增塑剂
染料,纺织材料,塑料
三.芳香烃
含有苯环的烃。
CH3
-CH3
-CH3
CH3
-CH3
CH3
CH3
甲苯
邻二甲苯
间二甲苯
对二甲苯
烃:仅由碳和氢两种元素组成的有机物。
㈠烃的分类
链烃
环烃
烷烃
CnH2n+2(n≥1)
CnH2n (n≥2)
CnH2n-2(n≥2)
烃
饱和链烃
不饱和链烃
芳香烃
烯烃
炔烃
知识总结
环烷烃
CnH2n (n≥3)
(含C≡C)
CnH2n-6(n≥6)
练4
CH3
H3C
CH3
CH3
如图的有机化合物中,共线的碳原子至少 个?
共面的碳原子至少 个?最多 个?
6
11
16
Wan?
完≠玩
归纳整理
补充:烯烃,苯及其同系物中 共面共线问题
理解空间构型
好好学习,天天向上!
七中实验校 王泽全
第三章 有机化合物
*
回忆:什么是 饱和烃(烷烃)
以及 烷烃的通式
烃分子中的碳原子之间只以 结合,剩余价键均与 原子结合,使每个碳原子的化合价都已达到“饱和”。这样的烃叫做饱和烃,也称为烷烃。
烷烃通式: 。
CnH2n+2 (n≥1整数)
单键
氢
*
煤和石油不仅是重要的燃料,还是重要的化工原料。
从石油中获得的乙烯、从石油和煤焦油中获得的苯,是两种重要的基本化工原料。
(1)通过收集生活中的乙烯材料,感受乙烯在生活中的广泛存在,感受乙烯在化学工业上应用价值。
(2)通过科学探究的方案进行实验,观察现象,分析结论,得出烯烃的概念。
(3)认识乙烯的分子结构模型,尝试书写乙烯的电子式、结构式、结构简式。
(4)知道乙烯能被KMnO4溶液氧化;乙烯的燃烧反应,会书写乙烯燃烧化学方程式;通过乙烯与溴的四氯化碳溶液反应,会书写加成反应的化学方程式;了解乙烯的加聚反应
第三章 有机化合物
第二节 来自石油和煤的两种基本化工原料
---乙烯
课时目标
重难点:乙烯的结构和性质
乙烯的用途:
塑料袋,薄膜等高分子材料
乳化剂,洗涤剂,防冻剂
燃料,塑料,增塑剂
植物生长调节剂,催熟剂
高分子材料
杀虫剂
无纺布 醋酸纤维 管材
乙烯被称为“石化工业之母”,乙烯的产量可以用来衡量一个国家的石油化工发展水平。2007年我国的乙烯产量超过1000万吨,稳居世界第二位 。
小资料
酸性KMnO4溶液
溴水或溴的CCl4溶液
点燃
现象:酸性高锰酸钾溶液逐渐褪色
现象:溴的四氯化碳溶液逐渐褪色
现象:气体燃烧火焰明亮,产生黑烟
思考:P67
推测:生成的气体不完全是烷烃,因为烷烃不能使高锰酸钾溶液褪色,也不能使溴的四氯化碳溶液褪色。
结论: 石蜡油分解的产物中有烯烃
定义:含有碳碳双键的烃
什么叫烯烃?
C
C
*
分子式 电子式 结构式 结构简式
一、乙烯的组成和结构:
C2H4
C=C
H
H
H
H
CH2 = CH2
平面型,键角120
C
:
C
:
:
:
H
H
H
H
:
:
空间构型:
*
乙烯是 色 气味的气体
溶于水;密度较空气 .
无
稍有
难
略小
二、乙烯的物理性质:
收集方法 : .
排水法
三、乙烯的化学性质:
1、氧化反应:
C2H4+3O2 → 2CO2+2H2O
点燃
(1)燃烧:
C
C
的性质!?
(2)被酸性高锰酸钾氧化
酸性高锰酸钾溶液褪色。
现象:
三、乙烯的化学性质:
用于鉴别乙烯和烷烃
用于鉴别乙烯和烷烃,但不用于除杂,如:除去甲烷中的乙烯,不能用高锰酸钾,因为乙烯被氧化成了CO2,会引入新杂质.
2 、加成反应
1,2-二溴乙烷
三、乙烯的化学性质:
C
H
H
C
H
H
Br Br
+
C
H
H
C
H
H
Br
Br
用于鉴别和除杂乙烯和烷烃
与高锰酸钾褪色原理一样吗?
有机物分子中的不饱和键(双键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应。
练一练:请写出乙烯与H2、HCl、Cl2、H2O 发生的加成反应的化学方程式。
2 、加成反应
三、乙烯的化学性质:
1,2-二溴乙烷
(无色液体)
CH2=CH2 + Br2
CH2BrCH2Br
乙烯与氢气加成
C
H
H
C
H
H
H
H
+
C
H
H
C
H
H
H
H
乙烷
催化剂
乙烯与氯化氢加成
C
H
H
C
H
H
H
Cl
+
C
H
H
C
H
H
H
Cl
一氯乙烷
催化剂
乙烯与氯气加成
C
H
H
C
H
H
Cl
Cl
+
C
H
H
C
H
H
Cl
Cl
催化剂
1,2-二氯乙烷
乙烯与水加成
C
H
H
C
H
H
H
OH
+
C
H
H
C
H
H
H
OH
乙醇
催化剂
乙烯分子之间相互加成可以聚合得到聚乙烯
n CH2=CH2
催化剂
四、用途: P68 最后一段 自学
分子式 CH4 (烷烃) C2H4 (烯烃)
通式
结构
燃烧
通入酸性KMnO4溶液
通入Br2水或Br2的CCl4溶液
含有C=C
烷烃只含碳碳单键
火焰明亮并伴有黑烟,生成CO2和H2O
淡蓝色火焰
生成CO2和H2O
不反应,无现象
不反应,无现象
褪色,发生加成反应
褪色,发生氧化反应
小结:
CnH2n
(n≥2整数)
CnH2n+2
(n≥1整数)
练1:
能用于鉴别甲烷和乙烯的试剂是 ( )
A. 溴水 B.酸性高锰酸钾溶液
C. NaOH溶液 D.四氯化碳溶液
AB
下列物质不可能是乙烯加成产物的是( )
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
制取一氯乙烷的最好方法是( )
A. 乙烷和氯气反应
B. 乙烯和氯气反应
C. 乙烯和氯化氢反应
D. 乙烯和氢气反应
B
C
练2:
练3:
Wan?
完≠玩
*
第三章 有机化合物
复 习
烷烃(甲烷) 烯烃(乙烯)
分子式
状态
碳碳键型
空间结构
取代反应
加成反应
燃烧反应
使溴水褪色
使KMnO4(H+)褪色
介绍另一种重要的化工原料 ----- 苯
(1)通过收集生活中苯的材料,感受苯在生活中的广泛存在,感受苯在化学工业上的应用价值。
(2)通过观察能描述苯的物理性质;
(3)比较苯的分子结构与烷烃、烯烃的结构的区别,能推测苯的化学性质;能够设计实验方案加以验证,从而得出结论。
(4)通过苯的燃烧反应,描述现象,书写化学方程式;通过苯与溴水的反应,知道苯可以发生取代反应,书写苯的溴化、硝化反应方程式;
(5)知道苯可以发生加成反应,书写苯与氢气的加成反应方程式。
第三章 有机化合物
第二节 来自石油和煤的两种基本化工原料
---苯
课时目标
重难点:苯的结构和性质
性质 颜色 气味 密度 熔沸点 毒性
苯
水
无色
特殊气味
比水小不溶于水
无色
无
熔点5.5℃沸点80.1 ℃
有毒
一、苯的物理性质:
苯的发现
苯是1825年由英国科学家法拉第(M. Faraday)首先发现的。
分子式:
1.根据分子式C6H6,它属于饱和烃还是不饱和
烃?
讨论:
2.根据饱和链烃的通式,苯分子中可能含有的
双键数目?
3.写出C6H6分子的可能链状结构简式。
(不饱和烃)
(4个)
二、苯的组成和结构:
C6H6
CH2=C=CH—CH=C=CH2
CH2 =C=C = C=CH—CH3
CH2 =C=C = CH—CH=CH2 等等 性质??
P69 学与问 实验3-1
1、向试管中加入少量苯,再加入溴水,震荡后,观察现象
2、向试管中加入少量苯,再加入酸性高锰酸钾溶液,震荡后,观察现象
现象1:不褪色,溶液分层,上层为橙红色(萃取)
现象2:不褪色,溶液分层。下层为紫红色
说明苯分子中不存在碳碳双键,是一种介于单键与双键之间的一种特殊键。
结论:
疑问:苯到底是怎样的结构呢?
凯库勒假设的苯分子的结构:1.苯分子中的6个碳原子形成平面六边形;2.苯环中的碳碳单键、双键交替排列。
现代科学方法测得的苯分子结构:
空间构型:平面正六边形
(凯库勒式)
C
C
C
C
C
C
H
H
H
H
H
H
x
x
x
x
和 是同种物质
2.结构式和结构简式:
1.分子式:C6H6
⑵碳碳键介于单键和双键之间的独特的键。(既不是碳碳单键也不是碳碳双键)
⑴平面正六边形;
⒊空间构型:
二、苯的组成和结构:
或
比例模型
1、氧化反应 (可燃性)
2C6H6+15O2
点燃
实验现象:火焰明亮并带有浓烟
三、苯的化学性质:
2、苯的取代反应
(1)溴代反应
溴苯(密度比水大的无色液体)
反应条件:液溴,催化剂 FeBr3
(2)硝化反应
硝酸分子中里的—NO2原子团叫做硝基,苯分子中的氢原子被—NO2所取代的反应,叫做硝化反应。
硝基苯
2、苯的取代反应
3、苯的加成反应 (难度大)
苯虽然不具有像烯烃一样经典的碳碳双键,但在特定的条件下,仍能发生加成反应。
在镍作催化剂的条件下,苯可以与氢气发生加成反应。
环己烷
镍
烷烃(甲烷) 烯烃(乙烯) 苯
分子式
状态
碳碳键型
空间结构
取代反应
加成反应
燃烧反应
使溴水褪色
使KMnO4(H+)褪色
复 习
能说明苯分子苯环的平面正六边形结构中,碳碳链不是单双键交替排布的事实是( )
A.苯的一元取代物没有同分异构体
B.苯的间位二元取代物只有一种
C.苯的邻位二元取代物只有一种
D.苯的对位二元取代物只有一种
练1
C
C11H15N
练2
有机物分子结构,可以用键线式表示,例如CH3CH=CHCH3可表示为: 人抽烟时,吸入肺部的众多有害物质中,除CO外还有一种称为尼古丁的有毒物质,它的结构简式用键线式表示为:
试写出尼古丁的分子式 。
N
练3
已知二氯苯的同分异构体有三种,从而可知四氯苯的同分异构体数目有 ( )
A、2 B、3 C、4 D、5
A
A
B
B
B
B
A是氯,B是氢......?种
A是氢,B是氯......?种
仍为3种
B
.3种
这种芳香烃的 2 氯取代物与______氯取代物一样多
6
洗涤剂,溶剂、消毒剂,增塑剂
染料,纺织材料,塑料
三.芳香烃
含有苯环的烃。
CH3
-CH3
-CH3
CH3
-CH3
CH3
CH3
甲苯
邻二甲苯
间二甲苯
对二甲苯
烃:仅由碳和氢两种元素组成的有机物。
㈠烃的分类
链烃
环烃
烷烃
CnH2n+2(n≥1)
CnH2n (n≥2)
CnH2n-2(n≥2)
烃
饱和链烃
不饱和链烃
芳香烃
烯烃
炔烃
知识总结
环烷烃
CnH2n (n≥3)
(含C≡C)
CnH2n-6(n≥6)
练4
CH3
H3C
CH3
CH3
如图的有机化合物中,共线的碳原子至少 个?
共面的碳原子至少 个?最多 个?
6
11
16
Wan?
完≠玩
归纳整理
补充:烯烃,苯及其同系物中 共面共线问题
理解空间构型
