河南省名校联盟2020-2021学年高一下学期期末考试化学试题 Word版含解析
文档属性
| 名称 | 河南省名校联盟2020-2021学年高一下学期期末考试化学试题 Word版含解析 |

|
|
| 格式 | docx | ||
| 文件大小 | 580.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-19 00:00:00 | ||
图片预览




文档简介
河南名校联盟
2020—2021学年高一(下)期末考试
化学
考生注意:
1.本试卷共8页。时间90分钟,满分100分。答题前,考生先将自己的姓名、考生号填写在试卷指定位置,并将姓名、考场号、座位号、考生号填写在答题卡上,然后认真核对条形码上的信息,并将条形码粘贴在答题卡上的指定位置。
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。作答非选择题时,将答案写在答题卡上对应的答题区域内。写在本试卷上无效。
3.考试结束后,将试卷和答题卡一并收回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Mg 24 Al 27 K 39
一、选择题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一个选项符合题意。.
1.化学与人类生活密切相关,下列有关物质的用途不正确的是( )
A.用false制作光导纤维 B.用澄清石灰水制取漂白液
C.用葡萄糖制取银镜 D.用false萃取碘水中的碘
2.超级电容器是介于普通电容器与电池之间的储能装置。石墨烯/聚3,4-乙烯二氧噻吩(PEDOP)可用于制备超级电容器。下列有关说法正确的是( )
A.石墨烯/聚3,4-乙烯二氧噻吩是一种新型化合物
B.石墨与false互为同位素
C.聚3,4-乙烯二氧噻吩是人工合成高分子化合物
D.聚3,4-乙烯二氧噻吩是纯净物
3.false具有极强的辐射性,常用于辐射育种,癌症和肿瘤的放射治疗。下列有关false的说法不正确的是( )
A.与会false的化学性质不同 B.质子数比中子数少6
C.电子数为27 D.属于过渡元素
4.“十四五规划”国家提出了一个明确的目标,到2025年,新能源汽车新车销售量达到汽车新车销售总量的20%左右。新能源汽车指除燃料为汽油、柴油之外的所有使用其他能源(比如电能、太阳能)的汽车。下列关于能源的说法正确的是( )
A.汽油、柴油都是石油发生化学变化的产物
B.电动汽车内部的电池能量转化率可以达到百分之百
C.太阳能不能直接转化为电能
D.天然气属于气态化石燃料
5.下列说法不正确的是( )
A.甲烷的氯代反应与苯的溴代反应类型相同
B.乙烯能使酸性false溶液和溴水褪色,且褪色原理相同
C.等物质的量的乙醇,乙酸分别与足量Na反应产生false的量相同
D.淀粉和纤维素的最终水解产物相同
6.氯气通入碳酸氢钠溶液中发生反应false,下列有关化学用语正确的是( )
A.false的结构示意图: B.false的结构式:O—C—O
C.HClO的电子式:false D.false内部既含离子键又含共价键
7.我国从1966年开始进行海水提溴,主要采用的方法是空气吹出法,其从海水中提取溴的流程如下:
下列叙述不正确的是( )
A.过程①应使用蒸馏烧瓶
B.过程②可证明还原性false
C.过程④的化学方程式为false
D.萃取过程可选用酒精为萃取剂
8.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X同周期且二者可形成两种以上的二元化合物,Y的族序数与周期数相等,Z单质常温下呈气态。下列有关说法不正确的是( )
A.原子半径:Y>W>X
B.简单氢化物的稳定性:W>X
C.Y与Z形成的二元化合物为电解质
D.W、Z的最高价氧化物对应的水化物均为强酸
9.钾离子电池由于其低成本,电解液中快的离子传导性以及高的工作电压等优点,近年来引起了科研工作者极大的关注。false在两极间脱嵌实现电池的充放电过程。下图为钾离子二次电池充电时的工作原图,工作前两电极质量相等且均为false。下列有关说法正确的是( )
A.放电时,false向a极移动
B.充电时,转移0.1molfalse时,理论上两极质量差为7.8g
C.充电时,a电极发生的反应为false
D.充电时,b电极反应前后,碳元素的化合价不发生变化
10.常温下,将铁片置于稀硫酸中发生反应false,下列措施不能增大false生成速率的是( )
A.将铁片换成铁粉 B.加入少量false固体
C.将稀硫酸换成浓硫酸 D.适当升高温度
11.下列关于热化学方程式的说法正确的是( )
A.false false,则false的燃烧热为false
B.false false,则该反应为放热反应
C.已知false false,则false false
D.false false,则false false
12.设false为阿伏加德罗常数的值,下列叙述不正确的是( )
A.标准状况下,2.24Lfalse中含共用电子对数目为0.7false
B.false溶液中含false的数目为0.6false
C.7.2g正戊烷与新戊烷的混合物中含H原子的数目为1.2false
D.false与足量水反应,当水溶液增重10.8g时,转移的电子数为0.2false
13.下列实验操作能达到实验目的的是( )
选项
实验操作
实验目的
A
向饱和false溶液中通入false
证明非金属性:S>Si
B
向false溶液中加入过量氨水
制备false
C
将5g干燥的MgO粉末和2g铝粉均匀混合后放入纸漏斗中
用铝热法制备金属Mg
D
向混有少量水的乙醇中加入浓硫酸
除去乙醇中的水
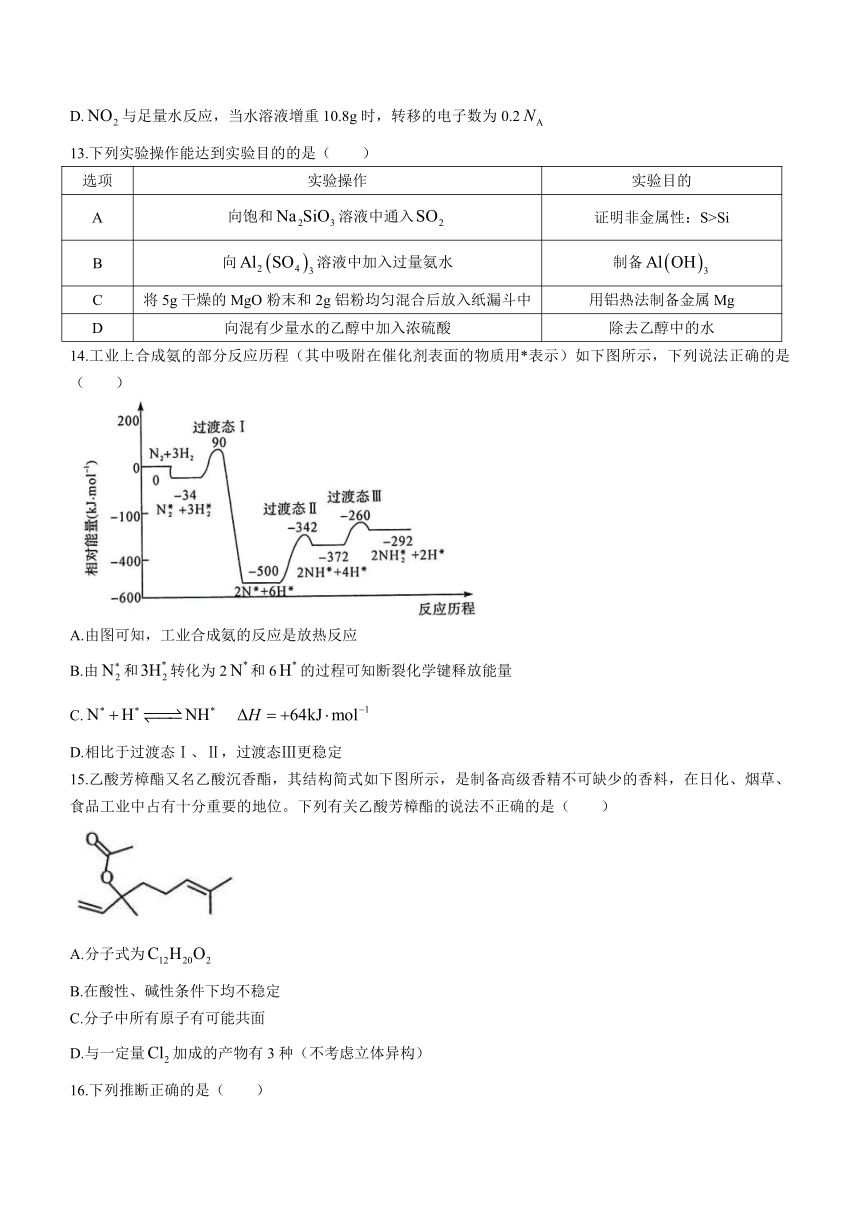
14.工业上合成氨的部分反应历程(其中吸附在催化剂表面的物质用*表示)如下图所示,下列说法正确的是( )
A.由图可知,工业合成氨的反应是放热反应
B.由false和false转化为2false和6false的过程可知断裂化学键释放能量
C.false false
D.相比于过渡态Ⅰ、Ⅱ,过渡态Ⅲ更稳定
15.乙酸芳樟酯又名乙酸沉香酯,其结构简式如下图所示,是制备高级香精不可缺少的香料,在日化、烟草、食品工业中占有十分重要的地位。下列有关乙酸芳樟酯的说法不正确的是( )
A.分子式为false
B.在酸性、碱性条件下均不稳定
C.分子中所有原子有可能共面
D.与一定量false加成的产物有3种(不考虑立体异构)
16.下列推断正确的是( )
A.由稳定性false,推断稳定性false
B.由同周期主族元素最高正价依次升高,推断最高正价F>O
C.由Na在false中燃烧生成false,推断Li在false中燃烧生成false
D.由同主族单质false、false、false、false熔沸点依次升高,推断Li、Na、K、Rb、Cs熔沸点依次升高
二、非选择题:本题共4小题,共52分。
17.(14分)物质M可用作调味剂、乳化剂、抗氧化增效剂、吸湿剂、pH调节剂、增香剂、缓冲剂。其结构式如下图所示,其组成元素X、Y、Z、Q为原子序数依次增大的短周期主族元素,且Y的一种核素常用于检测文物的年代。
请回答下列问题:
(1)元素Q在周期表中的位置为 ,工业上采用 法冶炼Q的单质。
(2)物质M中所含化学键的类型为 ,物质M与稀硫酸反应生成有机物N,N中所含官能团的名称为 。
(3)相同条件下,等质量的Y的两种单质false、false分别在足量false中燃烧,放出热量前者大于后者.则两种单质中, (填“false”或“false”)更稳定。Y与Z分别形成的简单氢化物的沸点由高到低的顺序为 (填化学式)。
(4)QX的电子式为 ,与水反应的化学方程式为 。
18.(13分)原电池体现化学对社会发展的又一伟大贡献。请回答下列问题:
(1)将Cu电极、石墨电极用导线连接好后插入false溶液中,电子的流向为 (填“由Cu电极到石墨电极”或“由石墨电极到Cu电极”),石墨电极的电极反应式为 。
(2)一种可充电锂—空气电池如图所示。当电池放电时,false与false在多孔碳材料电极处生成false(false或1)。
①放电时,多孔碳材料电极为 (填“正”或“负”)极。
②放电时,外电路每转移0.1molfalse,锂电极的质量变化为 。
③放电时,电池正极的电极反应式为 。
(3)燃料电池大大提高了能量的转化效率。燃料电池工作时将燃料内部的 能转化为 能。碱性甲烷燃料电池工作时负极的电极反应式为 。
19.(11分)石油是宝贵的能源,属于战略资源。false、false均是石油裂解的产物。
请回答下列问题:
(1)石油裂化、裂解为 (填“物理”或“化学")变化。
(2)已知false false
false false
false false
false false
则反应false false false。
(3)一定温度下,在某2L恒容密闭容器中充入1molfalse和1molfalse发生反应false,10min后达到平衡,容器内压强为起始压强的1.25倍。
①下列说法可以判定反应到达平衡状态的是 。(填字母序号)
A.false
B.相同时间内,断裂2molfalse的同时断裂1molfalse
C.容器内气体的密度不再发生变化
D.容器内气体的平均相对分子质量不再发生变化
②0~10min,v(CO)= false,false的转化率为 %,false的体积分数为 %。
20.(14分)甲酸丁酯(false)可用作漆用溶剂和制造胶片时的溶剂,还可用于人造革、香料和有机合成等领域。某小组在实验室进行甲酸丁酯的制备。
【实验原料】甲酸(HCOOH)和正丁醇(false)
【实验装置】
【实验步骤】
向仪器M中加入98%的甲酸47g,正丁醇37g,适量浓硫酸,几粒沸石,加热回流反应24h。冷却后用饱和NaCl溶液洗涤,再依次用饱和false溶液、饱和NaCl溶液洗涤。再经无水false干燥,分馏,收集106~107℃的馏分,得甲酸丁酯38g。
【相关物质的物理性质】
物质
摩尔质量/(false)
熔点/℃
沸点/℃
溶解性
甲酸
46
8.6
100.8
与水、乙醇、乙醚或甘油任意混溶
正丁醇
74
false
117.7
微溶于水,溶于乙醇、乙醚
甲酸丁酯
102
false
106.8
微溶于水,可混溶于醇类、醚类
已知:NaCl能降低甲酸丁酯在水中的溶解度
请回答下列问题:
(1)仪器M的名称为 ,冷凝水的进口为 (填“a”或“b”)。
(2)甲酸和正丁醇反应的化学方程式为 。
(3)甲酸丁酯中的杂质为 。
(4)两次用饱和NaCl溶液洗涤的目的分别是除去 、 。
(5)每次洗涤后均需进行的操作为 。
(6)该实验的产率为 %。(保留小数点后一位)
河南名校联盟
2020—2021学年高一(下)期末考试
化学答案
一、选择题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一个选项符合题意。
1
2
3
4
5
6
7
8
9
10
11
12
B
C
A
D
B
D
D
B
B
C
D
B
13
14
15
16
B
C
C
A
1.【答案】B
【解析】用false制作光导纤维,A项正确;用false和NaOH制取漂白液,B项错误;用葡萄糖制取银镜,C项正确;用false萃取碘水中的碘,D项正确。
2.【答案】C
【解析】石墨烯/聚3,4-乙烯二氧噻吩是混合物,A项错误;石墨与false互为同素异形体,B项错误;聚3,4-乙烯二氧噻吩是人工合成高分子化合物,C项正确;聚3,4-乙烯二氧噻吩是聚合物,是混合物,D项错误。
3.【答案】A
【解析】false与false互为同位素,同位素的化学性质基本相同,A项错误;中子数=质量数false质子数=60-27=33,中子数-质子数=6,B项正确;电子数=质子数,C项正确;根据0族定位法,可知D项正确。
4.【答案】D
【解析】直馏汽油是石油分馏的产物,属于物理变化,A项错误;任何能量转化率都不能达到百分之百,B项错误;太阳能可以直接转化为电能,C项错误;天然气属于气态化石燃料,D项正确。
5.【答案】B
【解析】甲烷的氯代反应与苯的溴代反应都属于取代反应,反应类型相同,A项正确;乙烯使酸性false溶液褪色是乙烯发生了氧化反应,乙烯使溴水褪色是乙烯发生了加成反应,二者褪色原理不同,B项错误;等物质的量的乙醇和乙酸分别与足量Na反应产生false的量相同,C项正确;淀粉和纤维素的最终水解产物均为葡萄糖,D项正确。
6.【答案】D
【解析】false核内有11个质子,A项错误;false分子中应为碳氧双键,B项错误;HClO的电子式应为false,C项错误;false内部既含有false和false形成的离子键,也含有false中各原子间形成的共价键,D项正确。
7.【答案】D
【解析】过程①是蒸馏操作应使用蒸馏烧瓶,A项正确;过程②通入氯气,发生反应false,false是还原剂,false是还原产物,还原性false,B项正确;过程④的化学方程式为false,C项正确;酒精与水互溶,不可选酒精作为萃取剂,D项错误。
8.【答案】B
【解析】由题意可知W、X、Y、Z分别为N、O、Al、Cl。元素周期表中原子半径越往左下越大,原子半径Al>N>O,A项正确;水的稳定性强于氨,B项错误;false为电解质,C项正确;W、Z的最高价氧化物对应的水化物分别为false、false,二者均为强酸,D项正确。
9.【答案】B
【解析】由a电极物质变化false变为false可知,a电极的反应式为false,a电极为阴极,发生还原反应,则放电时,a电极发生氧化反应,为负极,false向正极b电极移动,A、C项错误;转移0.1molfalse,理论上两极质量差为7.8g,B项正确;b电极反应前后,钾元素的化合价不发生变化,碳元素的化合价发生变化,D项错误。
10.【答案】C
【解析】将铁片换成铁粉能增大反应物的接触面积,增大反应速率,A项正确;加入少量false固体,铁会置换出铜,形成Fe—Cu原电池,Fe作负极,可增大反应速率,B项正确;将稀硫酸换成浓硫酸,铁会发生钝化,不再生成false,C项错误;适当升温能增大反应速率,D项正确。
11.【答案】D
【解析】燃烧热是指101kpa时,1mol纯物质完全燃烧生成稳定氧化物时放出的热量,A项错误;物质的三态变化不属于化学反应,B项错误;在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热,C项错误;false false,则false false,D项正确。
12.【答案】B
【解析】标准状况下,false为气体,2.24Lfalse的物质的量为0.1mol,含共用电子对数目为0.7false,A项正确;未说明溶液体积,无法计算false数目,B项错误;正戊烷与新戊烷互为同分异构体,7.2g正戊烷与新戊烷的混合物中含H原子的数目为1.2false,C项正确;由false false可知,当水溶液增重10.8g时,转移的电子数为0.2false,D项正确。
13.【答案】B
【解析】false溶于水生成false,false和false溶液反应生成false,说明酸性false,但false不是S的最高价含氧酸,无法证明非金属性S>Si,A项错误;向false溶液中加入过量氨水会发生反应false,B项正确;Mg比Al活泼,不能用铝热法制备Mg,C项错误;除去乙醇中混有的少量水应该加入CaO后蒸馏,D项错误。
14.【答案】C
【解析】本图只是合成氨反应过程的部分反应历程,不能由图得出合成氨的反应为放热反应,A项错误;false和false转化为2false和6false的过程除了有化学键的断裂,也有原子的吸附,而吸附过程能量降低,无法判断该过程热量的变化,B项错误;观察图象可知false false,C项正确;能量越低物质越稳定,故过渡态Ⅱ最稳定,D项错误。
15.【答案】C
【解析】由图可知,乙酸芳樟酯的分子式为false,A项正确;乙酸芳樟酯在酸性、碱性条件下均能水解,B项正确;乙酸芳樟酯分子中有饱和碳原子,所有原子不可能都处于同一平面,C项错误;1分子乙酸芳樟酯与1分子false加成有如图两种结构,,1分子乙酸芳樟酯与2分子false加成有一种结构,共3种结构,D项正确。
16.【答案】A
【解析】由稳定性false,推断稳定性false,A项正确;F、O元素无最高正价,B项错误;Li在false中燃烧只能生成false,C项错误;Li、Na、K、Rb、Cs熔沸点依次降低,D项错误。
二、非选择题:本题共4小题,共52分。
17.【答案】(14分)
(1)第三周期第ⅠA族(2分) 电解(1分)
(2)离子键、共价键(极性键、非极性键)(2分) 羟基、羧基(2分)
(3)false(1分) false(2分)
(4)false(2分) false(2分)
【解析】由图可知X、Y、Z、Q对应的元素分别为H、C、O、Na。
(1)Q在周期表中的位置为第三周期第ⅠA族,工业上采用电解法冶炼钠的单质。
(2)M为false,所含化学键的类型为离子键、共价键(极性键、非极性键);N为false,所含官能团的名称为羟基、羧基。
(3)相同条件下,等质量的Y的两种单质false、false分别在足量false中燃烧,放出热量前者大于后者,说明false本身能量更低,更稳定;Z的简单氢化物为false,Y的简单氢化物为false,沸点false。
(4)QX的电子式为false,与水反应的化学方程式为false。
18.【答案】(13分)
(1)由Cu电极到石墨电极(2分) false(2分)
(2)①正(1分) ②减重0.7g(2分) ③false(2分)
(3)化学(1分) 电(1分) false(2分)
【解析】(1)在false溶液中,Cu与false发生反应生成false和false,故Cu电极为负极,石墨是正极,电子由Cu电极到石墨电极。
(2)由题意知,放电时负极反应为false,正极反应为false(false或1)。①该电池放电时,金属锂为负极,多孔碳材料为正极;
②放电时,外电路每转移0.1molfalse,锂电极的质量变化为减重0.7g。
(3)燃料电池工作时将燃料内部的化学能转化为电能。碱性甲烷燃料电池工作时负极的电极反应式为false。
19.【答案】(11分)
(1)化学(1分) (2)+178.7(2分)
(3)①BD(2分) ②0.025(2分) 50(2分) 20(2分)
【解析】(1)石油裂化、裂解均为化学变化。
(3)将热化学方程式分别编号为a.false false、b.false false、c.false false、d.false false,c-b-a-d得目标热化学方程式false false。
(3)①false未标明正逆反应,不能判定平衡,A项错误。相同时间内,断裂2.molfalse的同时断裂1molfalse说明正逆反应速率相等,可以判定平衡,B项正确。容器体积,气体质量一直不变,容器内气体的密度一直不变,不能判定平衡,C项错误。容器内气体的质量一直不变,没平衡时气体的物质的量在发生改变,平均相对分子质量不再发生变化可以判定平衡,D项正确。
②设平衡时CO转化的物质的量为falsemol,列三段式:
false
起始/mol 1 1 0
转化/mol false false false
平衡/mol false false false
false,解得false
false,false的转化率false,false的体积分数=false的物质的量分数false。
20.【答案】(14分)
(1)圆底烧瓶(1分) b(1分)
(2)false(2分,写成false也给分)
(3)甲酸、正丁醇、少量浓硫酸(2分,少写给1分)
(4)甲酸、硫酸等酸性杂质(2分) false(2分)
(5)分液(2分) (6)74.5(2分)
【解析】(1)仪器M的名称为圆底烧瓶,冷凝水的进口为b。
(2)甲酸和正丁醇反应的化学方程式为false。
(3)酯化反应为可逆反应,反应物不可能全部转化为生成物,催化剂不参与反应,因此甲酸丁醇中的杂质为甲酸、正丁醇、少量浓硫酸。
(4)两次用饱和NaCl溶液洗涤的目的分别是除去甲酸、硫酸等酸性杂质和第二次洗涤引入的少量false。
(5)每次洗涤后均需进行的操作为分液。
(6)该实验中甲酸的物质的量为false,正丁醇的物质的量为false,产率false。
2020—2021学年高一(下)期末考试
化学
考生注意:
1.本试卷共8页。时间90分钟,满分100分。答题前,考生先将自己的姓名、考生号填写在试卷指定位置,并将姓名、考场号、座位号、考生号填写在答题卡上,然后认真核对条形码上的信息,并将条形码粘贴在答题卡上的指定位置。
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。作答非选择题时,将答案写在答题卡上对应的答题区域内。写在本试卷上无效。
3.考试结束后,将试卷和答题卡一并收回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Mg 24 Al 27 K 39
一、选择题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一个选项符合题意。.
1.化学与人类生活密切相关,下列有关物质的用途不正确的是( )
A.用false制作光导纤维 B.用澄清石灰水制取漂白液
C.用葡萄糖制取银镜 D.用false萃取碘水中的碘
2.超级电容器是介于普通电容器与电池之间的储能装置。石墨烯/聚3,4-乙烯二氧噻吩(PEDOP)可用于制备超级电容器。下列有关说法正确的是( )
A.石墨烯/聚3,4-乙烯二氧噻吩是一种新型化合物
B.石墨与false互为同位素
C.聚3,4-乙烯二氧噻吩是人工合成高分子化合物
D.聚3,4-乙烯二氧噻吩是纯净物
3.false具有极强的辐射性,常用于辐射育种,癌症和肿瘤的放射治疗。下列有关false的说法不正确的是( )
A.与会false的化学性质不同 B.质子数比中子数少6
C.电子数为27 D.属于过渡元素
4.“十四五规划”国家提出了一个明确的目标,到2025年,新能源汽车新车销售量达到汽车新车销售总量的20%左右。新能源汽车指除燃料为汽油、柴油之外的所有使用其他能源(比如电能、太阳能)的汽车。下列关于能源的说法正确的是( )
A.汽油、柴油都是石油发生化学变化的产物
B.电动汽车内部的电池能量转化率可以达到百分之百
C.太阳能不能直接转化为电能
D.天然气属于气态化石燃料
5.下列说法不正确的是( )
A.甲烷的氯代反应与苯的溴代反应类型相同
B.乙烯能使酸性false溶液和溴水褪色,且褪色原理相同
C.等物质的量的乙醇,乙酸分别与足量Na反应产生false的量相同
D.淀粉和纤维素的最终水解产物相同
6.氯气通入碳酸氢钠溶液中发生反应false,下列有关化学用语正确的是( )
A.false的结构示意图: B.false的结构式:O—C—O
C.HClO的电子式:false D.false内部既含离子键又含共价键
7.我国从1966年开始进行海水提溴,主要采用的方法是空气吹出法,其从海水中提取溴的流程如下:
下列叙述不正确的是( )
A.过程①应使用蒸馏烧瓶
B.过程②可证明还原性false
C.过程④的化学方程式为false
D.萃取过程可选用酒精为萃取剂
8.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X同周期且二者可形成两种以上的二元化合物,Y的族序数与周期数相等,Z单质常温下呈气态。下列有关说法不正确的是( )
A.原子半径:Y>W>X
B.简单氢化物的稳定性:W>X
C.Y与Z形成的二元化合物为电解质
D.W、Z的最高价氧化物对应的水化物均为强酸
9.钾离子电池由于其低成本,电解液中快的离子传导性以及高的工作电压等优点,近年来引起了科研工作者极大的关注。false在两极间脱嵌实现电池的充放电过程。下图为钾离子二次电池充电时的工作原图,工作前两电极质量相等且均为false。下列有关说法正确的是( )
A.放电时,false向a极移动
B.充电时,转移0.1molfalse时,理论上两极质量差为7.8g
C.充电时,a电极发生的反应为false
D.充电时,b电极反应前后,碳元素的化合价不发生变化
10.常温下,将铁片置于稀硫酸中发生反应false,下列措施不能增大false生成速率的是( )
A.将铁片换成铁粉 B.加入少量false固体
C.将稀硫酸换成浓硫酸 D.适当升高温度
11.下列关于热化学方程式的说法正确的是( )
A.false false,则false的燃烧热为false
B.false false,则该反应为放热反应
C.已知false false,则false false
D.false false,则false false
12.设false为阿伏加德罗常数的值,下列叙述不正确的是( )
A.标准状况下,2.24Lfalse中含共用电子对数目为0.7false
B.false溶液中含false的数目为0.6false
C.7.2g正戊烷与新戊烷的混合物中含H原子的数目为1.2false
D.false与足量水反应,当水溶液增重10.8g时,转移的电子数为0.2false
13.下列实验操作能达到实验目的的是( )
选项
实验操作
实验目的
A
向饱和false溶液中通入false
证明非金属性:S>Si
B
向false溶液中加入过量氨水
制备false
C
将5g干燥的MgO粉末和2g铝粉均匀混合后放入纸漏斗中
用铝热法制备金属Mg
D
向混有少量水的乙醇中加入浓硫酸
除去乙醇中的水
14.工业上合成氨的部分反应历程(其中吸附在催化剂表面的物质用*表示)如下图所示,下列说法正确的是( )
A.由图可知,工业合成氨的反应是放热反应
B.由false和false转化为2false和6false的过程可知断裂化学键释放能量
C.false false
D.相比于过渡态Ⅰ、Ⅱ,过渡态Ⅲ更稳定
15.乙酸芳樟酯又名乙酸沉香酯,其结构简式如下图所示,是制备高级香精不可缺少的香料,在日化、烟草、食品工业中占有十分重要的地位。下列有关乙酸芳樟酯的说法不正确的是( )
A.分子式为false
B.在酸性、碱性条件下均不稳定
C.分子中所有原子有可能共面
D.与一定量false加成的产物有3种(不考虑立体异构)
16.下列推断正确的是( )
A.由稳定性false,推断稳定性false
B.由同周期主族元素最高正价依次升高,推断最高正价F>O
C.由Na在false中燃烧生成false,推断Li在false中燃烧生成false
D.由同主族单质false、false、false、false熔沸点依次升高,推断Li、Na、K、Rb、Cs熔沸点依次升高
二、非选择题:本题共4小题,共52分。
17.(14分)物质M可用作调味剂、乳化剂、抗氧化增效剂、吸湿剂、pH调节剂、增香剂、缓冲剂。其结构式如下图所示,其组成元素X、Y、Z、Q为原子序数依次增大的短周期主族元素,且Y的一种核素常用于检测文物的年代。
请回答下列问题:
(1)元素Q在周期表中的位置为 ,工业上采用 法冶炼Q的单质。
(2)物质M中所含化学键的类型为 ,物质M与稀硫酸反应生成有机物N,N中所含官能团的名称为 。
(3)相同条件下,等质量的Y的两种单质false、false分别在足量false中燃烧,放出热量前者大于后者.则两种单质中, (填“false”或“false”)更稳定。Y与Z分别形成的简单氢化物的沸点由高到低的顺序为 (填化学式)。
(4)QX的电子式为 ,与水反应的化学方程式为 。
18.(13分)原电池体现化学对社会发展的又一伟大贡献。请回答下列问题:
(1)将Cu电极、石墨电极用导线连接好后插入false溶液中,电子的流向为 (填“由Cu电极到石墨电极”或“由石墨电极到Cu电极”),石墨电极的电极反应式为 。
(2)一种可充电锂—空气电池如图所示。当电池放电时,false与false在多孔碳材料电极处生成false(false或1)。
①放电时,多孔碳材料电极为 (填“正”或“负”)极。
②放电时,外电路每转移0.1molfalse,锂电极的质量变化为 。
③放电时,电池正极的电极反应式为 。
(3)燃料电池大大提高了能量的转化效率。燃料电池工作时将燃料内部的 能转化为 能。碱性甲烷燃料电池工作时负极的电极反应式为 。
19.(11分)石油是宝贵的能源,属于战略资源。false、false均是石油裂解的产物。
请回答下列问题:
(1)石油裂化、裂解为 (填“物理”或“化学")变化。
(2)已知false false
false false
false false
false false
则反应false false false。
(3)一定温度下,在某2L恒容密闭容器中充入1molfalse和1molfalse发生反应false,10min后达到平衡,容器内压强为起始压强的1.25倍。
①下列说法可以判定反应到达平衡状态的是 。(填字母序号)
A.false
B.相同时间内,断裂2molfalse的同时断裂1molfalse
C.容器内气体的密度不再发生变化
D.容器内气体的平均相对分子质量不再发生变化
②0~10min,v(CO)= false,false的转化率为 %,false的体积分数为 %。
20.(14分)甲酸丁酯(false)可用作漆用溶剂和制造胶片时的溶剂,还可用于人造革、香料和有机合成等领域。某小组在实验室进行甲酸丁酯的制备。
【实验原料】甲酸(HCOOH)和正丁醇(false)
【实验装置】
【实验步骤】
向仪器M中加入98%的甲酸47g,正丁醇37g,适量浓硫酸,几粒沸石,加热回流反应24h。冷却后用饱和NaCl溶液洗涤,再依次用饱和false溶液、饱和NaCl溶液洗涤。再经无水false干燥,分馏,收集106~107℃的馏分,得甲酸丁酯38g。
【相关物质的物理性质】
物质
摩尔质量/(false)
熔点/℃
沸点/℃
溶解性
甲酸
46
8.6
100.8
与水、乙醇、乙醚或甘油任意混溶
正丁醇
74
false
117.7
微溶于水,溶于乙醇、乙醚
甲酸丁酯
102
false
106.8
微溶于水,可混溶于醇类、醚类
已知:NaCl能降低甲酸丁酯在水中的溶解度
请回答下列问题:
(1)仪器M的名称为 ,冷凝水的进口为 (填“a”或“b”)。
(2)甲酸和正丁醇反应的化学方程式为 。
(3)甲酸丁酯中的杂质为 。
(4)两次用饱和NaCl溶液洗涤的目的分别是除去 、 。
(5)每次洗涤后均需进行的操作为 。
(6)该实验的产率为 %。(保留小数点后一位)
河南名校联盟
2020—2021学年高一(下)期末考试
化学答案
一、选择题:本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一个选项符合题意。
1
2
3
4
5
6
7
8
9
10
11
12
B
C
A
D
B
D
D
B
B
C
D
B
13
14
15
16
B
C
C
A
1.【答案】B
【解析】用false制作光导纤维,A项正确;用false和NaOH制取漂白液,B项错误;用葡萄糖制取银镜,C项正确;用false萃取碘水中的碘,D项正确。
2.【答案】C
【解析】石墨烯/聚3,4-乙烯二氧噻吩是混合物,A项错误;石墨与false互为同素异形体,B项错误;聚3,4-乙烯二氧噻吩是人工合成高分子化合物,C项正确;聚3,4-乙烯二氧噻吩是聚合物,是混合物,D项错误。
3.【答案】A
【解析】false与false互为同位素,同位素的化学性质基本相同,A项错误;中子数=质量数false质子数=60-27=33,中子数-质子数=6,B项正确;电子数=质子数,C项正确;根据0族定位法,可知D项正确。
4.【答案】D
【解析】直馏汽油是石油分馏的产物,属于物理变化,A项错误;任何能量转化率都不能达到百分之百,B项错误;太阳能可以直接转化为电能,C项错误;天然气属于气态化石燃料,D项正确。
5.【答案】B
【解析】甲烷的氯代反应与苯的溴代反应都属于取代反应,反应类型相同,A项正确;乙烯使酸性false溶液褪色是乙烯发生了氧化反应,乙烯使溴水褪色是乙烯发生了加成反应,二者褪色原理不同,B项错误;等物质的量的乙醇和乙酸分别与足量Na反应产生false的量相同,C项正确;淀粉和纤维素的最终水解产物均为葡萄糖,D项正确。
6.【答案】D
【解析】false核内有11个质子,A项错误;false分子中应为碳氧双键,B项错误;HClO的电子式应为false,C项错误;false内部既含有false和false形成的离子键,也含有false中各原子间形成的共价键,D项正确。
7.【答案】D
【解析】过程①是蒸馏操作应使用蒸馏烧瓶,A项正确;过程②通入氯气,发生反应false,false是还原剂,false是还原产物,还原性false,B项正确;过程④的化学方程式为false,C项正确;酒精与水互溶,不可选酒精作为萃取剂,D项错误。
8.【答案】B
【解析】由题意可知W、X、Y、Z分别为N、O、Al、Cl。元素周期表中原子半径越往左下越大,原子半径Al>N>O,A项正确;水的稳定性强于氨,B项错误;false为电解质,C项正确;W、Z的最高价氧化物对应的水化物分别为false、false,二者均为强酸,D项正确。
9.【答案】B
【解析】由a电极物质变化false变为false可知,a电极的反应式为false,a电极为阴极,发生还原反应,则放电时,a电极发生氧化反应,为负极,false向正极b电极移动,A、C项错误;转移0.1molfalse,理论上两极质量差为7.8g,B项正确;b电极反应前后,钾元素的化合价不发生变化,碳元素的化合价发生变化,D项错误。
10.【答案】C
【解析】将铁片换成铁粉能增大反应物的接触面积,增大反应速率,A项正确;加入少量false固体,铁会置换出铜,形成Fe—Cu原电池,Fe作负极,可增大反应速率,B项正确;将稀硫酸换成浓硫酸,铁会发生钝化,不再生成false,C项错误;适当升温能增大反应速率,D项正确。
11.【答案】D
【解析】燃烧热是指101kpa时,1mol纯物质完全燃烧生成稳定氧化物时放出的热量,A项错误;物质的三态变化不属于化学反应,B项错误;在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热,C项错误;false false,则false false,D项正确。
12.【答案】B
【解析】标准状况下,false为气体,2.24Lfalse的物质的量为0.1mol,含共用电子对数目为0.7false,A项正确;未说明溶液体积,无法计算false数目,B项错误;正戊烷与新戊烷互为同分异构体,7.2g正戊烷与新戊烷的混合物中含H原子的数目为1.2false,C项正确;由false false可知,当水溶液增重10.8g时,转移的电子数为0.2false,D项正确。
13.【答案】B
【解析】false溶于水生成false,false和false溶液反应生成false,说明酸性false,但false不是S的最高价含氧酸,无法证明非金属性S>Si,A项错误;向false溶液中加入过量氨水会发生反应false,B项正确;Mg比Al活泼,不能用铝热法制备Mg,C项错误;除去乙醇中混有的少量水应该加入CaO后蒸馏,D项错误。
14.【答案】C
【解析】本图只是合成氨反应过程的部分反应历程,不能由图得出合成氨的反应为放热反应,A项错误;false和false转化为2false和6false的过程除了有化学键的断裂,也有原子的吸附,而吸附过程能量降低,无法判断该过程热量的变化,B项错误;观察图象可知false false,C项正确;能量越低物质越稳定,故过渡态Ⅱ最稳定,D项错误。
15.【答案】C
【解析】由图可知,乙酸芳樟酯的分子式为false,A项正确;乙酸芳樟酯在酸性、碱性条件下均能水解,B项正确;乙酸芳樟酯分子中有饱和碳原子,所有原子不可能都处于同一平面,C项错误;1分子乙酸芳樟酯与1分子false加成有如图两种结构,,1分子乙酸芳樟酯与2分子false加成有一种结构,共3种结构,D项正确。
16.【答案】A
【解析】由稳定性false,推断稳定性false,A项正确;F、O元素无最高正价,B项错误;Li在false中燃烧只能生成false,C项错误;Li、Na、K、Rb、Cs熔沸点依次降低,D项错误。
二、非选择题:本题共4小题,共52分。
17.【答案】(14分)
(1)第三周期第ⅠA族(2分) 电解(1分)
(2)离子键、共价键(极性键、非极性键)(2分) 羟基、羧基(2分)
(3)false(1分) false(2分)
(4)false(2分) false(2分)
【解析】由图可知X、Y、Z、Q对应的元素分别为H、C、O、Na。
(1)Q在周期表中的位置为第三周期第ⅠA族,工业上采用电解法冶炼钠的单质。
(2)M为false,所含化学键的类型为离子键、共价键(极性键、非极性键);N为false,所含官能团的名称为羟基、羧基。
(3)相同条件下,等质量的Y的两种单质false、false分别在足量false中燃烧,放出热量前者大于后者,说明false本身能量更低,更稳定;Z的简单氢化物为false,Y的简单氢化物为false,沸点false。
(4)QX的电子式为false,与水反应的化学方程式为false。
18.【答案】(13分)
(1)由Cu电极到石墨电极(2分) false(2分)
(2)①正(1分) ②减重0.7g(2分) ③false(2分)
(3)化学(1分) 电(1分) false(2分)
【解析】(1)在false溶液中,Cu与false发生反应生成false和false,故Cu电极为负极,石墨是正极,电子由Cu电极到石墨电极。
(2)由题意知,放电时负极反应为false,正极反应为false(false或1)。①该电池放电时,金属锂为负极,多孔碳材料为正极;
②放电时,外电路每转移0.1molfalse,锂电极的质量变化为减重0.7g。
(3)燃料电池工作时将燃料内部的化学能转化为电能。碱性甲烷燃料电池工作时负极的电极反应式为false。
19.【答案】(11分)
(1)化学(1分) (2)+178.7(2分)
(3)①BD(2分) ②0.025(2分) 50(2分) 20(2分)
【解析】(1)石油裂化、裂解均为化学变化。
(3)将热化学方程式分别编号为a.false false、b.false false、c.false false、d.false false,c-b-a-d得目标热化学方程式false false。
(3)①false未标明正逆反应,不能判定平衡,A项错误。相同时间内,断裂2.molfalse的同时断裂1molfalse说明正逆反应速率相等,可以判定平衡,B项正确。容器体积,气体质量一直不变,容器内气体的密度一直不变,不能判定平衡,C项错误。容器内气体的质量一直不变,没平衡时气体的物质的量在发生改变,平均相对分子质量不再发生变化可以判定平衡,D项正确。
②设平衡时CO转化的物质的量为falsemol,列三段式:
false
起始/mol 1 1 0
转化/mol false false false
平衡/mol false false false
false,解得false
false,false的转化率false,false的体积分数=false的物质的量分数false。
20.【答案】(14分)
(1)圆底烧瓶(1分) b(1分)
(2)false(2分,写成false也给分)
(3)甲酸、正丁醇、少量浓硫酸(2分,少写给1分)
(4)甲酸、硫酸等酸性杂质(2分) false(2分)
(5)分液(2分) (6)74.5(2分)
【解析】(1)仪器M的名称为圆底烧瓶,冷凝水的进口为b。
(2)甲酸和正丁醇反应的化学方程式为false。
(3)酯化反应为可逆反应,反应物不可能全部转化为生成物,催化剂不参与反应,因此甲酸丁醇中的杂质为甲酸、正丁醇、少量浓硫酸。
(4)两次用饱和NaCl溶液洗涤的目的分别是除去甲酸、硫酸等酸性杂质和第二次洗涤引入的少量false。
(5)每次洗涤后均需进行的操作为分液。
(6)该实验中甲酸的物质的量为false,正丁醇的物质的量为false,产率false。
同课章节目录
