4.3 质量守恒定律 同步训练(含答案)
文档属性
| 名称 | 4.3 质量守恒定律 同步训练(含答案) | 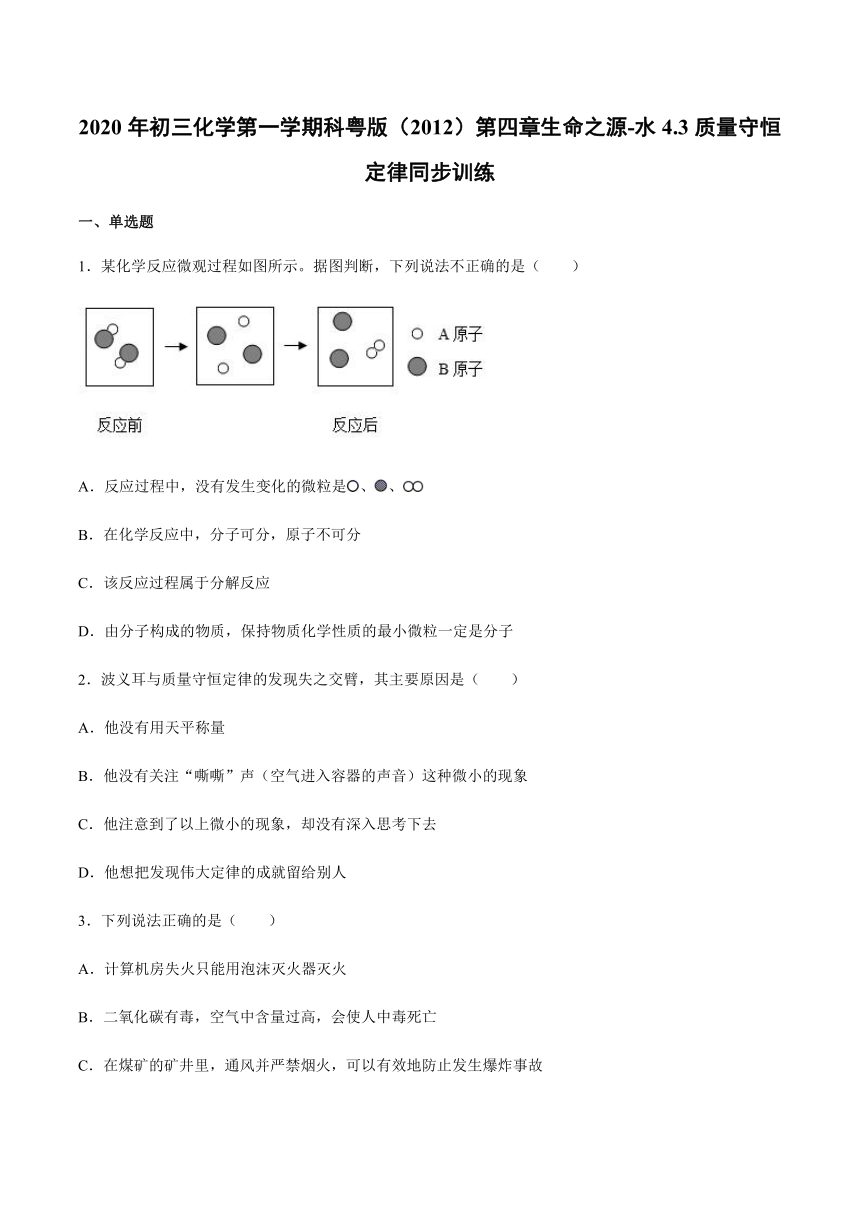 | |
| 格式 | docx | ||
| 文件大小 | 101.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-21 15:46:27 | ||
图片预览



文档简介
2020年初三化学第一学期科粤版(2012)第四章生命之源-水4.3质量守恒定律同步训练
一、单选题
1.某化学反应微观过程如图所示。据图判断,下列说法不正确的是( )
A.反应过程中,没有发生变化的微粒是、、
B.在化学反应中,分子可分,原子不可分
C.该反应过程属于分解反应
D.由分子构成的物质,保持物质化学性质的最小微粒一定是分子
2.波义耳与质量守恒定律的发现失之交臂,其主要原因是( )
A.他没有用天平称量
B.他没有关注“嘶嘶”声(空气进入容器的声音)这种微小的现象
C.他注意到了以上微小的现象,却没有深入思考下去
D.他想把发现伟大定律的成就留给别人
3.下列说法正确的是( )
A.计算机房失火只能用泡沫灭火器灭火
B.二氧化碳有毒,空气中含量过高,会使人中毒死亡
C.在煤矿的矿井里,通风并严禁烟火,可以有效地防止发生爆炸事故
D.某物质完全燃烧后生成二氧化碳和水,则该物质一定由碳、氢、氧三种元素组成
4.在一密闭容器内有A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得反应前后各物质的质量如下表,则下列说法中正确的是( )
物 质
A
B
C
D
反应前物质质量(g)
10
90
8
2
反应后物质质量(g)
38
56
14
X
A.根据质量守恒定律,X的值为0 B.该反应是分解反应
C.该反应是复分解反应 D.在这个反应中A、B、C之间的质量比为38∶56∶14
5.2019年5月,华为宣布做好了启动备用芯片的准备,硅是计算机芯片的基体材料。高温下氢气与四氯化硅反成制硅的化学方程式为:2H2+SiCl4Si+4X,其中X的化学式为( )
A.Cl2 B.HCl C.H2O D.SiH4
6.某物质由碳、氢、氧三种元素中的一种或几种组成,将该物质燃烧后的产物依次通过澄清石灰水和无水硫酸铜,观察到石灰水变浑浊,无水硫酸铜变成蓝色。有关该物质的组成,推断正确的是( )
A.一定有碳、氢、氧元素 B.一定有碳、氢元素,可能有氧元素
C.一定有碳元素,可能有氢、氧元素 D.一定有碳、氧元素,可能有氢元素
7.在化学反应A +2B=C+2D中,已知B和C的相对分子质量之比为8∶11,当16 g A与一定量B恰好完全反应后,生成44 g C,则生成D的质量是( )
A.9 g B.18 g C.36 g D.48 g
8.下列事实能用质量守恒定律解释的是( )
A.2g食盐溶于10g水得到12g食盐水 B.5g水加热蒸发得到5g水蒸气
C.1体积的氢气和1体积的氯气点燃后生成2体积氯化氢气体 D.白磷在空气中燃烧后生成物的质量增加
9.1.6g某物质在氧气中完全燃烧生成4.4g二氧化碳和3.6g水,关于该物质的组成有下列论断:①一定含有C、H;②一定不含有O;③可能含有O;④一定含有O.其中正确的是( )
A.①② B.①②③ C.①②④ D.①
10.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是( )
物质
甲
乙
丙
丁
反应前的质量(g)
30
10
20
0
反应后的质量(g)
0
20
20
x
A.丙物质一定是该反应的催化剂 B.该反应为化合反应
C.反应生成的乙和丁的质量比为2:1 D.甲物质含有乙和丁中的所有元素种类
11.在反应2A+B=3C+D中,A和B的相对分子质量之比为5﹕1,已知20克A与一定质量的B恰好反应,生成5克D,则在此反应中B和C的质量比为( )
A.2﹕17 B.4﹕19 C.3﹕5 D.1﹕3
12.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质质量如图所示。下列说法正确的是( )
A.该反应为化合反应 B.乙一定为该反应的催化剂
C.该反应中,甲、丁的质量变化之比为9∶8 D.甲和丁一定属于单质
13.如图所示,下列实验装置不能用来证明质量守恒定律的是( )
A.B.C. D.
14.从化学的视角看,下列描述的变化具有科学道理的是( )
A.水变油 B.点石成金 C.氯化钠变硝酸钾 D.石油变汽油
15.硝酸铵(NH4NO3)的外观与氯化钠很相似,均为白色固体。区别它们的一种方法是将两者分别隔绝空气加热,氯化钠不分解,硝酸铵能分解。硝酸铵分解得到的气体不可能是( )
A.NH3 B.SO2 C.NO2 D.N2
二、实验题
16.某兴趣小组依据教材实验对质量守恒定律进行了如下探究(已知碳酸钠与盐酸反应和碳酸钙与盐酸反应原理相似)。根据下图回答问题:
(1)甲组反应过程中气球的变化是_____,反应的化学方程式为_____。
(2)乙组反应后天平指针会向_____(“左”或“右”)偏转,原因是:_____;某同学将乙组烧杯换成甲组中的带气球的锥形瓶装置,药品不变重新反应后仍达不到实验效果,则造成误差的原因可能是_____干扰了实验结果。
(3)已知丙组反应前称量的装置总质量是118.4g,则反应后称量的总质量应该是_____g。
(4)请从分子原子的角度解释反应前后质量守恒的原因_____。
三、简答题
17.为了研究质量守恒定律,设计了如图“红磷燃烧前后质量的测定”实验请回答下面问题。
(1)锥形瓶底部铺一层细沙的作用是什么?_______
(2)红磷燃烧过程中看到的实验现象是什么?_______
(3)燃烧后称量,发现托盘天平指针偏向右边,造成的原因可能是什么?_______
18.在一定条件下,A 和 B 反应生成 C 和 D。反应前后分子种类的微观示意图如下:
(1)结合图示从微观角度解释此类变化的实质是___________________。
(2)写出此反应的化学方程式_________________, 该化学反应前后氮元素的化合价分别为______________。
参考答案
1.A2.C3.C4.B5.B6.C7.C8.D9.A10.D11.A12.C13.C14.D15.B
16.先膨胀再缩小到比原来还小 右 盐酸和碳酸钠反应生成的二氧化碳排到空气中,使天平左边质量减小 气球漏气 118.4 化学反应前后,原子的种类、数目、质量保持不变
17.防止底部局部受热而炸裂瓶底 冒白烟,气球先涨大后缩小 装置漏气
18.在化学变化中,(一定条件下)分子分成原子,原子又结合成新的分子 2NH3+3Cl2 6HCl+N2 -3(价)、0(价)
一、单选题
1.某化学反应微观过程如图所示。据图判断,下列说法不正确的是( )
A.反应过程中,没有发生变化的微粒是、、
B.在化学反应中,分子可分,原子不可分
C.该反应过程属于分解反应
D.由分子构成的物质,保持物质化学性质的最小微粒一定是分子
2.波义耳与质量守恒定律的发现失之交臂,其主要原因是( )
A.他没有用天平称量
B.他没有关注“嘶嘶”声(空气进入容器的声音)这种微小的现象
C.他注意到了以上微小的现象,却没有深入思考下去
D.他想把发现伟大定律的成就留给别人
3.下列说法正确的是( )
A.计算机房失火只能用泡沫灭火器灭火
B.二氧化碳有毒,空气中含量过高,会使人中毒死亡
C.在煤矿的矿井里,通风并严禁烟火,可以有效地防止发生爆炸事故
D.某物质完全燃烧后生成二氧化碳和水,则该物质一定由碳、氢、氧三种元素组成
4.在一密闭容器内有A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得反应前后各物质的质量如下表,则下列说法中正确的是( )
物 质
A
B
C
D
反应前物质质量(g)
10
90
8
2
反应后物质质量(g)
38
56
14
X
A.根据质量守恒定律,X的值为0 B.该反应是分解反应
C.该反应是复分解反应 D.在这个反应中A、B、C之间的质量比为38∶56∶14
5.2019年5月,华为宣布做好了启动备用芯片的准备,硅是计算机芯片的基体材料。高温下氢气与四氯化硅反成制硅的化学方程式为:2H2+SiCl4Si+4X,其中X的化学式为( )
A.Cl2 B.HCl C.H2O D.SiH4
6.某物质由碳、氢、氧三种元素中的一种或几种组成,将该物质燃烧后的产物依次通过澄清石灰水和无水硫酸铜,观察到石灰水变浑浊,无水硫酸铜变成蓝色。有关该物质的组成,推断正确的是( )
A.一定有碳、氢、氧元素 B.一定有碳、氢元素,可能有氧元素
C.一定有碳元素,可能有氢、氧元素 D.一定有碳、氧元素,可能有氢元素
7.在化学反应A +2B=C+2D中,已知B和C的相对分子质量之比为8∶11,当16 g A与一定量B恰好完全反应后,生成44 g C,则生成D的质量是( )
A.9 g B.18 g C.36 g D.48 g
8.下列事实能用质量守恒定律解释的是( )
A.2g食盐溶于10g水得到12g食盐水 B.5g水加热蒸发得到5g水蒸气
C.1体积的氢气和1体积的氯气点燃后生成2体积氯化氢气体 D.白磷在空气中燃烧后生成物的质量增加
9.1.6g某物质在氧气中完全燃烧生成4.4g二氧化碳和3.6g水,关于该物质的组成有下列论断:①一定含有C、H;②一定不含有O;③可能含有O;④一定含有O.其中正确的是( )
A.①② B.①②③ C.①②④ D.①
10.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是( )
物质
甲
乙
丙
丁
反应前的质量(g)
30
10
20
0
反应后的质量(g)
0
20
20
x
A.丙物质一定是该反应的催化剂 B.该反应为化合反应
C.反应生成的乙和丁的质量比为2:1 D.甲物质含有乙和丁中的所有元素种类
11.在反应2A+B=3C+D中,A和B的相对分子质量之比为5﹕1,已知20克A与一定质量的B恰好反应,生成5克D,则在此反应中B和C的质量比为( )
A.2﹕17 B.4﹕19 C.3﹕5 D.1﹕3
12.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质质量如图所示。下列说法正确的是( )
A.该反应为化合反应 B.乙一定为该反应的催化剂
C.该反应中,甲、丁的质量变化之比为9∶8 D.甲和丁一定属于单质
13.如图所示,下列实验装置不能用来证明质量守恒定律的是( )
A.B.C. D.
14.从化学的视角看,下列描述的变化具有科学道理的是( )
A.水变油 B.点石成金 C.氯化钠变硝酸钾 D.石油变汽油
15.硝酸铵(NH4NO3)的外观与氯化钠很相似,均为白色固体。区别它们的一种方法是将两者分别隔绝空气加热,氯化钠不分解,硝酸铵能分解。硝酸铵分解得到的气体不可能是( )
A.NH3 B.SO2 C.NO2 D.N2
二、实验题
16.某兴趣小组依据教材实验对质量守恒定律进行了如下探究(已知碳酸钠与盐酸反应和碳酸钙与盐酸反应原理相似)。根据下图回答问题:
(1)甲组反应过程中气球的变化是_____,反应的化学方程式为_____。
(2)乙组反应后天平指针会向_____(“左”或“右”)偏转,原因是:_____;某同学将乙组烧杯换成甲组中的带气球的锥形瓶装置,药品不变重新反应后仍达不到实验效果,则造成误差的原因可能是_____干扰了实验结果。
(3)已知丙组反应前称量的装置总质量是118.4g,则反应后称量的总质量应该是_____g。
(4)请从分子原子的角度解释反应前后质量守恒的原因_____。
三、简答题
17.为了研究质量守恒定律,设计了如图“红磷燃烧前后质量的测定”实验请回答下面问题。
(1)锥形瓶底部铺一层细沙的作用是什么?_______
(2)红磷燃烧过程中看到的实验现象是什么?_______
(3)燃烧后称量,发现托盘天平指针偏向右边,造成的原因可能是什么?_______
18.在一定条件下,A 和 B 反应生成 C 和 D。反应前后分子种类的微观示意图如下:
(1)结合图示从微观角度解释此类变化的实质是___________________。
(2)写出此反应的化学方程式_________________, 该化学反应前后氮元素的化合价分别为______________。
参考答案
1.A2.C3.C4.B5.B6.C7.C8.D9.A10.D11.A12.C13.C14.D15.B
16.先膨胀再缩小到比原来还小 右 盐酸和碳酸钠反应生成的二氧化碳排到空气中,使天平左边质量减小 气球漏气 118.4 化学反应前后,原子的种类、数目、质量保持不变
17.防止底部局部受热而炸裂瓶底 冒白烟,气球先涨大后缩小 装置漏气
18.在化学变化中,(一定条件下)分子分成原子,原子又结合成新的分子 2NH3+3Cl2 6HCl+N2 -3(价)、0(价)
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
