4.1 常见的化学反应——燃烧 课件(35张PPT)
文档属性
| 名称 | 4.1 常见的化学反应——燃烧 课件(35张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-21 00:00:00 | ||
图片预览











文档简介
常见的化学反应
燃烧
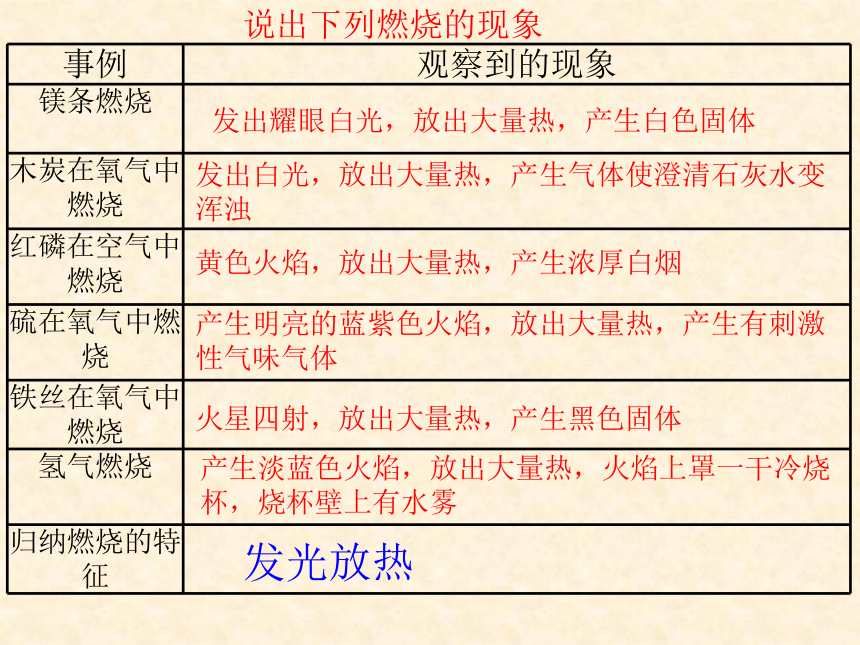
说出下列燃烧的现象
事例
观察到的现象
镁条燃烧
木炭在氧气中燃烧
红磷在空气中燃烧
硫在氧气中燃烧
铁丝在氧气中燃烧
氢气燃烧
归纳燃烧的特征
发出耀眼白光,放出大量热,产生白色固体
发出白光,放出大量热,产生气体使澄清石灰水变浑浊
黄色火焰,放出大量热,产生浓厚白烟
产生明亮的蓝紫色火焰,放出大量热,产生有刺激性气味气体
火星四射,放出大量热,产生黑色固体
产生淡蓝色火焰,放出大量热,火焰上罩一干冷烧杯,烧杯壁上有水雾
发光放热
燃烧的定义:
燃烧是一种发光、发热的剧烈的化学反应。
讨论:
物质燃烧需要哪些条件?
燃烧的条件
实验内容
实验现象
实验结论
取木条和玻璃棒在酒精灯火焰上加热,观察两种物质是否可以燃烧
将蜡烛点燃用烧杯罩住,观察
取小木条和纸条在酒精灯上点燃,观察燃烧所需时间
实验
木条能燃烧,玻璃棒不能燃烧
物质要有可燃性
蜡烛过一会熄灭
物质燃烧需要氧气
纸条比木条容易燃烧
物质燃烧需要达到一定温度
结合上述实验,我们可以得出物质燃烧需要同时满足三个条件:
1、物质具有可燃性
2、可燃物与氧气接触
3、可燃物达到燃烧所需要的最低温度
燃烧所需要的最低温度也叫着火点
燃烧的条件
实验
燃烧的条件
实验内容
实验现象
解释原因
将酒精和水以2:1体积混合,将一块棉布手绢浸入配好的混合液中,浸透后取出轻轻拧干,用镊子夹持在酒精灯上点燃,并轻轻抖动手绢。火熄灭后观察手绢有什么变化。
手绢没有燃烧损坏
酒精燃烧产生的热被水吸收,使温度达不到手绢的着火点,所以手绢不燃烧
灭火的方法
你能说出几种熄灭蜡烛火焰的方法
用嘴吹灭
用水浇灭
用烧杯盖灭
用剪刀剪去烛心
… …
灭火的方法:
1、将可燃物撤离燃烧区,与火源隔离
2、将燃着的可燃物与空气隔离
3、使用大量的冷却剂使燃烧物冷却,让燃烧物的温度降到着火点以下
完全燃烧和不完全燃烧
回顾:
用烧杯罩住燃烧的蜡烛时,除了蜡烛熄灭外,在烧杯底部还出现了什么现象?你能解释其中原因吗?
完全燃烧和不完全燃烧
当氧气充足时,可燃物完全燃烧,燃烧得快,放出的热量多,对环境污染小;当氧气不充足时,可燃物不完全燃烧,燃烧得慢,放出的热量少,对环境污染大。
完全燃烧和不完全燃烧
含碳、氢元素的可燃物完全燃烧时,碳、氢元素分别生成二氧化碳和水;当氧气不充足时,可燃物中的部分碳、氢元素生成一氧化碳、碳氢化合物等有毒气体和微小的炭黑颗粒等物质。
石墨、金刚石、木炭等燃烧均是如此!
完全燃烧与不完全燃烧的比较
完全燃烧
不完全燃烧
发生条件
燃烧速率
放出热量
燃烧产物
O2充足
O2不足
快
慢
多
少
二氧化碳和水
CO、碳氢化合物等有毒气体和炭黑等小颗粒
完全燃烧和不完全燃烧
为什么要使燃料完全燃烧?
完全燃烧
放出热量多
不完全燃烧会生成CO等有毒气体,污染大气
完全燃烧能
节约资源,保护环境
交流与讨论
总结与反思
在日常生活中,使燃料完全燃烧的具体做法有哪些呢?
1.提供充足的氧气
2.增大可燃物与氧气的接触面积
一氧化碳
物理性质:
通常状况下,一氧化碳是一种无色无气味的剧毒气体,难溶于水。标准状况下其密度为1.28g/L,稍小于空气密度。
化学性质:
(1)可燃性:
一氧化碳
现象:
一氧化碳在空气中燃烧,产生蓝色火焰,放出大量热,产生气体使澄清石灰水变浑浊。
化学方程式:
2CO+O2 2CO2
点燃
(2)还原性:一氧化碳还原氧化铁实验(第五章)
化学性质:
一氧化碳
(3)毒性:
吸入人体的一氧化碳跟血液里的血红蛋白结合,使血红蛋白丧失了输氧功能,会导致人体缺氧。人吸入少量的一氧化碳就会感到头痛,吸入较多量的一氧化碳,就可能因缺少氧气而窒息死亡。
当发生一氧化碳中毒时,应立即打开门窗通风,并迅速将中毒者移至空气新鲜处,严重者应立即送医院救治。
问题一:一氧化碳从哪里来的呢?
燃料的不完全燃烧
汽车排放的废气
煤气的泄漏
如何避免一氧化碳中毒事件的发生呢?
加强室内通风;
保证燃料充分燃烧。
问题二
爆 炸
爆炸类型:
1.由物理膨胀导致的爆炸
2.由化学反应引起的爆炸
3.核爆炸
急速的燃烧发生在有限的空间内,短时间聚积大量的热,使气体的体积迅速膨胀,就会引起爆炸。
爆炸的条件:
1、有限空间内
2、急剧的燃烧
情况一:
如果氧气的浓度较高,或者可燃物(气体、粉尘)与氧气的接触面积很大,燃烧范围广,周围的空气迅速猛烈膨胀,也会发生爆炸。
情况二:
爆炸的条件:
氧气浓度较高,
或:可燃物与氧气的接触面积较大
如:点燃浸满液氧的棉花球
爆炸
如:加油站
反思
任何可燃性气体,可燃性固体粉末,与空气接触充分,遇明火都有可能发生爆炸。因此,汽油加油站、面粉加工场和煤矿坑道等场所,应杜绝一切火种,防止发生爆炸。 。
爆炸
常见气体的爆炸极限
气 体
爆炸极限(体积分数)
H2
4%----75%
CH4
5%----15%
CO
12.5%----74%
可燃性气体在点燃前必须检验纯度!
爆炸极限:容易导致爆炸的空气中可燃性气体的体积分数范围
爆炸
防火与灭火
易燃易爆物在遇到明火、高温或撞击时,极易发生燃烧和爆炸。
在生产、运输、使用、储存易燃物和易爆物时,一定要严格遵守有关规定,要严禁烟火,防止撞击和高温,决不允许违章操作。
灭火器
防火与灭火
泡沫灭火器,利用二氧化碳和水来覆盖在燃 烧物表面
适用范围:扑灭一些木材,橡胶等固体的初起火灾,但不适用于扑灭电器,油类物质起火。
干粉灭火器,利用高压二氧化碳作为动力,将干粉(主要含有碳酸氢钠和滑石粉等)覆盖在燃烧物表面
适用范围:扑灭油类、可燃气体和电气设备的初起火灾。
液态二氧化碳灭火器,主要是利用液态二氧化碳气化吸收热量,使燃烧物的温度达到着火点以下从而达到灭火的目的,并且产生的二氧化碳又能覆盖在燃烧物的表面。
你认识吗?
练习实践
1.下列有关燃烧与灭火的说法正确的是 ( )。
A.为防止森林大火蔓延可开挖隔离带,其目的是将可燃物与火隔离
B.房屋失火,消防队员用水灭火是为了降低可燃物的着火点
C.汽油放置在空气中没有燃烧是因为汽油不是可燃物
D.用灯帽盖灭酒精灯.是为了降低可燃物的温度
A
练习实践
2.为探究物质的燃烧条件,某同学进行了如右图所示的实验,下列有关说法正确的是 ( )。
A.现象①②说明物质燃烧需要达到一定的温度
B.现象②③说明物质燃烧需要氧气
C.现象③说明红磷不是可燃物
D.现象①③说明白磷的着火点比红磷的着火点低
D
练习实践
3.寒冷的冬季,常有人在房间里放置一个燃烧木炭的火盆取暖。请你谈谈采用这种方式取暖应注意的问题。
答:必须保持房间内空气的流通,有充足的氧气,使木炭能完全燃烧,避免产生一氧化碳气体,以免引起中毒;降低室内二氧化碳浓度,以免危害健康。
练习实践
4.为了安全,交通部门规定旅客乘坐车、船时,严禁随身携带易燃易爆物品。请列举一些你所知道的易燃易爆物品。
答:列举易燃易爆物如:酒精、打火机、气雾杀虫剂、烟花爆竹、火药、雷管、汽油、煤油、柴油等。
练习实践
5.室内起火时,为什么不能急于打开门窗?请说明其中的道理。从火灾现场逃生时,常要用湿毛巾捂住鼻子和嘴。你知道这一做法的理由吗?
答:室内发生火灾时,如果打开门窗,会使空气流通,造成火势加大。这时用湿毛巾捂住鼻子和嘴,主要作用是防止烟尘进入鼻子和嘴,起过滤作用。
练习实践
6.家庭用煤经过从“煤球”到“蜂窝煤”的变化。以前人们把煤粉加工成略大于乒乓球的球体,后来把煤粉加工成圆柱体,并在圆柱内打上一些孔。请你说说这种变化的优点是什么。
答:煤球加工成蜂窝煤,使煤与空气接触面积增大,容易完全燃烧。
练习实践
7.请你从燃烧获取能量和保护环境两个方面,谈谈燃料完全燃烧的重要性。使燃料完全燃烧的条件是什么?
答:获取能量:燃料完全燃烧,燃烧得快,放出的热量多;不完全燃烧,燃烧得慢,放出的热量少。
保护环境:不完全燃烧会生成有毒有污染物的物质。
使燃料完全燃烧的条件是可燃物与充足的氧气接触。
练习实践
8.许多工厂特别是化工厂,工人上班、来人参观都会被告知:“不允许穿鞋底带铁钉的鞋子。”你知道这是为什么吗?
答:穿有铁钉的鞋子,由于行走时产生火花,可能引起弥漫在空气中的可燃气体或粉尘发生燃烧爆炸。
燃烧
说出下列燃烧的现象
事例
观察到的现象
镁条燃烧
木炭在氧气中燃烧
红磷在空气中燃烧
硫在氧气中燃烧
铁丝在氧气中燃烧
氢气燃烧
归纳燃烧的特征
发出耀眼白光,放出大量热,产生白色固体
发出白光,放出大量热,产生气体使澄清石灰水变浑浊
黄色火焰,放出大量热,产生浓厚白烟
产生明亮的蓝紫色火焰,放出大量热,产生有刺激性气味气体
火星四射,放出大量热,产生黑色固体
产生淡蓝色火焰,放出大量热,火焰上罩一干冷烧杯,烧杯壁上有水雾
发光放热
燃烧的定义:
燃烧是一种发光、发热的剧烈的化学反应。
讨论:
物质燃烧需要哪些条件?
燃烧的条件
实验内容
实验现象
实验结论
取木条和玻璃棒在酒精灯火焰上加热,观察两种物质是否可以燃烧
将蜡烛点燃用烧杯罩住,观察
取小木条和纸条在酒精灯上点燃,观察燃烧所需时间
实验
木条能燃烧,玻璃棒不能燃烧
物质要有可燃性
蜡烛过一会熄灭
物质燃烧需要氧气
纸条比木条容易燃烧
物质燃烧需要达到一定温度
结合上述实验,我们可以得出物质燃烧需要同时满足三个条件:
1、物质具有可燃性
2、可燃物与氧气接触
3、可燃物达到燃烧所需要的最低温度
燃烧所需要的最低温度也叫着火点
燃烧的条件
实验
燃烧的条件
实验内容
实验现象
解释原因
将酒精和水以2:1体积混合,将一块棉布手绢浸入配好的混合液中,浸透后取出轻轻拧干,用镊子夹持在酒精灯上点燃,并轻轻抖动手绢。火熄灭后观察手绢有什么变化。
手绢没有燃烧损坏
酒精燃烧产生的热被水吸收,使温度达不到手绢的着火点,所以手绢不燃烧
灭火的方法
你能说出几种熄灭蜡烛火焰的方法
用嘴吹灭
用水浇灭
用烧杯盖灭
用剪刀剪去烛心
… …
灭火的方法:
1、将可燃物撤离燃烧区,与火源隔离
2、将燃着的可燃物与空气隔离
3、使用大量的冷却剂使燃烧物冷却,让燃烧物的温度降到着火点以下
完全燃烧和不完全燃烧
回顾:
用烧杯罩住燃烧的蜡烛时,除了蜡烛熄灭外,在烧杯底部还出现了什么现象?你能解释其中原因吗?
完全燃烧和不完全燃烧
当氧气充足时,可燃物完全燃烧,燃烧得快,放出的热量多,对环境污染小;当氧气不充足时,可燃物不完全燃烧,燃烧得慢,放出的热量少,对环境污染大。
完全燃烧和不完全燃烧
含碳、氢元素的可燃物完全燃烧时,碳、氢元素分别生成二氧化碳和水;当氧气不充足时,可燃物中的部分碳、氢元素生成一氧化碳、碳氢化合物等有毒气体和微小的炭黑颗粒等物质。
石墨、金刚石、木炭等燃烧均是如此!
完全燃烧与不完全燃烧的比较
完全燃烧
不完全燃烧
发生条件
燃烧速率
放出热量
燃烧产物
O2充足
O2不足
快
慢
多
少
二氧化碳和水
CO、碳氢化合物等有毒气体和炭黑等小颗粒
完全燃烧和不完全燃烧
为什么要使燃料完全燃烧?
完全燃烧
放出热量多
不完全燃烧会生成CO等有毒气体,污染大气
完全燃烧能
节约资源,保护环境
交流与讨论
总结与反思
在日常生活中,使燃料完全燃烧的具体做法有哪些呢?
1.提供充足的氧气
2.增大可燃物与氧气的接触面积
一氧化碳
物理性质:
通常状况下,一氧化碳是一种无色无气味的剧毒气体,难溶于水。标准状况下其密度为1.28g/L,稍小于空气密度。
化学性质:
(1)可燃性:
一氧化碳
现象:
一氧化碳在空气中燃烧,产生蓝色火焰,放出大量热,产生气体使澄清石灰水变浑浊。
化学方程式:
2CO+O2 2CO2
点燃
(2)还原性:一氧化碳还原氧化铁实验(第五章)
化学性质:
一氧化碳
(3)毒性:
吸入人体的一氧化碳跟血液里的血红蛋白结合,使血红蛋白丧失了输氧功能,会导致人体缺氧。人吸入少量的一氧化碳就会感到头痛,吸入较多量的一氧化碳,就可能因缺少氧气而窒息死亡。
当发生一氧化碳中毒时,应立即打开门窗通风,并迅速将中毒者移至空气新鲜处,严重者应立即送医院救治。
问题一:一氧化碳从哪里来的呢?
燃料的不完全燃烧
汽车排放的废气
煤气的泄漏
如何避免一氧化碳中毒事件的发生呢?
加强室内通风;
保证燃料充分燃烧。
问题二
爆 炸
爆炸类型:
1.由物理膨胀导致的爆炸
2.由化学反应引起的爆炸
3.核爆炸
急速的燃烧发生在有限的空间内,短时间聚积大量的热,使气体的体积迅速膨胀,就会引起爆炸。
爆炸的条件:
1、有限空间内
2、急剧的燃烧
情况一:
如果氧气的浓度较高,或者可燃物(气体、粉尘)与氧气的接触面积很大,燃烧范围广,周围的空气迅速猛烈膨胀,也会发生爆炸。
情况二:
爆炸的条件:
氧气浓度较高,
或:可燃物与氧气的接触面积较大
如:点燃浸满液氧的棉花球
爆炸
如:加油站
反思
任何可燃性气体,可燃性固体粉末,与空气接触充分,遇明火都有可能发生爆炸。因此,汽油加油站、面粉加工场和煤矿坑道等场所,应杜绝一切火种,防止发生爆炸。 。
爆炸
常见气体的爆炸极限
气 体
爆炸极限(体积分数)
H2
4%----75%
CH4
5%----15%
CO
12.5%----74%
可燃性气体在点燃前必须检验纯度!
爆炸极限:容易导致爆炸的空气中可燃性气体的体积分数范围
爆炸
防火与灭火
易燃易爆物在遇到明火、高温或撞击时,极易发生燃烧和爆炸。
在生产、运输、使用、储存易燃物和易爆物时,一定要严格遵守有关规定,要严禁烟火,防止撞击和高温,决不允许违章操作。
灭火器
防火与灭火
泡沫灭火器,利用二氧化碳和水来覆盖在燃 烧物表面
适用范围:扑灭一些木材,橡胶等固体的初起火灾,但不适用于扑灭电器,油类物质起火。
干粉灭火器,利用高压二氧化碳作为动力,将干粉(主要含有碳酸氢钠和滑石粉等)覆盖在燃烧物表面
适用范围:扑灭油类、可燃气体和电气设备的初起火灾。
液态二氧化碳灭火器,主要是利用液态二氧化碳气化吸收热量,使燃烧物的温度达到着火点以下从而达到灭火的目的,并且产生的二氧化碳又能覆盖在燃烧物的表面。
你认识吗?
练习实践
1.下列有关燃烧与灭火的说法正确的是 ( )。
A.为防止森林大火蔓延可开挖隔离带,其目的是将可燃物与火隔离
B.房屋失火,消防队员用水灭火是为了降低可燃物的着火点
C.汽油放置在空气中没有燃烧是因为汽油不是可燃物
D.用灯帽盖灭酒精灯.是为了降低可燃物的温度
A
练习实践
2.为探究物质的燃烧条件,某同学进行了如右图所示的实验,下列有关说法正确的是 ( )。
A.现象①②说明物质燃烧需要达到一定的温度
B.现象②③说明物质燃烧需要氧气
C.现象③说明红磷不是可燃物
D.现象①③说明白磷的着火点比红磷的着火点低
D
练习实践
3.寒冷的冬季,常有人在房间里放置一个燃烧木炭的火盆取暖。请你谈谈采用这种方式取暖应注意的问题。
答:必须保持房间内空气的流通,有充足的氧气,使木炭能完全燃烧,避免产生一氧化碳气体,以免引起中毒;降低室内二氧化碳浓度,以免危害健康。
练习实践
4.为了安全,交通部门规定旅客乘坐车、船时,严禁随身携带易燃易爆物品。请列举一些你所知道的易燃易爆物品。
答:列举易燃易爆物如:酒精、打火机、气雾杀虫剂、烟花爆竹、火药、雷管、汽油、煤油、柴油等。
练习实践
5.室内起火时,为什么不能急于打开门窗?请说明其中的道理。从火灾现场逃生时,常要用湿毛巾捂住鼻子和嘴。你知道这一做法的理由吗?
答:室内发生火灾时,如果打开门窗,会使空气流通,造成火势加大。这时用湿毛巾捂住鼻子和嘴,主要作用是防止烟尘进入鼻子和嘴,起过滤作用。
练习实践
6.家庭用煤经过从“煤球”到“蜂窝煤”的变化。以前人们把煤粉加工成略大于乒乓球的球体,后来把煤粉加工成圆柱体,并在圆柱内打上一些孔。请你说说这种变化的优点是什么。
答:煤球加工成蜂窝煤,使煤与空气接触面积增大,容易完全燃烧。
练习实践
7.请你从燃烧获取能量和保护环境两个方面,谈谈燃料完全燃烧的重要性。使燃料完全燃烧的条件是什么?
答:获取能量:燃料完全燃烧,燃烧得快,放出的热量多;不完全燃烧,燃烧得慢,放出的热量少。
保护环境:不完全燃烧会生成有毒有污染物的物质。
使燃料完全燃烧的条件是可燃物与充足的氧气接触。
练习实践
8.许多工厂特别是化工厂,工人上班、来人参观都会被告知:“不允许穿鞋底带铁钉的鞋子。”你知道这是为什么吗?
答:穿有铁钉的鞋子,由于行走时产生火花,可能引起弥漫在空气中的可燃气体或粉尘发生燃烧爆炸。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
