人教版(2019)化学必修一 同步课件 3.1.1铁单质和铁的氧化物(37张ppt)
文档属性
| 名称 | 人教版(2019)化学必修一 同步课件 3.1.1铁单质和铁的氧化物(37张ppt) |  | |
| 格式 | ppt | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-23 10:16:56 | ||
图片预览






文档简介
(共38张PPT)
必修第一册
人教版 高一上
第一节
铁及其化合物
第二节
金属材料
第三章
铁 金属材料
CONTENTS 本节内容
铁单质的性质
铁的存在和冶炼
二
一
铁的氧化物
三
课堂讲解
知识点一、铁的存在和冶炼
铁元素在自然界中的存在
1
铁元素在地壳中的含量低于___________,居________。在自然界中的形态有游离态和化合态,即
O、Si、Al
第四位
课堂讲解
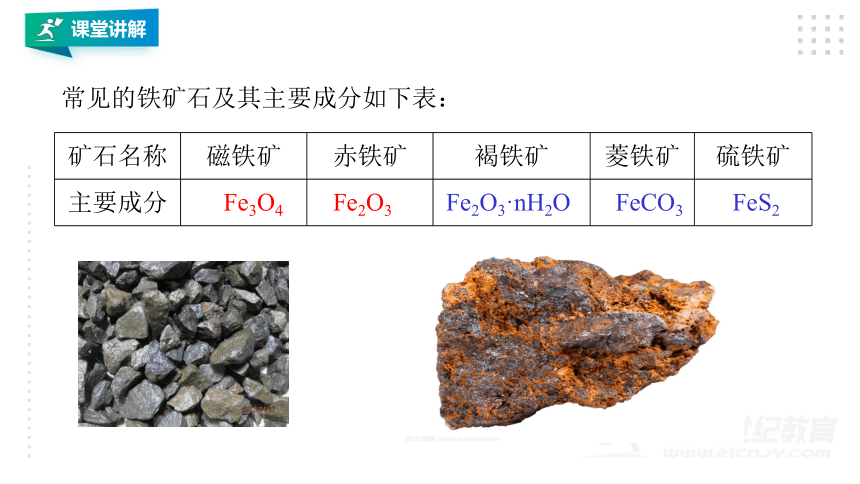
常见的铁矿石及其主要成分如下表:
矿石名称 磁铁矿 赤铁矿 褐铁矿 菱铁矿 硫铁矿
主要成分
FeS2
FeCO3
Fe2O3·nH2O
Fe3O4
Fe2O3
课堂讲解
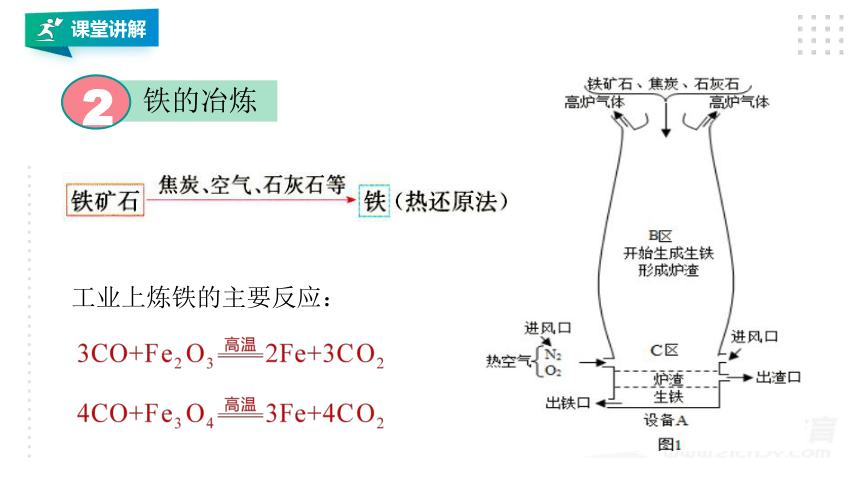
铁的冶炼
2
工业上炼铁的主要反应:
【例1】在高炉炼铁中将铁的氧化物还原成单质铁的主要还原剂是( )
A.CaCO3 B.C C.SiO2 D.CO
课堂练习
D
【例2】联合国卫生组织经过考核和研究,认为我国使用的铁锅是有益于人类健康的理想炊具,并向全世界推广。其主要原因是( )
A.价格便宜,不易生锈
B.铁锅含有碳元素
C.烹调的食物中留有人体需要的铁元素
D.传热慢,保温性能好
C
课堂练习
【例3】判断正误
(1)铁屑和沙子的混合物可用磁铁分离。( )
(2)铁是人体必需的微量元素。( )
(3)铁的导电性比铜和铝差。( )
(4)铁是一种黑色、无光泽的金属。( )
(5)菠菜等食品中富含铁元素。( )
√
√
√
√
×
二、铁单质的性质
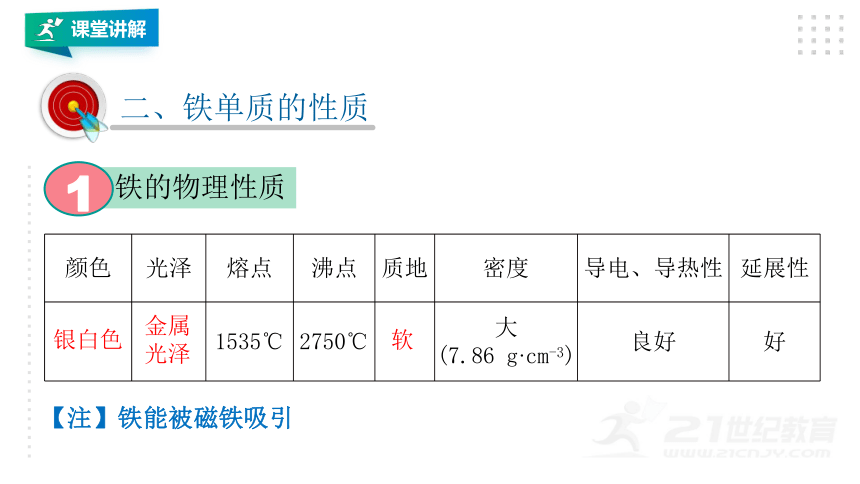
铁的物理性质
1
颜色 光泽 熔点 沸点 质地 密度 导电、导热性 延展性
1535℃ 2750℃ 大 (7.86 g·cm-3) 良好 好
【注】铁能被磁铁吸引
银白色
金属
光泽
软
课堂讲解
铁的化学性质
2
(1)铁与非金属单质反应
①在O2中燃烧
现象:剧烈燃烧,火星四射,放出大量的热,生成黑色固
化学方程式:
【注】常温下,铁在潮湿的空气中被锈蚀,铁锈的主要成分为Fe2O3·xH2O
课堂讲解
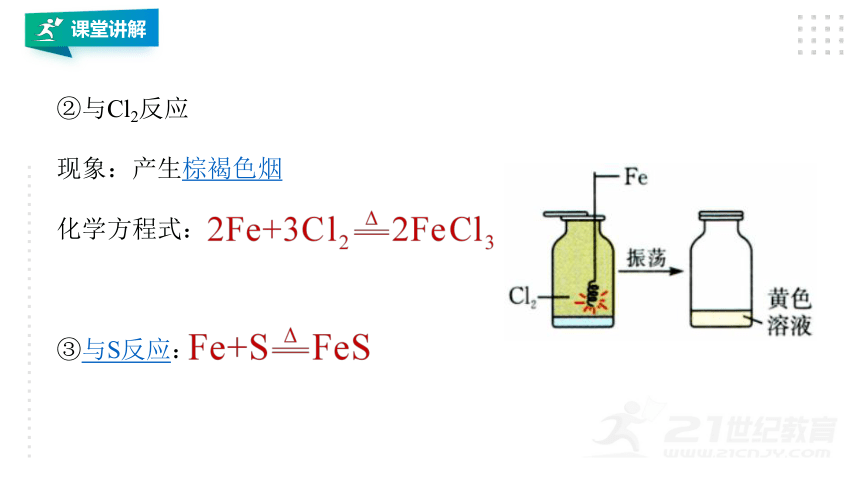
②与Cl2反应
现象:产生棕褐色烟
化学方程式:
③与S反应:
课堂讲解
(2)铁与酸的反应
①与盐酸、稀硫酸反应:
②与强氧化性酸反应
常温下,铁遇浓硫酸、浓硝酸会_____,表面生成致密氧化膜。铁与稀硝酸在常温下能反应但__________
钝化
不产生H2
课堂讲解
(3)铁与铜盐、铁盐等溶液的反应
Fe+CuSO4=Cu+FeSO4
Fe+2FeCl3=3FeCl2
课堂讲解
【结论】Fe在反应中作还原剂,遇到较强的氧化剂(如Cl2等)生成+3价铁的化合物,遇到较弱的氧化剂(如稀硫酸等)生成+2价铁的化合物。
(4)铁与水蒸气的反应
课堂讲解
实验装置图
实验操作
实验现象
化学方程式
在如图所示装置的试管中依次放入湿棉花和还原铁粉,加热。把生成的气体通入蒸发皿中的肥皂液中。一段时间后,用坩埚钳夹取燃着的火柴点燃肥皂泡,观察现象。实验结束时,应先从肥皂液中撤出导管,再移走燃着的酒精灯
红热的铁与水蒸气反应放出气体,蒸发皿中产生大量肥皂泡,用火柴点燃肥皂泡,能燃烧或发生爆鸣。反应后,试管中固体仍呈黑色
实验探究
【思考】
①湿棉花的作用是什么
在受热时提供反应所需的水蒸气
②实验中肥皂泡的作用是什么
肥皂泡是为了储存氢气,当点火时就会有爆鸣声,以此证明生成了氢气,方便检验产物
课堂讲解
【思考】
③将试管中铁粉与水蒸气加热,肥皂液冒泡,能说明铁与水蒸气在加热条件下发生了反应吗
因试管中气体受热膨胀,也会导致肥皂液冒泡,
故不能说明Fe与水蒸气发生了反应
④实验结束时,应先从肥皂液中撤出导管,再移走酒精灯,为什么
为了防止产生倒吸
课堂讲解
【思考】
利用如图装置也可以实现Fe与水蒸气的反应。反应开始时,应先点燃 _____处的酒精灯,其目的是________________________,若点燃顺序反了,可能有什么后果?
后果:
①Fe与O2生成了Fe3O4,无法与水蒸气反应
②Fe与水蒸气反应生成H2,在高温下与空气中的O2反应可能发生爆炸
课堂讲解
b
用水蒸气排装置内的空气
课堂练习
【例4】下列说法正确的是( )
A.我国在战国中期就开始使用铁制品
B.自然界中的铁元素只存在于化合物中
C.铁能与所有金属的盐溶液反应生成亚铁盐和金属
D.高炉炼铁是用还原剂将铁从它的化合物中还原出来
D
课堂练习
【例5】下列说法不正确的是( )
A.铁与纯氧气和水蒸气反应都能生成四氧化三铁
B.铁在高温下与水蒸气的反应是置换反应
C.Fe与盐酸反应的离子方程式为2Fe+6H+=2Fe3++3H2↑
D.铁与盐酸或水蒸气反应,都做还原剂
C
课堂练习
【例6】将一枚洁净的铁钉浸入稀硫酸中,下列叙述正确的是________
①铁钉表面产生气泡 ②溶液由无色逐渐变为浅绿色
③铁钉的质量减轻 ④溶液的质量减轻
①②③
课堂练习
【例7】等量的铁分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的体积比是_______
3:4
课堂练习
【例8】铁与下列物质反应能生成+3价铁盐的是( )
A.硫黄 B.稀硫酸 C.硫酸铜溶液 D.氯气
D
【例9】下列叙述中正确的是( )
A.Fe在少量Cl2中燃烧生成FeCl2
B.Fe与S混合加热生成FeS2
C.3 mol Fe单质完全转变为Fe3O4,失去8NA个电子
D.氧化性:Fe3+>Fe2+>Cu2+
课堂练习
C
【例10】某不纯铁片可能含有Mg、Al、Cu等金属杂质,取这种铁片5.6 g 与足量的稀盐酸反应,得到0.2 g氢气,则该铁片中( )
A.一定含有金属镁 B.一定含有金属铝
C.一定含有金属铜 D.一定同时含有四种金属
课堂练习
C
【例11】某学生以铁丝和Cl2为原料进行下列三个实验。从分类角度分析,下列说法正确的是( )
A.实验①②所涉及的物质均为电解质
B.实验①③发生的均为离子反应
C.实验②③均未发生氧化还原反应
D.实验①③反应制得的物质均为纯净物
课堂练习
C
课堂练习
【例12】(1)活泼金属如K、Na等可与冷水剧烈反应。写出K与水反应的离子方程式:__________________________。
(2)Mg与冷水反应缓慢,但与沸水反应现象明显。写出Mg与沸水反应的化学方程式:________________________。
(3)Fe、Zn等可以和水蒸气反应生成金属氧化物和H2。写出铁粉与水蒸气反应的化学方程式并用单线桥标出电子转移情况。
【例13】用如图所示装置进行Fe与水蒸气反应的
实验,下列有关说法不正确的是( )
A.装置A的作用是为实验提供持续不断的水蒸气
B.装置B中反应的化学方程式是2Fe+3H2O(g) Fe2O3+3H2
C.装置C中加入的固体干燥剂可能是碱石灰
D.点燃装置D处的气体前必须检验气体的纯度
课堂练习
B
【例14】如图在铁与水反应的实验中,下列做法不正确的是( )
A.试管中的铁粉用绕成团的细铁丝代替
B.将试管底部的湿棉花移到试管口处
C.用铁丝网罩住酒精灯火焰
D.点燃肥皂泡验证氢气的生成
课堂练习
B
(1)写出铁在高温下与水蒸气反应的
化学方程式:_____ 。
(2)干燥管C中盛放的药品是 _ ;干燥管的 (填“m”或“n”)
端与g导管相连接。
【例15】已知红热的铁能与水蒸气反应生成氢气。现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题。
课堂练习
碱石灰
n
(3)在D处画出用试管收集氢气的装置图(所需其他仪器自行选择)。
(4)怎样用简单的方法检验收集到的气体是氢气?简述实验操作步骤和现象: 。
(5)若收集到标准状况下的H2 22.4 L,则参
加反应的铁粉的质量为_____g。
(6)当固体质量增加32 g时,生成H2的质量为____g。
课堂练习
42
4
用拇指堵住试管口,试管口向上,靠近酒精灯火焰,松开拇指,发出爆鸣声,说明收集到的气体是H2
三、铁的氧化物
物质 氧化亚铁(FeO) 氧化铁(Fe2O3) 四氧化三铁(Fe3O4)
俗称
颜色、状态
与盐酸反应
(Fe3O4中Fe有+2、+3两种价态,可表示成FeO·Fe2O3形式)
稳定性
共性 用途 ——
磁性氧化铁
铁红
黑色粉末
黑色晶体
红棕色粉末
稳定
稳定
不溶于水,与CO、C、H2反应生成单质铁
Fe2O3常用作红色油漆与涂料,赤铁矿(主要成分是Fe2O3)是炼铁的原料
【例16】关于氧化铁、氧化亚铁、四氧化三铁三种氧化物的下列说法中不正确的是( )
A.铁元素化合价不完全相同
B.氧元素的化合价完全相同
C.氧化亚铁俗称铁红,为红棕色固体
D.铁在氧气中燃烧的产物为黑色固体
C
课堂练习
【例17】指南针是我国古代四大发明之一,制造指南针的磁性物质是( )
A.FeO B.Fe2O3 C.Fe3O4 D.Fe
C
课堂练习
【例18】有关铁的氧化物的说法中,不正确的是( )
A.赤铁矿主要成分是Fe2O3,Fe2O3是红棕色的,常用作红色油漆和涂料
B.Fe3O4是黑色晶体,其中的铁显+2价,的铁显+3价
C.FeO、Fe2O3、Fe3O4都不溶于水,但都能和盐酸反应生成相应的盐
D.FeO不稳定,在空气中加热迅速被氧化成Fe2O3
课堂练习
D
【例19】某铁的氧化物中铁元素和氧元素的质量比为21∶8,该氧化物的化学式可能是( )
A.FeO B.Fe2O3 C.Fe3O4 D.Fe4O5
C
课堂练习
课堂小结
https://www.21cnjy.com/help/help_extract.php
必修第一册
人教版 高一上
第一节
铁及其化合物
第二节
金属材料
第三章
铁 金属材料
CONTENTS 本节内容
铁单质的性质
铁的存在和冶炼
二
一
铁的氧化物
三
课堂讲解
知识点一、铁的存在和冶炼
铁元素在自然界中的存在
1
铁元素在地壳中的含量低于___________,居________。在自然界中的形态有游离态和化合态,即
O、Si、Al
第四位
课堂讲解
常见的铁矿石及其主要成分如下表:
矿石名称 磁铁矿 赤铁矿 褐铁矿 菱铁矿 硫铁矿
主要成分
FeS2
FeCO3
Fe2O3·nH2O
Fe3O4
Fe2O3
课堂讲解
铁的冶炼
2
工业上炼铁的主要反应:
【例1】在高炉炼铁中将铁的氧化物还原成单质铁的主要还原剂是( )
A.CaCO3 B.C C.SiO2 D.CO
课堂练习
D
【例2】联合国卫生组织经过考核和研究,认为我国使用的铁锅是有益于人类健康的理想炊具,并向全世界推广。其主要原因是( )
A.价格便宜,不易生锈
B.铁锅含有碳元素
C.烹调的食物中留有人体需要的铁元素
D.传热慢,保温性能好
C
课堂练习
【例3】判断正误
(1)铁屑和沙子的混合物可用磁铁分离。( )
(2)铁是人体必需的微量元素。( )
(3)铁的导电性比铜和铝差。( )
(4)铁是一种黑色、无光泽的金属。( )
(5)菠菜等食品中富含铁元素。( )
√
√
√
√
×
二、铁单质的性质
铁的物理性质
1
颜色 光泽 熔点 沸点 质地 密度 导电、导热性 延展性
1535℃ 2750℃ 大 (7.86 g·cm-3) 良好 好
【注】铁能被磁铁吸引
银白色
金属
光泽
软
课堂讲解
铁的化学性质
2
(1)铁与非金属单质反应
①在O2中燃烧
现象:剧烈燃烧,火星四射,放出大量的热,生成黑色固
化学方程式:
【注】常温下,铁在潮湿的空气中被锈蚀,铁锈的主要成分为Fe2O3·xH2O
课堂讲解
②与Cl2反应
现象:产生棕褐色烟
化学方程式:
③与S反应:
课堂讲解
(2)铁与酸的反应
①与盐酸、稀硫酸反应:
②与强氧化性酸反应
常温下,铁遇浓硫酸、浓硝酸会_____,表面生成致密氧化膜。铁与稀硝酸在常温下能反应但__________
钝化
不产生H2
课堂讲解
(3)铁与铜盐、铁盐等溶液的反应
Fe+CuSO4=Cu+FeSO4
Fe+2FeCl3=3FeCl2
课堂讲解
【结论】Fe在反应中作还原剂,遇到较强的氧化剂(如Cl2等)生成+3价铁的化合物,遇到较弱的氧化剂(如稀硫酸等)生成+2价铁的化合物。
(4)铁与水蒸气的反应
课堂讲解
实验装置图
实验操作
实验现象
化学方程式
在如图所示装置的试管中依次放入湿棉花和还原铁粉,加热。把生成的气体通入蒸发皿中的肥皂液中。一段时间后,用坩埚钳夹取燃着的火柴点燃肥皂泡,观察现象。实验结束时,应先从肥皂液中撤出导管,再移走燃着的酒精灯
红热的铁与水蒸气反应放出气体,蒸发皿中产生大量肥皂泡,用火柴点燃肥皂泡,能燃烧或发生爆鸣。反应后,试管中固体仍呈黑色
实验探究
【思考】
①湿棉花的作用是什么
在受热时提供反应所需的水蒸气
②实验中肥皂泡的作用是什么
肥皂泡是为了储存氢气,当点火时就会有爆鸣声,以此证明生成了氢气,方便检验产物
课堂讲解
【思考】
③将试管中铁粉与水蒸气加热,肥皂液冒泡,能说明铁与水蒸气在加热条件下发生了反应吗
因试管中气体受热膨胀,也会导致肥皂液冒泡,
故不能说明Fe与水蒸气发生了反应
④实验结束时,应先从肥皂液中撤出导管,再移走酒精灯,为什么
为了防止产生倒吸
课堂讲解
【思考】
利用如图装置也可以实现Fe与水蒸气的反应。反应开始时,应先点燃 _____处的酒精灯,其目的是________________________,若点燃顺序反了,可能有什么后果?
后果:
①Fe与O2生成了Fe3O4,无法与水蒸气反应
②Fe与水蒸气反应生成H2,在高温下与空气中的O2反应可能发生爆炸
课堂讲解
b
用水蒸气排装置内的空气
课堂练习
【例4】下列说法正确的是( )
A.我国在战国中期就开始使用铁制品
B.自然界中的铁元素只存在于化合物中
C.铁能与所有金属的盐溶液反应生成亚铁盐和金属
D.高炉炼铁是用还原剂将铁从它的化合物中还原出来
D
课堂练习
【例5】下列说法不正确的是( )
A.铁与纯氧气和水蒸气反应都能生成四氧化三铁
B.铁在高温下与水蒸气的反应是置换反应
C.Fe与盐酸反应的离子方程式为2Fe+6H+=2Fe3++3H2↑
D.铁与盐酸或水蒸气反应,都做还原剂
C
课堂练习
【例6】将一枚洁净的铁钉浸入稀硫酸中,下列叙述正确的是________
①铁钉表面产生气泡 ②溶液由无色逐渐变为浅绿色
③铁钉的质量减轻 ④溶液的质量减轻
①②③
课堂练习
【例7】等量的铁分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的体积比是_______
3:4
课堂练习
【例8】铁与下列物质反应能生成+3价铁盐的是( )
A.硫黄 B.稀硫酸 C.硫酸铜溶液 D.氯气
D
【例9】下列叙述中正确的是( )
A.Fe在少量Cl2中燃烧生成FeCl2
B.Fe与S混合加热生成FeS2
C.3 mol Fe单质完全转变为Fe3O4,失去8NA个电子
D.氧化性:Fe3+>Fe2+>Cu2+
课堂练习
C
【例10】某不纯铁片可能含有Mg、Al、Cu等金属杂质,取这种铁片5.6 g 与足量的稀盐酸反应,得到0.2 g氢气,则该铁片中( )
A.一定含有金属镁 B.一定含有金属铝
C.一定含有金属铜 D.一定同时含有四种金属
课堂练习
C
【例11】某学生以铁丝和Cl2为原料进行下列三个实验。从分类角度分析,下列说法正确的是( )
A.实验①②所涉及的物质均为电解质
B.实验①③发生的均为离子反应
C.实验②③均未发生氧化还原反应
D.实验①③反应制得的物质均为纯净物
课堂练习
C
课堂练习
【例12】(1)活泼金属如K、Na等可与冷水剧烈反应。写出K与水反应的离子方程式:__________________________。
(2)Mg与冷水反应缓慢,但与沸水反应现象明显。写出Mg与沸水反应的化学方程式:________________________。
(3)Fe、Zn等可以和水蒸气反应生成金属氧化物和H2。写出铁粉与水蒸气反应的化学方程式并用单线桥标出电子转移情况。
【例13】用如图所示装置进行Fe与水蒸气反应的
实验,下列有关说法不正确的是( )
A.装置A的作用是为实验提供持续不断的水蒸气
B.装置B中反应的化学方程式是2Fe+3H2O(g) Fe2O3+3H2
C.装置C中加入的固体干燥剂可能是碱石灰
D.点燃装置D处的气体前必须检验气体的纯度
课堂练习
B
【例14】如图在铁与水反应的实验中,下列做法不正确的是( )
A.试管中的铁粉用绕成团的细铁丝代替
B.将试管底部的湿棉花移到试管口处
C.用铁丝网罩住酒精灯火焰
D.点燃肥皂泡验证氢气的生成
课堂练习
B
(1)写出铁在高温下与水蒸气反应的
化学方程式:_____ 。
(2)干燥管C中盛放的药品是 _ ;干燥管的 (填“m”或“n”)
端与g导管相连接。
【例15】已知红热的铁能与水蒸气反应生成氢气。现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题。
课堂练习
碱石灰
n
(3)在D处画出用试管收集氢气的装置图(所需其他仪器自行选择)。
(4)怎样用简单的方法检验收集到的气体是氢气?简述实验操作步骤和现象: 。
(5)若收集到标准状况下的H2 22.4 L,则参
加反应的铁粉的质量为_____g。
(6)当固体质量增加32 g时,生成H2的质量为____g。
课堂练习
42
4
用拇指堵住试管口,试管口向上,靠近酒精灯火焰,松开拇指,发出爆鸣声,说明收集到的气体是H2
三、铁的氧化物
物质 氧化亚铁(FeO) 氧化铁(Fe2O3) 四氧化三铁(Fe3O4)
俗称
颜色、状态
与盐酸反应
(Fe3O4中Fe有+2、+3两种价态,可表示成FeO·Fe2O3形式)
稳定性
共性 用途 ——
磁性氧化铁
铁红
黑色粉末
黑色晶体
红棕色粉末
稳定
稳定
不溶于水,与CO、C、H2反应生成单质铁
Fe2O3常用作红色油漆与涂料,赤铁矿(主要成分是Fe2O3)是炼铁的原料
【例16】关于氧化铁、氧化亚铁、四氧化三铁三种氧化物的下列说法中不正确的是( )
A.铁元素化合价不完全相同
B.氧元素的化合价完全相同
C.氧化亚铁俗称铁红,为红棕色固体
D.铁在氧气中燃烧的产物为黑色固体
C
课堂练习
【例17】指南针是我国古代四大发明之一,制造指南针的磁性物质是( )
A.FeO B.Fe2O3 C.Fe3O4 D.Fe
C
课堂练习
【例18】有关铁的氧化物的说法中,不正确的是( )
A.赤铁矿主要成分是Fe2O3,Fe2O3是红棕色的,常用作红色油漆和涂料
B.Fe3O4是黑色晶体,其中的铁显+2价,的铁显+3价
C.FeO、Fe2O3、Fe3O4都不溶于水,但都能和盐酸反应生成相应的盐
D.FeO不稳定,在空气中加热迅速被氧化成Fe2O3
课堂练习
D
【例19】某铁的氧化物中铁元素和氧元素的质量比为21∶8,该氧化物的化学式可能是( )
A.FeO B.Fe2O3 C.Fe3O4 D.Fe4O5
C
课堂练习
课堂小结
https://www.21cnjy.com/help/help_extract.php
