辽宁省葫芦岛市普通高中2020-2021学年高一下学期期末学业质量监测化学试题 Word版含答案
文档属性
| 名称 | 辽宁省葫芦岛市普通高中2020-2021学年高一下学期期末学业质量监测化学试题 Word版含答案 |  | |
| 格式 | docx | ||
| 文件大小 | 806.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-23 14:56:16 | ||
图片预览



文档简介
葫芦岛市普通高中2020-2021学年高一下学期期末学业质量监测
化学
考生注意:
1.试卷满分100分,考试时间75分钟。
2.本考试分设试卷和答题纸。试卷包括Ⅰ卷和Ⅱ卷两部分。
3.答题前,务必在答题纸上按要求填写信息,并将核对后的条形码贴在指定位置上。作答必须涂或写在答题纸上,在试卷上作答一律不得分。Ⅰ卷部分的作答必须涂在答题纸上相应的区域,Ⅱ卷部分的作答必须写在答题纸上与试卷题号对应的位置。
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Al:27 S:32 Cl:35.5 Fe:56 Cu:64 Br:80 Ag:108 Ba:137
第Ⅰ卷(选择题,共45分)
一、选择题(本题包括15小题,每小题3分,共45分,每小题只有一个选项符合题意)
1.下列我国科研成果所涉及材料中,主要成分是有机物的是( )
A. C919发动机的新型材料氮化硅陶瓷
B.中国天眼用到传输信息用的光纤材料
C.“人造太阳”核聚变实验装置的钨合金
D.高铁轨道与地基之间填隙减震材料聚氨酯
2.下列金属中,通常用热分解法冶炼的是( )
A.银 B.铁 C.铝 D.钠
3.实验室中,下列行为不符合安全要求的是( )
A.点燃甲烷前,先验纯
B.铜与稀硝酸反应实验结束后,将废液倒入指定容器中
C.用手将灼热的蒸发皿拿离火焰,直接放在实验台上
D.稀释浓硫酸时,将浓硫酸沿烧杯壁缓缓倒入水中并不断搅拌
4.下列关于化学反应与能量的说法不正确的是( )
A.乙醇的燃烧是放热反应
B. Mg与盐酸的反应是吸热反应
C.反应物化学键的断裂娶吸收能量
D.化学反应伴随有能量的变化
5.下列说法正确的是( )
A.玻璃与酸不反应,可以盛放任何酸溶液
B.粗硅制备高纯硅的过程只发生了物理变化
C.富勒烯是一种烃类有机物
D.制造计算机芯片的材料主要是高纯度的硅
6.下列各组离子中,能在溶液中大量共存的一组是( )
A.false、false、false、false B.false、false、false、false
C.false、false、false、false D.false、false、false、false
7.以下化学用语表述正确的是( )
A.乙烯的结构简式:false B.false的空间充填模型:
C.乙醇的分子式:false D.羟基的电子式:false
8.下列说法错误的是( )
A.蛋白质都难溶于水
B.油脂可用于生产甘油
C.蔗糖可以发生水解反应生成葡萄糖和果糖
D.糖类、油脂、蛋白质均含C、H、O三种元素
9.下列物质的一氯代物只有一种的是( )
A.新戊烷 B.2-甲基丙烷 C.丙烷 D.乙醇
10.下列解释事实的方程式不正确的是( )
A.false遇HCl产生白烟:false
B.NO遇空气变为红棕色:false
C.false发生催化氧化反应生成NO:false
D.Cu与稀false混合产生无色气体:false
11.研究表明,氮氧化物(false)和二氧化硫形成雾霾的转化关系如下图所示。
下列关于雾霾及其形成的叙述中,不正确的是( )
A.与燃料燃烧有关
B.涉及氧化还原反应
C.false是形成无机颗粒物的催化剂
D.雾霾中含有false和false
12.可逆反应:false在不同条件下的反应速率如下,其中反应速率最快的是( )
A.false B.false
C.false D.false
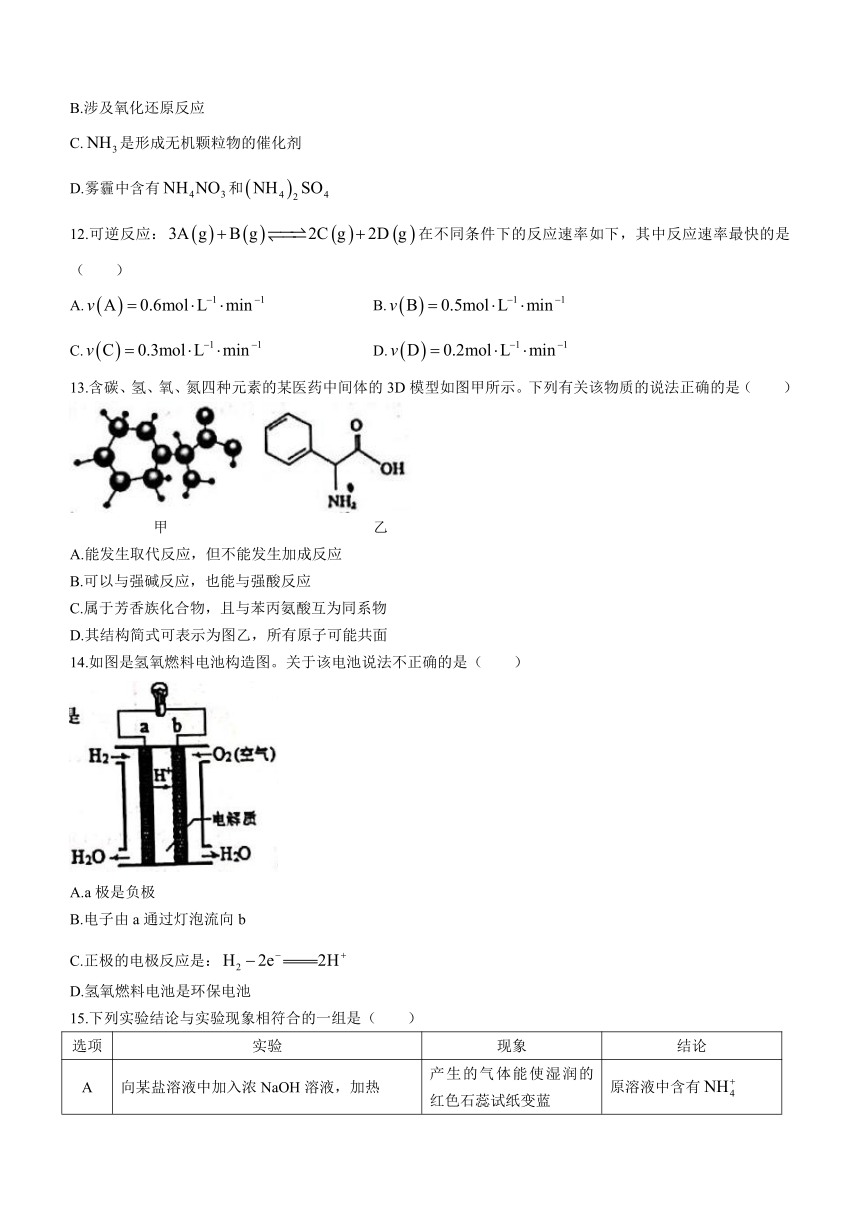
13.含碳、氢、氧、氮四种元素的某医药中间体的3D模型如图甲所示。下列有关该物质的说法正确的是( )
甲 乙
A.能发生取代反应,但不能发生加成反应
B.可以与强碱反应,也能与强酸反应
C.属于芳香族化合物,且与苯丙氨酸互为同系物
D.其结构简式可表示为图乙,所有原子可能共面
14.如图是氢氧燃料电池构造图。关于该电池说法不正确的是( )
A.a极是负极
B.电子由a通过灯泡流向b
C.正极的电极反应是:false
D.氢氧燃料电池是环保电池
15.下列实验结论与实验现象相符合的一组是( )
选项
实验
现象
结论
A
向某盐溶液中加入浓NaOH溶液,加热
产生的气体能使湿润的红色石蕊试纸变蓝
原溶液中含有false
B
把false通入紫色的酸性高锰酸钾溶液中
溶液紫色褪去
false具有漂白性
C
向蔗糖中滴加浓硫酸
蔗糖变黑
浓硫酸具有吸水性
D
向盛有Cu片的试管中加入稀false,无明显现象,再加入false固体
Cu片逐渐溶解,产生气泡,溶液变蓝
false是催化剂,可增大Cu与稀false反应的化学反应速率
第Ⅱ卷(非选择题,共55分)
二、非选择题(本题包括4小题,共55分)
16.(8分)化学能在一定条件下可转化为电能。
(1)将锌片放入盛有稀硫酸的烧杯中,反应的离子方程式是 。
(2)将锌片、铜片按照图所示装置连接,能证明化学能转化为电能的实验现象是:铜片上有气泡产生、 。
(3)稀硫酸在图所示装置中的作用是:传导离子、 。
(4)下列反应通过原电池装置,可实现化学能直接转化为电能的是 (填序号)。
①false
②false
③false
17.(19分)false具有广泛的用途。
Ⅰ.验室常用如图所示装置制取并收集false。
图1 图2
(1)实验室用false和false制取false的化学方程式为 。
(2)干燥false应选用的干燥剂是 。
(3)图1中方框内收集false的装置可选用图2中的 (填序号)。理由是 。
(4)尾气处理装置中使用倒置漏斗的作用是 。
Ⅱ.合成氨的反应对人类解决粮食问题贡献巨大。
反应为false。一定温度下,向恒容的密闭容器中充入一定量的false和false发生反应,测得各组分浓度随时间变化如图所示。
(5)表示false变化的曲线是 (填“A”“B”或“C”)。
(6)0~false时用false表示的化学反应速率:false false。
(7)下列能说明该反应达到平衡状态的是 (填序号,可多选)。
a容器中的压强不随时间变化
b.false
c.容器中混合气体的密度不随时间变化
d.断裂3molH—H键的同时断裂6molN—H键
(8)人们曾认为false化学反应速率小,请写出两条能增大正反应速率的措施 。
18.(12分)海水资源的利用具有广阔的前景。从海水中提取false与false的流程如下:
(1)为节约成本,试剂①最好选用 。[填“NaOH”或“false”]
(2)提取溴过程中,从“溶液1”到“溶液4”,两次进行false的转化,目的是 。
(3)提取溴过程中,形成“溶液3”的化学方程式是 。
(4)用原子结构原理解释false的氧化性强于false的原因 。
(5)提镁过程中,加入试剂②发生反应的离子方程式是 。
(6)从false溶液获得false晶体的主要操作为 。
19.(16分)乙烯是重要化工原料。结合以下路线回答下列问题。
(1)反应①的化学方程式是 。
(2)B的官能团是 。
(3)反应④的化学方程式是 。
(4)F是一种高分子物质,可用于制作食品塑料袋等,F的结构简式是 。
(5)E的分子式是false能使紫色石蕊试液变红;G是一种油状、有香味的物质,实验室用D和E通过反应⑥制取G,裝置如图所示。
①甲试管中反应的化学方程式是 ;反应类型是 。
②分离出试管乙中油状液体用到的主要仪器是 。
③如果将4.6gD和3gE在催化剂条件下发生上述反应,充分反应后,如果实际产率为60%,实际得到G的质量是 g。(已知:实际产率=实际得到质量/理论计算质量)
(6)丙烯(false)与乙烯互为同系物,在催化剂、加热条件下与false反应生成一种重要的化工原料丙烯酸(false)。下列关于丙烯酸的说法正确的是 。
a与乙酸互为同系物
b.能发生加成、酯化、氧化反应
c.能与false溶液反应
d.一定条件下能发生加聚反应,生成
葫芦岛市普通高中2020-2021学年高一下学期期末学业质量监测
化学参考答案及评分标准
一、选择题(每小题3分,共45分)
1.D 2.A 3.C 4.B 5.D 6.B 7.B 8.A 9.A 10.D
11.C 12.C 13.B 14.C 15.A
二、非选择题(共55分)
5313045723908分
8分
16.(8分)
(1).Zn + 2H+=Zn2++ H2↑
(2).电流表指针偏转
(3) 参与电极反应
(4) ①③
17.(19分)
531304514668510分
10分
(1)Ca(OH)2+2NH4ClCaCl2+2NH3↑+2H2O (2分)
(2)碱石灰(2分)
(3) ②(2分) ;氨气密度比空气小,需要用向下排空气法(2分)
52038252781309分
9分
(4) 防止倒吸(2分)
(5) A(1分)(6)false(2分)(7)ad(2分)
(8)加入催化剂;增大氮气或氢气的浓度;增大压强;升高温度。(4分)
54565551739906分
6分
18.(12分)
53130458858256分
6分
(1) Ca(OH)2 (2分)
(2) 富集溴 (2分)
(3. Br2+SO2+2H2O=2HBr+H2SO4 (2分)
(4) 氯原子半径较小,得电子的能力更强 (2分)
(5) Mg(OH)2+2H+=Mg2++2H2O (2分)
(6) 蒸发浓缩、冷却结晶、过滤(2分)
19.(16分)
53130457340607分
7分
(1) CH2=CH2+Br2=BrCH2CH2Br (2分)
(2) 羟基(-OH)(1分)
(3)false (2分)
(4) (2分)
50463456477009分
9分
(5) ①false (2分) ; 酯化反应(或取代反应) (1分)
②分液漏斗 (2分)
③ 2.64g (2分)
(6) bc(2分)
化学
考生注意:
1.试卷满分100分,考试时间75分钟。
2.本考试分设试卷和答题纸。试卷包括Ⅰ卷和Ⅱ卷两部分。
3.答题前,务必在答题纸上按要求填写信息,并将核对后的条形码贴在指定位置上。作答必须涂或写在答题纸上,在试卷上作答一律不得分。Ⅰ卷部分的作答必须涂在答题纸上相应的区域,Ⅱ卷部分的作答必须写在答题纸上与试卷题号对应的位置。
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Al:27 S:32 Cl:35.5 Fe:56 Cu:64 Br:80 Ag:108 Ba:137
第Ⅰ卷(选择题,共45分)
一、选择题(本题包括15小题,每小题3分,共45分,每小题只有一个选项符合题意)
1.下列我国科研成果所涉及材料中,主要成分是有机物的是( )
A. C919发动机的新型材料氮化硅陶瓷
B.中国天眼用到传输信息用的光纤材料
C.“人造太阳”核聚变实验装置的钨合金
D.高铁轨道与地基之间填隙减震材料聚氨酯
2.下列金属中,通常用热分解法冶炼的是( )
A.银 B.铁 C.铝 D.钠
3.实验室中,下列行为不符合安全要求的是( )
A.点燃甲烷前,先验纯
B.铜与稀硝酸反应实验结束后,将废液倒入指定容器中
C.用手将灼热的蒸发皿拿离火焰,直接放在实验台上
D.稀释浓硫酸时,将浓硫酸沿烧杯壁缓缓倒入水中并不断搅拌
4.下列关于化学反应与能量的说法不正确的是( )
A.乙醇的燃烧是放热反应
B. Mg与盐酸的反应是吸热反应
C.反应物化学键的断裂娶吸收能量
D.化学反应伴随有能量的变化
5.下列说法正确的是( )
A.玻璃与酸不反应,可以盛放任何酸溶液
B.粗硅制备高纯硅的过程只发生了物理变化
C.富勒烯是一种烃类有机物
D.制造计算机芯片的材料主要是高纯度的硅
6.下列各组离子中,能在溶液中大量共存的一组是( )
A.false、false、false、false B.false、false、false、false
C.false、false、false、false D.false、false、false、false
7.以下化学用语表述正确的是( )
A.乙烯的结构简式:false B.false的空间充填模型:
C.乙醇的分子式:false D.羟基的电子式:false
8.下列说法错误的是( )
A.蛋白质都难溶于水
B.油脂可用于生产甘油
C.蔗糖可以发生水解反应生成葡萄糖和果糖
D.糖类、油脂、蛋白质均含C、H、O三种元素
9.下列物质的一氯代物只有一种的是( )
A.新戊烷 B.2-甲基丙烷 C.丙烷 D.乙醇
10.下列解释事实的方程式不正确的是( )
A.false遇HCl产生白烟:false
B.NO遇空气变为红棕色:false
C.false发生催化氧化反应生成NO:false
D.Cu与稀false混合产生无色气体:false
11.研究表明,氮氧化物(false)和二氧化硫形成雾霾的转化关系如下图所示。
下列关于雾霾及其形成的叙述中,不正确的是( )
A.与燃料燃烧有关
B.涉及氧化还原反应
C.false是形成无机颗粒物的催化剂
D.雾霾中含有false和false
12.可逆反应:false在不同条件下的反应速率如下,其中反应速率最快的是( )
A.false B.false
C.false D.false
13.含碳、氢、氧、氮四种元素的某医药中间体的3D模型如图甲所示。下列有关该物质的说法正确的是( )
甲 乙
A.能发生取代反应,但不能发生加成反应
B.可以与强碱反应,也能与强酸反应
C.属于芳香族化合物,且与苯丙氨酸互为同系物
D.其结构简式可表示为图乙,所有原子可能共面
14.如图是氢氧燃料电池构造图。关于该电池说法不正确的是( )
A.a极是负极
B.电子由a通过灯泡流向b
C.正极的电极反应是:false
D.氢氧燃料电池是环保电池
15.下列实验结论与实验现象相符合的一组是( )
选项
实验
现象
结论
A
向某盐溶液中加入浓NaOH溶液,加热
产生的气体能使湿润的红色石蕊试纸变蓝
原溶液中含有false
B
把false通入紫色的酸性高锰酸钾溶液中
溶液紫色褪去
false具有漂白性
C
向蔗糖中滴加浓硫酸
蔗糖变黑
浓硫酸具有吸水性
D
向盛有Cu片的试管中加入稀false,无明显现象,再加入false固体
Cu片逐渐溶解,产生气泡,溶液变蓝
false是催化剂,可增大Cu与稀false反应的化学反应速率
第Ⅱ卷(非选择题,共55分)
二、非选择题(本题包括4小题,共55分)
16.(8分)化学能在一定条件下可转化为电能。
(1)将锌片放入盛有稀硫酸的烧杯中,反应的离子方程式是 。
(2)将锌片、铜片按照图所示装置连接,能证明化学能转化为电能的实验现象是:铜片上有气泡产生、 。
(3)稀硫酸在图所示装置中的作用是:传导离子、 。
(4)下列反应通过原电池装置,可实现化学能直接转化为电能的是 (填序号)。
①false
②false
③false
17.(19分)false具有广泛的用途。
Ⅰ.验室常用如图所示装置制取并收集false。
图1 图2
(1)实验室用false和false制取false的化学方程式为 。
(2)干燥false应选用的干燥剂是 。
(3)图1中方框内收集false的装置可选用图2中的 (填序号)。理由是 。
(4)尾气处理装置中使用倒置漏斗的作用是 。
Ⅱ.合成氨的反应对人类解决粮食问题贡献巨大。
反应为false。一定温度下,向恒容的密闭容器中充入一定量的false和false发生反应,测得各组分浓度随时间变化如图所示。
(5)表示false变化的曲线是 (填“A”“B”或“C”)。
(6)0~false时用false表示的化学反应速率:false false。
(7)下列能说明该反应达到平衡状态的是 (填序号,可多选)。
a容器中的压强不随时间变化
b.false
c.容器中混合气体的密度不随时间变化
d.断裂3molH—H键的同时断裂6molN—H键
(8)人们曾认为false化学反应速率小,请写出两条能增大正反应速率的措施 。
18.(12分)海水资源的利用具有广阔的前景。从海水中提取false与false的流程如下:
(1)为节约成本,试剂①最好选用 。[填“NaOH”或“false”]
(2)提取溴过程中,从“溶液1”到“溶液4”,两次进行false的转化,目的是 。
(3)提取溴过程中,形成“溶液3”的化学方程式是 。
(4)用原子结构原理解释false的氧化性强于false的原因 。
(5)提镁过程中,加入试剂②发生反应的离子方程式是 。
(6)从false溶液获得false晶体的主要操作为 。
19.(16分)乙烯是重要化工原料。结合以下路线回答下列问题。
(1)反应①的化学方程式是 。
(2)B的官能团是 。
(3)反应④的化学方程式是 。
(4)F是一种高分子物质,可用于制作食品塑料袋等,F的结构简式是 。
(5)E的分子式是false能使紫色石蕊试液变红;G是一种油状、有香味的物质,实验室用D和E通过反应⑥制取G,裝置如图所示。
①甲试管中反应的化学方程式是 ;反应类型是 。
②分离出试管乙中油状液体用到的主要仪器是 。
③如果将4.6gD和3gE在催化剂条件下发生上述反应,充分反应后,如果实际产率为60%,实际得到G的质量是 g。(已知:实际产率=实际得到质量/理论计算质量)
(6)丙烯(false)与乙烯互为同系物,在催化剂、加热条件下与false反应生成一种重要的化工原料丙烯酸(false)。下列关于丙烯酸的说法正确的是 。
a与乙酸互为同系物
b.能发生加成、酯化、氧化反应
c.能与false溶液反应
d.一定条件下能发生加聚反应,生成
葫芦岛市普通高中2020-2021学年高一下学期期末学业质量监测
化学参考答案及评分标准
一、选择题(每小题3分,共45分)
1.D 2.A 3.C 4.B 5.D 6.B 7.B 8.A 9.A 10.D
11.C 12.C 13.B 14.C 15.A
二、非选择题(共55分)
5313045723908分
8分
16.(8分)
(1).Zn + 2H+=Zn2++ H2↑
(2).电流表指针偏转
(3) 参与电极反应
(4) ①③
17.(19分)
531304514668510分
10分
(1)Ca(OH)2+2NH4ClCaCl2+2NH3↑+2H2O (2分)
(2)碱石灰(2分)
(3) ②(2分) ;氨气密度比空气小,需要用向下排空气法(2分)
52038252781309分
9分
(4) 防止倒吸(2分)
(5) A(1分)(6)false(2分)(7)ad(2分)
(8)加入催化剂;增大氮气或氢气的浓度;增大压强;升高温度。(4分)
54565551739906分
6分
18.(12分)
53130458858256分
6分
(1) Ca(OH)2 (2分)
(2) 富集溴 (2分)
(3. Br2+SO2+2H2O=2HBr+H2SO4 (2分)
(4) 氯原子半径较小,得电子的能力更强 (2分)
(5) Mg(OH)2+2H+=Mg2++2H2O (2分)
(6) 蒸发浓缩、冷却结晶、过滤(2分)
19.(16分)
53130457340607分
7分
(1) CH2=CH2+Br2=BrCH2CH2Br (2分)
(2) 羟基(-OH)(1分)
(3)false (2分)
(4) (2分)
50463456477009分
9分
(5) ①false (2分) ; 酯化反应(或取代反应) (1分)
②分液漏斗 (2分)
③ 2.64g (2分)
(6) bc(2分)
同课章节目录
