《大自然中的二氧化碳》 说课课件
文档属性
| 名称 | 《大自然中的二氧化碳》 说课课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-05-21 00:00:00 | ||
图片预览







文档简介
(共30张PPT)
威远县严陵中学 袁正超
2、教材的地位和作用
* 承上:本节课是学生在学习了化石燃料及其利用之后,学习了氧气的性质、制法、用途之后又一重要的化学物质,二氧化碳是学生熟悉的物质,但学生还不能系统地了解二氧化碳在自然界中的循环和二氧化碳的含量增加对环境的影响 ,教师从引导学生从对课本中两个图片提供的信息分析入手,在更高的层次上去系统地认识二氧化碳 。通过二氧化碳性质的探究实验,知道二氧化碳的性质,了解人类研究化学物质的一般方法——实验法。
启下:为学习《酸、碱》的知识起到铺垫作用
1、教材内容:初中化学教材(山东版)上册第四章第四节《大自然中的二氧化碳》,完成本节课新课内容需要3课时,本节课主要学习二氧化碳的性质和用途。
了解二氧化碳在自然界物质循环中的地位、作用,认识二氧化碳对人类生活和生产的作用,激发学生的好奇心和探究欲;培养学生对环境的关注及理论联系实际的方法。发扬善于合作、勤于思考、勇于创新和实践的精神。
通过实验探究认识二氧化碳的物理和化学性质;了解二氧化碳
在自然界碳循环中的作用以及对人类生活和生产的意义。
初步学会运用观察、实验等方法获取信息;初步学会用归纳、概括、对比等方法对获取的信息进行加工;培养学生分析、加工处理图片信息的能力;学会研究物质性质的基本方法。
⑴、知识与技能:
⑵、过程与方法:
⑶、情感态度与价值观:
重点:二氧化碳的性质、制法与用途
难点:二氧化碳与水、澄清石灰水的化学反应原理
我采用实验探究教学法。主要是通过学生:发现问题→设计实验→实验探究→观察→分析、归纳解决问题→反思等一系列学习活动过程;这样充分调动学生的学习积极性和主动性,激发学生学习化学的兴趣,保持学生学习化学的兴趣,体验学习化学的快乐,使学生学会“探究学习、合作学习、自主学习”。在教学过程中,以问题为中心组织教学,将新知识置于问题情境当中,启发学生探索和发现,激发学生思维,让学生分析问题,解决问题,并把化学思维引入课堂。
1.注意实验探究,它是获得化学知识的重要途径,主动地体验探究活动在知识的形成、联系、应用过程中的作用,养成科学的学习态度,掌握科学的学习方法,培养观察、分析、归纳、总结问题的能力,从而提高学生解决问题的能力;
2、合作学习法,让学生分组准备实验,分组讨论,使学生在交流中取长补短,培养学生的合作竞争意识;
3、重视理论联系实际,注重对生产、生活现象的本质理解和认识。
实验准备:学生分组(2人为一小组):收集二氧化碳3瓶、试管、紫色石蕊试液、盐酸、酒精灯、试管夹、火柴、装梯形铁皮高低不同蜡烛r烧杯、澄清石灰水、托盘天平、烧杯、一个装满二氧化碳的矿泉水瓶、玻璃导管。 课前布置学生预习,
①阅读课本P106—P110;
②分组准备有关的实验。
从而培养学生的课前预习能力,阅读能力。
三、教具准备:多媒体、分组实验
四、教学程序设计
问题情景:你知道吗?
人造舞台云雾
人工降雨
O C O
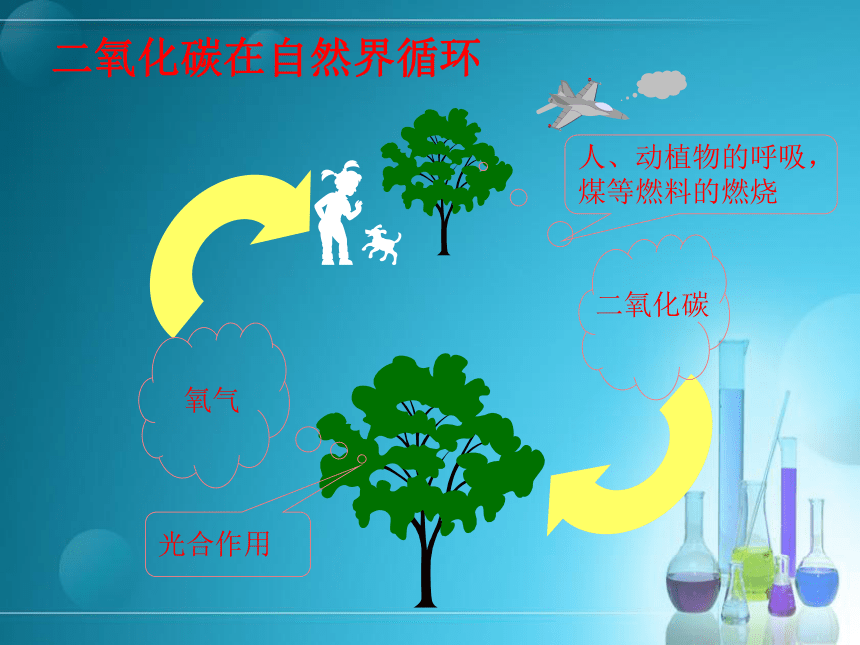
二氧化碳
氧气
人、动植物的呼吸,
煤等燃料的燃烧
光合作用
二氧化碳在自然界循环
温室效应的产生、危害、防治
P109实验探究二氧化碳的物理性质?
(2个同学为一个小组,老师指导)
得出结论:
1、通常情况下是无色、无味的气体。
一瓶收满
二氧化碳气体
得出结论:
2、通常情况下二氧化碳的密度比空气大。
得出结论:
3、能溶于水(通常状况下体积比1:1),压强增大溶解量增大。
1、通常情况下是无色、无气味的气体。
3、能溶于水(通常状况下体积比1:1),压强增大溶解量增大。
2、通常情况下二氧化碳的密度比空气大。
CO2的三态变化
CO2气体
无色液体
雪花状固体
干 冰
加压
降温
降温
压缩
101kPa
-78.5 0C
升华
干冰形成的示意图
干冰不是冰,是
二氧化碳的固体。
P109实验探究二氧化碳的化学性质
CO2
CO2
得出结论
1、一般情况下,CO2不能燃烧,也不能支持燃烧。
用途:二氧化碳可以灭火。
(所有的火都能用二氧化碳来灭吗?课后查资料)
现象:下面的蜡烛先熄灭,上面的蜡烛后熄灭。
菜 窖
[讨论] 进入一些久未开启的菜窖、干涸的深井及深洞的底部等CO2含量比较大的地方之前,如何保证人身安全?
做灯火熄灭实验
讲死狗洞的故事:
说明二氧化碳不能供人呼吸
如何证明二氧化碳与水反应了呢?(说明紫色石蕊是一种色素,是紫色的固体,把它溶解在蒸馏水中得到紫色的石蕊试液,酸性物质能使它变成红色。)
(5-1A)在A试管的紫色石蕊溶液中滴入稀盐酸,观察现象;
(5-2B)在 B试管的紫色石蕊溶液中滴入实验三的矿泉水瓶中的液体,观察现象。
稀盐酸
石 蕊 溶 液
观察:它们都能使紫色石蕊试液变红。
A
B
二氧化碳的水溶液
(2)(问题):是什么物质使紫色石蕊变红呢?
老师引导学生猜想:
①是CO2?②是H2O?③是CO2和H2O反应生成的新物质?
(讨论设计实验):根据自己的猜想,设计一个实验来进行验证。
CO2+H2O = H2CO3 现象:石蕊由紫色变成红色
得出:二氧化碳的水溶液中有一种酸性物质
分析、对比现象:
CO2
CO2
石蕊固体
石 蕊 溶 液
在石蕊固体和石蕊溶液中分别通入二氧化碳气体
盐酸
对比得出结论:是二氧化碳和水反应生成的物质(碳酸)使紫色石蕊变红
CO2+H2O = H2CO3 现象:石蕊由紫色变成红色
探究实验: 加热含有石蕊的二氧化碳的水溶液?观察现象。
讨论得出:碳酸不稳定受热易分解
化学方程式:H2CO3 = CO2↑ +H2O
▲
现象:石蕊由红色变成紫色
观察现象。
现象:澄清石灰水变浑浊
化学方程式:CO2+ Ca(OH)2 = H2O +CaCO3 ↓(检验CO2)
二、CO2的化学性质
1、一般情况下,CO2既不能燃烧,也不能支持燃烧,CO2不能供呼吸。
2、CO2跟水反应。
CO2+H2O = H2CO3 现象:石蕊由紫色变成红色
H2CO3 = CO2↑ +H2O 现象:石蕊由红色变成紫色
3、CO2与石灰水[Ca(OH)2]反应。
CO2+ Ca(OH)2 = H2O +CaCO3 ↓(鉴定CO2的重要方法)
CO2
纯碱
汽水
尿素
人工降雨
温度计
灭火
工业原料
致冷剂
光合作用
三、CO2的用途
温室中气体肥料
(A) 课本P111练习第1、2、3题;
(B) 练习册 P55习题第1-7题
本节课采用了探究实验、观察、对比、合作、分析、表达等的方法,从实际生活中的问题出发,通过研究物质的一般方法,探究了二氧化碳的性质、用途,体现了化学产生于生活,又服务于生活,发挥了学生的主观能动性,体现了学生是学习的主体,真正成为学习的主人。这节课由于学生实验多,让学生进行实验探究时注意强调实验操作的规范性,小组成员要密切的合作,还要合理安排40分钟,并且还要布置好习题做好知识点的巩固。
练习:通过练习巩固提高
六、说课反思:
二氧化碳的循环
威远县严陵中学 袁正超
2、教材的地位和作用
* 承上:本节课是学生在学习了化石燃料及其利用之后,学习了氧气的性质、制法、用途之后又一重要的化学物质,二氧化碳是学生熟悉的物质,但学生还不能系统地了解二氧化碳在自然界中的循环和二氧化碳的含量增加对环境的影响 ,教师从引导学生从对课本中两个图片提供的信息分析入手,在更高的层次上去系统地认识二氧化碳 。通过二氧化碳性质的探究实验,知道二氧化碳的性质,了解人类研究化学物质的一般方法——实验法。
启下:为学习《酸、碱》的知识起到铺垫作用
1、教材内容:初中化学教材(山东版)上册第四章第四节《大自然中的二氧化碳》,完成本节课新课内容需要3课时,本节课主要学习二氧化碳的性质和用途。
了解二氧化碳在自然界物质循环中的地位、作用,认识二氧化碳对人类生活和生产的作用,激发学生的好奇心和探究欲;培养学生对环境的关注及理论联系实际的方法。发扬善于合作、勤于思考、勇于创新和实践的精神。
通过实验探究认识二氧化碳的物理和化学性质;了解二氧化碳
在自然界碳循环中的作用以及对人类生活和生产的意义。
初步学会运用观察、实验等方法获取信息;初步学会用归纳、概括、对比等方法对获取的信息进行加工;培养学生分析、加工处理图片信息的能力;学会研究物质性质的基本方法。
⑴、知识与技能:
⑵、过程与方法:
⑶、情感态度与价值观:
重点:二氧化碳的性质、制法与用途
难点:二氧化碳与水、澄清石灰水的化学反应原理
我采用实验探究教学法。主要是通过学生:发现问题→设计实验→实验探究→观察→分析、归纳解决问题→反思等一系列学习活动过程;这样充分调动学生的学习积极性和主动性,激发学生学习化学的兴趣,保持学生学习化学的兴趣,体验学习化学的快乐,使学生学会“探究学习、合作学习、自主学习”。在教学过程中,以问题为中心组织教学,将新知识置于问题情境当中,启发学生探索和发现,激发学生思维,让学生分析问题,解决问题,并把化学思维引入课堂。
1.注意实验探究,它是获得化学知识的重要途径,主动地体验探究活动在知识的形成、联系、应用过程中的作用,养成科学的学习态度,掌握科学的学习方法,培养观察、分析、归纳、总结问题的能力,从而提高学生解决问题的能力;
2、合作学习法,让学生分组准备实验,分组讨论,使学生在交流中取长补短,培养学生的合作竞争意识;
3、重视理论联系实际,注重对生产、生活现象的本质理解和认识。
实验准备:学生分组(2人为一小组):收集二氧化碳3瓶、试管、紫色石蕊试液、盐酸、酒精灯、试管夹、火柴、装梯形铁皮高低不同蜡烛r烧杯、澄清石灰水、托盘天平、烧杯、一个装满二氧化碳的矿泉水瓶、玻璃导管。 课前布置学生预习,
①阅读课本P106—P110;
②分组准备有关的实验。
从而培养学生的课前预习能力,阅读能力。
三、教具准备:多媒体、分组实验
四、教学程序设计
问题情景:你知道吗?
人造舞台云雾
人工降雨
O C O
二氧化碳
氧气
人、动植物的呼吸,
煤等燃料的燃烧
光合作用
二氧化碳在自然界循环
温室效应的产生、危害、防治
P109实验探究二氧化碳的物理性质?
(2个同学为一个小组,老师指导)
得出结论:
1、通常情况下是无色、无味的气体。
一瓶收满
二氧化碳气体
得出结论:
2、通常情况下二氧化碳的密度比空气大。
得出结论:
3、能溶于水(通常状况下体积比1:1),压强增大溶解量增大。
1、通常情况下是无色、无气味的气体。
3、能溶于水(通常状况下体积比1:1),压强增大溶解量增大。
2、通常情况下二氧化碳的密度比空气大。
CO2的三态变化
CO2气体
无色液体
雪花状固体
干 冰
加压
降温
降温
压缩
101kPa
-78.5 0C
升华
干冰形成的示意图
干冰不是冰,是
二氧化碳的固体。
P109实验探究二氧化碳的化学性质
CO2
CO2
得出结论
1、一般情况下,CO2不能燃烧,也不能支持燃烧。
用途:二氧化碳可以灭火。
(所有的火都能用二氧化碳来灭吗?课后查资料)
现象:下面的蜡烛先熄灭,上面的蜡烛后熄灭。
菜 窖
[讨论] 进入一些久未开启的菜窖、干涸的深井及深洞的底部等CO2含量比较大的地方之前,如何保证人身安全?
做灯火熄灭实验
讲死狗洞的故事:
说明二氧化碳不能供人呼吸
如何证明二氧化碳与水反应了呢?(说明紫色石蕊是一种色素,是紫色的固体,把它溶解在蒸馏水中得到紫色的石蕊试液,酸性物质能使它变成红色。)
(5-1A)在A试管的紫色石蕊溶液中滴入稀盐酸,观察现象;
(5-2B)在 B试管的紫色石蕊溶液中滴入实验三的矿泉水瓶中的液体,观察现象。
稀盐酸
石 蕊 溶 液
观察:它们都能使紫色石蕊试液变红。
A
B
二氧化碳的水溶液
(2)(问题):是什么物质使紫色石蕊变红呢?
老师引导学生猜想:
①是CO2?②是H2O?③是CO2和H2O反应生成的新物质?
(讨论设计实验):根据自己的猜想,设计一个实验来进行验证。
CO2+H2O = H2CO3 现象:石蕊由紫色变成红色
得出:二氧化碳的水溶液中有一种酸性物质
分析、对比现象:
CO2
CO2
石蕊固体
石 蕊 溶 液
在石蕊固体和石蕊溶液中分别通入二氧化碳气体
盐酸
对比得出结论:是二氧化碳和水反应生成的物质(碳酸)使紫色石蕊变红
CO2+H2O = H2CO3 现象:石蕊由紫色变成红色
探究实验: 加热含有石蕊的二氧化碳的水溶液?观察现象。
讨论得出:碳酸不稳定受热易分解
化学方程式:H2CO3 = CO2↑ +H2O
▲
现象:石蕊由红色变成紫色
观察现象。
现象:澄清石灰水变浑浊
化学方程式:CO2+ Ca(OH)2 = H2O +CaCO3 ↓(检验CO2)
二、CO2的化学性质
1、一般情况下,CO2既不能燃烧,也不能支持燃烧,CO2不能供呼吸。
2、CO2跟水反应。
CO2+H2O = H2CO3 现象:石蕊由紫色变成红色
H2CO3 = CO2↑ +H2O 现象:石蕊由红色变成紫色
3、CO2与石灰水[Ca(OH)2]反应。
CO2+ Ca(OH)2 = H2O +CaCO3 ↓(鉴定CO2的重要方法)
CO2
纯碱
汽水
尿素
人工降雨
温度计
灭火
工业原料
致冷剂
光合作用
三、CO2的用途
温室中气体肥料
(A) 课本P111练习第1、2、3题;
(B) 练习册 P55习题第1-7题
本节课采用了探究实验、观察、对比、合作、分析、表达等的方法,从实际生活中的问题出发,通过研究物质的一般方法,探究了二氧化碳的性质、用途,体现了化学产生于生活,又服务于生活,发挥了学生的主观能动性,体现了学生是学习的主体,真正成为学习的主人。这节课由于学生实验多,让学生进行实验探究时注意强调实验操作的规范性,小组成员要密切的合作,还要合理安排40分钟,并且还要布置好习题做好知识点的巩固。
练习:通过练习巩固提高
六、说课反思:
二氧化碳的循环
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
