物质的检验与鉴别
图片预览










文档简介
(共44张PPT)
专题复习 物质的检验与鉴别
考纲要求:
1知道检验与鉴别的区别,了解常见物质或离子的检验方法
2理解用物理方法和化学方法进行物质的鉴别
3掌握鉴别物质的基本思路和步骤
专题复习 物质的检验与鉴别
是确认一种物质是什么物质。
是在知道是什么物质的情况下用物理或化学的方法将其区分出来。
考点一 物质的检验
①.常见气体的检验方法
②.常见有特殊颜色的物质
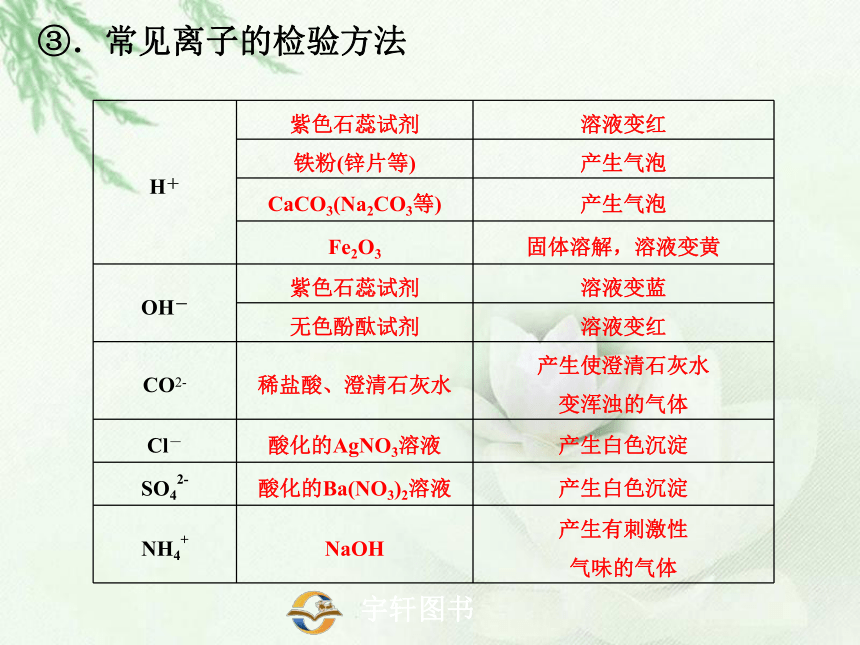
③.常见离子的检验方法
1.考点知识梳理
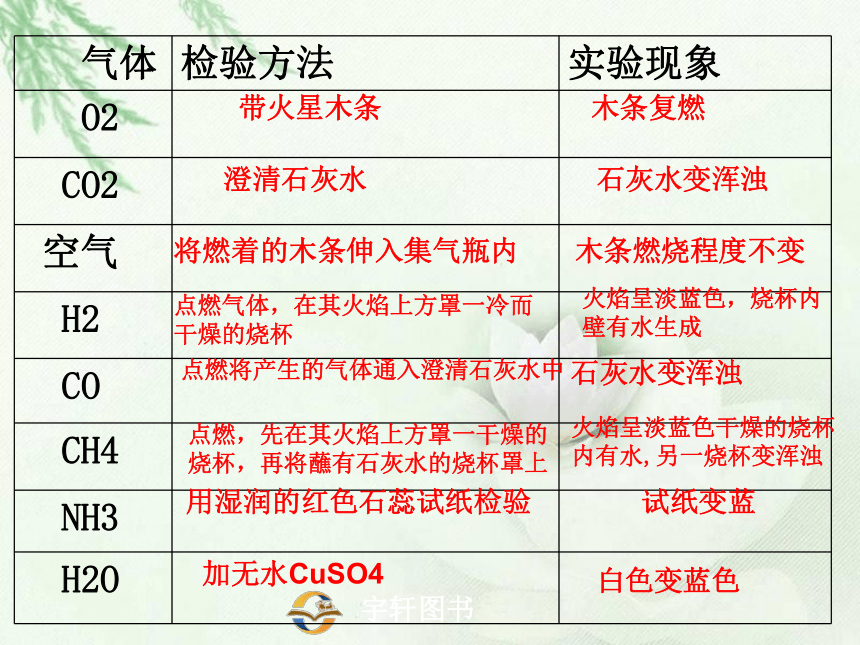
气体 检验方法 实验现象
O2
CO2
空气
H2
CO
CH4
NH3
H2O
带火星木条
木条复燃
澄清石灰水
石灰水变浑浊
将燃着的木条伸入集气瓶内
木条燃烧程度不变
点燃气体,在其火焰上方罩一冷而干燥的烧杯
火焰呈淡蓝色,烧杯内壁有水生成
点燃将产生的气体通入澄清石灰水中
石灰水变浑浊
点燃,先在其火焰上方罩一干燥的烧杯,再将蘸有石灰水的烧杯罩上
火焰呈淡蓝色干燥的烧杯内有水,另一烧杯变浑浊
用湿润的红色石蕊试纸检验
试纸变蓝
加无水CuSO4
白色变蓝色
2.常见有特殊颜色的物质(注:离子代表含有这种离子的溶液)
Fe2O3:______色 Fe3O4:______色
Fe2+:________色 Fe3+:_____色
Fe(OH)3:_______色 Cu:__________色
CuO:_____色 无水 CuSO4:_____色
CuSO4·5H2O:______色 Cu2+:______色
Cu(OH)2:_______色 S:_______色
红棕
黑
浅绿
黄
红褐
紫红
黑
白
蓝
蓝
蓝
黄
H+ 紫色石蕊试剂 溶液变红
铁粉(锌片等) 产生气泡
CaCO3(Na2CO3等) 产生气泡
Fe2O3 固体溶解,溶液变黄
OH- 紫色石蕊试剂 溶液变蓝
无色酚酞试剂 溶液变红
CO2- 稀盐酸、澄清石灰水 产生使澄清石灰水
变浑浊的气体
Cl- 酸化的AgNO3溶液 产生白色沉淀
SO42- 酸化的Ba(NO3)2溶液 产生白色沉淀
NH4+ NaOH 产生有刺激性
气味的气体
③.常见离子的检验方法
有关气体检验的专题训练
有CH4、CO、H2三种纯净的气体,分别燃烧后,将生成的气体先通过无水硫酸铜固体(A装置),再通过澄清的石灰水(B装置),则:
(1)如果A装置变蓝,B装置无现象,则原气体是______
(2)如果A装置不变蓝,B装置变浑浊,则原气体是______
(3)如果A装置变蓝,B装置变浑浊,则原气体是______
H2
CO
CH4
有关离子检验的专题训练
1、往珍珠中加入稀盐酸,有气体产生,该气体能使澄清石灰水变混浊,则珍珠中含有 离子。
2、往某溶液中加入碱液,微热,产生有刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝,则该溶液中含有 离子
3、碱溶液滴入某黄色溶液中,生成红褐色沉淀,则该黄色溶液可能是 溶液。
4、把下列某种溶液分别盛入两支试管中,往其中一支试管中滴入氢氧化钠溶液,再往另一支试管中滴入硝酸银溶液,前者有蓝色沉淀,后者观察不到明显现象,则这是( )溶液.
CO32-
NH4+
FeCl3
A
(2011·苏州)下列有关物质的检验方法和结论都合理的是( )
A.加入稀盐酸,有无色气体产生的物质中一定含有碳酸盐
B.用燃着的木条伸入某气体中,火焰熄灭,则该气体一定是二氧化碳
C.经点燃,产生蓝色火焰的气体不一定是一氧化碳
D.尝一下,有咸味的白色固体一定是食盐
中考例题精选
C
2.(2011·潍坊)某同学在自己家厨房中找到一种白色粉末,到学校实验室进行实验,实验过程与现象如下:
对此粉末的成分判断正确的是( )
A.该粉末一定是碳酸钠
B.该粉末一定是碳酸氢钠
C.该粉末一定是氯化钠
D.该粉末可能是碳酸钠或碳酸氢钠
考点二 物质的鉴别
① 酒精、水、醋酸
② 固体粉末NaCl CaCO3 NaOH NH4NO3
③固体粉末CuSO4 、Na2CO3 、 CaCO3
④铁粉、碳粉
探究活动一
鉴别以下各组物质
① 酒精、水、醋酸
② 固体粉末NaCl CaCO3 NaOH NH4NO3
③固体粉末CuSO4 、Na2CO3 、 CaCO3
④铁粉、碳粉
-----闻味
----溶于水
----------------用磁铁吸引
溶解
不溶
放热
吸热
探究活动一
----溶于水
鉴别以下各组物质
一、鉴别的方法
1.物理方法
2.化学方法
①色、态、味
②用水:溶解性、放吸热
小结
用化学方法鉴别物质的几种典型例题
一、不同类别物质的鉴别 1组探究并展示
二、同种类别物质的鉴别 2组探究并展示
三、综合物质的鉴别
(一)加入一种试剂一次鉴别 3组探究并展示
(二)不加其它试剂,互相鉴别 4组探究并展示
要求:操作方法简单易行,必须有明显的现象以示区别。
探究活动二
例如: HCl NaOH NaCl
H2SO4 Na2CO3 H2O
用指示剂
一、不同类别物质的鉴别
二、同种类别物质的鉴别
一碳 二硫 三氯
例如:HCl H2SO4
[ Ba(NO3)2 ]
Na2SO4 Na2CO3
[ HCL]
Na2CO3 Na2SO4 NaCl
(一)加入一种试剂一次鉴别
三、综合物质的鉴别
温馨提示 :鉴别时,遇到碳酸盐选择酸;遇到酸选择可溶性碳酸盐。
例如 BaCl2 NaCl Na2CO3
[ H2SO4 ]
AgNO3 KCl Na2CO3
[ Na2CO3 ]
[ HCl ]
KNO3 CaCl2 H2SO4
↓
↑
-
↓
↑
-
(二)不加其它试剂,互相鉴别
方法:编号取液,两两混合,
根据现象, 得出结论。
例如: HCl Na2CO3 Ba(NO3)2
①
②
③
↑
↑
↓
↓
三、综合物质的鉴别
②FeCl3 NaOH NaNO3
③KOH CuSO4 KNO3 H2SO4
(三)、涉及顺序的物质鉴别
例、有五瓶失去标签的溶液,分别为硝酸钾、氯化钡、氢氧化钾、硫酸镁、氯化铁,不用任何其它试剂,以实验报告形式,写出确定它们的步骤、现象、结论和有关化学方程式。
三、综合物质的鉴别
结论及化学方程式
观察到的现象
实验步骤
①KNO3 ②BaCl2 ③ KOH ④MgSO4 ⑤ FeCl3
产生白色沉淀的原溶液为BaCl2 ; MgSO4 + BaCl2 = MgCl2 +BaSO4 ↓ ;剩下的溶液为KNO3溶液
有一支试管内产生白色沉淀;另一支试管内无变化
⑷取其余两种溶液少许于两支试中,分别滴加MgSO4溶液
原溶液为MgSO4溶液 MgSO4 +2 KOH= Mg (OH)2↓ +K2SO4
有白色沉淀
⑶取其余三种溶液少许于三支试管中,分别滴加KOH溶液
原溶液为KOH溶液 FeCl3+3 KOH=Fe(OH)3 ↓ +3KCl
有红褐色沉淀
⑵取其余四种无色溶液少许于四支试管中,分别滴加FeCl3溶液
该溶液为FeCl3溶液
黄色溶液
⑴观察溶液颜色
结论及化学方程式
观察到的现象
实验步骤
①KNO3 ②BaCl2 ③ KOH ④MgSO4 ⑤ FeCl3
二、鉴别题的答题步骤
1.取样试剂于指定的仪器中。
2.分别向样品试剂中加入鉴别药品,观察现象。
3.得出结论。
一 鉴别的基本思路
1 鉴别主要是依据各物质的特殊现象,包括颜色、状态、气味、反应情况等。
2 如果要加入试剂进行鉴别,一定要先取样,不能直接对样品进行鉴别。
3 选用鉴别方法时先简单后复杂,先考虑物理方法后化学方法。
总结
1、(2011·上海)只用一种试剂就能将NaOH、NaCl、BaCl2三种溶液鉴别出来,它是( )
A.CuSO4溶液
B.Na2SO4溶液
C.酚酞溶液
D.Fe(NO3)3溶液
【答案】A
中考例题精选
2.(2011·黄冈)下列各组物质的溶液不用其他试剂就可鉴别的是( )
A.HCl CuCl2 NaNO3 Na2SO4
B.BaCl2 Na2CO3 HCl (NH4)2CO3
C.FeCl3 HCl NaCl NaOH
D.Na2CO3 Na2SO4 HCl H2SO4
【答案】C
某混合溶液可能含Na2SO4、Na2CO3、NaCl、NaNO3中的一种或几种溶质,为验证其组成,实验如下:
(1)混合溶液的溶质中一定有________________,一定没有_______,可能有____________。
(2)第②步的反应方程式_________________________________。
Na2CO3、NaCl
Na2SO4
NaNO3
BaCO3+2HNO3===Ba(NO3)2+H2O+CO2↑
(10鞍山)下列试剂中,能把KOH溶液、稀硫酸、
CaCl2溶液一次鉴别出来的是( )
A.KCl溶液 B.K2CO3溶液
C.NaNO3溶液 D.稀盐酸
B
实验室有两瓶失去标签的溶液,一瓶是稀盐酸,另一瓶是氢氧化钠溶液,下列试剂中不能将它们鉴别出来的是 ( )
A.酚酞试液 B.镁条
C.氯化钾溶液 D.氯化铜溶液
C
·人教版
变式题 [2011·哈尔滨]区分下列各组物质的两种方法都正确的是 ( )
需区分物质 方法一 方法二
A 空气和氧气 用带火星的木条检验 闻气味
B 硬水和软水 观察颜色 加肥皂水搅拌
C 铝丝和银丝 用磁铁吸引 浸入硫酸铜溶液
D 氢氧化钠和
硫酸铵 加水溶解测pH 加熟石灰
研磨闻气味
D
(10广州)用下列方法鉴别各组无色溶液,能够达到目的的是( )
待鉴别溶液 试剂(均为溶液)
A HNO3和KNO3 酚酞
B HCl和NaCl AgNO3
C AgNO3和Na2SO4 BaCl2
D Ca(OH)2和NaOH Na2CO3
(10宁夏)氯化铵、硫酸铵、硝酸铵和尿素都是白色固体,也是重要的化肥。下列物质能够将尿素从这四种化肥中鉴别出来的是 ( )
A. 氢氧化钙 B.稀盐酸 C.氯化钠 D.水
D
A
填空题
1、某溶液含有Na+、H+、Cl-、SO42-,欲证明两种阴离子存在,选用的最佳方案是:先向溶液中滴加足量的 溶液,直到沉淀完全,再取上层清液,滴加 溶液,又出现白色沉淀,则可得出结论。
Ba(NO3)2
AgNO3
(10重庆)有四种澄清透明的溶液:①MgCl2溶液 ②Cu(NO3)2溶液③K2SO4溶液 ④KOH溶液。不用其他试剂就可进行鉴别,鉴别出来的先后顺序是( )
A.④①②③ B.②④①③
C.③②①④ D①④②③
B
(宁夏)用石灰浆粉刷不久的墙壁上掉下一块 白色固体,为探究其成分,应选用的一组试剂 ( ) A.水、酚酞溶液、氯化钠溶液
B.水、稀盐酸、氢氧化钠溶液
C.水、酚酞溶液、稀盐酸
D.水、酚酞溶液、氢氧化钠溶液
C
1、自来水生产中通常使用少量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,用自来水冒充纯净水(蒸馏水)出售。为辨别真伪,可用下列一种化学试剂来鉴别,该试剂是 。
A.酚酞试液 B.氯化钡溶液C.氢氧化钠溶液 D.硝酸银溶液
D
3.(2011·黄石)不用其他试剂,仅仅利用试管和胶头滴管就可以区别下列四种物质的溶液:①CuSO4;②MgCl2;③KOH;④NaNO3,则正确的鉴别顺序是( )
A.②③①④ B. ①②③④
C.①③②④ D.②①③④
【答案】C
5.(2011·新疆)在区别下列四组常见物质的方法中(括号内为实验操作),你认为错误的是( )
A.CO2与CO(点燃)
B.稀盐酸与稀硫酸(加入锌粒)
C.硬水和软水(加肥皂水,振荡)
D.N2与O2(用带火星的木条)
【解析】CO2无可燃性,CO有可燃性,故A正确;稀盐酸与稀硫酸都能跟锌粒反应,产生气泡,现象相同,故B错误;向水样中加入肥皂水,若泡沫少而浮渣多是硬水,反之是软水,故C正确;N2不支持燃烧,不能使带火星的木条复燃,O2支持燃烧,能使带火星的木条复燃,故D正确。
【答案】B
7.(2011·泰州)下列鉴别物质的方法中错误的是( )
A.用燃着的木条鉴别氧气和二氧化碳
B.用酚酞溶液鉴别稀盐酸和稀硫酸
C.用水鉴别碳酸钙粉末和碳酸钠粉末
D.用灼烧的方法鉴别棉布和丝绸
【解析】根据物质的性质不同对物质进行鉴别。稀盐酸和稀硫酸都不能使酚酞溶液变色,故B错误;氧气能使木条燃烧得更旺,二氧化碳能使燃着的木条熄灭;碳酸钙粉末不能溶于水,碳酸钠粉末能溶于水;灼烧棉布有烧纸的气味,而灼烧丝绸则有烧羽毛或头发的特殊气味,故A、C、D的鉴别方法正确。
【答案】B
8.(2011·黄冈)下列各组物质的溶液不用其他试剂就可鉴别的是( )
A.HCl CuCl2 NaNO3 Na2SO4
B.BaCl2 Na2CO3 HCl (NH4)2CO3
C.FeCl3 HCl NaCl NaOH
D.Na2CO3 Na2SO4 HCl H2SO4
【解析】首先根据颜色鉴别出氯化铁,然后再将氯化铁分别滴加到另外三种溶液中,有红褐色沉淀生成的是氢氧化钠溶液;再过滤,将两种未鉴别的溶液分别与红褐色沉淀混合,能使红褐色沉淀溶解的是盐酸,无明显现象的是氯化钠。
【答案】C
9.(2012中考预测题)下表列举了两组待鉴别的物质和对应的鉴别方法,其中不合理的是( )
待鉴别的物质 鉴别方法
A 烧碱和熟石灰 加入无色酚酞,观察溶液颜色的变化
B 氢气、氧气、二氧化碳 用燃着的木条检验,观察燃烧情况
C 硝酸铵和生石灰 加水溶解,用手触摸试管外壁,感觉温度的变化
D 食盐水和蒸馏水 滴加硝酸银溶液,观察有无白色沉淀生成
10.(2010中考变式题)下列区分物质的试剂或方法不正确的是( )
A.用水区分氯化钙和碳酸钙
B.用闻气味的方法区分白酒和白醋
C.用盐酸区分黄金和黄铜(含锌)
D.用酚酞溶液区分氯化钠溶液和盐酸
【解析】氯化钙易溶于水,而碳酸钙难溶于水,可以用水区分,A正确;白酒有芳香气味,而白醋有酸味,它们气味不同,可以用闻气味的方法区分,B正确;黄金不能和盐酸反应,而黄铜中的锌可以和盐酸反应放出气体,可以用盐酸区分,C正确;氯化钠和盐酸都不能使酚酞变色,不能区分,D错,所以应该选择D。
【答案】D
11.(2010中考变式题)下列各组物质对应的鉴别方法正确的是( )
A.硬水和软水——观察是否澄清
B.合成纤维和羊毛——用手触摸
C.黄金和假黄金(铜锌合金)——滴加稀盐酸
D.食盐水和白糖水——观察颜色
【答案】C
二、填空题(共56分)
12.(8分)(2010·襄樊)小强在化学实验室做实验时,拿出一瓶久置的氢氧化钙粉末[Ca(OH)2],进行如下实验:
(1)取氢氧化钙粉末样品少量溶于足量水中,有____________现象出现,小强判断该药品已变质。
(2)小强进一步做如下实验探究,请你参与并完成下表。
实验操作步骤 实验现象 实验结论
取样,加适量水,搅拌,过滤 ①取少量滤渣于试管中,加入____________ 有气泡
产生 氢氧化钙粉末已经变质
②取少量滤液于试管中,滴入___________溶液 _____________ 氢氧化钙粉末只是部分变质
沉淀
稀盐酸
酚酞
溶液变红色
16.(10分)(2010中考变式题)(1)有一包白色粉末,可能是由Na2CO3、Na2SO4、Ba(OH)2、BaCl2中的一种或几种组成,现做如下实验。
(Ⅰ):将少量粉末放在烧杯中加足量水,搅拌、静置、过滤,得无色溶液及白色沉淀;
(Ⅱ):向(Ⅰ)过滤得到的白色沉淀中加足量稀硝酸,沉淀全部溶解并有气体产生;
(Ⅲ):向(Ⅰ)过滤得到的滤液中滴加硝酸银溶液,立即有较多的白色沉淀生成,再加稀硝酸,沉淀不溶解。
根据以上实验现象推断:
白色粉末中:①一定存在的是________,②一定不存在的是________,③可能存在的是________。
鉴别、检验的依据:
物质的性质(物理性质和化学性质)
鉴别、检验的原则:
现象要明显,操作要尽量简便易行
方法归纳
先根据物质的物理性质来检验和鉴别,如观察颜色、 状态、气味、溶解性等;再根据物质的化学性质来检验和鉴别,如可燃性、还原性、热稳定性及其它特性。
注意点:
先取样后操作,先现象后结论。
专题复习 物质的检验与鉴别
考纲要求:
1知道检验与鉴别的区别,了解常见物质或离子的检验方法
2理解用物理方法和化学方法进行物质的鉴别
3掌握鉴别物质的基本思路和步骤
专题复习 物质的检验与鉴别
是确认一种物质是什么物质。
是在知道是什么物质的情况下用物理或化学的方法将其区分出来。
考点一 物质的检验
①.常见气体的检验方法
②.常见有特殊颜色的物质
③.常见离子的检验方法
1.考点知识梳理
气体 检验方法 实验现象
O2
CO2
空气
H2
CO
CH4
NH3
H2O
带火星木条
木条复燃
澄清石灰水
石灰水变浑浊
将燃着的木条伸入集气瓶内
木条燃烧程度不变
点燃气体,在其火焰上方罩一冷而干燥的烧杯
火焰呈淡蓝色,烧杯内壁有水生成
点燃将产生的气体通入澄清石灰水中
石灰水变浑浊
点燃,先在其火焰上方罩一干燥的烧杯,再将蘸有石灰水的烧杯罩上
火焰呈淡蓝色干燥的烧杯内有水,另一烧杯变浑浊
用湿润的红色石蕊试纸检验
试纸变蓝
加无水CuSO4
白色变蓝色
2.常见有特殊颜色的物质(注:离子代表含有这种离子的溶液)
Fe2O3:______色 Fe3O4:______色
Fe2+:________色 Fe3+:_____色
Fe(OH)3:_______色 Cu:__________色
CuO:_____色 无水 CuSO4:_____色
CuSO4·5H2O:______色 Cu2+:______色
Cu(OH)2:_______色 S:_______色
红棕
黑
浅绿
黄
红褐
紫红
黑
白
蓝
蓝
蓝
黄
H+ 紫色石蕊试剂 溶液变红
铁粉(锌片等) 产生气泡
CaCO3(Na2CO3等) 产生气泡
Fe2O3 固体溶解,溶液变黄
OH- 紫色石蕊试剂 溶液变蓝
无色酚酞试剂 溶液变红
CO2- 稀盐酸、澄清石灰水 产生使澄清石灰水
变浑浊的气体
Cl- 酸化的AgNO3溶液 产生白色沉淀
SO42- 酸化的Ba(NO3)2溶液 产生白色沉淀
NH4+ NaOH 产生有刺激性
气味的气体
③.常见离子的检验方法
有关气体检验的专题训练
有CH4、CO、H2三种纯净的气体,分别燃烧后,将生成的气体先通过无水硫酸铜固体(A装置),再通过澄清的石灰水(B装置),则:
(1)如果A装置变蓝,B装置无现象,则原气体是______
(2)如果A装置不变蓝,B装置变浑浊,则原气体是______
(3)如果A装置变蓝,B装置变浑浊,则原气体是______
H2
CO
CH4
有关离子检验的专题训练
1、往珍珠中加入稀盐酸,有气体产生,该气体能使澄清石灰水变混浊,则珍珠中含有 离子。
2、往某溶液中加入碱液,微热,产生有刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝,则该溶液中含有 离子
3、碱溶液滴入某黄色溶液中,生成红褐色沉淀,则该黄色溶液可能是 溶液。
4、把下列某种溶液分别盛入两支试管中,往其中一支试管中滴入氢氧化钠溶液,再往另一支试管中滴入硝酸银溶液,前者有蓝色沉淀,后者观察不到明显现象,则这是( )溶液.
CO32-
NH4+
FeCl3
A
(2011·苏州)下列有关物质的检验方法和结论都合理的是( )
A.加入稀盐酸,有无色气体产生的物质中一定含有碳酸盐
B.用燃着的木条伸入某气体中,火焰熄灭,则该气体一定是二氧化碳
C.经点燃,产生蓝色火焰的气体不一定是一氧化碳
D.尝一下,有咸味的白色固体一定是食盐
中考例题精选
C
2.(2011·潍坊)某同学在自己家厨房中找到一种白色粉末,到学校实验室进行实验,实验过程与现象如下:
对此粉末的成分判断正确的是( )
A.该粉末一定是碳酸钠
B.该粉末一定是碳酸氢钠
C.该粉末一定是氯化钠
D.该粉末可能是碳酸钠或碳酸氢钠
考点二 物质的鉴别
① 酒精、水、醋酸
② 固体粉末NaCl CaCO3 NaOH NH4NO3
③固体粉末CuSO4 、Na2CO3 、 CaCO3
④铁粉、碳粉
探究活动一
鉴别以下各组物质
① 酒精、水、醋酸
② 固体粉末NaCl CaCO3 NaOH NH4NO3
③固体粉末CuSO4 、Na2CO3 、 CaCO3
④铁粉、碳粉
-----闻味
----溶于水
----------------用磁铁吸引
溶解
不溶
放热
吸热
探究活动一
----溶于水
鉴别以下各组物质
一、鉴别的方法
1.物理方法
2.化学方法
①色、态、味
②用水:溶解性、放吸热
小结
用化学方法鉴别物质的几种典型例题
一、不同类别物质的鉴别 1组探究并展示
二、同种类别物质的鉴别 2组探究并展示
三、综合物质的鉴别
(一)加入一种试剂一次鉴别 3组探究并展示
(二)不加其它试剂,互相鉴别 4组探究并展示
要求:操作方法简单易行,必须有明显的现象以示区别。
探究活动二
例如: HCl NaOH NaCl
H2SO4 Na2CO3 H2O
用指示剂
一、不同类别物质的鉴别
二、同种类别物质的鉴别
一碳 二硫 三氯
例如:HCl H2SO4
[ Ba(NO3)2 ]
Na2SO4 Na2CO3
[ HCL]
Na2CO3 Na2SO4 NaCl
(一)加入一种试剂一次鉴别
三、综合物质的鉴别
温馨提示 :鉴别时,遇到碳酸盐选择酸;遇到酸选择可溶性碳酸盐。
例如 BaCl2 NaCl Na2CO3
[ H2SO4 ]
AgNO3 KCl Na2CO3
[ Na2CO3 ]
[ HCl ]
KNO3 CaCl2 H2SO4
↓
↑
-
↓
↑
-
(二)不加其它试剂,互相鉴别
方法:编号取液,两两混合,
根据现象, 得出结论。
例如: HCl Na2CO3 Ba(NO3)2
①
②
③
↑
↑
↓
↓
三、综合物质的鉴别
②FeCl3 NaOH NaNO3
③KOH CuSO4 KNO3 H2SO4
(三)、涉及顺序的物质鉴别
例、有五瓶失去标签的溶液,分别为硝酸钾、氯化钡、氢氧化钾、硫酸镁、氯化铁,不用任何其它试剂,以实验报告形式,写出确定它们的步骤、现象、结论和有关化学方程式。
三、综合物质的鉴别
结论及化学方程式
观察到的现象
实验步骤
①KNO3 ②BaCl2 ③ KOH ④MgSO4 ⑤ FeCl3
产生白色沉淀的原溶液为BaCl2 ; MgSO4 + BaCl2 = MgCl2 +BaSO4 ↓ ;剩下的溶液为KNO3溶液
有一支试管内产生白色沉淀;另一支试管内无变化
⑷取其余两种溶液少许于两支试中,分别滴加MgSO4溶液
原溶液为MgSO4溶液 MgSO4 +2 KOH= Mg (OH)2↓ +K2SO4
有白色沉淀
⑶取其余三种溶液少许于三支试管中,分别滴加KOH溶液
原溶液为KOH溶液 FeCl3+3 KOH=Fe(OH)3 ↓ +3KCl
有红褐色沉淀
⑵取其余四种无色溶液少许于四支试管中,分别滴加FeCl3溶液
该溶液为FeCl3溶液
黄色溶液
⑴观察溶液颜色
结论及化学方程式
观察到的现象
实验步骤
①KNO3 ②BaCl2 ③ KOH ④MgSO4 ⑤ FeCl3
二、鉴别题的答题步骤
1.取样试剂于指定的仪器中。
2.分别向样品试剂中加入鉴别药品,观察现象。
3.得出结论。
一 鉴别的基本思路
1 鉴别主要是依据各物质的特殊现象,包括颜色、状态、气味、反应情况等。
2 如果要加入试剂进行鉴别,一定要先取样,不能直接对样品进行鉴别。
3 选用鉴别方法时先简单后复杂,先考虑物理方法后化学方法。
总结
1、(2011·上海)只用一种试剂就能将NaOH、NaCl、BaCl2三种溶液鉴别出来,它是( )
A.CuSO4溶液
B.Na2SO4溶液
C.酚酞溶液
D.Fe(NO3)3溶液
【答案】A
中考例题精选
2.(2011·黄冈)下列各组物质的溶液不用其他试剂就可鉴别的是( )
A.HCl CuCl2 NaNO3 Na2SO4
B.BaCl2 Na2CO3 HCl (NH4)2CO3
C.FeCl3 HCl NaCl NaOH
D.Na2CO3 Na2SO4 HCl H2SO4
【答案】C
某混合溶液可能含Na2SO4、Na2CO3、NaCl、NaNO3中的一种或几种溶质,为验证其组成,实验如下:
(1)混合溶液的溶质中一定有________________,一定没有_______,可能有____________。
(2)第②步的反应方程式_________________________________。
Na2CO3、NaCl
Na2SO4
NaNO3
BaCO3+2HNO3===Ba(NO3)2+H2O+CO2↑
(10鞍山)下列试剂中,能把KOH溶液、稀硫酸、
CaCl2溶液一次鉴别出来的是( )
A.KCl溶液 B.K2CO3溶液
C.NaNO3溶液 D.稀盐酸
B
实验室有两瓶失去标签的溶液,一瓶是稀盐酸,另一瓶是氢氧化钠溶液,下列试剂中不能将它们鉴别出来的是 ( )
A.酚酞试液 B.镁条
C.氯化钾溶液 D.氯化铜溶液
C
·人教版
变式题 [2011·哈尔滨]区分下列各组物质的两种方法都正确的是 ( )
需区分物质 方法一 方法二
A 空气和氧气 用带火星的木条检验 闻气味
B 硬水和软水 观察颜色 加肥皂水搅拌
C 铝丝和银丝 用磁铁吸引 浸入硫酸铜溶液
D 氢氧化钠和
硫酸铵 加水溶解测pH 加熟石灰
研磨闻气味
D
(10广州)用下列方法鉴别各组无色溶液,能够达到目的的是( )
待鉴别溶液 试剂(均为溶液)
A HNO3和KNO3 酚酞
B HCl和NaCl AgNO3
C AgNO3和Na2SO4 BaCl2
D Ca(OH)2和NaOH Na2CO3
(10宁夏)氯化铵、硫酸铵、硝酸铵和尿素都是白色固体,也是重要的化肥。下列物质能够将尿素从这四种化肥中鉴别出来的是 ( )
A. 氢氧化钙 B.稀盐酸 C.氯化钠 D.水
D
A
填空题
1、某溶液含有Na+、H+、Cl-、SO42-,欲证明两种阴离子存在,选用的最佳方案是:先向溶液中滴加足量的 溶液,直到沉淀完全,再取上层清液,滴加 溶液,又出现白色沉淀,则可得出结论。
Ba(NO3)2
AgNO3
(10重庆)有四种澄清透明的溶液:①MgCl2溶液 ②Cu(NO3)2溶液③K2SO4溶液 ④KOH溶液。不用其他试剂就可进行鉴别,鉴别出来的先后顺序是( )
A.④①②③ B.②④①③
C.③②①④ D①④②③
B
(宁夏)用石灰浆粉刷不久的墙壁上掉下一块 白色固体,为探究其成分,应选用的一组试剂 ( ) A.水、酚酞溶液、氯化钠溶液
B.水、稀盐酸、氢氧化钠溶液
C.水、酚酞溶液、稀盐酸
D.水、酚酞溶液、氢氧化钠溶液
C
1、自来水生产中通常使用少量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,用自来水冒充纯净水(蒸馏水)出售。为辨别真伪,可用下列一种化学试剂来鉴别,该试剂是 。
A.酚酞试液 B.氯化钡溶液C.氢氧化钠溶液 D.硝酸银溶液
D
3.(2011·黄石)不用其他试剂,仅仅利用试管和胶头滴管就可以区别下列四种物质的溶液:①CuSO4;②MgCl2;③KOH;④NaNO3,则正确的鉴别顺序是( )
A.②③①④ B. ①②③④
C.①③②④ D.②①③④
【答案】C
5.(2011·新疆)在区别下列四组常见物质的方法中(括号内为实验操作),你认为错误的是( )
A.CO2与CO(点燃)
B.稀盐酸与稀硫酸(加入锌粒)
C.硬水和软水(加肥皂水,振荡)
D.N2与O2(用带火星的木条)
【解析】CO2无可燃性,CO有可燃性,故A正确;稀盐酸与稀硫酸都能跟锌粒反应,产生气泡,现象相同,故B错误;向水样中加入肥皂水,若泡沫少而浮渣多是硬水,反之是软水,故C正确;N2不支持燃烧,不能使带火星的木条复燃,O2支持燃烧,能使带火星的木条复燃,故D正确。
【答案】B
7.(2011·泰州)下列鉴别物质的方法中错误的是( )
A.用燃着的木条鉴别氧气和二氧化碳
B.用酚酞溶液鉴别稀盐酸和稀硫酸
C.用水鉴别碳酸钙粉末和碳酸钠粉末
D.用灼烧的方法鉴别棉布和丝绸
【解析】根据物质的性质不同对物质进行鉴别。稀盐酸和稀硫酸都不能使酚酞溶液变色,故B错误;氧气能使木条燃烧得更旺,二氧化碳能使燃着的木条熄灭;碳酸钙粉末不能溶于水,碳酸钠粉末能溶于水;灼烧棉布有烧纸的气味,而灼烧丝绸则有烧羽毛或头发的特殊气味,故A、C、D的鉴别方法正确。
【答案】B
8.(2011·黄冈)下列各组物质的溶液不用其他试剂就可鉴别的是( )
A.HCl CuCl2 NaNO3 Na2SO4
B.BaCl2 Na2CO3 HCl (NH4)2CO3
C.FeCl3 HCl NaCl NaOH
D.Na2CO3 Na2SO4 HCl H2SO4
【解析】首先根据颜色鉴别出氯化铁,然后再将氯化铁分别滴加到另外三种溶液中,有红褐色沉淀生成的是氢氧化钠溶液;再过滤,将两种未鉴别的溶液分别与红褐色沉淀混合,能使红褐色沉淀溶解的是盐酸,无明显现象的是氯化钠。
【答案】C
9.(2012中考预测题)下表列举了两组待鉴别的物质和对应的鉴别方法,其中不合理的是( )
待鉴别的物质 鉴别方法
A 烧碱和熟石灰 加入无色酚酞,观察溶液颜色的变化
B 氢气、氧气、二氧化碳 用燃着的木条检验,观察燃烧情况
C 硝酸铵和生石灰 加水溶解,用手触摸试管外壁,感觉温度的变化
D 食盐水和蒸馏水 滴加硝酸银溶液,观察有无白色沉淀生成
10.(2010中考变式题)下列区分物质的试剂或方法不正确的是( )
A.用水区分氯化钙和碳酸钙
B.用闻气味的方法区分白酒和白醋
C.用盐酸区分黄金和黄铜(含锌)
D.用酚酞溶液区分氯化钠溶液和盐酸
【解析】氯化钙易溶于水,而碳酸钙难溶于水,可以用水区分,A正确;白酒有芳香气味,而白醋有酸味,它们气味不同,可以用闻气味的方法区分,B正确;黄金不能和盐酸反应,而黄铜中的锌可以和盐酸反应放出气体,可以用盐酸区分,C正确;氯化钠和盐酸都不能使酚酞变色,不能区分,D错,所以应该选择D。
【答案】D
11.(2010中考变式题)下列各组物质对应的鉴别方法正确的是( )
A.硬水和软水——观察是否澄清
B.合成纤维和羊毛——用手触摸
C.黄金和假黄金(铜锌合金)——滴加稀盐酸
D.食盐水和白糖水——观察颜色
【答案】C
二、填空题(共56分)
12.(8分)(2010·襄樊)小强在化学实验室做实验时,拿出一瓶久置的氢氧化钙粉末[Ca(OH)2],进行如下实验:
(1)取氢氧化钙粉末样品少量溶于足量水中,有____________现象出现,小强判断该药品已变质。
(2)小强进一步做如下实验探究,请你参与并完成下表。
实验操作步骤 实验现象 实验结论
取样,加适量水,搅拌,过滤 ①取少量滤渣于试管中,加入____________ 有气泡
产生 氢氧化钙粉末已经变质
②取少量滤液于试管中,滴入___________溶液 _____________ 氢氧化钙粉末只是部分变质
沉淀
稀盐酸
酚酞
溶液变红色
16.(10分)(2010中考变式题)(1)有一包白色粉末,可能是由Na2CO3、Na2SO4、Ba(OH)2、BaCl2中的一种或几种组成,现做如下实验。
(Ⅰ):将少量粉末放在烧杯中加足量水,搅拌、静置、过滤,得无色溶液及白色沉淀;
(Ⅱ):向(Ⅰ)过滤得到的白色沉淀中加足量稀硝酸,沉淀全部溶解并有气体产生;
(Ⅲ):向(Ⅰ)过滤得到的滤液中滴加硝酸银溶液,立即有较多的白色沉淀生成,再加稀硝酸,沉淀不溶解。
根据以上实验现象推断:
白色粉末中:①一定存在的是________,②一定不存在的是________,③可能存在的是________。
鉴别、检验的依据:
物质的性质(物理性质和化学性质)
鉴别、检验的原则:
现象要明显,操作要尽量简便易行
方法归纳
先根据物质的物理性质来检验和鉴别,如观察颜色、 状态、气味、溶解性等;再根据物质的化学性质来检验和鉴别,如可燃性、还原性、热稳定性及其它特性。
注意点:
先取样后操作,先现象后结论。
同课章节目录
- 专题一 物质的分离与提纯
- 课题1 海带中碘元素的分离及检验
- 拓展课题1-1 茶叶中某些元素的鉴定
- 课题2 用纸层析法分离铁离子和铜离子
- 拓展课题1-2 菠菜的叶绿体中色素的提取和分离
- 拓展课题1-3 用粉笔进行层析分离
- 课题3 硝酸钾晶体的制备
- 拓展课题1-4 粗盐提纯
- 专题二 物质性质的研究
- 课题1 铝及其化合物的性质
- 拓展课题2-1 铝热反应
- 课题2 乙醇和苯酚的性质
- 拓展课题2-2 苯酚与甲醛的反应
- 专题三 物质的检验与鉴别
- 课题1 牙膏和火柴中某些成分的检验
- 拓展课题3-1 新装修居室内空气中甲醛浓度的检测
- 拓展课题3-2 汽车尾气成分的检验
- 课题2 亚硝酸钠和食盐的鉴别
- 拓展课题3-3 真假碘盐的鉴别
- 专题四 化学反应条件的控制
- 课题1 硫代硫酸钠与酸反应速率的影响因素
- 拓展课题4-1 “蓝瓶子”实验
- 课题2 催化剂对过氧化氢分解反应速率的影响
- 拓展课题4-2 过氧化氢酶的催化作用
- 拓展课题4-3 蔗糖的燃烧
- 课题3 反应条件对化学平衡的影响
- 拓展课题4-4 淀粉与碘显色现象的探究
- 拓展课题4-5 压强对化学平衡的影响
- 专题五 电化学问题研究
- 课题1 原电池
- 拓展课题5-1 干电池模拟实验
- 课题2 电解与电镀
- 拓展课题5-2 阿伏加德罗常数的测定
- 专题六 物质的定量分析
- 课题1 食醋总酸含量的测定
- 拓展课题6-1 配制并标定氢氧化钠溶液
- 课题2 镀锌铁皮锌镀层厚度的测定
- 拓展课题6-2 水果中维生素C含量的测定
- 专题七 物质的制备与合成
- 课题1 硫酸亚铁铵的制备
- 拓展课题7-1 用制氢废液制备硫酸锌晶体
- 课题2 阿司匹林的合成
- 拓展课题7-2 对氨基苯磺酸的合成
