2021-2022学年九年级化学 沪教版上册第4章认识化学变化测试题(含答案)
文档属性
| 名称 | 2021-2022学年九年级化学 沪教版上册第4章认识化学变化测试题(含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 330.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-28 14:18:10 | ||
图片预览




文档简介
第4章《认识化学变化》测试题
一、单选题
1.家庭用煤经过从“煤球”到“蜂窝煤”的变化,其目的是(
)
A.增大可燃物的热值
B.降低可燃物的着火点
C.提高空气中氧气的含量
D.增大可燃物与空气的接触面积
2.下列指定反应的化学方程式正确的是
A.铁丝在氧气中燃烧:
B.碳酸氢按受热分解:
C.氢氧化钠与硫酸铜:
D.甲烧完全燃烧:
3.下列属于节约用水标识的是(
)
A.
B.
C.
D.
4.Ca(HCO3)2(碳酸氢钙)在一定条件下会发生分解反应,不可能生成的物质是
A.SO2
B.CaCO3
C.CO2
D.H2O
5.下列物质的化学式书写不正确的是
A.氧化铝AlO
B.碳酸钙CaCO3
C.氢氧化钙Ca(OH)2
D.氯化镁MgCl2
6.下列化学方程式符合题意且书写正确的是(
)
A.实验室制;
B.铁和稀硫酸反应:
C.铁在氧气中燃烧:
D.工业上用赤铁矿炼铁的原理:
7.化学反应前后,下列各项中:①原子总数;②分子总数;③物质总质量;④
物质的种类;⑤元素的种类,一定发生改变的是
A.②④
B.①③⑤
C.①②③④⑤
D.④
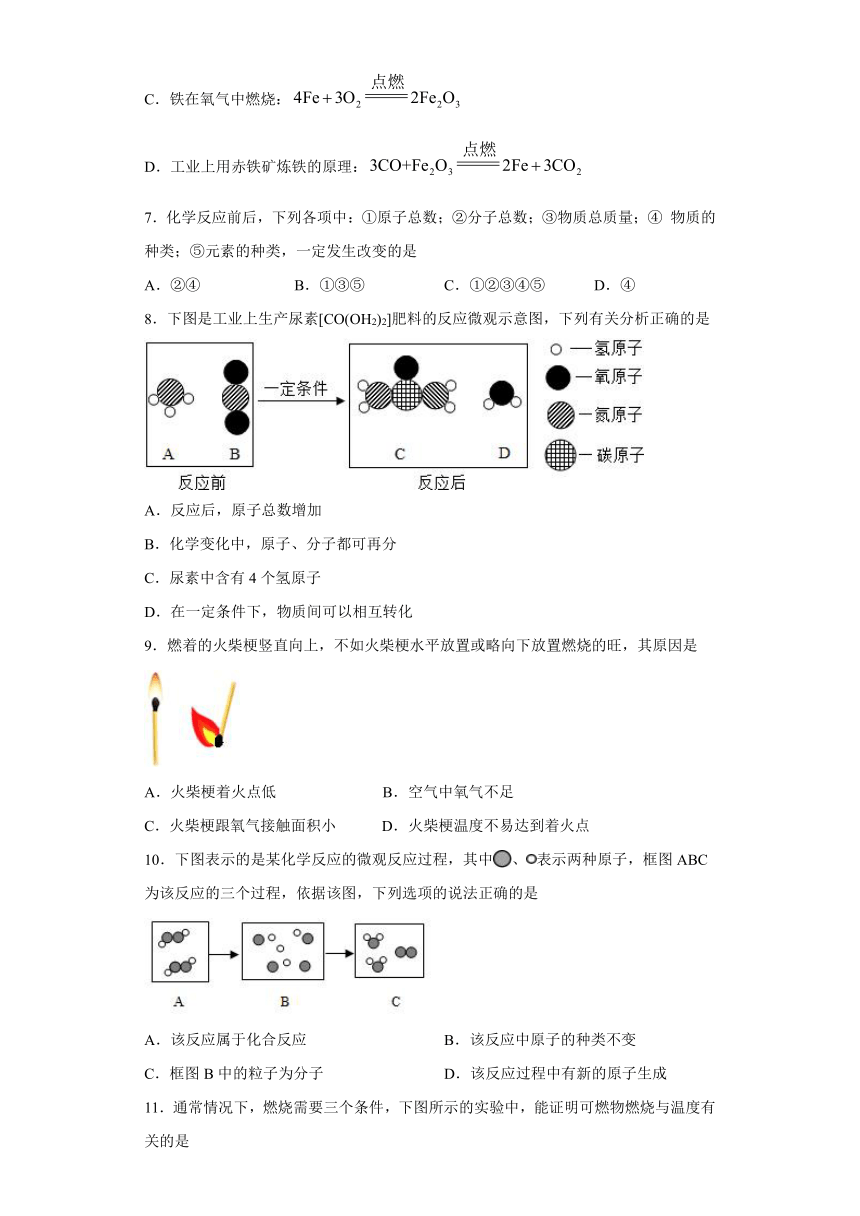
8.下图是工业上生产尿素[CO(OH2)2]肥料的反应微观示意图,下列有关分析正确的是
A.反应后,原子总数增加
B.化学变化中,原子、分子都可再分
C.尿素中含有4个氢原子
D.在一定条件下,物质间可以相互转化
9.燃着的火柴梗竖直向上,不如火柴梗水平放置或略向下放置燃烧的旺,其原因是
A.火柴梗着火点低
B.空气中氧气不足
C.火柴梗跟氧气接触面积小
D.火柴梗温度不易达到着火点
10.下图表示的是某化学反应的微观反应过程,其中、表示两种原子,框图ABC为该反应的三个过程,依据该图,下列选项的说法正确的是
A.该反应属于化合反应
B.该反应中原子的种类不变
C.框图B中的粒子为分子
D.该反应过程中有新的原子生成
11.通常情况下,燃烧需要三个条件,下图所示的实验中,能证明可燃物燃烧与温度有关的是
A.②④
B.②③
C.③④
D.①②
12.逻辑推理是化学学习常用的思维方法,下列说法错误的是
(??
)
A.某物质在氧气中燃烧生成二氧化碳和水,证明该物质中一定含有碳、氢两种元素
B.分子、原子不带电呈中性而离子带电,但带电的粒子不一定是离子
C.化学变化常伴随能量的吸收或释放,但有能量吸收或释放的变化不一定是化学变化
D.由分子构成的物质,分子是保持物质化学性质的最小粒子;而原子在化学变化中是可以再分的最小粒子
13.物质的性质和用途密切相关,下列物质的用途与性质不对应的是( )
A.氮气可用作保护气﹣﹣氮气的化学性质稳定
B.一氧化碳可用于冶炼金属﹣﹣一氧化碳具有可燃性
C.干冰可用作人工降雨﹣﹣干冰升华吸热
D.金刚石可用作切割玻璃﹣﹣金刚石硬度大
14.分析下列化学反应,有关说法正确的是
反应①:
反应②:
反应③:
A.上述反应的生成物都是氧化物
B.在实验室中进行上述反应,反应现象均相同
C.Fe2O3、Fe3O4中铁、氧元素的质量比不同
D.CO→CO2的转化只能通过反应①、③实现
二、填空题
15.如图是一款家用燃气灶具示意图:
(1)塑料属于_______材料
(2)管道天然气完全燃烧时火焰呈蓝色,反应的化学方程式为_____如果燃烧时火焰呈黄色并有黑烟浮升,说明燃气燃烧不充分,这时应将空气进风口____(填“调大”或“调小”)
,其原理是____。
(3)天然气也是一种易燃易爆气体,使用不当,很容易造成危险,请你写出一条安全使用天然气的注意事项____。
16.在宏观、微观和符号之间建立联系是化学学科的特点
(1)请用数字和化学符号表示:
2个氢分子_____;3个亚铁离子_____.
(2)A、B、C、D表示4种物质,其微观示意图如图所示:
若反应后生成1.4gD,则生成C的质量为_____g.
17.十九大报告对于“精准扶贫”做出了总体安排。脱贫先治水,让贫困地区喝上干净安全的自来水是脱贫的基本要求。
(1)自来水的生产过程中,常用活性炭去除水中异味,这是利用活性炭的
______
性。
(2)有些村民用地下水作生活用水,人们常用
______
检验地下水是硬水还是软水,生活中可用
______
的方法降低水的硬度。
(3)净化水的方法有:①过滤、②加明矾吸附沉降、③蒸馏、④消毒杀菌。要将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为
______
A
①②③④
B
②④①③
C
①③④
D
②①④
(4)自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用如图表示:(
、
、
分别表示氯原子、氧原子、氢原子)
①乙图所示反应的基本反应类型为
______
反应(填“化合”或“分解”);
②上述物质中,D属于
______
(填“单质”或“化合物”);
③以甲图为例分析,你能总结出的一条结论是:
______
。
18.“倡导低碳生活”是今年4月22日世界地球日的主题内容。“低碳”,意即较少或更少二氧化碳等气体的排放,因此能源与环境已成为人们关注的焦点。
(1)下列物质中:①煤;
②石油;
③天然气;
④氢气等,其中属于最清洁燃料的是_____(填序号)。
(2)硅(Si)是太阳能电池和电脑芯片中不可缺少的材料。硅生产过程中的一个重要化学反应为:SiO2+2C
Si+2x↑.由此推断x的化学式为_____。
(3)同学们野外春游用捡来的枯树枝来做饭,要使树枝燃烧还需要的条件是_____。
(4)含硫煤或石油制品燃烧排放的SO2和氮氧化物会引起“酸雨”现象。若汽油中某分子X(相对分子质量为112)由碳、氢两种元素组成,其中氢的质量分数约为14.3%,则分子X中碳原子与氢原子数之比为_____。
三、推断题
19.甲、乙、丙是初中化学常见的物质,三种物质都含有同一种元素,它们之间有如图所示的转化关系(→表示反应一步实现,部分物质和反应条例略去)。
(1)若甲、乙、丙都含有地壳中含量最多的元素,甲、乙组成元素相同,丙是单质,则甲转化为丙的化学方程式为______。
(2)若甲、乙、丙都含有碳元素,甲为单质,乙、丙组成元素相同,乙是有毒气体,则乙转化为丙的化学方程式为______;丙的一种用途为______;甲在氧气中充分燃烧生成丙,不充分燃烧生成乙,对比说明______不同,生成物可能不同。
20.已知A是红棕色粉末,B是白色沉淀,D为红褐色沉淀,Y的溶液显蓝色,X和G都是黑色固体,结合图中信息,回答有关问题
(1)沉淀D的化学式是:__________,固体H的化学式:________
(2)写出反应②的化学方程式:_________,写出反应③的化学方程式:___________,该反应属于_________反应(填基本反应类型)
(3)溶液C的颜色是:_________
(4)Y溶液在农业上的应用:_________
四、实验题
21.如图所示,回答下列问题(温馨提示:白磷的着火点为40℃,红磷的着火点为240℃;它们在空气中燃烧都生成有毒的白烟——五氧化二磷,五氧化二磷易溶于水)。
(1)如果用A装置进行实验,观察到得现象:_____;
(2)用导气管将氧气通入A装置的烧杯与白磷(甲)接触,观察到_____;其燃烧的化学方程式为:_____。
(3)如果用B装置进行实验,得到以下事实:
①不通空气时,冷水中的白磷不燃烧;
②通入空气时,冷水中的白磷不燃烧;
③不通空气时,热水中的白磷不燃烧;
④通入空气时,热水中的白磷燃烧。
该实验得出燃烧应具备的条件有:①可燃物,②_____,③_____。
(4)白磷与红磷相比,更容易着火燃烧是因为_____,少量的白磷应保存在_____中。
(5)“化学实验的绿色化”要求实验室的“三废”排放降低到最低程度并能得到妥善处理。图A与图B所示实验相比,_____(填A或B)更体现了化学实验的绿色化的追求。
22.下图为应用Y形管进行的不同实验探究。
(1)实验室利用装置甲制备少量二氧化碳Y形管中盛放的固体物质是_________(填名称,下同),液体物质是____________。
(2)实验室利用装置乙制备少量氧气实验时,酒精灯应加热Y形管内______(填“a”或“b”)处的高锰酸钾。反应的化学方程式为__________________________。
(3)利用装置丙探究燃烧的条件(白磷着火点为40
℃;红磷的着火点为240
℃)
①通过比较装置丙内________(填标号)处的实验现象,可推导出燃烧条件之一是温度达到可燃物的着火点。
A.a和b
B.b和c
C.a和c
②图中能正确反映气球内气压(P)随反应时间(t)而发生变化的是______(填标号)。
五、计算题
23.小英同学取石灰石样品15g,将75mL的稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表:
实验
第一次
第二次
第三次
加入稀盐酸的量/mL
25
25
25
生成气体的质量/g
2.2
m
1.1
(1)m的值是_____g。
(2)求该样品中碳酸钙的质量。
24.氧气是人体维持生命所必需的,蛟龙号深海载人潜水器中使用“金属过氧化物处理系统”使氧“再生”,其原理是过氧化钠固体在常温下与二氧化碳反应生成氧气。
(1)请将该原理化学方程式补充完整,2Na2O2+2CO2=2_____+O2;
(2)在蛟龙号密闭空间内用这种方法制取氧气最大优点是_____;
(3)取一定量的过氧化钠,在密闭的容器中与充足的二氧化碳充分反应,记录产生氧气的质量与反应时间的关系如图甲所示。请通过计算回答下列问题(写出计算过程):
①参与反应的过氧化钠的质量为多少_____?
②请在图乙的坐标中,画出反应过程中钠元素质量在t0﹣t3时段变化的示意图_____。
参考答案
1.D
2.B
3.D
4.A
5.A
6.D
7.D
8.D
9.D
10.B
11.A
12.D
13.B
14.C
15.合成
CH4+2O2CO2+2H2O
调大
使可燃物与充足的氧气接触
室内要注意通风
16.2H2
3Fe2+
4.4
17.吸附
肥皂水
煮沸
D
分解
化合物
化学反应前后原子的种类、数目不变
18.④
CO
温度要达到着火点
1:2
19.
灭火(合理即可)
反应物的量
20.Fe(OH)3
Cu
Fe
+
CuSO4
=
FeSO4
+
Cu
3NaOH
+
FeCl3
=
Fe(OH)3↓
+
3NaCl
复分解
黄色
配置农药波尔多液
21.薄铜片上的白磷燃烧,红磷和水中的白磷不燃烧
热水中的白磷燃烧
与氧气(或空气)接触
温度达到着火点
白磷的着火点较低
冷水
B
22.大理石(或石灰石)
稀盐酸
a
2KMnO4
K2MnO4
+
MnO2+
O2↑
A
B
23.(1)2.2
(2)由表格可知,最终生成二氧化碳质量为2.2g+2.2g+1.1g=5.5g
解:设石灰石中CaCO3的质量为x
答:石灰石样品中CaCO3的质量12.5g。
24.(1)Na2CO3(2)反应在常温下进行、操作简便、能将人呼吸产生的二氧化碳转变为呼吸所需的氧气(3)①参与反应的过氧化钠的质量为15.6g;②
一、单选题
1.家庭用煤经过从“煤球”到“蜂窝煤”的变化,其目的是(
)
A.增大可燃物的热值
B.降低可燃物的着火点
C.提高空气中氧气的含量
D.增大可燃物与空气的接触面积
2.下列指定反应的化学方程式正确的是
A.铁丝在氧气中燃烧:
B.碳酸氢按受热分解:
C.氢氧化钠与硫酸铜:
D.甲烧完全燃烧:
3.下列属于节约用水标识的是(
)
A.
B.
C.
D.
4.Ca(HCO3)2(碳酸氢钙)在一定条件下会发生分解反应,不可能生成的物质是
A.SO2
B.CaCO3
C.CO2
D.H2O
5.下列物质的化学式书写不正确的是
A.氧化铝AlO
B.碳酸钙CaCO3
C.氢氧化钙Ca(OH)2
D.氯化镁MgCl2
6.下列化学方程式符合题意且书写正确的是(
)
A.实验室制;
B.铁和稀硫酸反应:
C.铁在氧气中燃烧:
D.工业上用赤铁矿炼铁的原理:
7.化学反应前后,下列各项中:①原子总数;②分子总数;③物质总质量;④
物质的种类;⑤元素的种类,一定发生改变的是
A.②④
B.①③⑤
C.①②③④⑤
D.④
8.下图是工业上生产尿素[CO(OH2)2]肥料的反应微观示意图,下列有关分析正确的是
A.反应后,原子总数增加
B.化学变化中,原子、分子都可再分
C.尿素中含有4个氢原子
D.在一定条件下,物质间可以相互转化
9.燃着的火柴梗竖直向上,不如火柴梗水平放置或略向下放置燃烧的旺,其原因是
A.火柴梗着火点低
B.空气中氧气不足
C.火柴梗跟氧气接触面积小
D.火柴梗温度不易达到着火点
10.下图表示的是某化学反应的微观反应过程,其中、表示两种原子,框图ABC为该反应的三个过程,依据该图,下列选项的说法正确的是
A.该反应属于化合反应
B.该反应中原子的种类不变
C.框图B中的粒子为分子
D.该反应过程中有新的原子生成
11.通常情况下,燃烧需要三个条件,下图所示的实验中,能证明可燃物燃烧与温度有关的是
A.②④
B.②③
C.③④
D.①②
12.逻辑推理是化学学习常用的思维方法,下列说法错误的是
(??
)
A.某物质在氧气中燃烧生成二氧化碳和水,证明该物质中一定含有碳、氢两种元素
B.分子、原子不带电呈中性而离子带电,但带电的粒子不一定是离子
C.化学变化常伴随能量的吸收或释放,但有能量吸收或释放的变化不一定是化学变化
D.由分子构成的物质,分子是保持物质化学性质的最小粒子;而原子在化学变化中是可以再分的最小粒子
13.物质的性质和用途密切相关,下列物质的用途与性质不对应的是( )
A.氮气可用作保护气﹣﹣氮气的化学性质稳定
B.一氧化碳可用于冶炼金属﹣﹣一氧化碳具有可燃性
C.干冰可用作人工降雨﹣﹣干冰升华吸热
D.金刚石可用作切割玻璃﹣﹣金刚石硬度大
14.分析下列化学反应,有关说法正确的是
反应①:
反应②:
反应③:
A.上述反应的生成物都是氧化物
B.在实验室中进行上述反应,反应现象均相同
C.Fe2O3、Fe3O4中铁、氧元素的质量比不同
D.CO→CO2的转化只能通过反应①、③实现
二、填空题
15.如图是一款家用燃气灶具示意图:
(1)塑料属于_______材料
(2)管道天然气完全燃烧时火焰呈蓝色,反应的化学方程式为_____如果燃烧时火焰呈黄色并有黑烟浮升,说明燃气燃烧不充分,这时应将空气进风口____(填“调大”或“调小”)
,其原理是____。
(3)天然气也是一种易燃易爆气体,使用不当,很容易造成危险,请你写出一条安全使用天然气的注意事项____。
16.在宏观、微观和符号之间建立联系是化学学科的特点
(1)请用数字和化学符号表示:
2个氢分子_____;3个亚铁离子_____.
(2)A、B、C、D表示4种物质,其微观示意图如图所示:
若反应后生成1.4gD,则生成C的质量为_____g.
17.十九大报告对于“精准扶贫”做出了总体安排。脱贫先治水,让贫困地区喝上干净安全的自来水是脱贫的基本要求。
(1)自来水的生产过程中,常用活性炭去除水中异味,这是利用活性炭的
______
性。
(2)有些村民用地下水作生活用水,人们常用
______
检验地下水是硬水还是软水,生活中可用
______
的方法降低水的硬度。
(3)净化水的方法有:①过滤、②加明矾吸附沉降、③蒸馏、④消毒杀菌。要将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为
______
A
①②③④
B
②④①③
C
①③④
D
②①④
(4)自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用如图表示:(
、
、
分别表示氯原子、氧原子、氢原子)
①乙图所示反应的基本反应类型为
______
反应(填“化合”或“分解”);
②上述物质中,D属于
______
(填“单质”或“化合物”);
③以甲图为例分析,你能总结出的一条结论是:
______
。
18.“倡导低碳生活”是今年4月22日世界地球日的主题内容。“低碳”,意即较少或更少二氧化碳等气体的排放,因此能源与环境已成为人们关注的焦点。
(1)下列物质中:①煤;
②石油;
③天然气;
④氢气等,其中属于最清洁燃料的是_____(填序号)。
(2)硅(Si)是太阳能电池和电脑芯片中不可缺少的材料。硅生产过程中的一个重要化学反应为:SiO2+2C
Si+2x↑.由此推断x的化学式为_____。
(3)同学们野外春游用捡来的枯树枝来做饭,要使树枝燃烧还需要的条件是_____。
(4)含硫煤或石油制品燃烧排放的SO2和氮氧化物会引起“酸雨”现象。若汽油中某分子X(相对分子质量为112)由碳、氢两种元素组成,其中氢的质量分数约为14.3%,则分子X中碳原子与氢原子数之比为_____。
三、推断题
19.甲、乙、丙是初中化学常见的物质,三种物质都含有同一种元素,它们之间有如图所示的转化关系(→表示反应一步实现,部分物质和反应条例略去)。
(1)若甲、乙、丙都含有地壳中含量最多的元素,甲、乙组成元素相同,丙是单质,则甲转化为丙的化学方程式为______。
(2)若甲、乙、丙都含有碳元素,甲为单质,乙、丙组成元素相同,乙是有毒气体,则乙转化为丙的化学方程式为______;丙的一种用途为______;甲在氧气中充分燃烧生成丙,不充分燃烧生成乙,对比说明______不同,生成物可能不同。
20.已知A是红棕色粉末,B是白色沉淀,D为红褐色沉淀,Y的溶液显蓝色,X和G都是黑色固体,结合图中信息,回答有关问题
(1)沉淀D的化学式是:__________,固体H的化学式:________
(2)写出反应②的化学方程式:_________,写出反应③的化学方程式:___________,该反应属于_________反应(填基本反应类型)
(3)溶液C的颜色是:_________
(4)Y溶液在农业上的应用:_________
四、实验题
21.如图所示,回答下列问题(温馨提示:白磷的着火点为40℃,红磷的着火点为240℃;它们在空气中燃烧都生成有毒的白烟——五氧化二磷,五氧化二磷易溶于水)。
(1)如果用A装置进行实验,观察到得现象:_____;
(2)用导气管将氧气通入A装置的烧杯与白磷(甲)接触,观察到_____;其燃烧的化学方程式为:_____。
(3)如果用B装置进行实验,得到以下事实:
①不通空气时,冷水中的白磷不燃烧;
②通入空气时,冷水中的白磷不燃烧;
③不通空气时,热水中的白磷不燃烧;
④通入空气时,热水中的白磷燃烧。
该实验得出燃烧应具备的条件有:①可燃物,②_____,③_____。
(4)白磷与红磷相比,更容易着火燃烧是因为_____,少量的白磷应保存在_____中。
(5)“化学实验的绿色化”要求实验室的“三废”排放降低到最低程度并能得到妥善处理。图A与图B所示实验相比,_____(填A或B)更体现了化学实验的绿色化的追求。
22.下图为应用Y形管进行的不同实验探究。
(1)实验室利用装置甲制备少量二氧化碳Y形管中盛放的固体物质是_________(填名称,下同),液体物质是____________。
(2)实验室利用装置乙制备少量氧气实验时,酒精灯应加热Y形管内______(填“a”或“b”)处的高锰酸钾。反应的化学方程式为__________________________。
(3)利用装置丙探究燃烧的条件(白磷着火点为40
℃;红磷的着火点为240
℃)
①通过比较装置丙内________(填标号)处的实验现象,可推导出燃烧条件之一是温度达到可燃物的着火点。
A.a和b
B.b和c
C.a和c
②图中能正确反映气球内气压(P)随反应时间(t)而发生变化的是______(填标号)。
五、计算题
23.小英同学取石灰石样品15g,将75mL的稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表:
实验
第一次
第二次
第三次
加入稀盐酸的量/mL
25
25
25
生成气体的质量/g
2.2
m
1.1
(1)m的值是_____g。
(2)求该样品中碳酸钙的质量。
24.氧气是人体维持生命所必需的,蛟龙号深海载人潜水器中使用“金属过氧化物处理系统”使氧“再生”,其原理是过氧化钠固体在常温下与二氧化碳反应生成氧气。
(1)请将该原理化学方程式补充完整,2Na2O2+2CO2=2_____+O2;
(2)在蛟龙号密闭空间内用这种方法制取氧气最大优点是_____;
(3)取一定量的过氧化钠,在密闭的容器中与充足的二氧化碳充分反应,记录产生氧气的质量与反应时间的关系如图甲所示。请通过计算回答下列问题(写出计算过程):
①参与反应的过氧化钠的质量为多少_____?
②请在图乙的坐标中,画出反应过程中钠元素质量在t0﹣t3时段变化的示意图_____。
参考答案
1.D
2.B
3.D
4.A
5.A
6.D
7.D
8.D
9.D
10.B
11.A
12.D
13.B
14.C
15.合成
CH4+2O2CO2+2H2O
调大
使可燃物与充足的氧气接触
室内要注意通风
16.2H2
3Fe2+
4.4
17.吸附
肥皂水
煮沸
D
分解
化合物
化学反应前后原子的种类、数目不变
18.④
CO
温度要达到着火点
1:2
19.
灭火(合理即可)
反应物的量
20.Fe(OH)3
Cu
Fe
+
CuSO4
=
FeSO4
+
Cu
3NaOH
+
FeCl3
=
Fe(OH)3↓
+
3NaCl
复分解
黄色
配置农药波尔多液
21.薄铜片上的白磷燃烧,红磷和水中的白磷不燃烧
热水中的白磷燃烧
与氧气(或空气)接触
温度达到着火点
白磷的着火点较低
冷水
B
22.大理石(或石灰石)
稀盐酸
a
2KMnO4
K2MnO4
+
MnO2+
O2↑
A
B
23.(1)2.2
(2)由表格可知,最终生成二氧化碳质量为2.2g+2.2g+1.1g=5.5g
解:设石灰石中CaCO3的质量为x
答:石灰石样品中CaCO3的质量12.5g。
24.(1)Na2CO3(2)反应在常温下进行、操作简便、能将人呼吸产生的二氧化碳转变为呼吸所需的氧气(3)①参与反应的过氧化钠的质量为15.6g;②
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
