3.3元素(二)第三单元物质构成的奥秘2021_2022学年九年级化学人教版上册(word版 含解析)
文档属性
| 名称 | 3.3元素(二)第三单元物质构成的奥秘2021_2022学年九年级化学人教版上册(word版 含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 123.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-29 00:00:00 | ||
图片预览


文档简介
课题三元素(二)第三单元物质构成的奥秘2021~2022学年九年级化学同步练习(人教版)
一.选择题(共15小题)
1.元素观、微粒观是化学的重要观念。下列有关元素和微粒的说法正确的是( )
A.分子、原子能直接构成物质,但离子不能
B.元素的原子核内质子数与中子数一定相等
C.元素的原子序数与该元素原子核电荷数在数值上相同
D.原子是保持物质化学性质的最小微粒
2.生活中接触到的“富硒茶叶”、“加铁酱油”、“加碘食盐”等用品,这里的硒、铁、碘指的是( )
A.原子
B.元素
C.离子
D.单质
3.金属元素种类高达八十余种,性质相似。地球上金属资源广泛存在于地壳和海洋中,地壳中含量最高的金属元素是( )
A.铜
B.铁
C.钠
D.铝
4.氧化汞受热时的变化可用如图表示,下列对于图示的理解错误的是( )
A.原子可结合成分子
B.分子在化学变化中可以再分
C.所有的物质都是由分子构成
D.可用表示氧分子的形成过程
5.下列说法中正确的是( )
A.氯化氢是由氢、氯两种元素组成的
B.氯化氢是由氢气和氯气混合而成的
C.氯化氢是由一个氢原子和一个氯原子构成的
D.一个氯化氢分子是由一个氢元素和一个氯元素组成的
6.铝元素与氯元素最本质的区别是( )
A.相对原子质量不同
B.中子数不同
C.中子数与核外电子数之和不同
D.质子数不同
7.“含氟牙膏”、“加碘食盐”中的“氟”、“碘”指的是( )
A.分子
B.原子
C.离子
D.元素
8.“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为( )
A.硒
B.硅
C.铝
D.锡
9.“中国芯”的主要材料是高纯度的单质硅,其结构类似于金刚石。下列有关硅的说法正确的是( )
A.元素符号为SI
B.属于非金属元素
C.硅是地壳中含量最多的元素
D.单质硅由分子构成
10.银可制作感光材料,银的元素符号是( )
A.Hg
B.AG
C.Ag
D.Mg
11.下列元素符号书写正确的是( )
A.氦
Ne
B.钡
Be
C.锰
MN
D.汞
Hg
12.下列属于非金属元素的是( )
A.铝
B.铁
C.钙
D.氧
13.属于金属元素的是( )
A.Zn
B.Si
C.N
D.H
14.溴元素在元素周期表中的信息如图所示,下列说法正确的是( )
A.1个溴原子的质量是79.90
g
B.溴原子的质量由构成其原子的质子和电子决定
C.溴属于非金属元素
D.溴原子的中子数为35
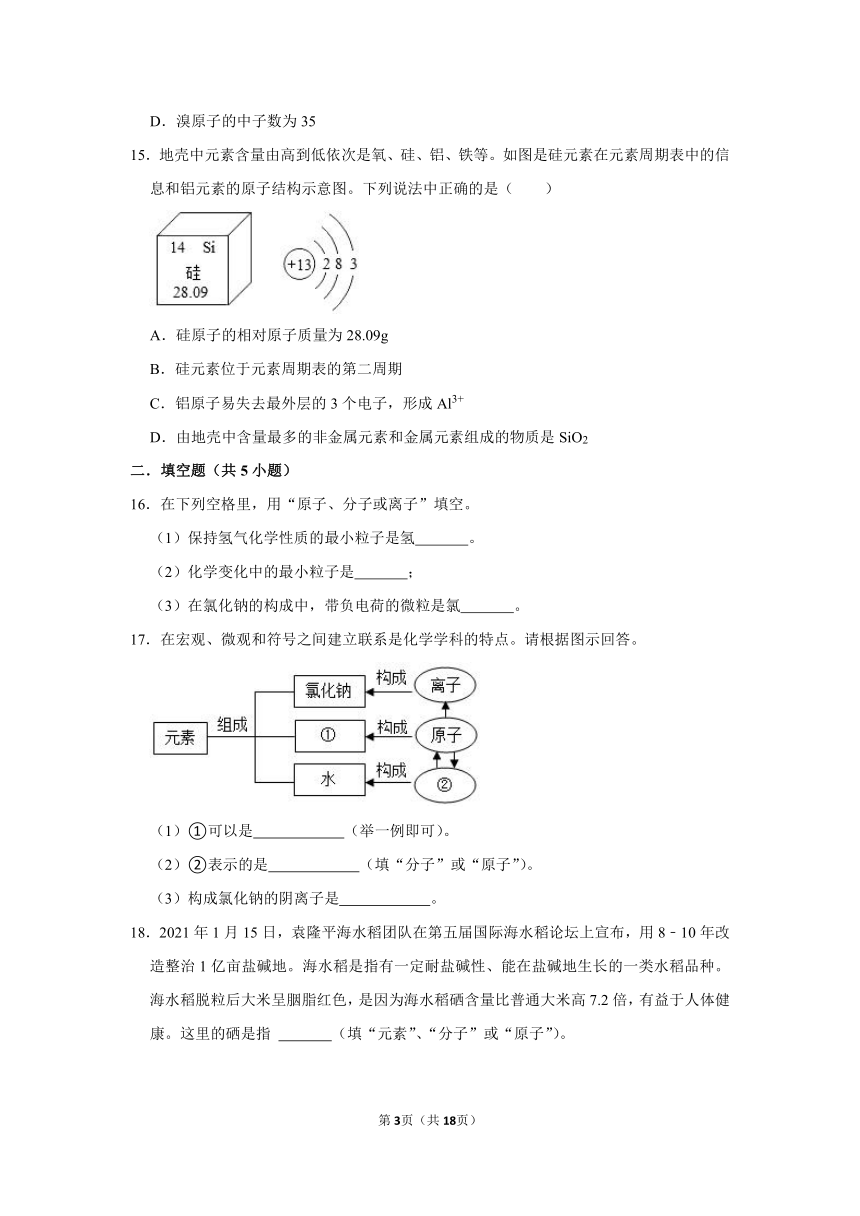
15.地壳中元素含量由高到低依次是氧、硅、铝、铁等。如图是硅元素在元素周期表中的信息和铝元素的原子结构示意图。下列说法中正确的是( )
A.硅原子的相对原子质量为28.09g
B.硅元素位于元素周期表的第二周期
C.铝原子易失去最外层的3个电子,形成Al3+
D.由地壳中含量最多的非金属元素和金属元素组成的物质是SiO2
二.填空题(共5小题)
16.在下列空格里,用“原子、分子或离子”填空。
(1)保持氢气化学性质的最小粒子是氢
。
(2)化学变化中的最小粒子是
;
(3)在氯化钠的构成中,带负电荷的微粒是氯
。
17.在宏观、微观和符号之间建立联系是化学学科的特点。请根据图示回答。
(1)①可以是
(举一例即可)。
(2)②表示的是
(填“分子”或“原子”)。
(3)构成氯化钠的阴离子是
。
18.2021年1月15日,袁隆平海水稻团队在第五届国际海水稻论坛上宣布,用8﹣10年改造整治1亿亩盐碱地。海水稻是指有一定耐盐碱性、能在盐碱地生长的一类水稻品种。海水稻脱粒后大米呈胭脂红色,是因为海水稻硒含量比普通大米高7.2倍,有益于人体健康。这里的硒是指
(填“元素”、“分子”或“原子”)。
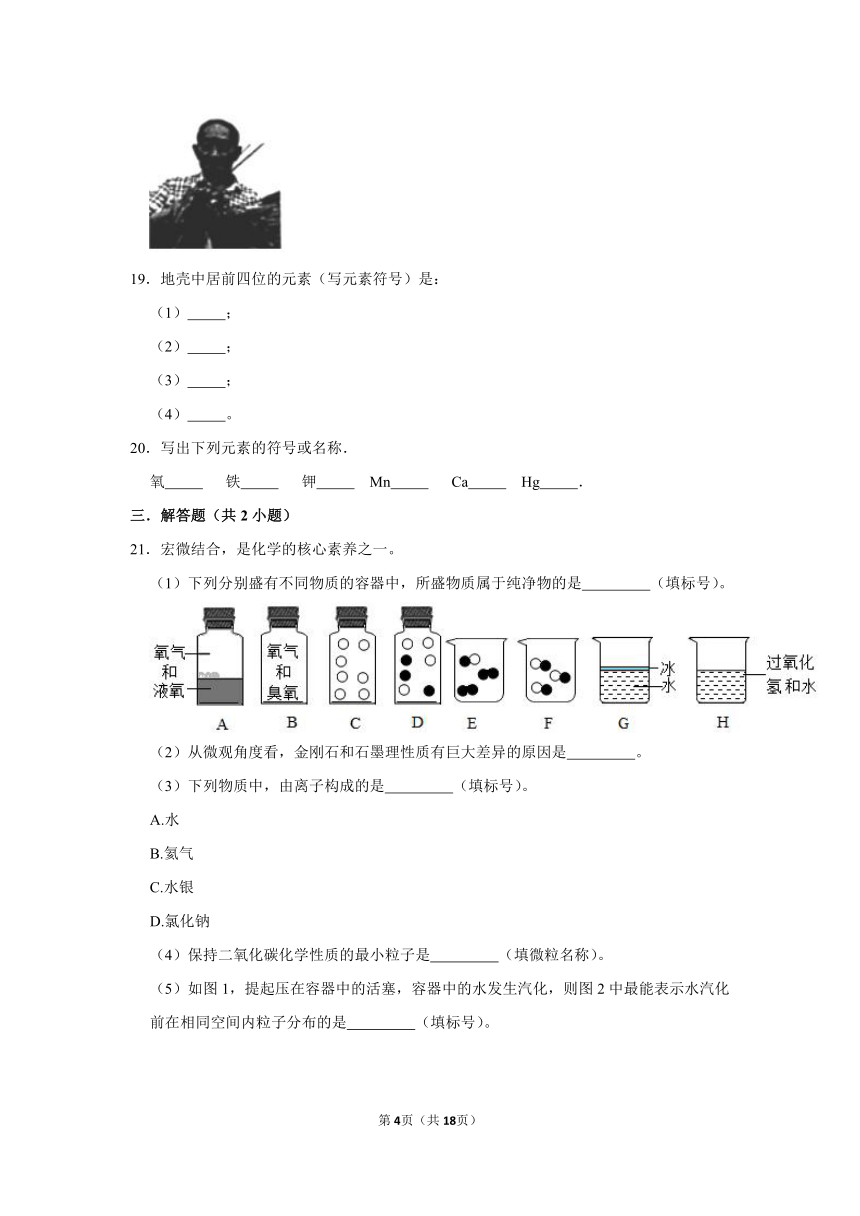
19.地壳中居前四位的元素(写元素符号)是:
(1)
;
(2)
;
(3)
;
(4)
。
20.写出下列元素的符号或名称.
氧
铁
钾
Mn
Ca
Hg
.
三.解答题(共2小题)
21.宏微结合,是化学的核心素养之一。
(1)下列分别盛有不同物质的容器中,所盛物质属于纯净物的是
(填标号)。
(2)从微观角度看,金刚石和石墨理性质有巨大差异的原因是
。
(3)下列物质中,由离子构成的是
(填标号)。
A.水
B.氦气
C.水银
D.氯化钠
(4)保持二氧化碳化学性质的最小粒子是
(填微粒名称)。
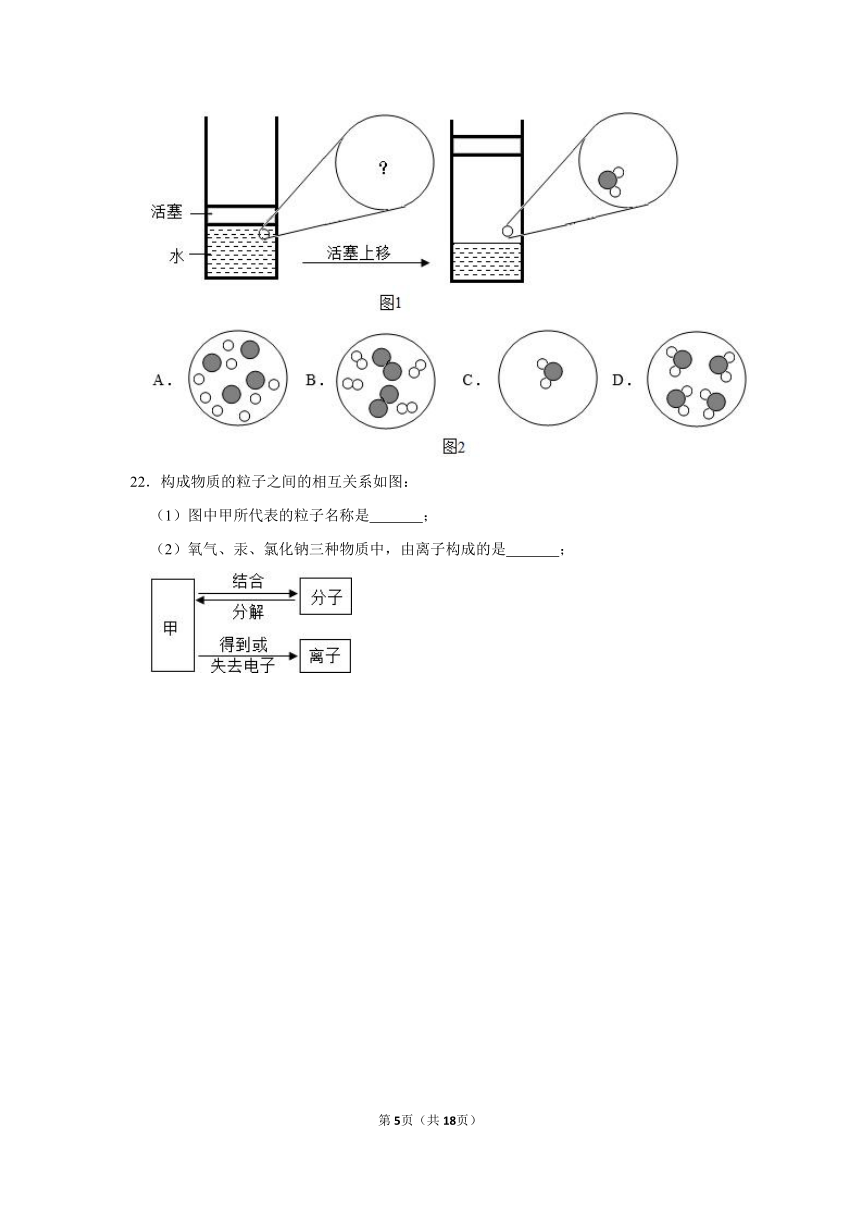
(5)如图1,提起压在容器中的活塞,容器中的水发生汽化,则图2中最能表示水汽化前在相同空间内粒子分布的是
(填标号)。
22.构成物质的粒子之间的相互关系如图:
(1)图中甲所代表的粒子名称是
;
(2)氧气、汞、氯化钠三种物质中,由离子构成的是
;
课题三元素(二)第三单元物质构成的奥秘2021~2022学年九年级化学同步练习(人教版)
参考答案与试题解析
一.选择题(共15小题)
1.元素观、微粒观是化学的重要观念。下列有关元素和微粒的说法正确的是( )
A.分子、原子能直接构成物质,但离子不能
B.元素的原子核内质子数与中子数一定相等
C.元素的原子序数与该元素原子核电荷数在数值上相同
D.原子是保持物质化学性质的最小微粒
【分析】A、根据构成物质的基本粒子来分析;
B、根据核内质子数与中子数不一定相等解答;
C、根据元素的原子序数=核电荷数=核内质子数=核外电子数解答;
D、根据由原子构成的物质原子是保持物质化学性质的最小微粒解答。
【解答】解:A、原子、离子和分子是构成物质的三种基本粒子,离子也能直接构成物质,如氯化钠就是由钠离子和氯离子构成的,故A错误;
B、同种元素的原子核内质子数与中子数不一定相等,例如钠原子中质子数为11,中子数为12,故B错误;
C、元素的原子序数=核电荷数=核内质子数=核外电子数,所以元素的原子序数与该元素原子核电荷数在数值上相同,故C正确;
D、由原子构成的物质原子是保持物质化学性质的最小微粒,故D错误。
故选:C。
【点评】本题难度不是很大,熟练掌握分子、原子、离子的概念、特征及掌握构成物质的基本微粒等即可正确解答本题。
2.生活中接触到的“富硒茶叶”、“加铁酱油”、“加碘食盐”等用品,这里的硒、铁、碘指的是( )
A.原子
B.元素
C.离子
D.单质
【分析】食品、药品、营养品、矿泉水等物质中的“氟、钙、碘、硒、铁”不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【解答】解:“加碘食盐”、“富硒茶叶”、“加铁酱油”等用品中的“硒、铁、碘”不是以单质、分子、原子等形式存在,这里所指的“硒、铁、碘”是强调存在的元素,与具体形态无关。
故选:B。
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键。
3.金属元素种类高达八十余种,性质相似。地球上金属资源广泛存在于地壳和海洋中,地壳中含量最高的金属元素是( )
A.铜
B.铁
C.钠
D.铝
【分析】根据地壳中各元素含量的排序及元素的分类进行分析判断。
【解答】解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的金属元素是铝元素。
故选:D。
【点评】本题难度不大,熟记地壳里各元素的含量、了解元素的分类是正确解答本题的关键。
4.氧化汞受热时的变化可用如图表示,下列对于图示的理解错误的是( )
A.原子可结合成分子
B.分子在化学变化中可以再分
C.所有的物质都是由分子构成
D.可用表示氧分子的形成过程
【分析】根据氧化汞分子在加热条件下能分解成汞原子和氧原子,汞原子直接聚集成金属汞,氧原子构成氧分子,氧分子聚集成氧气,进行分析判断。
【解答】解:A、氧原子可以构成氧分子,原子可结合成分子,故选项说法正确。
B、氧化汞分子在加热条件下能分解成汞原子和氧原子,分子在化学变化中可以再分,故选项说法正确。
C、不是所有的物质都是由分子构成,汞是由原子直接构成的,故选项说法错误。
D、1个氧分子是由2个氧原子构成的,可用表示氧分子的形成过程,故选项说法正确。
故选:C。
【点评】本题难度不大,明确氧化汞分子分解的过程、分子和原子的区别等是正确解答本题的关键。
5.下列说法中正确的是( )
A.氯化氢是由氢、氯两种元素组成的
B.氯化氢是由氢气和氯气混合而成的
C.氯化氢是由一个氢原子和一个氯原子构成的
D.一个氯化氢分子是由一个氢元素和一个氯元素组成的
【分析】A、根据物质是由元素组成进行解答;
B、根据氯化氢属于纯净物进行解答;
C、根据物质是由元素组成,分子是由原子构成进行解答;
D、根据分子是由原子构成进行解答.
【解答】解:A、氯化氢是由氢、氯两种元素组成的,故A正确;
B、氯化氢属于纯净物,是由氢、氯两种元素组成的,故B错误;
C、氯化氢是由氢、氯两种元素组成的,一个氯化氢分子是由一个氢原子和一个氯原子构成的,故C错误;
D、一个氯化氢分子是由一个氢原子和一个氯原子构成的,故D错误。
故选:A。
【点评】本题考查了物质的宏观组成和微观构成的知识,完成此题,可以依据已有的知识进行.
6.铝元素与氯元素最本质的区别是( )
A.相对原子质量不同
B.中子数不同
C.中子数与核外电子数之和不同
D.质子数不同
【分析】元素是质子数(即核电荷数)相同的一类原子的总称,进行分析判断。
【解答】解:元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),不同种元素最本质的区别是质子数不同,则铝元素与氯元素最本质的区别是质子数不同。
故选:D。
【点评】本题难度不大,明确决定元素种类的是质子数(即核电荷数)是正确解答本题的关键。
7.“含氟牙膏”、“加碘食盐”中的“氟”、“碘”指的是( )
A.分子
B.原子
C.离子
D.元素
【分析】“含氟牙膏”、“加碘食盐”中的“氟”、“碘”等有多种形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【解答】解:“含氟牙膏”、“加碘食盐”中的“氟”、“碘”等有多种形式存在,如钙元素可能为碳酸钙或氢氧化钙等,题目中的“氟”、“碘”是指元素,与具体形态无关。
故选:D。
【点评】本题考查物质的组成知识,难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键
8.“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为( )
A.硒
B.硅
C.铝
D.锡
【分析】根据题意,《化学鉴原》一书把地壳中含量第二的元素翻译成“矽(xi)”,结合地壳中元素含量,进行分析判断。
【解答】解:《化学鉴原》一书把地壳中含量第二的元素翻译成“矽(xi)”,地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,则如今把这种“矽”元素命名为硅。
故选:B。
【点评】本题难度不大,熟记地壳里各元素的含量是正确解答本题的关键。
9.“中国芯”的主要材料是高纯度的单质硅,其结构类似于金刚石。下列有关硅的说法正确的是( )
A.元素符号为SI
B.属于非金属元素
C.硅是地壳中含量最多的元素
D.单质硅由分子构成
【分析】A、根据元素符号书写方法分析;
B、根据元素的分类方法分析;
C、根据地壳中元素含量高低分析;
D、根据物质的构成进行分析。
【解答】解:A、硅元素符号为Si,故说法错误;
B、地壳中含量最高的金属元素是铝,硅是非金属元素;故说法正确;
C、硅是地壳中含量排第二的元素,故说法错误;
D、单质硅是由硅原子构成的,故说法错误。
故选:B。
【点评】此题难度不大,掌握硅的有关知识即可顺利解答。
10.银可制作感光材料,银的元素符号是( )
A.Hg
B.AG
C.Ag
D.Mg
【分析】书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写。
【解答】解:书写元素符号注意“一大二小”,银的元素符号是Ag。
故选:C。
【点评】本题难度不大,考查元素符号的书写方法(“一大二小”),熟记常见的元素符号是正确解答本题的关键。
11.下列元素符号书写正确的是( )
A.氦
Ne
B.钡
Be
C.锰
MN
D.汞
Hg
【分析】书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写.
【解答】解:A、书写元素符号注意“一大二小”,氦的元素符号是He,故选项错误。
B、书写元素符号注意“一大二小”,钡的元素符号是Ba,故选项错误。
C、书写元素符号注意“一大二小”,锰的元素符号是Mn,故选项错误。
D、书写元素符号注意“一大二小”,汞的元素符号是Hg,故选项正确。
故选:D。
【点评】本题难度不大,考查元素符号的书写方法(“一大二小”),熟记常见的元素符号是正确解答本题的关键.
12.下列属于非金属元素的是( )
A.铝
B.铁
C.钙
D.氧
【分析】金属元素名称一般有“钅”字旁,固态非金属元素名称有“石”字旁,气态非金属元素名称有“气”字头,据此进行分析解答即可。
【解答】解:A、铝带“钅”字旁,属于金属元素,故选项错误。
B、铁带“钅”字旁,属于金属元素,故选项错误。
C、钙带“钅”字旁,属于金属元素,故选项错误。
D、氧带“气”字头,属于气态非金属元素,故选项正确。
故选:D。
【点评】本题难度不大,考查学生辨别元素种类的方法,了解元素的简单分类是正确解答本题的关键。
13.属于金属元素的是( )
A.Zn
B.Si
C.N
D.H
【分析】金属元素名称一般有“钅”字旁,固态非金属元素名称有“石”字旁,气态非金属元素名称有“气”字头,据此进行解答即可。
【解答】解:A、Zn为锌元素的元素符号,带“钅”字旁,属于金属元素,故选项正确。
B、硅为硅元素的元素符号,带“石”字旁,属于固态非金属元素,故选项错误。
C、N为氮元素的元素符号,带“气”字旁,属于气态非金属元素,故选项错误。
D、H为氢元素的元素符号,带“气”字旁,属于气态非金属元素,故选项错误。
故选:A。
【点评】本题难度不大,掌握元素符号的意义、了解元素的简单分类是正确解答本题的关键。
14.溴元素在元素周期表中的信息如图所示,下列说法正确的是( )
A.1个溴原子的质量是79.90
g
B.溴原子的质量由构成其原子的质子和电子决定
C.溴属于非金属元素
D.溴原子的中子数为35
【分析】根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
【解答】解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为79.90,而不是1个溴原子的质量是79.90
g,故选项说法错误。
B、原子的质量主要集中在原子核上,溴原子的质量由构成其原子的质子和中子决定的,故选项说法错误。
C、溴带“氵”字旁,属于液态非金属元素,故选项说法正确。
D、根据元素周期表中的一格可知,左上角的数字为35,表示原子序数为35;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数和核外电子数为35,而不是中子数为35,故选项说法错误。
故选:C。
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力。
15.地壳中元素含量由高到低依次是氧、硅、铝、铁等。如图是硅元素在元素周期表中的信息和铝元素的原子结构示意图。下列说法中正确的是( )
A.硅原子的相对原子质量为28.09g
B.硅元素位于元素周期表的第二周期
C.铝原子易失去最外层的3个电子,形成Al3+
D.由地壳中含量最多的非金属元素和金属元素组成的物质是SiO2
【分析】图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量。
原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层。若原子的最外层电子数为8,则为稀有气体元素,属于相对稳定结构;若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子。
【解答】解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为28.09,相对原子质量单位是“1”,不是“克”,故选项说法错误。
B、根据元素周期表中的一格可知,左上角的数字为14,表示原子序数为14;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为14;核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有4个电子;周期数=原子核外电子层数,硅元素的原子核外有3个电子层,则在元素周期表中,硅元素位于第3周期,故选项说法错误。
C、最外层电子数是3,在化学反应中易失去3个电子而形成带3个单位正电荷的阳离子,形成Al3+,故选项说法正确。
D、地壳中含量最多的非金属元素和金属元素分别是氧元素和铝元素,组成的化合物为氧化铝,氧化铝中铝元素显+3价,氧元素显﹣2价,其化学式为:Al2O3,故选项说法错误。
故选:C。
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、原子结构示意图的含义是正确解答本题的关键。
二.填空题(共5小题)
16.在下列空格里,用“原子、分子或离子”填空。
(1)保持氢气化学性质的最小粒子是氢 原子 。
(2)化学变化中的最小粒子是 原子 ;
(3)在氯化钠的构成中,带负电荷的微粒是氯 离子 。
【分析】物质是由元素组成的,是由微粒构成的,构成物质的微粒有分子、原子和离子;由分子构成的物质,分子是保持物质化学性质的最小微粒,原子是化学变化中的最小微粒。
【解答】解:
(1)保持氢气的化学性质的最小粒子是氢原子。
(2)化学变化中的最小粒子是原子。
(3)在氯化钠的构成中,带负电荷的微粒是氯离子;
故答案为:
(1)原子;
(2)原子;
(3)离子。
【点评】本题考查物质的组成与构成,分子、原子与离子的定义,属基础知识考查。
17.在宏观、微观和符号之间建立联系是化学学科的特点。请根据图示回答。
(1)①可以是 铁(合理即可) (举一例即可)。
(2)②表示的是 分子 (填“分子”或“原子”)。
(3)构成氯化钠的阴离子是 氯离子(或Cl﹣) 。
【分析】(1)根据由原子构成的物质来分析;
(2)根据构成水的基本粒子来分析;
(3)根据氯化钠的构成情况来分析。
【解答】解:(1)金属单质、固态非金属单质与稀有气体是由原子直接构成的,如铁是由铁原子构成的,硫是由硫原子构成的,氦气是由氦原子构成的;故填:铁(合理即可);
(2)水是由水分子构成的,所以②表示分子;故填:分子;
(3)氯化钠是由钠离子与氯离子构成的,其中的阴离子是氯离子﹣﹣Cl﹣;故填:氯离子(或Cl﹣)。
【点评】要想解答好这类题目,要理解和熟记分子、原子、离子、元素与物质之间的关系,以及与之相关的知识.
18.2021年1月15日,袁隆平海水稻团队在第五届国际海水稻论坛上宣布,用8﹣10年改造整治1亿亩盐碱地。海水稻是指有一定耐盐碱性、能在盐碱地生长的一类水稻品种。海水稻脱粒后大米呈胭脂红色,是因为海水稻硒含量比普通大米高7.2倍,有益于人体健康。这里的硒是指
元素 (填“元素”、“分子”或“原子”)。
【分析】食品、药品、营养品等物质中的“硒”等不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【解答】解:海水稻硒含量比普通大米高7.2倍,这里的“硒”等不是以单质、分子、原子等形式存在,这里所指的“硒”是强调存在的元素,与具体形态无关。
故答案为:
元素。
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键。
19.地壳中居前四位的元素(写元素符号)是:
(1) O ;
(2) Si ;
(3) Al ;
(4) Fe 。
【分析】根据地壳中各元素含量的排序及元素符号的书写方法,进行分析解答。
【解答】解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其元素符号分别是O、Si、Al、Fe。
故答案为:
(1)O;
(2)Si;
(3)Al;
(4)Fe。
【点评】本题难度不大,熟记地壳里各元素的含量、元素符号的书写方法是正确解答本题的关键.
20.写出下列元素的符号或名称.
氧 O
铁 Fe
钾 K
Mn 锰
Ca 钙
Hg 汞 .
【分析】根据元素符号的名称、书写原则进行分析解答即可;正确书写元素符号,可以概括为“一大二小”.
【解答】解:书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写.
氧的元素符号是:O;铁的元素符号为Fe;钾的元素符号为K;Mn表示的是锰元素;Ca表示的是钙元素,Hg表示的汞元素;
故填:O;Fe;K;锰;钙;汞.
【点评】本题难度不大,掌握元素符号的书写方法(“一大二小”)是正确解答本题的关键.
三.解答题(共2小题)
21.宏微结合,是化学的核心素养之一。
(1)下列分别盛有不同物质的容器中,所盛物质属于纯净物的是 ACFG (填标号)。
(2)从微观角度看,金刚石和石墨理性质有巨大差异的原因是 碳原子排列方式不同 。
(3)下列物质中,由离子构成的是 D (填标号)。
A.水
B.氦气
C.水银
D.氯化钠
(4)保持二氧化碳化学性质的最小粒子是 二氧化碳分子 (填微粒名称)。
(5)如图1,提起压在容器中的活塞,容器中的水发生汽化,则图2中最能表示水汽化前在相同空间内粒子分布的是 C (填标号)。
【分析】根据纯净物是由一种分子或是原子构成的、物质的微观构成粒子等知识进行分析解答即可。
【解答】解:(1)据图可以看出,A中氧气和液氧都是由氧分子构成的,属于纯净物,B中是氧气和臭氧两种物质,属于混合物,C中只含有一种由原子直接构成的物质,属于纯净物,D中含有两种由原子构成的物质,属于混合物,E中含有两种不同的分子,属于混合物,F中只含有一种分子,属于纯净物,G中的冰和水只含有一种分子,属于纯净物,H中含有过氧化氢和水两种物质,属于混合物,故所盛物质属于纯净物的是ACFG,故填:ACFG;
(2)从微观角度看,金刚石和石墨理性质有巨大差异是因为二者的碳原子排列方式不同,故填:碳原子排列方式不同;
(3)A.水是由水分子构成的;
B.氦气是由氦原子直接构成的;
C.水银是由银原子直接构成的;
D.氯化钠是由钠离子和氯离子构成的;
故填:D;
(4)保持二氧化碳化学性质的最小粒子是二氧化碳分子,故填:二氧化碳分子;
(5)如图1中,提起压在容器中的活塞,容器中的水发生汽化,则水分子间的间隔变大,故图2中最能表示水汽化前在相同空间内粒子分布的是D,故填:D。
【点评】本题考查的是物质的类别以及构成的知识,完成此题,可以依据已有的知识进行。
22.构成物质的粒子之间的相互关系如图:
(1)图中甲所代表的粒子名称是 原子 ;
(2)氧气、汞、氯化钠三种物质中,由离子构成的是 氯化钠 ;
【分析】(1)根据分子是由原子构成以及原子得失电子形成离子进行解答;
(2)根据氯化钠是由离子构成的进行解答。
【解答】解:(1)分子是由原子构成以及原子得失电子形成离子,所以图中甲所代表的粒子名称是原子;故填:原子;
(2)氧气是由氧分子构成的,汞俗称水银,是由汞原子构成的,而氯化钠是由钠离子和氯离子构成的。故填:氯化钠。
【点评】本题考查了分子、原子和离子之间的关系,完成此题,可以依据已有的知识进行。
第2页(共3页)
一.选择题(共15小题)
1.元素观、微粒观是化学的重要观念。下列有关元素和微粒的说法正确的是( )
A.分子、原子能直接构成物质,但离子不能
B.元素的原子核内质子数与中子数一定相等
C.元素的原子序数与该元素原子核电荷数在数值上相同
D.原子是保持物质化学性质的最小微粒
2.生活中接触到的“富硒茶叶”、“加铁酱油”、“加碘食盐”等用品,这里的硒、铁、碘指的是( )
A.原子
B.元素
C.离子
D.单质
3.金属元素种类高达八十余种,性质相似。地球上金属资源广泛存在于地壳和海洋中,地壳中含量最高的金属元素是( )
A.铜
B.铁
C.钠
D.铝
4.氧化汞受热时的变化可用如图表示,下列对于图示的理解错误的是( )
A.原子可结合成分子
B.分子在化学变化中可以再分
C.所有的物质都是由分子构成
D.可用表示氧分子的形成过程
5.下列说法中正确的是( )
A.氯化氢是由氢、氯两种元素组成的
B.氯化氢是由氢气和氯气混合而成的
C.氯化氢是由一个氢原子和一个氯原子构成的
D.一个氯化氢分子是由一个氢元素和一个氯元素组成的
6.铝元素与氯元素最本质的区别是( )
A.相对原子质量不同
B.中子数不同
C.中子数与核外电子数之和不同
D.质子数不同
7.“含氟牙膏”、“加碘食盐”中的“氟”、“碘”指的是( )
A.分子
B.原子
C.离子
D.元素
8.“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为( )
A.硒
B.硅
C.铝
D.锡
9.“中国芯”的主要材料是高纯度的单质硅,其结构类似于金刚石。下列有关硅的说法正确的是( )
A.元素符号为SI
B.属于非金属元素
C.硅是地壳中含量最多的元素
D.单质硅由分子构成
10.银可制作感光材料,银的元素符号是( )
A.Hg
B.AG
C.Ag
D.Mg
11.下列元素符号书写正确的是( )
A.氦
Ne
B.钡
Be
C.锰
MN
D.汞
Hg
12.下列属于非金属元素的是( )
A.铝
B.铁
C.钙
D.氧
13.属于金属元素的是( )
A.Zn
B.Si
C.N
D.H
14.溴元素在元素周期表中的信息如图所示,下列说法正确的是( )
A.1个溴原子的质量是79.90
g
B.溴原子的质量由构成其原子的质子和电子决定
C.溴属于非金属元素
D.溴原子的中子数为35
15.地壳中元素含量由高到低依次是氧、硅、铝、铁等。如图是硅元素在元素周期表中的信息和铝元素的原子结构示意图。下列说法中正确的是( )
A.硅原子的相对原子质量为28.09g
B.硅元素位于元素周期表的第二周期
C.铝原子易失去最外层的3个电子,形成Al3+
D.由地壳中含量最多的非金属元素和金属元素组成的物质是SiO2
二.填空题(共5小题)
16.在下列空格里,用“原子、分子或离子”填空。
(1)保持氢气化学性质的最小粒子是氢
。
(2)化学变化中的最小粒子是
;
(3)在氯化钠的构成中,带负电荷的微粒是氯
。
17.在宏观、微观和符号之间建立联系是化学学科的特点。请根据图示回答。
(1)①可以是
(举一例即可)。
(2)②表示的是
(填“分子”或“原子”)。
(3)构成氯化钠的阴离子是
。
18.2021年1月15日,袁隆平海水稻团队在第五届国际海水稻论坛上宣布,用8﹣10年改造整治1亿亩盐碱地。海水稻是指有一定耐盐碱性、能在盐碱地生长的一类水稻品种。海水稻脱粒后大米呈胭脂红色,是因为海水稻硒含量比普通大米高7.2倍,有益于人体健康。这里的硒是指
(填“元素”、“分子”或“原子”)。
19.地壳中居前四位的元素(写元素符号)是:
(1)
;
(2)
;
(3)
;
(4)
。
20.写出下列元素的符号或名称.
氧
铁
钾
Mn
Ca
Hg
.
三.解答题(共2小题)
21.宏微结合,是化学的核心素养之一。
(1)下列分别盛有不同物质的容器中,所盛物质属于纯净物的是
(填标号)。
(2)从微观角度看,金刚石和石墨理性质有巨大差异的原因是
。
(3)下列物质中,由离子构成的是
(填标号)。
A.水
B.氦气
C.水银
D.氯化钠
(4)保持二氧化碳化学性质的最小粒子是
(填微粒名称)。
(5)如图1,提起压在容器中的活塞,容器中的水发生汽化,则图2中最能表示水汽化前在相同空间内粒子分布的是
(填标号)。
22.构成物质的粒子之间的相互关系如图:
(1)图中甲所代表的粒子名称是
;
(2)氧气、汞、氯化钠三种物质中,由离子构成的是
;
课题三元素(二)第三单元物质构成的奥秘2021~2022学年九年级化学同步练习(人教版)
参考答案与试题解析
一.选择题(共15小题)
1.元素观、微粒观是化学的重要观念。下列有关元素和微粒的说法正确的是( )
A.分子、原子能直接构成物质,但离子不能
B.元素的原子核内质子数与中子数一定相等
C.元素的原子序数与该元素原子核电荷数在数值上相同
D.原子是保持物质化学性质的最小微粒
【分析】A、根据构成物质的基本粒子来分析;
B、根据核内质子数与中子数不一定相等解答;
C、根据元素的原子序数=核电荷数=核内质子数=核外电子数解答;
D、根据由原子构成的物质原子是保持物质化学性质的最小微粒解答。
【解答】解:A、原子、离子和分子是构成物质的三种基本粒子,离子也能直接构成物质,如氯化钠就是由钠离子和氯离子构成的,故A错误;
B、同种元素的原子核内质子数与中子数不一定相等,例如钠原子中质子数为11,中子数为12,故B错误;
C、元素的原子序数=核电荷数=核内质子数=核外电子数,所以元素的原子序数与该元素原子核电荷数在数值上相同,故C正确;
D、由原子构成的物质原子是保持物质化学性质的最小微粒,故D错误。
故选:C。
【点评】本题难度不是很大,熟练掌握分子、原子、离子的概念、特征及掌握构成物质的基本微粒等即可正确解答本题。
2.生活中接触到的“富硒茶叶”、“加铁酱油”、“加碘食盐”等用品,这里的硒、铁、碘指的是( )
A.原子
B.元素
C.离子
D.单质
【分析】食品、药品、营养品、矿泉水等物质中的“氟、钙、碘、硒、铁”不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【解答】解:“加碘食盐”、“富硒茶叶”、“加铁酱油”等用品中的“硒、铁、碘”不是以单质、分子、原子等形式存在,这里所指的“硒、铁、碘”是强调存在的元素,与具体形态无关。
故选:B。
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键。
3.金属元素种类高达八十余种,性质相似。地球上金属资源广泛存在于地壳和海洋中,地壳中含量最高的金属元素是( )
A.铜
B.铁
C.钠
D.铝
【分析】根据地壳中各元素含量的排序及元素的分类进行分析判断。
【解答】解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的金属元素是铝元素。
故选:D。
【点评】本题难度不大,熟记地壳里各元素的含量、了解元素的分类是正确解答本题的关键。
4.氧化汞受热时的变化可用如图表示,下列对于图示的理解错误的是( )
A.原子可结合成分子
B.分子在化学变化中可以再分
C.所有的物质都是由分子构成
D.可用表示氧分子的形成过程
【分析】根据氧化汞分子在加热条件下能分解成汞原子和氧原子,汞原子直接聚集成金属汞,氧原子构成氧分子,氧分子聚集成氧气,进行分析判断。
【解答】解:A、氧原子可以构成氧分子,原子可结合成分子,故选项说法正确。
B、氧化汞分子在加热条件下能分解成汞原子和氧原子,分子在化学变化中可以再分,故选项说法正确。
C、不是所有的物质都是由分子构成,汞是由原子直接构成的,故选项说法错误。
D、1个氧分子是由2个氧原子构成的,可用表示氧分子的形成过程,故选项说法正确。
故选:C。
【点评】本题难度不大,明确氧化汞分子分解的过程、分子和原子的区别等是正确解答本题的关键。
5.下列说法中正确的是( )
A.氯化氢是由氢、氯两种元素组成的
B.氯化氢是由氢气和氯气混合而成的
C.氯化氢是由一个氢原子和一个氯原子构成的
D.一个氯化氢分子是由一个氢元素和一个氯元素组成的
【分析】A、根据物质是由元素组成进行解答;
B、根据氯化氢属于纯净物进行解答;
C、根据物质是由元素组成,分子是由原子构成进行解答;
D、根据分子是由原子构成进行解答.
【解答】解:A、氯化氢是由氢、氯两种元素组成的,故A正确;
B、氯化氢属于纯净物,是由氢、氯两种元素组成的,故B错误;
C、氯化氢是由氢、氯两种元素组成的,一个氯化氢分子是由一个氢原子和一个氯原子构成的,故C错误;
D、一个氯化氢分子是由一个氢原子和一个氯原子构成的,故D错误。
故选:A。
【点评】本题考查了物质的宏观组成和微观构成的知识,完成此题,可以依据已有的知识进行.
6.铝元素与氯元素最本质的区别是( )
A.相对原子质量不同
B.中子数不同
C.中子数与核外电子数之和不同
D.质子数不同
【分析】元素是质子数(即核电荷数)相同的一类原子的总称,进行分析判断。
【解答】解:元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),不同种元素最本质的区别是质子数不同,则铝元素与氯元素最本质的区别是质子数不同。
故选:D。
【点评】本题难度不大,明确决定元素种类的是质子数(即核电荷数)是正确解答本题的关键。
7.“含氟牙膏”、“加碘食盐”中的“氟”、“碘”指的是( )
A.分子
B.原子
C.离子
D.元素
【分析】“含氟牙膏”、“加碘食盐”中的“氟”、“碘”等有多种形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【解答】解:“含氟牙膏”、“加碘食盐”中的“氟”、“碘”等有多种形式存在,如钙元素可能为碳酸钙或氢氧化钙等,题目中的“氟”、“碘”是指元素,与具体形态无关。
故选:D。
【点评】本题考查物质的组成知识,难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键
8.“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为( )
A.硒
B.硅
C.铝
D.锡
【分析】根据题意,《化学鉴原》一书把地壳中含量第二的元素翻译成“矽(xi)”,结合地壳中元素含量,进行分析判断。
【解答】解:《化学鉴原》一书把地壳中含量第二的元素翻译成“矽(xi)”,地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,则如今把这种“矽”元素命名为硅。
故选:B。
【点评】本题难度不大,熟记地壳里各元素的含量是正确解答本题的关键。
9.“中国芯”的主要材料是高纯度的单质硅,其结构类似于金刚石。下列有关硅的说法正确的是( )
A.元素符号为SI
B.属于非金属元素
C.硅是地壳中含量最多的元素
D.单质硅由分子构成
【分析】A、根据元素符号书写方法分析;
B、根据元素的分类方法分析;
C、根据地壳中元素含量高低分析;
D、根据物质的构成进行分析。
【解答】解:A、硅元素符号为Si,故说法错误;
B、地壳中含量最高的金属元素是铝,硅是非金属元素;故说法正确;
C、硅是地壳中含量排第二的元素,故说法错误;
D、单质硅是由硅原子构成的,故说法错误。
故选:B。
【点评】此题难度不大,掌握硅的有关知识即可顺利解答。
10.银可制作感光材料,银的元素符号是( )
A.Hg
B.AG
C.Ag
D.Mg
【分析】书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写。
【解答】解:书写元素符号注意“一大二小”,银的元素符号是Ag。
故选:C。
【点评】本题难度不大,考查元素符号的书写方法(“一大二小”),熟记常见的元素符号是正确解答本题的关键。
11.下列元素符号书写正确的是( )
A.氦
Ne
B.钡
Be
C.锰
MN
D.汞
Hg
【分析】书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写.
【解答】解:A、书写元素符号注意“一大二小”,氦的元素符号是He,故选项错误。
B、书写元素符号注意“一大二小”,钡的元素符号是Ba,故选项错误。
C、书写元素符号注意“一大二小”,锰的元素符号是Mn,故选项错误。
D、书写元素符号注意“一大二小”,汞的元素符号是Hg,故选项正确。
故选:D。
【点评】本题难度不大,考查元素符号的书写方法(“一大二小”),熟记常见的元素符号是正确解答本题的关键.
12.下列属于非金属元素的是( )
A.铝
B.铁
C.钙
D.氧
【分析】金属元素名称一般有“钅”字旁,固态非金属元素名称有“石”字旁,气态非金属元素名称有“气”字头,据此进行分析解答即可。
【解答】解:A、铝带“钅”字旁,属于金属元素,故选项错误。
B、铁带“钅”字旁,属于金属元素,故选项错误。
C、钙带“钅”字旁,属于金属元素,故选项错误。
D、氧带“气”字头,属于气态非金属元素,故选项正确。
故选:D。
【点评】本题难度不大,考查学生辨别元素种类的方法,了解元素的简单分类是正确解答本题的关键。
13.属于金属元素的是( )
A.Zn
B.Si
C.N
D.H
【分析】金属元素名称一般有“钅”字旁,固态非金属元素名称有“石”字旁,气态非金属元素名称有“气”字头,据此进行解答即可。
【解答】解:A、Zn为锌元素的元素符号,带“钅”字旁,属于金属元素,故选项正确。
B、硅为硅元素的元素符号,带“石”字旁,属于固态非金属元素,故选项错误。
C、N为氮元素的元素符号,带“气”字旁,属于气态非金属元素,故选项错误。
D、H为氢元素的元素符号,带“气”字旁,属于气态非金属元素,故选项错误。
故选:A。
【点评】本题难度不大,掌握元素符号的意义、了解元素的简单分类是正确解答本题的关键。
14.溴元素在元素周期表中的信息如图所示,下列说法正确的是( )
A.1个溴原子的质量是79.90
g
B.溴原子的质量由构成其原子的质子和电子决定
C.溴属于非金属元素
D.溴原子的中子数为35
【分析】根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
【解答】解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为79.90,而不是1个溴原子的质量是79.90
g,故选项说法错误。
B、原子的质量主要集中在原子核上,溴原子的质量由构成其原子的质子和中子决定的,故选项说法错误。
C、溴带“氵”字旁,属于液态非金属元素,故选项说法正确。
D、根据元素周期表中的一格可知,左上角的数字为35,表示原子序数为35;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数和核外电子数为35,而不是中子数为35,故选项说法错误。
故选:C。
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力。
15.地壳中元素含量由高到低依次是氧、硅、铝、铁等。如图是硅元素在元素周期表中的信息和铝元素的原子结构示意图。下列说法中正确的是( )
A.硅原子的相对原子质量为28.09g
B.硅元素位于元素周期表的第二周期
C.铝原子易失去最外层的3个电子,形成Al3+
D.由地壳中含量最多的非金属元素和金属元素组成的物质是SiO2
【分析】图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量。
原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层。若原子的最外层电子数为8,则为稀有气体元素,属于相对稳定结构;若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子。
【解答】解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为28.09,相对原子质量单位是“1”,不是“克”,故选项说法错误。
B、根据元素周期表中的一格可知,左上角的数字为14,表示原子序数为14;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为14;核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有4个电子;周期数=原子核外电子层数,硅元素的原子核外有3个电子层,则在元素周期表中,硅元素位于第3周期,故选项说法错误。
C、最外层电子数是3,在化学反应中易失去3个电子而形成带3个单位正电荷的阳离子,形成Al3+,故选项说法正确。
D、地壳中含量最多的非金属元素和金属元素分别是氧元素和铝元素,组成的化合物为氧化铝,氧化铝中铝元素显+3价,氧元素显﹣2价,其化学式为:Al2O3,故选项说法错误。
故选:C。
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、原子结构示意图的含义是正确解答本题的关键。
二.填空题(共5小题)
16.在下列空格里,用“原子、分子或离子”填空。
(1)保持氢气化学性质的最小粒子是氢 原子 。
(2)化学变化中的最小粒子是 原子 ;
(3)在氯化钠的构成中,带负电荷的微粒是氯 离子 。
【分析】物质是由元素组成的,是由微粒构成的,构成物质的微粒有分子、原子和离子;由分子构成的物质,分子是保持物质化学性质的最小微粒,原子是化学变化中的最小微粒。
【解答】解:
(1)保持氢气的化学性质的最小粒子是氢原子。
(2)化学变化中的最小粒子是原子。
(3)在氯化钠的构成中,带负电荷的微粒是氯离子;
故答案为:
(1)原子;
(2)原子;
(3)离子。
【点评】本题考查物质的组成与构成,分子、原子与离子的定义,属基础知识考查。
17.在宏观、微观和符号之间建立联系是化学学科的特点。请根据图示回答。
(1)①可以是 铁(合理即可) (举一例即可)。
(2)②表示的是 分子 (填“分子”或“原子”)。
(3)构成氯化钠的阴离子是 氯离子(或Cl﹣) 。
【分析】(1)根据由原子构成的物质来分析;
(2)根据构成水的基本粒子来分析;
(3)根据氯化钠的构成情况来分析。
【解答】解:(1)金属单质、固态非金属单质与稀有气体是由原子直接构成的,如铁是由铁原子构成的,硫是由硫原子构成的,氦气是由氦原子构成的;故填:铁(合理即可);
(2)水是由水分子构成的,所以②表示分子;故填:分子;
(3)氯化钠是由钠离子与氯离子构成的,其中的阴离子是氯离子﹣﹣Cl﹣;故填:氯离子(或Cl﹣)。
【点评】要想解答好这类题目,要理解和熟记分子、原子、离子、元素与物质之间的关系,以及与之相关的知识.
18.2021年1月15日,袁隆平海水稻团队在第五届国际海水稻论坛上宣布,用8﹣10年改造整治1亿亩盐碱地。海水稻是指有一定耐盐碱性、能在盐碱地生长的一类水稻品种。海水稻脱粒后大米呈胭脂红色,是因为海水稻硒含量比普通大米高7.2倍,有益于人体健康。这里的硒是指
元素 (填“元素”、“分子”或“原子”)。
【分析】食品、药品、营养品等物质中的“硒”等不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述。
【解答】解:海水稻硒含量比普通大米高7.2倍,这里的“硒”等不是以单质、分子、原子等形式存在,这里所指的“硒”是强调存在的元素,与具体形态无关。
故答案为:
元素。
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键。
19.地壳中居前四位的元素(写元素符号)是:
(1) O ;
(2) Si ;
(3) Al ;
(4) Fe 。
【分析】根据地壳中各元素含量的排序及元素符号的书写方法,进行分析解答。
【解答】解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其元素符号分别是O、Si、Al、Fe。
故答案为:
(1)O;
(2)Si;
(3)Al;
(4)Fe。
【点评】本题难度不大,熟记地壳里各元素的含量、元素符号的书写方法是正确解答本题的关键.
20.写出下列元素的符号或名称.
氧 O
铁 Fe
钾 K
Mn 锰
Ca 钙
Hg 汞 .
【分析】根据元素符号的名称、书写原则进行分析解答即可;正确书写元素符号,可以概括为“一大二小”.
【解答】解:书写元素符号时应注意:①有一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写.
氧的元素符号是:O;铁的元素符号为Fe;钾的元素符号为K;Mn表示的是锰元素;Ca表示的是钙元素,Hg表示的汞元素;
故填:O;Fe;K;锰;钙;汞.
【点评】本题难度不大,掌握元素符号的书写方法(“一大二小”)是正确解答本题的关键.
三.解答题(共2小题)
21.宏微结合,是化学的核心素养之一。
(1)下列分别盛有不同物质的容器中,所盛物质属于纯净物的是 ACFG (填标号)。
(2)从微观角度看,金刚石和石墨理性质有巨大差异的原因是 碳原子排列方式不同 。
(3)下列物质中,由离子构成的是 D (填标号)。
A.水
B.氦气
C.水银
D.氯化钠
(4)保持二氧化碳化学性质的最小粒子是 二氧化碳分子 (填微粒名称)。
(5)如图1,提起压在容器中的活塞,容器中的水发生汽化,则图2中最能表示水汽化前在相同空间内粒子分布的是 C (填标号)。
【分析】根据纯净物是由一种分子或是原子构成的、物质的微观构成粒子等知识进行分析解答即可。
【解答】解:(1)据图可以看出,A中氧气和液氧都是由氧分子构成的,属于纯净物,B中是氧气和臭氧两种物质,属于混合物,C中只含有一种由原子直接构成的物质,属于纯净物,D中含有两种由原子构成的物质,属于混合物,E中含有两种不同的分子,属于混合物,F中只含有一种分子,属于纯净物,G中的冰和水只含有一种分子,属于纯净物,H中含有过氧化氢和水两种物质,属于混合物,故所盛物质属于纯净物的是ACFG,故填:ACFG;
(2)从微观角度看,金刚石和石墨理性质有巨大差异是因为二者的碳原子排列方式不同,故填:碳原子排列方式不同;
(3)A.水是由水分子构成的;
B.氦气是由氦原子直接构成的;
C.水银是由银原子直接构成的;
D.氯化钠是由钠离子和氯离子构成的;
故填:D;
(4)保持二氧化碳化学性质的最小粒子是二氧化碳分子,故填:二氧化碳分子;
(5)如图1中,提起压在容器中的活塞,容器中的水发生汽化,则水分子间的间隔变大,故图2中最能表示水汽化前在相同空间内粒子分布的是D,故填:D。
【点评】本题考查的是物质的类别以及构成的知识,完成此题,可以依据已有的知识进行。
22.构成物质的粒子之间的相互关系如图:
(1)图中甲所代表的粒子名称是 原子 ;
(2)氧气、汞、氯化钠三种物质中,由离子构成的是 氯化钠 ;
【分析】(1)根据分子是由原子构成以及原子得失电子形成离子进行解答;
(2)根据氯化钠是由离子构成的进行解答。
【解答】解:(1)分子是由原子构成以及原子得失电子形成离子,所以图中甲所代表的粒子名称是原子;故填:原子;
(2)氧气是由氧分子构成的,汞俗称水银,是由汞原子构成的,而氯化钠是由钠离子和氯离子构成的。故填:氯化钠。
【点评】本题考查了分子、原子和离子之间的关系,完成此题,可以依据已有的知识进行。
第2页(共3页)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
