1.5物质的溶解(课件 24张PPT)
文档属性
| 名称 | 1.5物质的溶解(课件 24张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 724.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-07-30 12:34:52 | ||
图片预览








文档简介
(共23张PPT)
第5节 物质的溶解
第1章 水和水的溶液
学习目标
1.理解饱和溶液和不饱和溶液的涵义;
2.了解溶液的饱和与不饱和跟溶液浓稀的区别和联系;
3.通过饱和溶液和不饱和溶液之间相互转化的学习,使学生接受事物是相互联系的、量变可以引起质变的科学观点。
新课导入
师:老师知道仓南有一项传统的文化遗产——晒盐。你们知道吗?它的历史已经有3千多年了。有没有同学知道晒盐呢?你能说说晒盐的过程或原理吗?
生:蒸发水。把海水引入盐田,然后太阳晒,盐就出来了。
师:对,古代仓南人民就是利用这些溶解的知识来生产食盐。今天我们就来学习物质在水中的溶解。《引出课题》
新课讲解
一、物质的溶解
老爸,我要喝最甜的糖水,还要加,一直加……
儿子,现在最甜了,再加也不会再变甜了……
思考、讨论:
是儿子还是老爸正确?
嘿,别吵了,去学好科学
就知道了!
新课讲解
物质能无限地溶解在水中吗?
1.定义:一种物质(溶质)在另一种物质(溶剂)里的溶解能力。
物质的溶解性
讨论
新课讲解
1.面粉和蔗糖放入水中,是否都能溶解
2.衣服上沾了油污,用水洗不干净,但汽油却能洗去油污。
3.你冲糖水的时候用热水还是冷水,为什么?
蔗糖能够溶解在水中,而面粉几乎不溶。
油污不溶于水,却很容易溶解在汽油中。
蔗糖在热水中溶解得既快又多。
联系生活
新课讲解
猜想一:溶解性与溶质的性质有关
猜想二:溶解性与溶剂的性质有关
猜想三:溶解性与温度有关
……
猜想:影响物质溶解性的因素?
如何设计实验验证猜想——控制变量法:对比实验
新课讲解
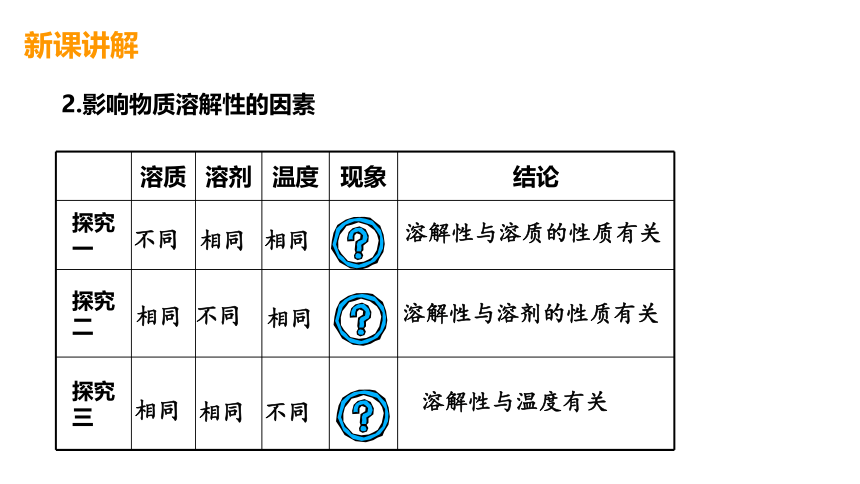
2.影响物质溶解性的因素
溶质 溶剂 温度 现象 结论
探究一
探究二
探究三
溶解性与温度有关
溶解性与溶质的性质有关
溶解性与溶剂的性质有关
相同
相同
不同
相同
相同
不同
相同
相同
不同
新课讲解
实验1: 用量筒各量取5 mL水,分别加入A、B、C三支试管中,再分别加入食盐、蔗糖、熟石灰各1 g,振荡片刻,静置,观察物质的溶解情况。
序号 溶质 溶剂 现象
1 食盐1 g 水5 mL
2 蔗糖1 g 水5 mL
3 熟石灰1 g 水5 mL
结论 食盐完全溶解
蔗糖完全溶解
熟石灰没有完全溶解
注意:固体物质的溶解性有强有弱,如食盐、蔗糖、硝酸钾等易溶于水,而熟石灰微溶于水,碳酸钙却不溶于水。
溶解性与溶质的性质有关
新课讲解
实验2:取A、B两支试管,分别滴入少量食用油。往试管A中加入少量水,往试管B中加入少量汽油,振荡,观察现象。
序号 溶质 溶剂 现象
4 植物油 水
5 植物油 汽油
结论 植物油不溶于水
植物油能溶于汽油中
注意:在生活和生产中,人们常用酒精、汽油、氯仿、苯、香蕉水等溶剂溶解某些在水中难以溶解的物质。
溶解性与溶剂的性质有关
新课讲解
实验3:取1支试管,加入5 mL水,然后加入3 g硝酸钾,充分振荡,硝酸钾是否能完全溶解?如不能完全溶解,将试管加热,观察实验现象。
序号 溶质 溶剂 温度 现象
6 硝酸钾3 g 水5 mL 室温
7 硝酸钾3 g 水5 mL 加热
结论 固体没有全部溶解
固体全部溶解
溶解性与温度有关
注意:(1)多数固体物质的溶解性随着温度的升高而增强,如硝酸钾 。(2)极少数固体物质的溶解性随着温度的升高而减弱,如熟石灰。
新课讲解
胡萝卜如果生吃,其中的β-胡萝卜素只有25%被吸收,如果用食用油烹调后,则能吸收95%,你知道吸收效率高低的道理吗?
β-胡萝卜素在水中的溶解性小,而在食用油中的溶解性大。
想一想
新课讲解
3.物质溶解性等级:
(1)易溶:如蔗糖、食盐、硝酸钾、酒精等……
(2)可溶:如硼酸、二氧化碳等……
(3)微溶:如熟石灰、氧气等……
(4)难溶:如石灰石、石膏粉、植物油、氢气等……
说明:上述例子中的物质均指在水中的溶解性
新课讲解
硝酸钾溶液
硝酸钾
晶体
氢氧化钠溶液
氢氧化钠
4.溶解过程中的热量变化
硝酸钾溶于水后温度明显降低
氢氧化钠溶于水后温度明显升高
结论:物质在溶解过程中有热量变化。
新课讲解
讨论
二、饱和溶液与不饱和溶液
实验1: 分别取出适量的硝酸钾溶液加入A、B、C三支试管中,再分别向试管中加入少量硝酸钾晶体,振荡,观察固体是否溶解。
实验现象:试管中的硝酸钾固体不能再溶解。
我们称之为硝酸钾的饱和溶液。
新课讲解
在一定温度、一定量的溶剂中, 不能再溶解某种溶质的溶液,称为这种溶质的饱和溶液。
饱和溶液:
不饱和溶液:
在一定温度、一定量的溶剂中, 还能继续溶解某种溶质的溶液,称为这种溶质的不饱和溶液。
新课讲解
实验2:
在A试管中再加入适量水,观察未溶解的硝酸钾是否继续溶解。
实验现象:试管中的硝酸钾固体能继续溶解。
实验3:
在酒精灯上加热B试管,观察未溶解的硝酸钾是否继续溶解。
实验现象:试管中的硝酸钾固体能继续溶解。
新课讲解
实验4:在C试管中再加入适量氯化钠固体,观察氯化钠固体是否能溶解。
实验现象:试管中的氯化钠固体能溶解。
新课讲解
交流讨论:
饱和溶液一定
是浓溶液。
稀溶液一定是
不饱和溶液。
他们的说法是否正确?为什么?
新课讲解
加溶质
蒸发溶剂
降温
饱和溶液
不饱和溶液
加溶剂
升温
浓溶液和稀溶液:
检验饱和溶液的方法:
取样,加入少量该溶质,观察能否继续溶解。
⑴饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀
溶液;
⑵相同温度,同一溶质的溶液,饱和溶液比不饱和溶液
要浓一些。
新课讲解
小结
4
定义:
影响因素:
溶质性质
溶剂性质
一种物质(溶质)在另一种物质(溶剂)里的溶解能力
温度
等级:
溶解过程中的热量变化:
易溶、可溶、微溶、难溶
硝酸钾溶于水会吸热
氢氧化钠溶于水会放热
物质的
溶解性
练习:判断下列说法是否正确?
(1)不能再溶解某种溶质的溶液叫饱和溶液。
(2)装有饱和溶液的瓶底,一定有这种溶质
的固体存在。
(3)固体溶质在溶液中稳定存在,则该溶液
一定是饱和溶液。
(4)使一不饱和的溶液变成饱和溶液,可采用
倒出一些溶液实现。
当堂小练
√
当堂小练
D
1.下列因素不会影响物质溶解性的是( )
A.溶质的性质 B.溶剂的质量
C.溶剂的性质 D.温度
2.在一定温度下,某物质的饱和溶液一定是( )
A.浓溶液 B.不能溶解任何物质的溶液
C.稀溶液 D.不能继续溶解该物质的溶液
B
第5节 物质的溶解
第1章 水和水的溶液
学习目标
1.理解饱和溶液和不饱和溶液的涵义;
2.了解溶液的饱和与不饱和跟溶液浓稀的区别和联系;
3.通过饱和溶液和不饱和溶液之间相互转化的学习,使学生接受事物是相互联系的、量变可以引起质变的科学观点。
新课导入
师:老师知道仓南有一项传统的文化遗产——晒盐。你们知道吗?它的历史已经有3千多年了。有没有同学知道晒盐呢?你能说说晒盐的过程或原理吗?
生:蒸发水。把海水引入盐田,然后太阳晒,盐就出来了。
师:对,古代仓南人民就是利用这些溶解的知识来生产食盐。今天我们就来学习物质在水中的溶解。《引出课题》
新课讲解
一、物质的溶解
老爸,我要喝最甜的糖水,还要加,一直加……
儿子,现在最甜了,再加也不会再变甜了……
思考、讨论:
是儿子还是老爸正确?
嘿,别吵了,去学好科学
就知道了!
新课讲解
物质能无限地溶解在水中吗?
1.定义:一种物质(溶质)在另一种物质(溶剂)里的溶解能力。
物质的溶解性
讨论
新课讲解
1.面粉和蔗糖放入水中,是否都能溶解
2.衣服上沾了油污,用水洗不干净,但汽油却能洗去油污。
3.你冲糖水的时候用热水还是冷水,为什么?
蔗糖能够溶解在水中,而面粉几乎不溶。
油污不溶于水,却很容易溶解在汽油中。
蔗糖在热水中溶解得既快又多。
联系生活
新课讲解
猜想一:溶解性与溶质的性质有关
猜想二:溶解性与溶剂的性质有关
猜想三:溶解性与温度有关
……
猜想:影响物质溶解性的因素?
如何设计实验验证猜想——控制变量法:对比实验
新课讲解
2.影响物质溶解性的因素
溶质 溶剂 温度 现象 结论
探究一
探究二
探究三
溶解性与温度有关
溶解性与溶质的性质有关
溶解性与溶剂的性质有关
相同
相同
不同
相同
相同
不同
相同
相同
不同
新课讲解
实验1: 用量筒各量取5 mL水,分别加入A、B、C三支试管中,再分别加入食盐、蔗糖、熟石灰各1 g,振荡片刻,静置,观察物质的溶解情况。
序号 溶质 溶剂 现象
1 食盐1 g 水5 mL
2 蔗糖1 g 水5 mL
3 熟石灰1 g 水5 mL
结论 食盐完全溶解
蔗糖完全溶解
熟石灰没有完全溶解
注意:固体物质的溶解性有强有弱,如食盐、蔗糖、硝酸钾等易溶于水,而熟石灰微溶于水,碳酸钙却不溶于水。
溶解性与溶质的性质有关
新课讲解
实验2:取A、B两支试管,分别滴入少量食用油。往试管A中加入少量水,往试管B中加入少量汽油,振荡,观察现象。
序号 溶质 溶剂 现象
4 植物油 水
5 植物油 汽油
结论 植物油不溶于水
植物油能溶于汽油中
注意:在生活和生产中,人们常用酒精、汽油、氯仿、苯、香蕉水等溶剂溶解某些在水中难以溶解的物质。
溶解性与溶剂的性质有关
新课讲解
实验3:取1支试管,加入5 mL水,然后加入3 g硝酸钾,充分振荡,硝酸钾是否能完全溶解?如不能完全溶解,将试管加热,观察实验现象。
序号 溶质 溶剂 温度 现象
6 硝酸钾3 g 水5 mL 室温
7 硝酸钾3 g 水5 mL 加热
结论 固体没有全部溶解
固体全部溶解
溶解性与温度有关
注意:(1)多数固体物质的溶解性随着温度的升高而增强,如硝酸钾 。(2)极少数固体物质的溶解性随着温度的升高而减弱,如熟石灰。
新课讲解
胡萝卜如果生吃,其中的β-胡萝卜素只有25%被吸收,如果用食用油烹调后,则能吸收95%,你知道吸收效率高低的道理吗?
β-胡萝卜素在水中的溶解性小,而在食用油中的溶解性大。
想一想
新课讲解
3.物质溶解性等级:
(1)易溶:如蔗糖、食盐、硝酸钾、酒精等……
(2)可溶:如硼酸、二氧化碳等……
(3)微溶:如熟石灰、氧气等……
(4)难溶:如石灰石、石膏粉、植物油、氢气等……
说明:上述例子中的物质均指在水中的溶解性
新课讲解
硝酸钾溶液
硝酸钾
晶体
氢氧化钠溶液
氢氧化钠
4.溶解过程中的热量变化
硝酸钾溶于水后温度明显降低
氢氧化钠溶于水后温度明显升高
结论:物质在溶解过程中有热量变化。
新课讲解
讨论
二、饱和溶液与不饱和溶液
实验1: 分别取出适量的硝酸钾溶液加入A、B、C三支试管中,再分别向试管中加入少量硝酸钾晶体,振荡,观察固体是否溶解。
实验现象:试管中的硝酸钾固体不能再溶解。
我们称之为硝酸钾的饱和溶液。
新课讲解
在一定温度、一定量的溶剂中, 不能再溶解某种溶质的溶液,称为这种溶质的饱和溶液。
饱和溶液:
不饱和溶液:
在一定温度、一定量的溶剂中, 还能继续溶解某种溶质的溶液,称为这种溶质的不饱和溶液。
新课讲解
实验2:
在A试管中再加入适量水,观察未溶解的硝酸钾是否继续溶解。
实验现象:试管中的硝酸钾固体能继续溶解。
实验3:
在酒精灯上加热B试管,观察未溶解的硝酸钾是否继续溶解。
实验现象:试管中的硝酸钾固体能继续溶解。
新课讲解
实验4:在C试管中再加入适量氯化钠固体,观察氯化钠固体是否能溶解。
实验现象:试管中的氯化钠固体能溶解。
新课讲解
交流讨论:
饱和溶液一定
是浓溶液。
稀溶液一定是
不饱和溶液。
他们的说法是否正确?为什么?
新课讲解
加溶质
蒸发溶剂
降温
饱和溶液
不饱和溶液
加溶剂
升温
浓溶液和稀溶液:
检验饱和溶液的方法:
取样,加入少量该溶质,观察能否继续溶解。
⑴饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀
溶液;
⑵相同温度,同一溶质的溶液,饱和溶液比不饱和溶液
要浓一些。
新课讲解
小结
4
定义:
影响因素:
溶质性质
溶剂性质
一种物质(溶质)在另一种物质(溶剂)里的溶解能力
温度
等级:
溶解过程中的热量变化:
易溶、可溶、微溶、难溶
硝酸钾溶于水会吸热
氢氧化钠溶于水会放热
物质的
溶解性
练习:判断下列说法是否正确?
(1)不能再溶解某种溶质的溶液叫饱和溶液。
(2)装有饱和溶液的瓶底,一定有这种溶质
的固体存在。
(3)固体溶质在溶液中稳定存在,则该溶液
一定是饱和溶液。
(4)使一不饱和的溶液变成饱和溶液,可采用
倒出一些溶液实现。
当堂小练
√
当堂小练
D
1.下列因素不会影响物质溶解性的是( )
A.溶质的性质 B.溶剂的质量
C.溶剂的性质 D.温度
2.在一定温度下,某物质的饱和溶液一定是( )
A.浓溶液 B.不能溶解任何物质的溶液
C.稀溶液 D.不能继续溶解该物质的溶液
B
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
