6.2二氧化碳制取的研究-2021-2022学年化学人教版九年级上册随堂小测(有答案)
文档属性
| 名称 | 6.2二氧化碳制取的研究-2021-2022学年化学人教版九年级上册随堂小测(有答案) | 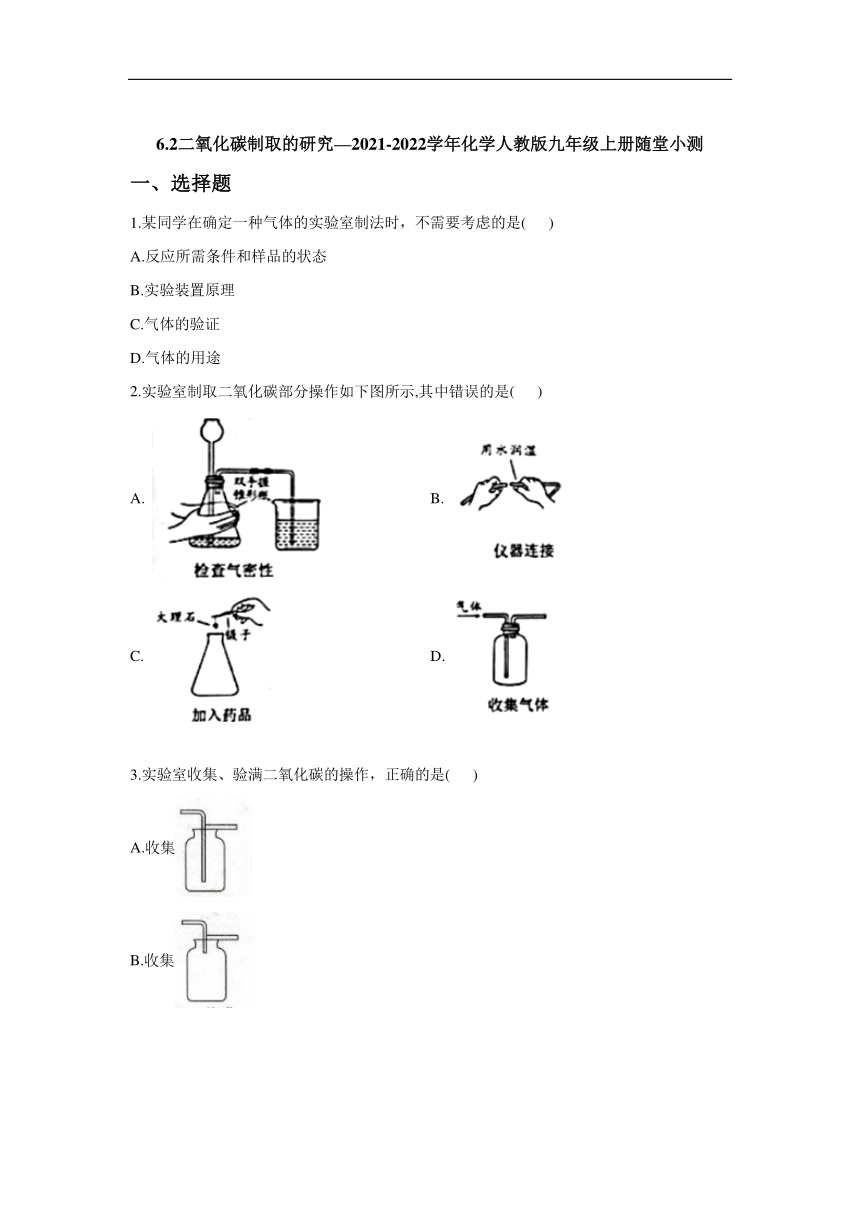 | |
| 格式 | doc | ||
| 文件大小 | 225.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-01 16:27:08 | ||
图片预览



文档简介
6.2二氧化碳制取的研究—2021-2022学年化学人教版九年级上册随堂小测
选择题
1.某同学在确定一种气体的实验室制法时,不需要考虑的是( )
A.反应所需条件和样品的状态
B.实验装置原理
C.气体的验证
D.气体的用途
2.实验室制取二氧化碳部分操作如下图所示,其中错误的是( )
A. B.
C. D.
3.实验室收集、验满二氧化碳的操作,正确的是( )
A.收集
B.收集
C.验满
D.验满
4.厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生。这种气体是( )
A.二氧化碳
B.氧气
C.氢气
D.二氧化硫
5.可生成二氧化碳的反应很多,例如:①酒精的燃烧 ②木炭在空气中燃烧 ③碳与氧化铜反应 ④高温煅烧石灰石 ⑤石灰石与稀硫酸反应 ⑥石灰石与稀盐酸反应 ⑦碳酸钙粉末与浓盐酸⑧人和动物的呼吸作用。其中可用于实验室中制取二氧化碳的是( )
A.①②③ B.③④⑤ C.⑥ D.全部
6.实验室制取二氧化碳有以下步骤:①连接好装置;②向试管中小心放入几小块石灰石;③向试管中小心注入适量稀盐酸;④检查装置的气密性;⑤收集产生的气体;⑥用燃着的木条检验是否收集满二氧化碳。以上操作按由先至后的顺序排列正确的是( )
A.①②③④⑤⑥ B.①④②③⑤⑥ C.①③②④⑤⑥ D.③①②④⑤⑥
7.实验室制取时需用到的仪器是( )
A.铁架台、单孔塞、长颈漏斗、导管、集气瓶
B.大试管、导管、集气瓶、玻璃片、水槽
C.集气瓶、导管、玻璃片、酒精灯、单孔塞
D.集气瓶、锥形瓶、双孔塞、长颈漏斗、导管
非选择题
8.为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究:取21g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,也不反应),并绘制了加入稀盐酸的质量与放出气体质量的坐标图如图。试计算:
(1)碳酸钙完全反应用去稀盐酸的质量为_______g。
(2)反应生成的二氧化碳的质量为_______g。
(3)计算该石灰石样品中碳酸钙的质量分数(写出计算过程,计算结果保留一位小数)。
9.同学们用大理石和稀盐酸制取二氧化碳后,小欣同学发现容器内液体是浑浊的,她很好奇,浑浊液体是什么?于是她和同学们一起将浑浊的液体过滤,得到滤液和固体,并对此展开了探究(溶解于水中的气体成分忽略不计)
【提出问题】滤液中的溶质以及过滤得到的固体的成分是什么?
【查阅资料】
①大理石中含有(不溶于水,且不与盐酸反应),可能含有少量的等。
②溶液遇到硫氰化钾()溶液能够很灵敏显现出红色。
【猜想验证】
Ⅰ经讨论,大家认为滤液中一定含有,原因是 (用化学方程式表示)。
Ⅱ小欣同学根据资料中大理石的成分,猜想滤液中可能含有少量 。
她取少量滤液于试管中,滴加硫氰化钾()溶液,观察到滤液颜色无变化,由此得出的结论是 。
Ⅲ小雨又提出猜想,滤液中还可能含有 (填化学式)。请你和小雨一起验证他的猜想。
实验操作 实验现象 实验结论
取少量滤液于试管中,向其中滴加 。 溶液变成红色 小雨的猜想成立
Ⅳ根据小雨的验证结果,可知过滤得到的固体中含有 。
【得出结论】最终同学们确定了滤液中的溶质以及过滤得到的固体的成分。
10.下列装置是实验室常用装置,请按要求回答下列问题。
(1) 请写出仪器①的名称 。
(2)实验室可用高锰酸钾制取氧气,该反应的化学方程式为 。 欲用该方法制取一瓶较纯净的氧气,要选择的发生装置和收集装置是 。
(3)实验室用E装置来收集集CO2,验满的方法是 。
(4)实验室在常温下用块状电石和水反应制取乙炔气体,由于该反应十分剧烈,所以必须严格控制反应速率.你认为上图中最适宜的发生装置是 。(填字母序号)
(5) 下图所示装置具有多种用途,下列有关它的用途说法中,正确的是 。(填字母序号)
A.该装置用于排空气法收集氢气时,气体应从a端管口通入
B.瓶内装满水,用于收集氧气时,气体应从a端管口通入
C.瓶内装入适量浓硫酸用于干燥CO2时,气体应从a端管口通入
D.瓶内装满氧气,要将氧气排出,水应从a端管口通入
答案以及解析
1.答案:D
2.答案:C
3.答案:A
4.答案:A
解析:稀盐酸和大理石的主要成分碳酸钙反应生成的气体是二氧化碳。
5.答案:C
6.答案:B
解析:制取二氧化碳的操作步骤是:连(连接仪器、组装实验装置)→查(检查装置的气密性)→加(加入固体药品)→倒(倒入液体药品)→定(用铁架台固定仪器装置)→收集(用向上排空气法收集).故正确的操作顺序为:① ④ ② ③ ⑤ ⑥.
故选B.
7.答案:D
解析:根据反应原理和条件确定反应装置的类型后,选择实验仪器。
8.答案:(1)100
(2)8.8
(3)95.2%
解析:(1)观察图象可知完全反应用去稀盐酸的质量为100g;
(2)观察图象可知生成的质量为8.8g;
(3)解:设21g石灰石样品中碳酸钙的质量为x。
则该石灰石样品中碳酸钙的质量分数为。
9.答案: 不含有 石蕊试液
解析:Ⅰ经讨论,大家认为滤液中一定含有,是因为碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳;
Ⅱ小欣同学根据资料中大理石的成分中含有氧化铁,氧化铁能与盐酸反应生成氯化铁,故可以猜想滤液中可能含有少量。
她取少量滤液于试管中,滴加硫氰化钾()溶液,观察到滤液颜色无变化,说明不含有氯化铁。
Ⅲ碳酸钙和盐酸反应时可能盐酸有剩余,故滤液中还可能含有。
要证明盐酸的存在,根据加入的试剂变成了红色,故滴加的是石蕊试液。
Ⅳ由于盐酸有剩余,故碳酸钙全部反应,故可知过滤得到的固体中含有。
10.答案:(1) 锥形瓶(2) ,A,D(3) 将一根燃着的木条放到集气瓶口,若燃着的木条熄灭,说明二氧化碳已经集满,否则不满; (4)C(5)C,D
解析:本题主要考查常见气体的制备与净化。(1)仪器①的名称为锥形瓶;(2)高锰酸钾受热分解会生成锰酸钾、二氧化锰和氧气,反应的化学方程式为;用高锰酸钾制取氛气需加热.故选A装置,收集较纯净的氧气需用排水法。(3)验满二氧化碳的方法为将一根燃着的木条放到集气瓶口,若燃着的木条熄灭,说明二氧化碳已经集满,否则不满;(4)用电石和水制取乙炔,反应物为固体和液体,反应条件为常温,所以发生装置应为固液常温型,又因为B装置无法控制液体的滴加速率.故选C装置,C装置中的注射器相当于分液漏斗.它可以控制液体的滴加速率,进而控制反应的速率;(5)由于氢气的密度比空气小,收集氢气时应从短管(b端)通入,故A错误;排水法收集气体时。气体一律应从短管(b端)通入,故B错误;干燥气体或除去杂质气体时.气体一律应从长管(a端)通入.故C正确;用水将气体排出时,水一律应从长管(a端)通入.故D正确。
选择题
1.某同学在确定一种气体的实验室制法时,不需要考虑的是( )
A.反应所需条件和样品的状态
B.实验装置原理
C.气体的验证
D.气体的用途
2.实验室制取二氧化碳部分操作如下图所示,其中错误的是( )
A. B.
C. D.
3.实验室收集、验满二氧化碳的操作,正确的是( )
A.收集
B.收集
C.验满
D.验满
4.厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生。这种气体是( )
A.二氧化碳
B.氧气
C.氢气
D.二氧化硫
5.可生成二氧化碳的反应很多,例如:①酒精的燃烧 ②木炭在空气中燃烧 ③碳与氧化铜反应 ④高温煅烧石灰石 ⑤石灰石与稀硫酸反应 ⑥石灰石与稀盐酸反应 ⑦碳酸钙粉末与浓盐酸⑧人和动物的呼吸作用。其中可用于实验室中制取二氧化碳的是( )
A.①②③ B.③④⑤ C.⑥ D.全部
6.实验室制取二氧化碳有以下步骤:①连接好装置;②向试管中小心放入几小块石灰石;③向试管中小心注入适量稀盐酸;④检查装置的气密性;⑤收集产生的气体;⑥用燃着的木条检验是否收集满二氧化碳。以上操作按由先至后的顺序排列正确的是( )
A.①②③④⑤⑥ B.①④②③⑤⑥ C.①③②④⑤⑥ D.③①②④⑤⑥
7.实验室制取时需用到的仪器是( )
A.铁架台、单孔塞、长颈漏斗、导管、集气瓶
B.大试管、导管、集气瓶、玻璃片、水槽
C.集气瓶、导管、玻璃片、酒精灯、单孔塞
D.集气瓶、锥形瓶、双孔塞、长颈漏斗、导管
非选择题
8.为测定石灰石样品中碳酸钙的质量分数,某学习小组进行了如下实验探究:取21g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,也不反应),并绘制了加入稀盐酸的质量与放出气体质量的坐标图如图。试计算:
(1)碳酸钙完全反应用去稀盐酸的质量为_______g。
(2)反应生成的二氧化碳的质量为_______g。
(3)计算该石灰石样品中碳酸钙的质量分数(写出计算过程,计算结果保留一位小数)。
9.同学们用大理石和稀盐酸制取二氧化碳后,小欣同学发现容器内液体是浑浊的,她很好奇,浑浊液体是什么?于是她和同学们一起将浑浊的液体过滤,得到滤液和固体,并对此展开了探究(溶解于水中的气体成分忽略不计)
【提出问题】滤液中的溶质以及过滤得到的固体的成分是什么?
【查阅资料】
①大理石中含有(不溶于水,且不与盐酸反应),可能含有少量的等。
②溶液遇到硫氰化钾()溶液能够很灵敏显现出红色。
【猜想验证】
Ⅰ经讨论,大家认为滤液中一定含有,原因是 (用化学方程式表示)。
Ⅱ小欣同学根据资料中大理石的成分,猜想滤液中可能含有少量 。
她取少量滤液于试管中,滴加硫氰化钾()溶液,观察到滤液颜色无变化,由此得出的结论是 。
Ⅲ小雨又提出猜想,滤液中还可能含有 (填化学式)。请你和小雨一起验证他的猜想。
实验操作 实验现象 实验结论
取少量滤液于试管中,向其中滴加 。 溶液变成红色 小雨的猜想成立
Ⅳ根据小雨的验证结果,可知过滤得到的固体中含有 。
【得出结论】最终同学们确定了滤液中的溶质以及过滤得到的固体的成分。
10.下列装置是实验室常用装置,请按要求回答下列问题。
(1) 请写出仪器①的名称 。
(2)实验室可用高锰酸钾制取氧气,该反应的化学方程式为 。 欲用该方法制取一瓶较纯净的氧气,要选择的发生装置和收集装置是 。
(3)实验室用E装置来收集集CO2,验满的方法是 。
(4)实验室在常温下用块状电石和水反应制取乙炔气体,由于该反应十分剧烈,所以必须严格控制反应速率.你认为上图中最适宜的发生装置是 。(填字母序号)
(5) 下图所示装置具有多种用途,下列有关它的用途说法中,正确的是 。(填字母序号)
A.该装置用于排空气法收集氢气时,气体应从a端管口通入
B.瓶内装满水,用于收集氧气时,气体应从a端管口通入
C.瓶内装入适量浓硫酸用于干燥CO2时,气体应从a端管口通入
D.瓶内装满氧气,要将氧气排出,水应从a端管口通入
答案以及解析
1.答案:D
2.答案:C
3.答案:A
4.答案:A
解析:稀盐酸和大理石的主要成分碳酸钙反应生成的气体是二氧化碳。
5.答案:C
6.答案:B
解析:制取二氧化碳的操作步骤是:连(连接仪器、组装实验装置)→查(检查装置的气密性)→加(加入固体药品)→倒(倒入液体药品)→定(用铁架台固定仪器装置)→收集(用向上排空气法收集).故正确的操作顺序为:① ④ ② ③ ⑤ ⑥.
故选B.
7.答案:D
解析:根据反应原理和条件确定反应装置的类型后,选择实验仪器。
8.答案:(1)100
(2)8.8
(3)95.2%
解析:(1)观察图象可知完全反应用去稀盐酸的质量为100g;
(2)观察图象可知生成的质量为8.8g;
(3)解:设21g石灰石样品中碳酸钙的质量为x。
则该石灰石样品中碳酸钙的质量分数为。
9.答案: 不含有 石蕊试液
解析:Ⅰ经讨论,大家认为滤液中一定含有,是因为碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳;
Ⅱ小欣同学根据资料中大理石的成分中含有氧化铁,氧化铁能与盐酸反应生成氯化铁,故可以猜想滤液中可能含有少量。
她取少量滤液于试管中,滴加硫氰化钾()溶液,观察到滤液颜色无变化,说明不含有氯化铁。
Ⅲ碳酸钙和盐酸反应时可能盐酸有剩余,故滤液中还可能含有。
要证明盐酸的存在,根据加入的试剂变成了红色,故滴加的是石蕊试液。
Ⅳ由于盐酸有剩余,故碳酸钙全部反应,故可知过滤得到的固体中含有。
10.答案:(1) 锥形瓶(2) ,A,D(3) 将一根燃着的木条放到集气瓶口,若燃着的木条熄灭,说明二氧化碳已经集满,否则不满; (4)C(5)C,D
解析:本题主要考查常见气体的制备与净化。(1)仪器①的名称为锥形瓶;(2)高锰酸钾受热分解会生成锰酸钾、二氧化锰和氧气,反应的化学方程式为;用高锰酸钾制取氛气需加热.故选A装置,收集较纯净的氧气需用排水法。(3)验满二氧化碳的方法为将一根燃着的木条放到集气瓶口,若燃着的木条熄灭,说明二氧化碳已经集满,否则不满;(4)用电石和水制取乙炔,反应物为固体和液体,反应条件为常温,所以发生装置应为固液常温型,又因为B装置无法控制液体的滴加速率.故选C装置,C装置中的注射器相当于分液漏斗.它可以控制液体的滴加速率,进而控制反应的速率;(5)由于氢气的密度比空气小,收集氢气时应从短管(b端)通入,故A错误;排水法收集气体时。气体一律应从短管(b端)通入,故B错误;干燥气体或除去杂质气体时.气体一律应从长管(a端)通入.故C正确;用水将气体排出时,水一律应从长管(a端)通入.故D正确。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
