2.4辨别物质的元素组成第2课时同步训练-2021-2022学年九年级化学粤教版上册(word版 含答案)
文档属性
| 名称 | 2.4辨别物质的元素组成第2课时同步训练-2021-2022学年九年级化学粤教版上册(word版 含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 144.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-03 07:28:02 | ||
图片预览


文档简介
第2课时 元素周期表、物质的简单分类
易错辨析
1.图是元素周期表中氧元素的信息示意图,请填写:
①表示 ;?②表示 ;?
③表示 ;?④表示 。?
2.请判断下列说法的正误:(在括号内打“√”或“×”)
(1)由一种元素组成的物质一定是单质( )
(2)高锰酸钾中含有氧元素,则高锰酸钾属于氧化物( )
(3)氧气与臭氧都是由氧元素组成的,所以含有氧气和臭氧的物质属于纯净物( )
能力训练
1.[2020·陕西]
认识物质是学习化学的基础。下列物质属于单质的是( )
A.空气
B.干冰
C.液氧
D.生铁
2.下列物质属于氧化物的是( )
A.氧气(O2)
B.五氧化二磷(P2O5)
C.氢氧化钠(NaOH)
D.硫酸(H2SO4)
3.[2020·大连]
我国的5G通信芯片主要由氮化镓材料制成。图是镓元素在元素周期表中的相关信息,下列说法错误的是( )
A.镓属于金属元素
B.镓原子的质子数是31
C.镓原子质量是69.72
g
D.镓原子核外有31个电子
4.[2020·常德]
元素观和微粒观是化学核心观念。下列说法不正确的是( )
A.构成物质的微粒有分子、原子和离子
B.质子数相同的微粒一定是由同种元素形成的
C.化学变化前后原子的种类和个数一定不变
D.原子序数与元素原子核电荷数在数值上相等
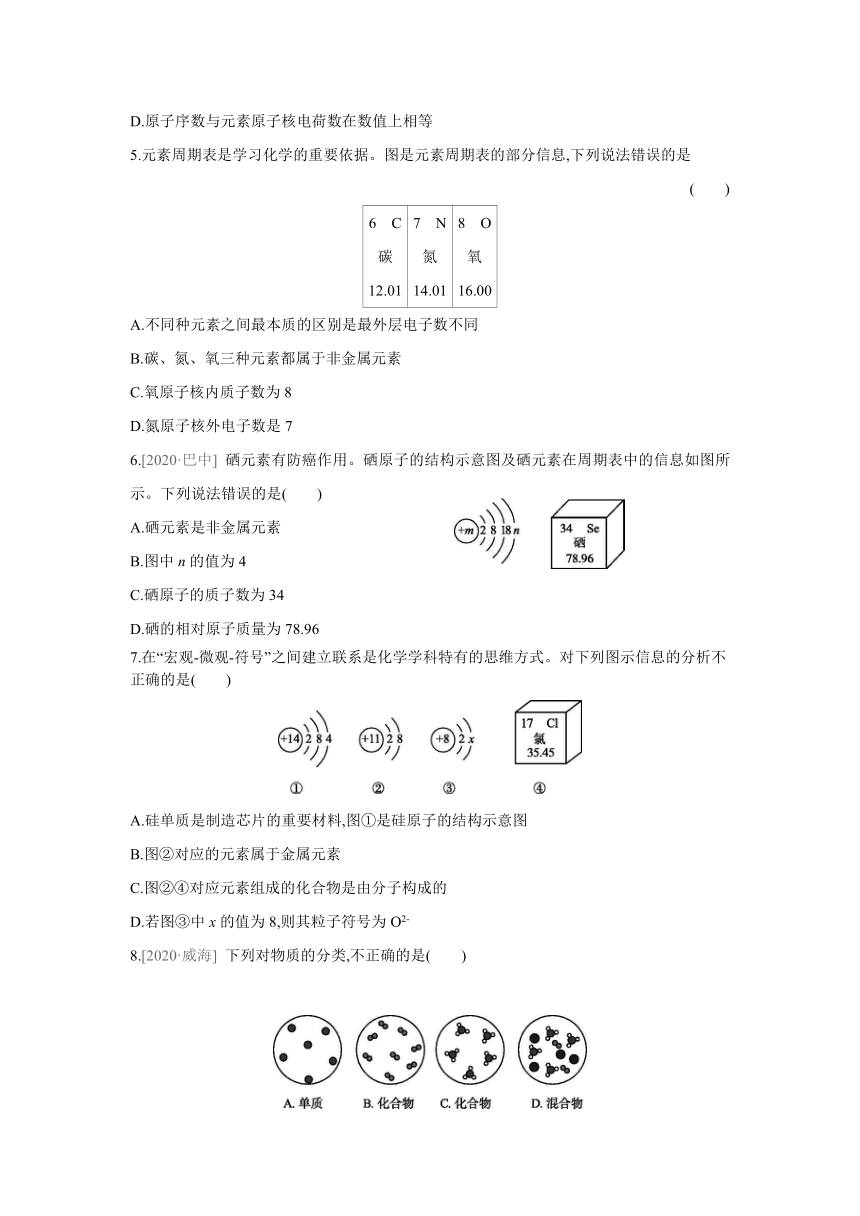
5.元素周期表是学习化学的重要依据。图是元素周期表的部分信息,下列说法错误的是
( )
6 C
碳
12.01
7 N
氮
14.01
8 O
氧
16.00
A.不同种元素之间最本质的区别是最外层电子数不同
B.碳、氮、氧三种元素都属于非金属元素
C.氧原子核内质子数为8
D.氮原子核外电子数是7
6.[2020·巴中]
硒元素有防癌作用。硒原子的结构示意图及硒元素在周期表中的信息如图所示。下列说法错误的是( )
A.硒元素是非金属元素
B.图中n的值为4
C.硒原子的质子数为34
D.硒的相对原子质量为78.96
7.在“宏观-微观-符号”之间建立联系是化学学科特有的思维方式。对下列图示信息的分析不正确的是( )
A.硅单质是制造芯片的重要材料,图①是硅原子的结构示意图
B.图②对应的元素属于金属元素
C.图②④对应元素组成的化合物是由分子构成的
D.若图③中x的值为8,则其粒子符号为O2-
8.[2020·威海]
下列对物质的分类,不正确的是( )
9.分类是研究物质及其变化的重要思想和方法,如图可表示纯净物、单质、化合物、氧化物之间的关系,若整个大圆圈表示纯净物,则下列物质中属于Z范围的是( )
A.氧气
B.澄清石灰水
C.二氧化碳
D.高锰酸钾
10.[2020·泰安]
下列各组物质按单质、化合物、混合物的顺序排列的是( )
A.氮气、过氧化氢、氯酸钾
B.汞、蒸馏水、石油
C.稀有气体、石灰石、烧碱
D.洁净空气、氧化镁、液态氧
11.下列物质:①澄清石灰水、②氧气、③牛奶、④矿泉水、⑤二氧化碳、⑥冰,其中属于混合物的是 (填序号,下同),属于纯净物的是 ,属于单质的是 ,属于化合物的是 。?
12.[2020·齐齐哈尔改编]
学习化学要建立元素观、粒子观和分类观。请根据图所示信息及所学化学知识回答下列问题。
(1)从图A中可知,碘元素的原子序数为 。?
(2)B~E是四种粒子的结构示意图,E形成离子的符号是
,属于同种元素的粒子是
(填字母,下同),B~E中化学性质相似的粒子是 。?
13.[2020·东营]
下表是元素周期表的一部分。
族
周期
ⅠA
0
1
1
H
1.008
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
He
4.003
2
3
Li
6.941
4
Be
9.012
5
B
10.81
6
C
12.01
7
N
14.01
8
O
16.00
9
F
19.00
10
Ne
20.18
3
11Na
22.99
12Mg
24.31
13Al
26.98
14Si
28.09
15P
30.97
16S
32.06
17Cl
35.45
18Ar
39.95
(1)写出空气中含量最多的元素的符号: 。?
(2)图是A、B、C三种粒子的结构示意图,其中属于同种元素的是 (填字母),A粒子与第二周期 元素的原子化学性质相似。?
(3)第8号元素的原子在化学反应中易 (填“得到”或“失去”)电子。?
(4)我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量已成为国际标准。关于相对原子质量,下列叙述错误的是 (填字母)。?
A.相对原子质量与原子质量没有什么差别
B.由于原子的质量太小,使用不方便,所以采用相对原子质量
C.两种原子的质量之比等于它们的相对原子质量之比
D.采用相对原子质量后,就增大了原子的质量
14.化学元素周期表是根据原子序数从小到大排序的化学元素列表。根据元素周期表可以推断原子的半径变化:(1)除第一周期外,其他周期元素(稀有气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。据此比较下列原子半径的大小:O、F、Mg、Al、P、S、K。
。?
典题讲评与答案详析
易错辨析
1.①原子序数 ②元素名称 ③元素符号 ④相对原子质量
2.(1)× (2)× (3)×
能力训练
1.C [解析]
液氧是液态的氧气,氧气是由氧元素一种元素组成的纯净物,属于单质。
2.B [解析]
由两种元素组成,其中一种元素是氧元素的化合物是氧化物。五氧化二磷是由磷、氧两种元素组成的化合物,属于氧化物;氧气只含氧元素,是单质,不属于氧化物;氢氧化钠和硫酸都是由三种元素组成的,不属于氧化物。
3.C [解析]
镓原子的相对原子质量为69.72,单位为“1”,一般省略不写。
4.B [解析]
质子数相同的微粒不一定是同种元素,例如水分子和氖原子质子数都是10。
5.A [解析]
元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素之间最本质的区别是质子数不同。
6.B [解析]
硒原子中,原子序数=核电荷数=质子数=核外电子数=34,即2+8+18+n=34,n=6。
7.C [解析]
本题主要考查元素周期表一格中的信息及原子结构示意图表示的意义。硅原子的质子数为14,图①所示粒子的核内质子数=核外电子数=14,为硅原子的结构示意图;图②对应元素的质子数为11,是钠元素,属于金属元素;图②④对应元素分别是钠元素和氯元素,二者组成的化合物是由离子构成的,不是由分子构成的;若图③中x的值为8,则核外电子数为10,核内质子数为8,该粒子为带2个单位负电荷的氧离子,其粒子符号为O2-。
8.B [解析]
B图中所示的是由同种原子构成的一种分子,属于单质。
9.C
10.B [解析]
氮气是单质,过氧化氢、氯酸钾是化合物;汞是单质,蒸馏水是化合物,石油是混合物;稀有气体、石灰石是混合物,烧碱是化合物;洁净空气是混合物,氧化镁是化合物,液态氧是单质。
11.①③④ ②⑤⑥ ② ⑤⑥
[解析]
澄清石灰水为混合物,氧气为纯净物中的单质,牛奶为混合物,矿泉水为混合物,二氧化碳为纯净物中的化合物,冰为纯净物中的化合物。
12.(1)53 (2)Cl- CD BE
[解析]
(1)碘元素的原子序数为53。(2)E形成离子的符号是Cl-,C、D的核内质子数相等,属于同种元素;B、E的化学性质相似,因为它们最外层电子数相等。
13.(1)N (2)AC 锂 (3)得到 (4)AD
[解析]
(1)空气中含量最多的元素是氮元素,其元素符号为N。(2)质子数决定元素的种类,属于同种元素的是A、C;原子的最外层电子数相同,化学性质相似,A粒子与第二周期锂元素的原子化学性质相似。(3)第8号元素的原子是氧原子,最外层电子数是6,在化学反应中易得到电子。(4)相对原子质量是一个比值,单位是“1”,原子质量的单位是“g”;原子的质量太小,使用不方便,所以采用相对原子质量;原子的相对原子质量与原子的质量成正比,两种原子的质量之比等于它们的相对原子质量之比;相对原子质量是一个比值,采用相对原子质量后,并没有增大原子的质量。
14.K>Mg>Al>P>S>O>F
能熟记前20号元素的名称和元素符号:氢(H)氦(He)锂(Li)铍(Be)硼(B);碳(C)氮(N)氧(O)氟(F)氖(Ne);钠(Na)镁(Mg)铝(Al)硅(Si)磷(P);硫(S)氯(Cl)氩(Ar)钾(K)钙(Ca)。
易错辨析
1.图是元素周期表中氧元素的信息示意图,请填写:
①表示 ;?②表示 ;?
③表示 ;?④表示 。?
2.请判断下列说法的正误:(在括号内打“√”或“×”)
(1)由一种元素组成的物质一定是单质( )
(2)高锰酸钾中含有氧元素,则高锰酸钾属于氧化物( )
(3)氧气与臭氧都是由氧元素组成的,所以含有氧气和臭氧的物质属于纯净物( )
能力训练
1.[2020·陕西]
认识物质是学习化学的基础。下列物质属于单质的是( )
A.空气
B.干冰
C.液氧
D.生铁
2.下列物质属于氧化物的是( )
A.氧气(O2)
B.五氧化二磷(P2O5)
C.氢氧化钠(NaOH)
D.硫酸(H2SO4)
3.[2020·大连]
我国的5G通信芯片主要由氮化镓材料制成。图是镓元素在元素周期表中的相关信息,下列说法错误的是( )
A.镓属于金属元素
B.镓原子的质子数是31
C.镓原子质量是69.72
g
D.镓原子核外有31个电子
4.[2020·常德]
元素观和微粒观是化学核心观念。下列说法不正确的是( )
A.构成物质的微粒有分子、原子和离子
B.质子数相同的微粒一定是由同种元素形成的
C.化学变化前后原子的种类和个数一定不变
D.原子序数与元素原子核电荷数在数值上相等
5.元素周期表是学习化学的重要依据。图是元素周期表的部分信息,下列说法错误的是
( )
6 C
碳
12.01
7 N
氮
14.01
8 O
氧
16.00
A.不同种元素之间最本质的区别是最外层电子数不同
B.碳、氮、氧三种元素都属于非金属元素
C.氧原子核内质子数为8
D.氮原子核外电子数是7
6.[2020·巴中]
硒元素有防癌作用。硒原子的结构示意图及硒元素在周期表中的信息如图所示。下列说法错误的是( )
A.硒元素是非金属元素
B.图中n的值为4
C.硒原子的质子数为34
D.硒的相对原子质量为78.96
7.在“宏观-微观-符号”之间建立联系是化学学科特有的思维方式。对下列图示信息的分析不正确的是( )
A.硅单质是制造芯片的重要材料,图①是硅原子的结构示意图
B.图②对应的元素属于金属元素
C.图②④对应元素组成的化合物是由分子构成的
D.若图③中x的值为8,则其粒子符号为O2-
8.[2020·威海]
下列对物质的分类,不正确的是( )
9.分类是研究物质及其变化的重要思想和方法,如图可表示纯净物、单质、化合物、氧化物之间的关系,若整个大圆圈表示纯净物,则下列物质中属于Z范围的是( )
A.氧气
B.澄清石灰水
C.二氧化碳
D.高锰酸钾
10.[2020·泰安]
下列各组物质按单质、化合物、混合物的顺序排列的是( )
A.氮气、过氧化氢、氯酸钾
B.汞、蒸馏水、石油
C.稀有气体、石灰石、烧碱
D.洁净空气、氧化镁、液态氧
11.下列物质:①澄清石灰水、②氧气、③牛奶、④矿泉水、⑤二氧化碳、⑥冰,其中属于混合物的是 (填序号,下同),属于纯净物的是 ,属于单质的是 ,属于化合物的是 。?
12.[2020·齐齐哈尔改编]
学习化学要建立元素观、粒子观和分类观。请根据图所示信息及所学化学知识回答下列问题。
(1)从图A中可知,碘元素的原子序数为 。?
(2)B~E是四种粒子的结构示意图,E形成离子的符号是
,属于同种元素的粒子是
(填字母,下同),B~E中化学性质相似的粒子是 。?
13.[2020·东营]
下表是元素周期表的一部分。
族
周期
ⅠA
0
1
1
H
1.008
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
He
4.003
2
3
Li
6.941
4
Be
9.012
5
B
10.81
6
C
12.01
7
N
14.01
8
O
16.00
9
F
19.00
10
Ne
20.18
3
11Na
22.99
12Mg
24.31
13Al
26.98
14Si
28.09
15P
30.97
16S
32.06
17Cl
35.45
18Ar
39.95
(1)写出空气中含量最多的元素的符号: 。?
(2)图是A、B、C三种粒子的结构示意图,其中属于同种元素的是 (填字母),A粒子与第二周期 元素的原子化学性质相似。?
(3)第8号元素的原子在化学反应中易 (填“得到”或“失去”)电子。?
(4)我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量已成为国际标准。关于相对原子质量,下列叙述错误的是 (填字母)。?
A.相对原子质量与原子质量没有什么差别
B.由于原子的质量太小,使用不方便,所以采用相对原子质量
C.两种原子的质量之比等于它们的相对原子质量之比
D.采用相对原子质量后,就增大了原子的质量
14.化学元素周期表是根据原子序数从小到大排序的化学元素列表。根据元素周期表可以推断原子的半径变化:(1)除第一周期外,其他周期元素(稀有气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。据此比较下列原子半径的大小:O、F、Mg、Al、P、S、K。
。?
典题讲评与答案详析
易错辨析
1.①原子序数 ②元素名称 ③元素符号 ④相对原子质量
2.(1)× (2)× (3)×
能力训练
1.C [解析]
液氧是液态的氧气,氧气是由氧元素一种元素组成的纯净物,属于单质。
2.B [解析]
由两种元素组成,其中一种元素是氧元素的化合物是氧化物。五氧化二磷是由磷、氧两种元素组成的化合物,属于氧化物;氧气只含氧元素,是单质,不属于氧化物;氢氧化钠和硫酸都是由三种元素组成的,不属于氧化物。
3.C [解析]
镓原子的相对原子质量为69.72,单位为“1”,一般省略不写。
4.B [解析]
质子数相同的微粒不一定是同种元素,例如水分子和氖原子质子数都是10。
5.A [解析]
元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素之间最本质的区别是质子数不同。
6.B [解析]
硒原子中,原子序数=核电荷数=质子数=核外电子数=34,即2+8+18+n=34,n=6。
7.C [解析]
本题主要考查元素周期表一格中的信息及原子结构示意图表示的意义。硅原子的质子数为14,图①所示粒子的核内质子数=核外电子数=14,为硅原子的结构示意图;图②对应元素的质子数为11,是钠元素,属于金属元素;图②④对应元素分别是钠元素和氯元素,二者组成的化合物是由离子构成的,不是由分子构成的;若图③中x的值为8,则核外电子数为10,核内质子数为8,该粒子为带2个单位负电荷的氧离子,其粒子符号为O2-。
8.B [解析]
B图中所示的是由同种原子构成的一种分子,属于单质。
9.C
10.B [解析]
氮气是单质,过氧化氢、氯酸钾是化合物;汞是单质,蒸馏水是化合物,石油是混合物;稀有气体、石灰石是混合物,烧碱是化合物;洁净空气是混合物,氧化镁是化合物,液态氧是单质。
11.①③④ ②⑤⑥ ② ⑤⑥
[解析]
澄清石灰水为混合物,氧气为纯净物中的单质,牛奶为混合物,矿泉水为混合物,二氧化碳为纯净物中的化合物,冰为纯净物中的化合物。
12.(1)53 (2)Cl- CD BE
[解析]
(1)碘元素的原子序数为53。(2)E形成离子的符号是Cl-,C、D的核内质子数相等,属于同种元素;B、E的化学性质相似,因为它们最外层电子数相等。
13.(1)N (2)AC 锂 (3)得到 (4)AD
[解析]
(1)空气中含量最多的元素是氮元素,其元素符号为N。(2)质子数决定元素的种类,属于同种元素的是A、C;原子的最外层电子数相同,化学性质相似,A粒子与第二周期锂元素的原子化学性质相似。(3)第8号元素的原子是氧原子,最外层电子数是6,在化学反应中易得到电子。(4)相对原子质量是一个比值,单位是“1”,原子质量的单位是“g”;原子的质量太小,使用不方便,所以采用相对原子质量;原子的相对原子质量与原子的质量成正比,两种原子的质量之比等于它们的相对原子质量之比;相对原子质量是一个比值,采用相对原子质量后,并没有增大原子的质量。
14.K>Mg>Al>P>S>O>F
能熟记前20号元素的名称和元素符号:氢(H)氦(He)锂(Li)铍(Be)硼(B);碳(C)氮(N)氧(O)氟(F)氖(Ne);钠(Na)镁(Mg)铝(Al)硅(Si)磷(P);硫(S)氯(Cl)氩(Ar)钾(K)钙(Ca)。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
