常考实验小练(5)配制一定溶质质量分数的溶液-2021-2022学年九年级化学鲁教版上册(含解析)
文档属性
| 名称 | 常考实验小练(5)配制一定溶质质量分数的溶液-2021-2022学年九年级化学鲁教版上册(含解析) |
|
|
| 格式 | doc | ||
| 文件大小 | 550.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-03 00:00:00 | ||
图片预览




文档简介
2021-2022学年九年级上册化学鲁教版常考实验小练
(5)配制一定溶质质量分数的溶液
一、知识讲解
仪器的选用及相关仪器的作用
(1)所用仪器:托盘天平(带砝码)、药匙(溶质为固体时)、量筒、胶头滴管、烧杯、玻璃棒。
(2)玻璃棒的作用:搅拌,加快固体或液体溶质的溶解速率。
(3)量筒的作用:量取一定体积的液体。
2、操作步骤
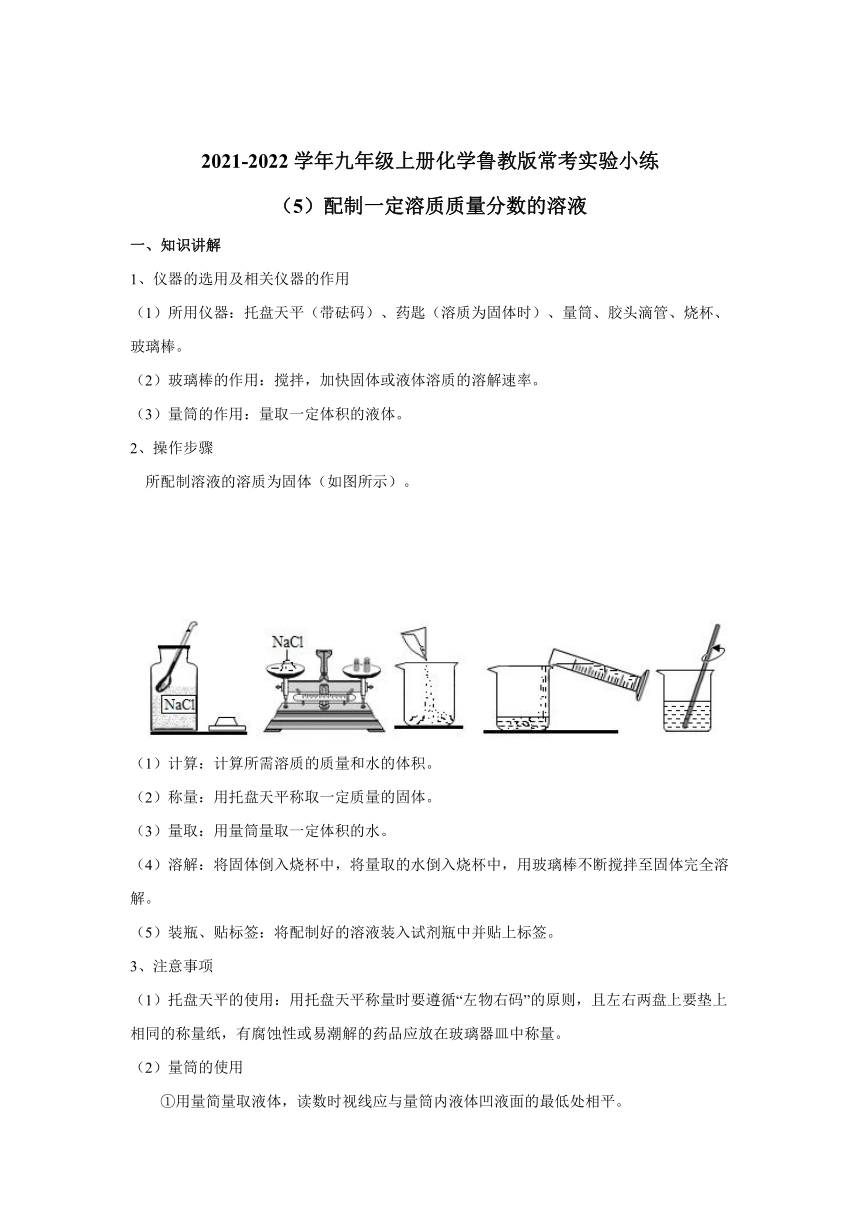
所配制溶液的溶质为固体(如图所示)。
(1)计算:计算所需溶质的质量和水的体积。
(2)称量:用托盘天平称取一定质量的固体。
(3)量取:用量筒量取一定体积的水。
(4)溶解:将固体倒入烧杯中,将量取的水倒入烧杯中,用玻璃棒不断搅拌至固体完全溶解。
(5)装瓶、贴标签:将配制好的溶液装入试剂瓶中并贴上标签。
3、注意事项
(1)托盘天平的使用:用托盘天平称量时要遵循“左物右码”的原则,且左右两盘上要垫上相同的称量纸,有腐蚀性或易潮解的药品应放在玻璃器皿中称量。
(2)量筒的使用
①用量简量取液体,读数时视线应与量筒内液体凹液面的最低处相平。
②选取量简的量程要比所要量取液体体积稍大且越接近越好。
用浓溶液配制一定溶质质量分数的溶液
(1)操作步骤
①计算:计算所需浓溶液的体积和所需水的体积。
②量取:用量简(很接近所需体积时改用胶头滴管)量取浓溶液和水。
③稀释:将量取的浓溶液和水倒入烧杯中用玻璃棒搅拌。
(2)误差分析
①溶质质量分数偏小:量取水的体积时仰视读数;烧杯中原来有少量水;稀释过程中有浓溶液溅出等。②溶质质量分数偏大:量取水时俯视读数等。
二、跟踪练习
1.实验室配制50g溶质质量分数为15%的氯化钠溶液。下列说法不正确的是( )
A.计算:需氯化钠的质量为7.5g,需要水的体积为42.5mL
B.称取氯化钠:托盘天平未经调零即用来称取氯化钠固体
C.量取水:用规格为50mL的量筒量取所需体积的水
D.把配制好的氯化钠溶液转移到指定的容器中,贴上标签备用
2.配制20%的氯化钠溶液时,会造成所配溶液中氯化钠的质量分数偏大的是( )
A.用量筒量取水时俯视读数
B.转移已配好的溶液时,有少量液体溅出
C.氯化钠晶体不纯(杂质难溶于水)
D.烧杯用蒸馏水润洗后,再配制溶液
3.某同学需要配制50g质量分数为15%的氯化钠溶液,步骤如图所示,下列分析正确的是( )
A.配制过程中出现了两处操作错误
B.实验操作步骤为计算、称量、量取、蒸发
C.若所有操作都正确,完全溶解后有液滴溅出,会导致溶质的质量分数偏小
D.配制时应称量氯化钠固体质量为70g
4.某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )
①需称取氢氧化钠固体2.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体(易潮解)时,为防止污染托盘,可将氢氧化钠放在纸上称量
④选用250mL量筒量取18mL的水
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A.①④
B.③④⑤
C.④⑤
D.②③⑤
5.用NaOH固体配制200g10%的NaOH溶液,下列装置或操作正确的是( )
A.用细口瓶保存NaOH固体
B.用托盘天平称取NaOH固体
C.用烧杯溶解NaOH固体
D.用广口瓶存放NaOH溶液
6.农业上常用质量分数为16%的NaCl溶液选种。实验室配制100g该浓度溶液的过程如图所示。下列说法不正确的是( )
A.实验操作顺序为②④①⑤③
B.②中需称量NaCl的质量为16g
C.选100mL量筒量取所需水的体积
D.①中有部分固体撒落,所得溶液的浓度将偏小
7.某同学在配制50g溶质质量分数为5%的食盐溶液的实验中,称量时将砝码放在左盘(1g以下用游码),食盐放在右盘,量水时仰视液面读数。这样配制的食盐溶液中溶质的质量分数( )
A.等于5%
B.大于5%
C.小于5%
D.不能确定
8.新型冠状病毒肺炎疫情期间,生活中使用的75%的消毒酒精是用95%的医用酒精稀释而成的,以下操作正确的是( )
A.配制溶液时要用到托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管等仪器
B.操作中量取水时,若仰视液面则配制所得溶液体积分数偏小
C.配制溶液的步骤是计算、称量、溶解
D.配制的酒精溶液在转移装瓶时,部分飞溅会导致溶液体积分数偏小
9.实验室选用下列仪器配制50 g质量分数为6%的氯化钠溶液。
(1) 所需氯化钠固体的质量为 g.
(2) 完成该实验,上图中有一种仪器不必用到,请写出该仪器的名称。
(3) 若其他操作正确,量取水时俯视量筒读数,对结果会造成什么影响?
10.实验室按如图步骤配制100g质量分数为22%的蔗糖溶液。回答下列问题:
(1)所需蔗糖的质量为______。
(2)用规格为______(填“50”“100”或“500”)mL的量筒量取______mL蒸馏水倒入盛有蔗糖的烧杯中进行溶解。(水的密度约为)
(3)溶解时玻璃棒的作用是______。
(4)下列情况会导致所配溶液中溶质的质量分数偏高的是______(填序号)。
A.蔗糖中混有少量杂质
B.称量时蔗糖和砝码位置放反了(使用了游码)
C.用于溶解蔗糖的烧杯洗净后残留有少量的水
D.用量筒量取水时,俯视读数
答案以及解析
1.答案:B
解析:A. 需氯化钠的质量为50g×15%=7.5g,需要水的质量为50g-7.5g=42.5g,即水的体积为42.5mL,故正确;
B. 托盘天平要先调零再用来称取氯化钠固体,故错误;
C. 需要水的体积为42.5mL,用规格为50mL的量筒量取所需体积的水,故正确;
D. 把配制好的氯化钠溶液转移到指定的容器中,贴上标签备用,正确;
故选:B。
2.答案:A
解析:用量筒量取水时,俯视读数,实际量取的水的体积偏小,使溶质质量分数偏大;溶液具有均一性,将配制好的溶液转移到试剂瓶时,有液体溅出溶质质量分数不变;氯化钠晶体不纯,会使所配溶液溶质质量分数偏小;配制溶液的烧杯先用蒸馏水润洗,烧杯内会残留少量的水,使所配溶液溶质质量分数偏小。故选A。
3.答案:A
解析:托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了;量取液体时,视线应与量筒内液体凹液面的最低处保持水平,图中仰视刻度;配制过程中出现了两处操作错误,故A选项说法正确。配制50g质量分数为15%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,不需要进行蒸发操作,故B选项说法错误。若所有操作都正确,完全溶解后有液滴溅出,因溶液具有均一性,所以溶质质量分数不变,故C选项说法错误。溶质质量=溶液质量×溶质的质量分数,配制50g质量分数为15%的氯化钠溶液,需氯化钠的质量为50g×15%=7.5g,故D选项说法错误。
4.答案:B
解析:溶质质量=溶液质量×溶质质量分数,配制20g溶质质量分数为10%的氢氧化钠溶液,需称取氢氧化钠固体20g×10%=2.0g,故①正确;称量前托盘天平应先检查游码是否归零,并调节平衡,故②正确;氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,故③错误;溶剂质量=溶液质量-溶质质量,则所需水的质量为20g-2g=18g(合18mL),不宜选用250mL的量筒量取,故④错误;用刚洗涤的试剂瓶盛装氢氧化钠溶液,会导致溶剂偏多,溶质质量分数偏低,故⑤错误。故选B。
5.答案:C
解析:氢氧化钠固体应保存在广口瓶中,故A错误;氢氧化钠固体易潮解且具有腐蚀性,应该放在玻璃器皿中称量,故B错误;烧杯可用于溶解固体,故C正确;氢氧化钠溶液应该存放在细口瓶内,故D错误。
6.答案:A
解析:配制100g16%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,实验操作顺序为④②①⑤③,A错误;配制16%的氯化钠溶液100g,需氯化钠的质量为100g×16%=16g,B正确;所需水的质量为100g-16g=84g(合84mL),应用规格为100mL的量筒量取水,C正确;①中有部分固体撒落,会造成实际所取的溶质的质量偏小,所得溶液的浓度将偏小,D正确。
7.答案:C
解析:计算可得,“配制50g溶质质量分数为5%的食盐溶液”需要食盐的质量为50g×5%=
25g,需要水的质量是47.5g。在称量时砝码放在左盘,食盐放在右盘,则食盐的实际质量2g-0.5g=1.5g;量取水时仰视液面读数,则量取的水的实际体积大于47.5mL。错误的操作造成了溶剂的量偏多,而溶质的质量偏少,因此,配制的食盐溶液的溶质质量分数小于5%,C正确。
8.答案:B
解析:利用浓溶液配制稀溶液,采用加水稀释的方法,其操作步骤是计算、量取、稀释,量筒和胶头滴管用于量取95%的医用酒精和水,烧杯、玻璃棒用于进行稀释操作,无需使用托盘天平、药匙,故A、C选项说法错误。用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则所配制溶液的体积分数偏小,故B选项说法正确。溶液具有均一性,配制的酒精溶液在转移装瓶时部分飞溅,溶液的体积分数不变,故D选项说法错误。
9.答案:(1) 3.0g(2)漏斗(3)会使量取的水的量偏小,溶质质量分数偏大
10.答案:(1)22g(2)100;78(3)搅拌,加速溶解(4)D
解析:(1)溶质质量=溶液质量×溶质的质量分数,配制100g质量分数为22%的蔗糖溶液,需蔗糖的质量为100g×22%=22g。
(2)量筒量程选择的依据有两点:一是保证一次量完,二是量程要与液体的取用量最接近。溶剂质量=溶液质量-溶质质量,所需溶剂的质量为100g-22g=78g(合78mL),应用规格为100mL的量筒量取78mL蒸馏水。
(3)溶解时玻璃棒的作用是搅拌,加快溶解速率。
(4)蔗糖中混有少量杂质,会造成实际所取的溶质的质量偏小,则使所配溶液的溶质质量分数偏小,故A选项错误。称量时蔗糖和砝码位置放反了(使用了游码),会造成实际所取的溶质的质量偏小,则使所配溶液的溶质质量分数偏小,故B选项错误。用于溶解蔗糖的烧杯洗净后残留有少量的水,会造成实际使用的水的体积偏大,则使所配溶液的溶质质量分数偏小,故C选项错误。用量筒量取水时,俯视读数,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使所配溶液的溶质质量分数偏大,故D选项正确。
(5)配制一定溶质质量分数的溶液
一、知识讲解
仪器的选用及相关仪器的作用
(1)所用仪器:托盘天平(带砝码)、药匙(溶质为固体时)、量筒、胶头滴管、烧杯、玻璃棒。
(2)玻璃棒的作用:搅拌,加快固体或液体溶质的溶解速率。
(3)量筒的作用:量取一定体积的液体。
2、操作步骤
所配制溶液的溶质为固体(如图所示)。
(1)计算:计算所需溶质的质量和水的体积。
(2)称量:用托盘天平称取一定质量的固体。
(3)量取:用量筒量取一定体积的水。
(4)溶解:将固体倒入烧杯中,将量取的水倒入烧杯中,用玻璃棒不断搅拌至固体完全溶解。
(5)装瓶、贴标签:将配制好的溶液装入试剂瓶中并贴上标签。
3、注意事项
(1)托盘天平的使用:用托盘天平称量时要遵循“左物右码”的原则,且左右两盘上要垫上相同的称量纸,有腐蚀性或易潮解的药品应放在玻璃器皿中称量。
(2)量筒的使用
①用量简量取液体,读数时视线应与量筒内液体凹液面的最低处相平。
②选取量简的量程要比所要量取液体体积稍大且越接近越好。
用浓溶液配制一定溶质质量分数的溶液
(1)操作步骤
①计算:计算所需浓溶液的体积和所需水的体积。
②量取:用量简(很接近所需体积时改用胶头滴管)量取浓溶液和水。
③稀释:将量取的浓溶液和水倒入烧杯中用玻璃棒搅拌。
(2)误差分析
①溶质质量分数偏小:量取水的体积时仰视读数;烧杯中原来有少量水;稀释过程中有浓溶液溅出等。②溶质质量分数偏大:量取水时俯视读数等。
二、跟踪练习
1.实验室配制50g溶质质量分数为15%的氯化钠溶液。下列说法不正确的是( )
A.计算:需氯化钠的质量为7.5g,需要水的体积为42.5mL
B.称取氯化钠:托盘天平未经调零即用来称取氯化钠固体
C.量取水:用规格为50mL的量筒量取所需体积的水
D.把配制好的氯化钠溶液转移到指定的容器中,贴上标签备用
2.配制20%的氯化钠溶液时,会造成所配溶液中氯化钠的质量分数偏大的是( )
A.用量筒量取水时俯视读数
B.转移已配好的溶液时,有少量液体溅出
C.氯化钠晶体不纯(杂质难溶于水)
D.烧杯用蒸馏水润洗后,再配制溶液
3.某同学需要配制50g质量分数为15%的氯化钠溶液,步骤如图所示,下列分析正确的是( )
A.配制过程中出现了两处操作错误
B.实验操作步骤为计算、称量、量取、蒸发
C.若所有操作都正确,完全溶解后有液滴溅出,会导致溶质的质量分数偏小
D.配制时应称量氯化钠固体质量为70g
4.某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )
①需称取氢氧化钠固体2.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体(易潮解)时,为防止污染托盘,可将氢氧化钠放在纸上称量
④选用250mL量筒量取18mL的水
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A.①④
B.③④⑤
C.④⑤
D.②③⑤
5.用NaOH固体配制200g10%的NaOH溶液,下列装置或操作正确的是( )
A.用细口瓶保存NaOH固体
B.用托盘天平称取NaOH固体
C.用烧杯溶解NaOH固体
D.用广口瓶存放NaOH溶液
6.农业上常用质量分数为16%的NaCl溶液选种。实验室配制100g该浓度溶液的过程如图所示。下列说法不正确的是( )
A.实验操作顺序为②④①⑤③
B.②中需称量NaCl的质量为16g
C.选100mL量筒量取所需水的体积
D.①中有部分固体撒落,所得溶液的浓度将偏小
7.某同学在配制50g溶质质量分数为5%的食盐溶液的实验中,称量时将砝码放在左盘(1g以下用游码),食盐放在右盘,量水时仰视液面读数。这样配制的食盐溶液中溶质的质量分数( )
A.等于5%
B.大于5%
C.小于5%
D.不能确定
8.新型冠状病毒肺炎疫情期间,生活中使用的75%的消毒酒精是用95%的医用酒精稀释而成的,以下操作正确的是( )
A.配制溶液时要用到托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管等仪器
B.操作中量取水时,若仰视液面则配制所得溶液体积分数偏小
C.配制溶液的步骤是计算、称量、溶解
D.配制的酒精溶液在转移装瓶时,部分飞溅会导致溶液体积分数偏小
9.实验室选用下列仪器配制50 g质量分数为6%的氯化钠溶液。
(1) 所需氯化钠固体的质量为 g.
(2) 完成该实验,上图中有一种仪器不必用到,请写出该仪器的名称。
(3) 若其他操作正确,量取水时俯视量筒读数,对结果会造成什么影响?
10.实验室按如图步骤配制100g质量分数为22%的蔗糖溶液。回答下列问题:
(1)所需蔗糖的质量为______。
(2)用规格为______(填“50”“100”或“500”)mL的量筒量取______mL蒸馏水倒入盛有蔗糖的烧杯中进行溶解。(水的密度约为)
(3)溶解时玻璃棒的作用是______。
(4)下列情况会导致所配溶液中溶质的质量分数偏高的是______(填序号)。
A.蔗糖中混有少量杂质
B.称量时蔗糖和砝码位置放反了(使用了游码)
C.用于溶解蔗糖的烧杯洗净后残留有少量的水
D.用量筒量取水时,俯视读数
答案以及解析
1.答案:B
解析:A. 需氯化钠的质量为50g×15%=7.5g,需要水的质量为50g-7.5g=42.5g,即水的体积为42.5mL,故正确;
B. 托盘天平要先调零再用来称取氯化钠固体,故错误;
C. 需要水的体积为42.5mL,用规格为50mL的量筒量取所需体积的水,故正确;
D. 把配制好的氯化钠溶液转移到指定的容器中,贴上标签备用,正确;
故选:B。
2.答案:A
解析:用量筒量取水时,俯视读数,实际量取的水的体积偏小,使溶质质量分数偏大;溶液具有均一性,将配制好的溶液转移到试剂瓶时,有液体溅出溶质质量分数不变;氯化钠晶体不纯,会使所配溶液溶质质量分数偏小;配制溶液的烧杯先用蒸馏水润洗,烧杯内会残留少量的水,使所配溶液溶质质量分数偏小。故选A。
3.答案:A
解析:托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了;量取液体时,视线应与量筒内液体凹液面的最低处保持水平,图中仰视刻度;配制过程中出现了两处操作错误,故A选项说法正确。配制50g质量分数为15%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,不需要进行蒸发操作,故B选项说法错误。若所有操作都正确,完全溶解后有液滴溅出,因溶液具有均一性,所以溶质质量分数不变,故C选项说法错误。溶质质量=溶液质量×溶质的质量分数,配制50g质量分数为15%的氯化钠溶液,需氯化钠的质量为50g×15%=7.5g,故D选项说法错误。
4.答案:B
解析:溶质质量=溶液质量×溶质质量分数,配制20g溶质质量分数为10%的氢氧化钠溶液,需称取氢氧化钠固体20g×10%=2.0g,故①正确;称量前托盘天平应先检查游码是否归零,并调节平衡,故②正确;氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,故③错误;溶剂质量=溶液质量-溶质质量,则所需水的质量为20g-2g=18g(合18mL),不宜选用250mL的量筒量取,故④错误;用刚洗涤的试剂瓶盛装氢氧化钠溶液,会导致溶剂偏多,溶质质量分数偏低,故⑤错误。故选B。
5.答案:C
解析:氢氧化钠固体应保存在广口瓶中,故A错误;氢氧化钠固体易潮解且具有腐蚀性,应该放在玻璃器皿中称量,故B错误;烧杯可用于溶解固体,故C正确;氢氧化钠溶液应该存放在细口瓶内,故D错误。
6.答案:A
解析:配制100g16%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,实验操作顺序为④②①⑤③,A错误;配制16%的氯化钠溶液100g,需氯化钠的质量为100g×16%=16g,B正确;所需水的质量为100g-16g=84g(合84mL),应用规格为100mL的量筒量取水,C正确;①中有部分固体撒落,会造成实际所取的溶质的质量偏小,所得溶液的浓度将偏小,D正确。
7.答案:C
解析:计算可得,“配制50g溶质质量分数为5%的食盐溶液”需要食盐的质量为50g×5%=
25g,需要水的质量是47.5g。在称量时砝码放在左盘,食盐放在右盘,则食盐的实际质量2g-0.5g=1.5g;量取水时仰视液面读数,则量取的水的实际体积大于47.5mL。错误的操作造成了溶剂的量偏多,而溶质的质量偏少,因此,配制的食盐溶液的溶质质量分数小于5%,C正确。
8.答案:B
解析:利用浓溶液配制稀溶液,采用加水稀释的方法,其操作步骤是计算、量取、稀释,量筒和胶头滴管用于量取95%的医用酒精和水,烧杯、玻璃棒用于进行稀释操作,无需使用托盘天平、药匙,故A、C选项说法错误。用量筒量取水时,仰视液面,读数比实际液体体积小,会造成实际量取的水的体积偏大,则所配制溶液的体积分数偏小,故B选项说法正确。溶液具有均一性,配制的酒精溶液在转移装瓶时部分飞溅,溶液的体积分数不变,故D选项说法错误。
9.答案:(1) 3.0g(2)漏斗(3)会使量取的水的量偏小,溶质质量分数偏大
10.答案:(1)22g(2)100;78(3)搅拌,加速溶解(4)D
解析:(1)溶质质量=溶液质量×溶质的质量分数,配制100g质量分数为22%的蔗糖溶液,需蔗糖的质量为100g×22%=22g。
(2)量筒量程选择的依据有两点:一是保证一次量完,二是量程要与液体的取用量最接近。溶剂质量=溶液质量-溶质质量,所需溶剂的质量为100g-22g=78g(合78mL),应用规格为100mL的量筒量取78mL蒸馏水。
(3)溶解时玻璃棒的作用是搅拌,加快溶解速率。
(4)蔗糖中混有少量杂质,会造成实际所取的溶质的质量偏小,则使所配溶液的溶质质量分数偏小,故A选项错误。称量时蔗糖和砝码位置放反了(使用了游码),会造成实际所取的溶质的质量偏小,则使所配溶液的溶质质量分数偏小,故B选项错误。用于溶解蔗糖的烧杯洗净后残留有少量的水,会造成实际使用的水的体积偏大,则使所配溶液的溶质质量分数偏小,故C选项错误。用量筒量取水时,俯视读数,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使所配溶液的溶质质量分数偏大,故D选项正确。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
