常考实验小练(6)测定空气中氧气的含量-2021-2022学年九年级化学鲁教版上册(含解析)
文档属性
| 名称 | 常考实验小练(6)测定空气中氧气的含量-2021-2022学年九年级化学鲁教版上册(含解析) |
|
|
| 格式 | doc | ||
| 文件大小 | 998.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-03 00:00:00 | ||
图片预览



文档简介
2021-2022学年九年级上册化学鲁教版常考实验小练
(6)测定空气中氧气的含量
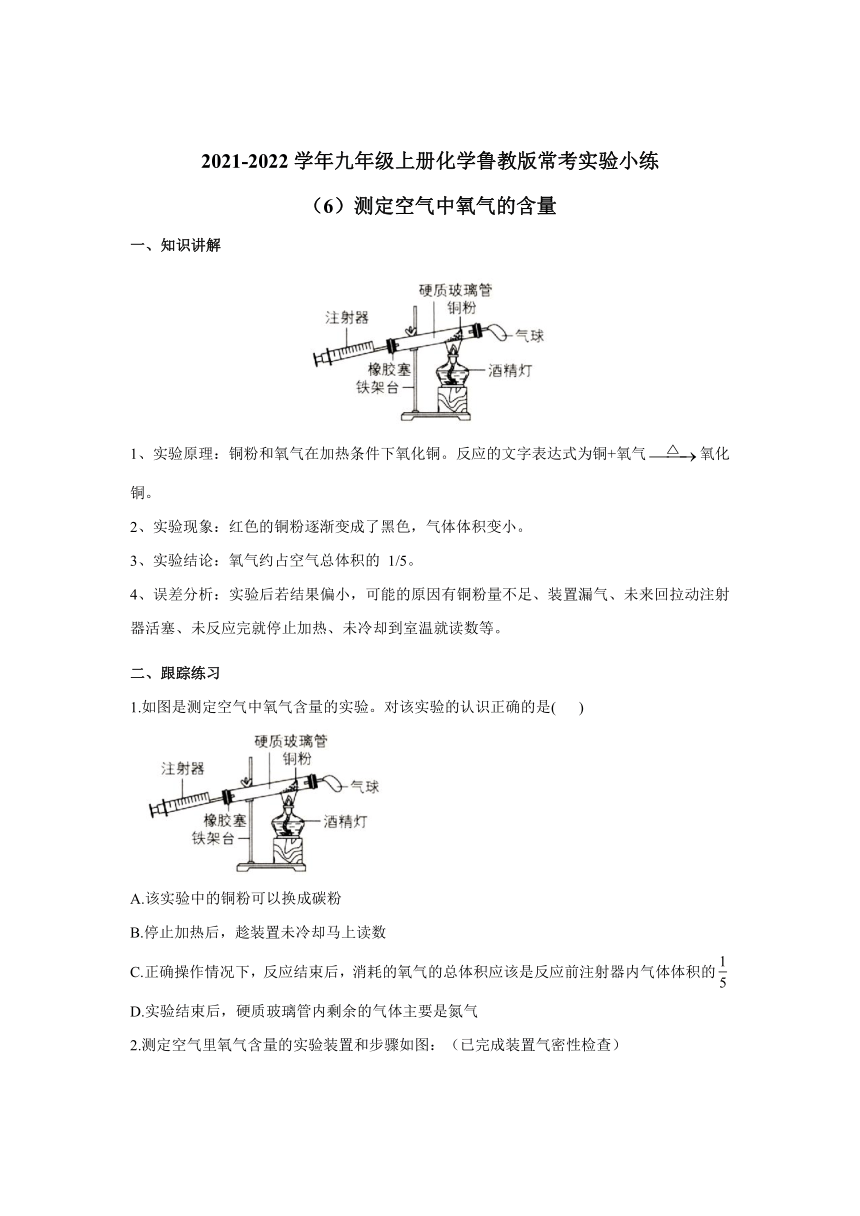
一、知识讲解
1、实验原理:铜粉和氧气在加热条件下氧化铜。反应的文字表达式为铜+氧气氧化铜。
2、实验现象:红色的铜粉逐渐变成了黑色,气体体积变小。
3、实验结论:氧气约占空气总体积的 1/5。
4、误差分析:实验后若结果偏小,可能的原因有铜粉量不足、装置漏气、未来回拉动注射器活塞、未反应完就停止加热、未冷却到室温就读数等。
二、跟踪练习
1.如图是测定空气中氧气含量的实验。对该实验的认识正确的是( )
A.该实验中的铜粉可以换成碳粉
B.停止加热后,趁装置未冷却马上读数
C.正确操作情况下,反应结束后,消耗的氧气的总体积应该是反应前注射器内气体体积的
D.实验结束后,硬质玻璃管内剩余的气体主要是氮气
2.测定空气里氧气含量的实验装置和步骤如图:(已完成装置气密性检查)
①在集气瓶内加入少量水,并将水面上方空间分为5等份;
②用弹簧夹夹紧胶皮管;
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;
④红磷熄灭后,立即打开弹簧夹,观察现象。
其中有错误的实验步骤是( )
A.① B.② C.③ D.④
3.已知铜和氧气在加热条件下会生成氧化铜,可用如图所示装置来测定空气中氧气的含量,实验时点燃酒精灯,反复推拉注射器和挤压气球。对该实验的认识正确的是( )
①铜粉的用量多少会影响实验结果;②实验结束后,待装置冷却至室温才能读数;③气球的作用是调节压强并使氧气完全反应;④在正常操作情况下,反应消耗氧气的体积应该约占反应前注射器内气体体积的
A.①③④ B.②③④ C.①②④ D.①②③
4.利用如图装置验证了空气中氧气的含量。下列叙述不正确的是( )
A.实验前需检查装置气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄灭、试管冷却后再打开止水夹
D.最终量筒中液面约降至40mL刻度线处
5.某校兴趣小组同学在课题组老师的指导下,将“测定空气中氧气的含量”实验装置(如甲图)改进为新的实验装置(如乙图),下列说法不恰当的是( )
A.乙反应容器与甲相比体积更小,药品消耗更少
B.乙反应容器装置简洁,减少了甲装置中导管引起的误差
C.甲装置中反应前若止水夹未夹紧,则进入集气瓶中的水量偏大
D.乙反应容器中点燃白磷,胶塞会先向左后向右移动
6.研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置。请根据图示实验回答下列问题:
(1)闭合电源开关,可以观察到红磷_________。
(2)装置冷却到室温时,可观察到U形管内左侧液面_________。
(3)通过这个实验得出的结论是_________。
(4)你认为影响该实验准确度的地方是_________。
(5)此实验还可推知反应后剩余气体的一条物理性质是_________,一条化学性质是_________。
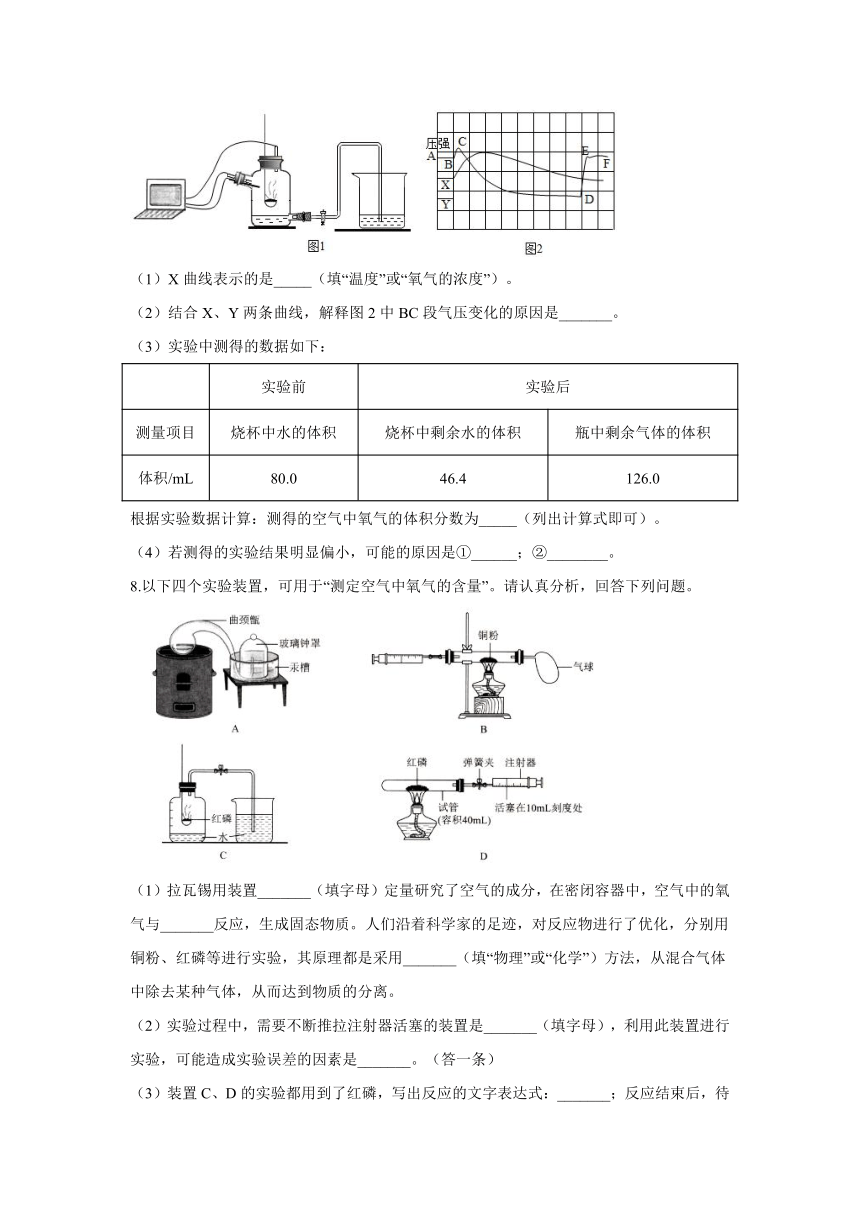
7.为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置图中图1内的压强、温度和氧气浓度,三条曲线变化如图2所示。
(1)X曲线表示的是_____(填“温度”或“氧气的浓度”)。
(2)结合X、Y两条曲线,解释图2中BC段气压变化的原因是_______。
(3)实验中测得的数据如下:
实验前 实验后
测量项目 烧杯中水的体积 烧杯中剩余水的体积 瓶中剩余气体的体积
体积/mL 80.0 46.4 126.0
根据实验数据计算:测得的空气中氧气的体积分数为_____(列出计算式即可)。
(4)若测得的实验结果明显偏小,可能的原因是①______;②________。
8.以下四个实验装置,可用于“测定空气中氧气的含量”。请认真分析,回答下列问题。
(1)拉瓦锡用装置_______(填字母)定量研究了空气的成分,在密闭容器中,空气中的氧气与_______反应,生成固态物质。人们沿着科学家的足迹,对反应物进行了优化,分别用铜粉、红磷等进行实验,其原理都是采用_______(填“物理”或“化学”)方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)实验过程中,需要不断推拉注射器活塞的装置是_______(填字母),利用此装置进行实验,可能造成实验误差的因素是_______。(答一条)
(3)装置C、D的实验都用到了红磷,写出反应的文字表达式:_______;反应结束后,待装置冷却至室温,打开弹簧夹,装置D中(试管容积为40mL),注射器活塞从10mL刻度处缓慢移动至_______mL刻度处停止(误差忽略不计)。
9.在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积的变化。(已知铜在加热的条件下能与空气中的氧气反应生成氧化铜)
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是__________。
(2)写出该实验中发生反应的文字表达式:__________。
(3)小强测得的实验结果如下:
反应前注射器内气体总体积 反应后注射器内气体总体积
25mL 22mL
由此数据可以推算出他测定的空气中氧气的体积分数__________(填“>”“=”或“<”)21%。造成该实验出现误差的原因可能是__________(填序号)。
①交替推动两个注射器活塞时次数过少
②读数时没有冷却至室温
③加入铜丝量太少
④加入铜丝量太多
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是__________。
10.1775年法国化学家拉瓦锡用定量的方法研究了空气的成分。仿照这个历史上著名实验的原理,如今我们的化学教育家积极探索、不断创新,先后设计出了如图所示的实验装置。
测得实验结果如下(气体体积):(单位:mL)
反应前玻璃管内 反应前注射器内 反应后注射器内
40 30 18
(1)在实验过程中,不断推拉注射器的目的是_________________;
(2)由此数据可以推算出他测定的空气中氧气的体积分数为_________________。(保留小数点后一位)
答案以及解析
1.答案:D
解析:碳燃烧生成二氧化碳气体,装置内的压强几乎不变,所以不能用碳粉代替铜粉测定空气中氧气的含量,A错误;停止加热后,要等到装置冷却至室温后再读数,否则测定结果偏小,B错误;正确操作情况下,反应结束后,消耗的氧气的总体积应该是反应前整个装置中气体体积总和的,C错误;足量的铜粉在加热的条件下将装置内的氧气完全耗尽,剩余的气体主要是氮气,D正确。
2.答案:D
解析:在集气瓶内加入少量水,并将水面上方空间分为5等份,①正确。用弹簧夹夹紧胶皮管,防止装置漏气,②正确。点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,防止空气受热膨胀逸出集气瓶,③正确。红磷熄灭后,立即打开弹簧夹,此时剩余的气体温度较高,处于膨胀状态,会使进入集气瓶中的水体积偏小,使测得的结果偏小,④错误。
3.答案:D
解析:铜粉的用量多少会影响实验结果,铜粉量不足时,不能将装置内的氧气除尽,会导致实验结果偏小,①正确;实验结束后,待装置冷却至室温才能读数,否则装置内的气体温度较高,仍处于膨胀状态,会导致实验结果偏小,②正确;气球的作用是调节压强并使氧气完全反应,③正确;在正常操作情况下,反应消耗氧气的体积应该约占反应前装置(注射器、硬质玻璃管、气球)内气体总体积的,④不正确。故选D。
4.答案:D
解析:A.实验前需检查装置气密性,以防止装置漏气造成结果不准确,故选项说法正确;B.白磷燃烧与氧气反应生成五氧化二磷,白磷的作用是消耗试管中的氧气,故选项说法正确;C.白磷熄灭、试管冷却后再打开止水夹,以防止剩余的气体在受热状态下,处于膨胀状态,占据了部分水的体积,造成结果偏小,故选项说法正确;D.氧气约占空气总体积的,130mL空气中氧气的体积约为130mL×=26mL,最终量筒中液面约降至50-26=24mL刻度线处,故选项说法错误。
5.答案:D
解析:乙改用玻璃管进行实验,比甲中集气瓶体积小,空气体积小,所以药品消耗更少,故A正确;乙反应容器装置简洁,减少了甲装置中导管引起的误差,故B正确;甲装置中反应前若上水夹未夹紧,白磷燃烧放热,导致部分气体通过导管逸出,则进入集气瓶中的水量偏大,故C正确;乙反应容器中点燃白磷,白磷燃烧放热,气体压强增大,胶塞向右移动,完全反应后温度降低,由于氧气被消耗,所以气体压强比开始时小,胶塞向左移动,故D不正确。
6.答案:(1)燃烧,产生大量的白烟
(2)上升至约1刻度处
(3)空气中氧气的体积约占空气体积的
(4)U形管左右液面存在高度差(合理即可)
(5)难溶于水;不燃烧也不支持燃烧
解析:(1)红磷燃烧产生大量的白烟。
(2)装置冷却到室温时,U形管内左侧压强减小,可观察到U形管内左侧液面上升至约1刻度处。
(3)该实验得出的结论是空气中氧气的体积约占空气体积的。
(4)影响该实验准确度的地方有装置漏气、红磷量不足、U形管左右液面存在高度差或红磷位置太高难将下面氧气消耗完等。
(5)剩余气体的物理性质是无色无味、难溶于水;化学性质是不燃烧也不支持燃烧。
7.答案:(1)温度(2)红磷燃烧放热温度升高,压强增大,同时消耗氧气,使气压减小;BC段燃烧放热造成的压强增大强于氧气减少造成的压强减小 (3)×100% (4)红磷的量不足;装置的气密性不好
解析: (1)随着反应进行,红磷燃烧放热,导致温度升高,完全反应后,不再放热,温度逐渐降低至室温,故X曲线表示的是温度。
(2)X、Y两条曲线可知,图2中BC段气压变化的原因是红磷燃烧放热温度升高,压强增大,同时消耗氧气,使气压减小。BC段燃烧放热造成的压强增大强于氧气减少造成的压强减小。
(3)烧杯中减少的水的体积即为瓶内氧气的体积,进入集气瓶内水的体积和剩余气体体积之和即为瓶内空气的体积,测得的空气中氧气的体积分数为。
(4)若测得的实验结果明显偏小,可能的原因是①红磷的量不足;②装置的气密性不好。
8.答案:(1)A;汞;化学
(2)B;反应前后气球的体积不相等
(3)磷+氧气五氧化二磷;2
解析:(3)注射器活塞从10mL刻度处缓慢移动至10mL-40mL×=2mL刻度处停止。
9.答案:(1)使氧气与铜丝充分反应
(2)铜+氧气氧化铜
(3);①②③
(4)通过化学反应除去混合物中的一种成分,再测量混合物在反应前后体积(或质量)的变化,从而得出某种成分的含量
解析:
10.答案:(1)使铜粉与氧气充分反应 (2)17.1%
(6)测定空气中氧气的含量
一、知识讲解
1、实验原理:铜粉和氧气在加热条件下氧化铜。反应的文字表达式为铜+氧气氧化铜。
2、实验现象:红色的铜粉逐渐变成了黑色,气体体积变小。
3、实验结论:氧气约占空气总体积的 1/5。
4、误差分析:实验后若结果偏小,可能的原因有铜粉量不足、装置漏气、未来回拉动注射器活塞、未反应完就停止加热、未冷却到室温就读数等。
二、跟踪练习
1.如图是测定空气中氧气含量的实验。对该实验的认识正确的是( )
A.该实验中的铜粉可以换成碳粉
B.停止加热后,趁装置未冷却马上读数
C.正确操作情况下,反应结束后,消耗的氧气的总体积应该是反应前注射器内气体体积的
D.实验结束后,硬质玻璃管内剩余的气体主要是氮气
2.测定空气里氧气含量的实验装置和步骤如图:(已完成装置气密性检查)
①在集气瓶内加入少量水,并将水面上方空间分为5等份;
②用弹簧夹夹紧胶皮管;
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;
④红磷熄灭后,立即打开弹簧夹,观察现象。
其中有错误的实验步骤是( )
A.① B.② C.③ D.④
3.已知铜和氧气在加热条件下会生成氧化铜,可用如图所示装置来测定空气中氧气的含量,实验时点燃酒精灯,反复推拉注射器和挤压气球。对该实验的认识正确的是( )
①铜粉的用量多少会影响实验结果;②实验结束后,待装置冷却至室温才能读数;③气球的作用是调节压强并使氧气完全反应;④在正常操作情况下,反应消耗氧气的体积应该约占反应前注射器内气体体积的
A.①③④ B.②③④ C.①②④ D.①②③
4.利用如图装置验证了空气中氧气的含量。下列叙述不正确的是( )
A.实验前需检查装置气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄灭、试管冷却后再打开止水夹
D.最终量筒中液面约降至40mL刻度线处
5.某校兴趣小组同学在课题组老师的指导下,将“测定空气中氧气的含量”实验装置(如甲图)改进为新的实验装置(如乙图),下列说法不恰当的是( )
A.乙反应容器与甲相比体积更小,药品消耗更少
B.乙反应容器装置简洁,减少了甲装置中导管引起的误差
C.甲装置中反应前若止水夹未夹紧,则进入集气瓶中的水量偏大
D.乙反应容器中点燃白磷,胶塞会先向左后向右移动
6.研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置。请根据图示实验回答下列问题:
(1)闭合电源开关,可以观察到红磷_________。
(2)装置冷却到室温时,可观察到U形管内左侧液面_________。
(3)通过这个实验得出的结论是_________。
(4)你认为影响该实验准确度的地方是_________。
(5)此实验还可推知反应后剩余气体的一条物理性质是_________,一条化学性质是_________。
7.为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置图中图1内的压强、温度和氧气浓度,三条曲线变化如图2所示。
(1)X曲线表示的是_____(填“温度”或“氧气的浓度”)。
(2)结合X、Y两条曲线,解释图2中BC段气压变化的原因是_______。
(3)实验中测得的数据如下:
实验前 实验后
测量项目 烧杯中水的体积 烧杯中剩余水的体积 瓶中剩余气体的体积
体积/mL 80.0 46.4 126.0
根据实验数据计算:测得的空气中氧气的体积分数为_____(列出计算式即可)。
(4)若测得的实验结果明显偏小,可能的原因是①______;②________。
8.以下四个实验装置,可用于“测定空气中氧气的含量”。请认真分析,回答下列问题。
(1)拉瓦锡用装置_______(填字母)定量研究了空气的成分,在密闭容器中,空气中的氧气与_______反应,生成固态物质。人们沿着科学家的足迹,对反应物进行了优化,分别用铜粉、红磷等进行实验,其原理都是采用_______(填“物理”或“化学”)方法,从混合气体中除去某种气体,从而达到物质的分离。
(2)实验过程中,需要不断推拉注射器活塞的装置是_______(填字母),利用此装置进行实验,可能造成实验误差的因素是_______。(答一条)
(3)装置C、D的实验都用到了红磷,写出反应的文字表达式:_______;反应结束后,待装置冷却至室温,打开弹簧夹,装置D中(试管容积为40mL),注射器活塞从10mL刻度处缓慢移动至_______mL刻度处停止(误差忽略不计)。
9.在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积的变化。(已知铜在加热的条件下能与空气中的氧气反应生成氧化铜)
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是__________。
(2)写出该实验中发生反应的文字表达式:__________。
(3)小强测得的实验结果如下:
反应前注射器内气体总体积 反应后注射器内气体总体积
25mL 22mL
由此数据可以推算出他测定的空气中氧气的体积分数__________(填“>”“=”或“<”)21%。造成该实验出现误差的原因可能是__________(填序号)。
①交替推动两个注射器活塞时次数过少
②读数时没有冷却至室温
③加入铜丝量太少
④加入铜丝量太多
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是__________。
10.1775年法国化学家拉瓦锡用定量的方法研究了空气的成分。仿照这个历史上著名实验的原理,如今我们的化学教育家积极探索、不断创新,先后设计出了如图所示的实验装置。
测得实验结果如下(气体体积):(单位:mL)
反应前玻璃管内 反应前注射器内 反应后注射器内
40 30 18
(1)在实验过程中,不断推拉注射器的目的是_________________;
(2)由此数据可以推算出他测定的空气中氧气的体积分数为_________________。(保留小数点后一位)
答案以及解析
1.答案:D
解析:碳燃烧生成二氧化碳气体,装置内的压强几乎不变,所以不能用碳粉代替铜粉测定空气中氧气的含量,A错误;停止加热后,要等到装置冷却至室温后再读数,否则测定结果偏小,B错误;正确操作情况下,反应结束后,消耗的氧气的总体积应该是反应前整个装置中气体体积总和的,C错误;足量的铜粉在加热的条件下将装置内的氧气完全耗尽,剩余的气体主要是氮气,D正确。
2.答案:D
解析:在集气瓶内加入少量水,并将水面上方空间分为5等份,①正确。用弹簧夹夹紧胶皮管,防止装置漏气,②正确。点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,防止空气受热膨胀逸出集气瓶,③正确。红磷熄灭后,立即打开弹簧夹,此时剩余的气体温度较高,处于膨胀状态,会使进入集气瓶中的水体积偏小,使测得的结果偏小,④错误。
3.答案:D
解析:铜粉的用量多少会影响实验结果,铜粉量不足时,不能将装置内的氧气除尽,会导致实验结果偏小,①正确;实验结束后,待装置冷却至室温才能读数,否则装置内的气体温度较高,仍处于膨胀状态,会导致实验结果偏小,②正确;气球的作用是调节压强并使氧气完全反应,③正确;在正常操作情况下,反应消耗氧气的体积应该约占反应前装置(注射器、硬质玻璃管、气球)内气体总体积的,④不正确。故选D。
4.答案:D
解析:A.实验前需检查装置气密性,以防止装置漏气造成结果不准确,故选项说法正确;B.白磷燃烧与氧气反应生成五氧化二磷,白磷的作用是消耗试管中的氧气,故选项说法正确;C.白磷熄灭、试管冷却后再打开止水夹,以防止剩余的气体在受热状态下,处于膨胀状态,占据了部分水的体积,造成结果偏小,故选项说法正确;D.氧气约占空气总体积的,130mL空气中氧气的体积约为130mL×=26mL,最终量筒中液面约降至50-26=24mL刻度线处,故选项说法错误。
5.答案:D
解析:乙改用玻璃管进行实验,比甲中集气瓶体积小,空气体积小,所以药品消耗更少,故A正确;乙反应容器装置简洁,减少了甲装置中导管引起的误差,故B正确;甲装置中反应前若上水夹未夹紧,白磷燃烧放热,导致部分气体通过导管逸出,则进入集气瓶中的水量偏大,故C正确;乙反应容器中点燃白磷,白磷燃烧放热,气体压强增大,胶塞向右移动,完全反应后温度降低,由于氧气被消耗,所以气体压强比开始时小,胶塞向左移动,故D不正确。
6.答案:(1)燃烧,产生大量的白烟
(2)上升至约1刻度处
(3)空气中氧气的体积约占空气体积的
(4)U形管左右液面存在高度差(合理即可)
(5)难溶于水;不燃烧也不支持燃烧
解析:(1)红磷燃烧产生大量的白烟。
(2)装置冷却到室温时,U形管内左侧压强减小,可观察到U形管内左侧液面上升至约1刻度处。
(3)该实验得出的结论是空气中氧气的体积约占空气体积的。
(4)影响该实验准确度的地方有装置漏气、红磷量不足、U形管左右液面存在高度差或红磷位置太高难将下面氧气消耗完等。
(5)剩余气体的物理性质是无色无味、难溶于水;化学性质是不燃烧也不支持燃烧。
7.答案:(1)温度(2)红磷燃烧放热温度升高,压强增大,同时消耗氧气,使气压减小;BC段燃烧放热造成的压强增大强于氧气减少造成的压强减小 (3)×100% (4)红磷的量不足;装置的气密性不好
解析: (1)随着反应进行,红磷燃烧放热,导致温度升高,完全反应后,不再放热,温度逐渐降低至室温,故X曲线表示的是温度。
(2)X、Y两条曲线可知,图2中BC段气压变化的原因是红磷燃烧放热温度升高,压强增大,同时消耗氧气,使气压减小。BC段燃烧放热造成的压强增大强于氧气减少造成的压强减小。
(3)烧杯中减少的水的体积即为瓶内氧气的体积,进入集气瓶内水的体积和剩余气体体积之和即为瓶内空气的体积,测得的空气中氧气的体积分数为。
(4)若测得的实验结果明显偏小,可能的原因是①红磷的量不足;②装置的气密性不好。
8.答案:(1)A;汞;化学
(2)B;反应前后气球的体积不相等
(3)磷+氧气五氧化二磷;2
解析:(3)注射器活塞从10mL刻度处缓慢移动至10mL-40mL×=2mL刻度处停止。
9.答案:(1)使氧气与铜丝充分反应
(2)铜+氧气氧化铜
(3);①②③
(4)通过化学反应除去混合物中的一种成分,再测量混合物在反应前后体积(或质量)的变化,从而得出某种成分的含量
解析:
10.答案:(1)使铜粉与氧气充分反应 (2)17.1%
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
