第5章 金属的冶炼与利用 测试题(含答案)—2020-2021学年九年级化学沪教版(全国)上册
文档属性
| 名称 | 第5章 金属的冶炼与利用 测试题(含答案)—2020-2021学年九年级化学沪教版(全国)上册 |

|
|
| 格式 | zip | ||
| 文件大小 | 195.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-03 00:00:00 | ||
图片预览




文档简介
第5章《金属的冶炼与利用》测试题
一、单选题
1.下列说法正确的是( )
A.铁燃烧生成氧化铁
B.合金的硬度更大,熔点更高
C.用青铜制作“马踏飞燕”是物理变化
D.铁矿石炼铁得到单质铁
2.下列说法错误的是( )
A.铁在潮湿的空气中容易生锈
B.铜是一种紫红色的金属单质
C.塑料、合金、合成橡胶属于合成材料
D.铝合金密度小,轻便
3.下列化学变化其反应类型属于化合反应的是( )
A.过氧化氢制氧气
B.蜡烛燃烧
C.高锰酸钾制氧气
D.加热金属汞
4.下列有关物质的鉴别方案错误的是
A.用燃着的木条区分氮气和二氧化碳
B.用闻气味的方法鉴别白酒和白醋
C.用二氧化锰区分水和过氧化氢溶液
D.用观察颜色的方法鉴别铜丝和铝丝
5.下图为某反应的微观示意图,下列说法正确的是
A.反应前后分子的种类保持不变
B.这是一个置换反应
C.反应中
与
两物质的质量比为2:1
D.若不放催化剂该反应不能进行
6.通过对下列有关化学反应的归纳,结论正确的是( )
A.,碳燃烧一定产生CO2
B.,属于置换反应
C.,铁桶不能装盐酸
D.,氢氧化钠可以治疗胃酸过多
7.下图所示实验不能用“分子在不停运动”解释的是
A.A
B.B
C.C
D.D
8.为了防止铁制品受腐蚀,下列采取的措施中不可行的是(
)
A.保持铁制品表面的洁净和干燥
B.将铁制品浸在水里使其与空气隔绝
C.制成不锈钢
D.在铁制品表面刷漆
9.有关铝、铁、铜的说法中错误的是
A.铝是地壳中含量最多的金属元素
B.铝能形成氧化保护膜
C.铜可以与稀硫酸反应
D.铝、铜可以用来做电线
10.若金属镍在金属活动性顺序中位于铁和锡之间,已知硫酸镍NiSO4溶于水,则下列反应不正确的是(
)
A.Ni+
H2SO4=NiSO4+H2↑
B.Fe
+
NiSO4=FeSO4+Ni
C.Ni+2AgNO3=Ni(NO3)2+2Ag
D.Cu+
NiSO4=CuSO4+Ni
11.金属活动性顺序表在化学学习中有重要作用。下列说法正确的是(
)
A.Zn不能置换出稀硫酸中的氢
B.Ag能将硫酸铜溶液中的铜置换出来
C.在Al、Mg、Fe中金属活动性最强的是Al
D.“真金不怕火炼”说明金在高温时也不与氧气反应
12.关于太阳能路灯的说法不正确的是( )
A.铝合金灯柱属于金属材料
B.灯泡中填充氮气作保护气
C.这种路灯可以节约能源,绿色环保
D.硅电池板中的硅元素是地壳中含量最多的元素
13.推理和分析是化学常用的思维方法,下列说法正确的是( )
A.中和反应的实质是H+和OH﹣反应生成水
B.一般情况下,合金的熔点和硬度都比组成合金的纯金属高
C.碱的溶液能使酚酞变红,能使酚酞溶液变红的溶液一定是碱的溶液
D.实验室用KClO3、H2O2溶液制氧气的催化剂都是二氧化锰,故化学反应只能用二氧化锰作催化剂
14.有一包金属粉末,可能由
Mg、Zn、Fe、Al、Ag
等金属中的一种或几种组成,取该样品
2.4g,加入
100g
稀硫酸恰好完全反应,得
0.2gH2
和无色溶液。下列说法不正确的是
A.样品中一定不含有
Ag,可能含有
Fe
B.无色溶液中溶质总质量量为
12g
C.稀硫酸的溶质质量分数为
39.2%
D.样品可能由
Zn
和
Al
组成
15.将一定量的铁粉加入到含有Zn(NO3)2、Cu(NO3)2和AgNO3的废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是
A.滤渣中一定含有Ag和Cu,滤液中一定含有Fe(NO3)2
B.滤渣中一定不含Fe,滤液的质量一定比原废液质量大
C.滤渣中一定含有Ag,滤液中可能含有Cu(NO3)2和AgNO3
D.滤渣中一定含有Ag和Cu,滤液中可能含有Cu(NO3)2和AgNO3
二、填空题
16.从下列物质中选择填空(填序号):①干冰
②石墨
③水银
④硝酸铵固体
(1)可做干电池电极的是_______;
(2)溶于水后溶液温度降低的是_______;
(3)用于人工降雨的是_______;
(4)温度计中含有的物质是_______.
17.某化学小组进行如下实验探究:将废铁屑(表面生锈)和铜粉的混合物放入烧杯中,加入稀硫酸,充分反应后烧杯中有固体。过滤,向滤渣中滴加稀硫酸,没有现象。
资料:
Fe+Fe2(SO
4)
3=3FeSO
4
Cu+
Fe2(SO4)3=2FeSO4
+CuSO4
(1)滤液中溶质一定有____________。
(2)自选一种试剂,检验滤液中溶质组成可能存在的几种情况,写出实验操作、预期现象及结论。____________
18.金属在生活生产中有着非常广泛的应用,请回答下列问题:
(1)根据如图金属应用实例推断,金属具有的物理性质有______(答三点);
(2)工业常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为______;
(3)在古代人们把烧红的生铁放在铁砧上反复捶打最终使生铁转化为钢,这就是“百炼成钢”的来历,这样做的目的是降低生铁中______元素的含量。
19.金属材料是在工农业和人们日常生活中用着广泛的应用。解答下列各题。
(1)我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志我国合金制造技术取得重大突破,根据所学知识回答:
①生铁和钢都是铁合金,其中含碳量较高的是__。
②生活中的下列物品,属于金属材料的是____。
A
四氧化三铁
B
玻璃钢
C
盛装饮料的易拉罐
D
有机玻璃
(2)金属钪(Sc)在化合物中常显+3价。在相同条件下取相同状态的Sc和Zn分别与同一种稀硫酸反应,Sc产生气泡明显比Zn快。则两金属的活动性Sc__Zn(填“>或“<”):结合上述结论判断,下列说法不正确的是__。
A、将打磨了的Sc伸入CuCl2溶液中无现象
B、用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag实验,能证明Fe和Sc的活动性
C、用Fe、Sc、稀H2SO4溶液能验证Sc的活动性强于Fe
(3)Sc2O3能与稀硫酸反应的化学方程式为____,该反应属于___反应。
20.2019年1月3日,我国“嫦娥四号”探测器成功登陆月球。“嫦娥四号”的制作材料有硅、石墨、铝合金、钛合金和铜等。
(1)纯金属制成合金,性能会发生改变,请写出其中一条
_______
。
(2)请写出一种比较钛和铜金属活动性强弱的方法
_______
(不要写现象与结论)。
(3)石墨是碳的单质,比较碳和硅的原子结构示意图:
①碳和硅的化学性质相似的原因是
____________
。
②请写出碳和硅原子结构不同的一处
_____________
。
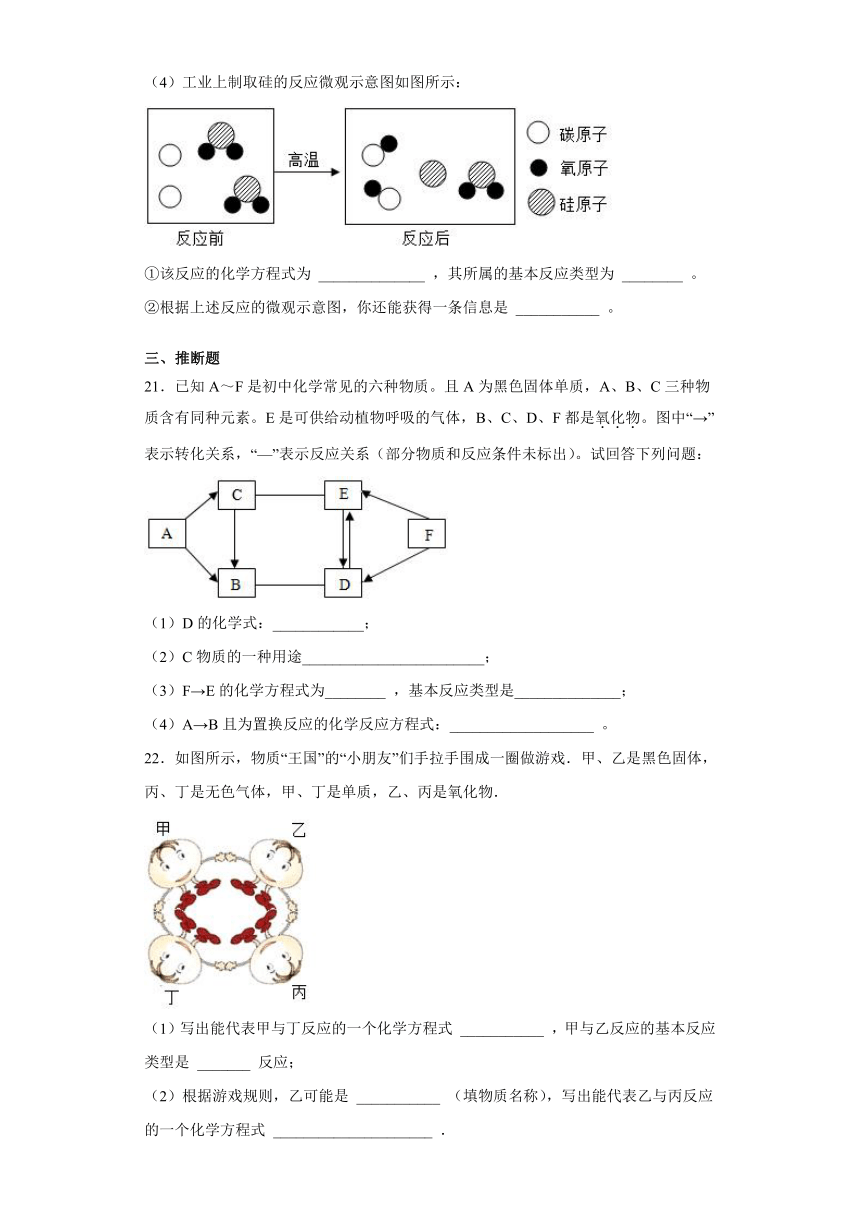
(4)工业上制取硅的反应微观示意图如图所示:
①该反应的化学方程式为
______________
,其所属的基本反应类型为
________
。
②根据上述反应的微观示意图,你还能获得一条信息是
___________
。
三、推断题
21.已知A~F是初中化学常见的六种物质。且A为黑色固体单质,A、B、C三种物质含有同种元素。E是可供给动植物呼吸的气体,B、C、D、F都是氧化物。图中“→”表示转化关系,“—”表示反应关系(部分物质和反应条件未标出)。试回答下列问题:
(1)D的化学式:____________;
(2)C物质的一种用途________________________;
(3)F→E的化学方程式为________
,基本反应类型是______________;
(4)A→B且为置换反应的化学反应方程式:___________________
。
22.如图所示,物质“王国”的“小朋友”们手拉手围成一圈做游戏.甲、乙是黑色固体,丙、丁是无色气体,甲、丁是单质,乙、丙是氧化物.
(1)写出能代表甲与丁反应的一个化学方程式
___________
,甲与乙反应的基本反应类型是
_______
反应;
(2)根据游戏规则,乙可能是
___________
(填物质名称),写出能代表乙与丙反应的一个化学方程式
_____________________
.
四、实验题
23.氧气是我们身边无法离开的物质。某兴趣小组对氧气的研究如下:
I.氧气的制备:
(1)该装置中棉花团的作用是________,图中装置一处明显的错误是________。
II.氧气的收集:
[实验1]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
[实验2]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
[实验3]用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1
实验2
实验3
氧气的体积分数(%)
79.7
79.6
79.9
88.4
89.0
87.9
90.0
89.8
89.3
氧气的平均体积分数(%)
79.7
88.4
89.7
数据分析:
(2)由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是________。
(3)不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是___。
Ⅲ.铁丝在氧气中燃烧
(4)铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是________(填化学式)。将燃烧后的黑色固体粉碎后,滴加稀硫酸,若产生气泡,则原因是__________(用化学反应方程式表示)。
24.某化学兴趣小组根据右图所示进行模拟炼铁的实验,并对产物成分进行探究。
经初步分析:无色气体A不含有单质气体,黑色粉末B含有两种单质中的一种或者两种。
高炉炼铁的原理为:Fe2O3+3CO2Fe+3CO2,请写出反应器中一氧化碳是如何产生的化学方程式:_________________________________________________。
兴趣小组又分成甲乙两组分别对无色气体A和黑色粉末B的成分进行探究。
(猜想与假设)
甲组在分析了炼铁的原理后,认为无色气体A中可能有CO2,也可能有未反应的_____。
乙组认为黑色粉末的成分中存在以下三种情况:
假设一:只含有铁。
假设二:只含有_______。
假设三:以上两种物质都含有。
(实验探究)
(1)为验证甲组的猜想,大家按下图示进行实验(箭头表示气体流向):
当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中灼热的氧化铜变红,可以确定无色气体A的成分为:_____________________,Ⅱ中浓硫酸的作用是:____________________________。
(2)为验证乙组中假设三成立,大家用物理和化学两种方法来进行探究
实验方法
实验操作
实验现象
实验结果
物理方法
_____________________
_______
假设三成立
化学方法
取少量黑色粉末B于试管中,加入过量的稀盐酸
______
假设三成立
写出黑色粉末B中加入过量的稀盐酸反应的化学方程式:______________________。
(交流反思)
在做甲组的实验中发现其存在一个很不环保的缺陷,请指出来_____________________。
五、计算题
25.工业上可利用“铝热反应”焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将某些金属从其氧化物中置换出来。若用铝与氧化铁反应来制取11.2
kg铁。请计算:
(1)氧化铁中铁元素的质量分数_____。
(2)理论上需要消耗铝的质量_____。
26.分别用两种方法测定10g铜锌合金中锌的含量。
加入的试剂
测得数据
方法1
足量稀硫酸
气体0.2
g
方法2
足量硫酸铜溶液
固体质量减少0.1
g
请任选1种方法的数据,计算合金中锌的质量分数(写出计算过程及结果)。
_______
参考答案
1.C
2.C
3.D
4.A
5.B
6.C
7.C
8.B
9.C
10.D
11.D
12.D
13.A
14.D
15.C
16.②
④
①
③
17.
硫酸亚铁
将铁丝伸入盛有滤液的试管中,若铁丝表面有红色固体出现,证明有硫酸铜;反之,没有
18.导电性、导热性、延展性
C
19.生铁
C
>
A
B
复分解
20.抗腐蚀性能变好(强度或硬度更高)
将钛放入硫酸铜(氯化铜)溶液中(将铜放入氯化钛溶液中或将钛和铜分别放入稀盐酸/稀硫酸中等)
最外层电子数相同(最外层电子数都是4
个)
质子数不同(电子层数不同/第二层电子数不同
2C
+
SiO2
2CO
+
Si
置换反应
化学变化中,分子可分(或原子不可分或分子种类改变或原子重新组合或原子种类、数量不变等)
21.H2O
冶炼金属
分解反应
22.C+O2CO2
置换
氧化铜或氧化铁
CO+CuOCu+CO2或Fe2O3+3CO2Fe+3CO2
23.防止高锰酸钾粉末进入导管
试管口向上倾斜(或试管口没有略向下倾斜或试管口不应向上倾斜等合理答案)
延长收集时间
集气瓶中含水蒸气
CO2
24.【猜想与假设】C+O2点燃
CO2
、CO2+C2CO
CO;
C
【实验探究】(1)CO2
、CO;干燥作用
(2)
实验方法
实验操作
实验现象
实验结果
物理方法
取少量黑色粉末B,用磁铁吸引
部分黑色粉末被吸引上来
化学方法
部分黑色粉末溶解,产生气泡
Fe+2HCl=
FeCl2+H2↑
没有进行尾气处理
25.(1)70%(2)5.4kg
26.65%
一、单选题
1.下列说法正确的是( )
A.铁燃烧生成氧化铁
B.合金的硬度更大,熔点更高
C.用青铜制作“马踏飞燕”是物理变化
D.铁矿石炼铁得到单质铁
2.下列说法错误的是( )
A.铁在潮湿的空气中容易生锈
B.铜是一种紫红色的金属单质
C.塑料、合金、合成橡胶属于合成材料
D.铝合金密度小,轻便
3.下列化学变化其反应类型属于化合反应的是( )
A.过氧化氢制氧气
B.蜡烛燃烧
C.高锰酸钾制氧气
D.加热金属汞
4.下列有关物质的鉴别方案错误的是
A.用燃着的木条区分氮气和二氧化碳
B.用闻气味的方法鉴别白酒和白醋
C.用二氧化锰区分水和过氧化氢溶液
D.用观察颜色的方法鉴别铜丝和铝丝
5.下图为某反应的微观示意图,下列说法正确的是
A.反应前后分子的种类保持不变
B.这是一个置换反应
C.反应中
与
两物质的质量比为2:1
D.若不放催化剂该反应不能进行
6.通过对下列有关化学反应的归纳,结论正确的是( )
A.,碳燃烧一定产生CO2
B.,属于置换反应
C.,铁桶不能装盐酸
D.,氢氧化钠可以治疗胃酸过多
7.下图所示实验不能用“分子在不停运动”解释的是
A.A
B.B
C.C
D.D
8.为了防止铁制品受腐蚀,下列采取的措施中不可行的是(
)
A.保持铁制品表面的洁净和干燥
B.将铁制品浸在水里使其与空气隔绝
C.制成不锈钢
D.在铁制品表面刷漆
9.有关铝、铁、铜的说法中错误的是
A.铝是地壳中含量最多的金属元素
B.铝能形成氧化保护膜
C.铜可以与稀硫酸反应
D.铝、铜可以用来做电线
10.若金属镍在金属活动性顺序中位于铁和锡之间,已知硫酸镍NiSO4溶于水,则下列反应不正确的是(
)
A.Ni+
H2SO4=NiSO4+H2↑
B.Fe
+
NiSO4=FeSO4+Ni
C.Ni+2AgNO3=Ni(NO3)2+2Ag
D.Cu+
NiSO4=CuSO4+Ni
11.金属活动性顺序表在化学学习中有重要作用。下列说法正确的是(
)
A.Zn不能置换出稀硫酸中的氢
B.Ag能将硫酸铜溶液中的铜置换出来
C.在Al、Mg、Fe中金属活动性最强的是Al
D.“真金不怕火炼”说明金在高温时也不与氧气反应
12.关于太阳能路灯的说法不正确的是( )
A.铝合金灯柱属于金属材料
B.灯泡中填充氮气作保护气
C.这种路灯可以节约能源,绿色环保
D.硅电池板中的硅元素是地壳中含量最多的元素
13.推理和分析是化学常用的思维方法,下列说法正确的是( )
A.中和反应的实质是H+和OH﹣反应生成水
B.一般情况下,合金的熔点和硬度都比组成合金的纯金属高
C.碱的溶液能使酚酞变红,能使酚酞溶液变红的溶液一定是碱的溶液
D.实验室用KClO3、H2O2溶液制氧气的催化剂都是二氧化锰,故化学反应只能用二氧化锰作催化剂
14.有一包金属粉末,可能由
Mg、Zn、Fe、Al、Ag
等金属中的一种或几种组成,取该样品
2.4g,加入
100g
稀硫酸恰好完全反应,得
0.2gH2
和无色溶液。下列说法不正确的是
A.样品中一定不含有
Ag,可能含有
Fe
B.无色溶液中溶质总质量量为
12g
C.稀硫酸的溶质质量分数为
39.2%
D.样品可能由
Zn
和
Al
组成
15.将一定量的铁粉加入到含有Zn(NO3)2、Cu(NO3)2和AgNO3的废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是
A.滤渣中一定含有Ag和Cu,滤液中一定含有Fe(NO3)2
B.滤渣中一定不含Fe,滤液的质量一定比原废液质量大
C.滤渣中一定含有Ag,滤液中可能含有Cu(NO3)2和AgNO3
D.滤渣中一定含有Ag和Cu,滤液中可能含有Cu(NO3)2和AgNO3
二、填空题
16.从下列物质中选择填空(填序号):①干冰
②石墨
③水银
④硝酸铵固体
(1)可做干电池电极的是_______;
(2)溶于水后溶液温度降低的是_______;
(3)用于人工降雨的是_______;
(4)温度计中含有的物质是_______.
17.某化学小组进行如下实验探究:将废铁屑(表面生锈)和铜粉的混合物放入烧杯中,加入稀硫酸,充分反应后烧杯中有固体。过滤,向滤渣中滴加稀硫酸,没有现象。
资料:
Fe+Fe2(SO
4)
3=3FeSO
4
Cu+
Fe2(SO4)3=2FeSO4
+CuSO4
(1)滤液中溶质一定有____________。
(2)自选一种试剂,检验滤液中溶质组成可能存在的几种情况,写出实验操作、预期现象及结论。____________
18.金属在生活生产中有着非常广泛的应用,请回答下列问题:
(1)根据如图金属应用实例推断,金属具有的物理性质有______(答三点);
(2)工业常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为______;
(3)在古代人们把烧红的生铁放在铁砧上反复捶打最终使生铁转化为钢,这就是“百炼成钢”的来历,这样做的目的是降低生铁中______元素的含量。
19.金属材料是在工农业和人们日常生活中用着广泛的应用。解答下列各题。
(1)我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志我国合金制造技术取得重大突破,根据所学知识回答:
①生铁和钢都是铁合金,其中含碳量较高的是__。
②生活中的下列物品,属于金属材料的是____。
A
四氧化三铁
B
玻璃钢
C
盛装饮料的易拉罐
D
有机玻璃
(2)金属钪(Sc)在化合物中常显+3价。在相同条件下取相同状态的Sc和Zn分别与同一种稀硫酸反应,Sc产生气泡明显比Zn快。则两金属的活动性Sc__Zn(填“>或“<”):结合上述结论判断,下列说法不正确的是__。
A、将打磨了的Sc伸入CuCl2溶液中无现象
B、用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag实验,能证明Fe和Sc的活动性
C、用Fe、Sc、稀H2SO4溶液能验证Sc的活动性强于Fe
(3)Sc2O3能与稀硫酸反应的化学方程式为____,该反应属于___反应。
20.2019年1月3日,我国“嫦娥四号”探测器成功登陆月球。“嫦娥四号”的制作材料有硅、石墨、铝合金、钛合金和铜等。
(1)纯金属制成合金,性能会发生改变,请写出其中一条
_______
。
(2)请写出一种比较钛和铜金属活动性强弱的方法
_______
(不要写现象与结论)。
(3)石墨是碳的单质,比较碳和硅的原子结构示意图:
①碳和硅的化学性质相似的原因是
____________
。
②请写出碳和硅原子结构不同的一处
_____________
。
(4)工业上制取硅的反应微观示意图如图所示:
①该反应的化学方程式为
______________
,其所属的基本反应类型为
________
。
②根据上述反应的微观示意图,你还能获得一条信息是
___________
。
三、推断题
21.已知A~F是初中化学常见的六种物质。且A为黑色固体单质,A、B、C三种物质含有同种元素。E是可供给动植物呼吸的气体,B、C、D、F都是氧化物。图中“→”表示转化关系,“—”表示反应关系(部分物质和反应条件未标出)。试回答下列问题:
(1)D的化学式:____________;
(2)C物质的一种用途________________________;
(3)F→E的化学方程式为________
,基本反应类型是______________;
(4)A→B且为置换反应的化学反应方程式:___________________
。
22.如图所示,物质“王国”的“小朋友”们手拉手围成一圈做游戏.甲、乙是黑色固体,丙、丁是无色气体,甲、丁是单质,乙、丙是氧化物.
(1)写出能代表甲与丁反应的一个化学方程式
___________
,甲与乙反应的基本反应类型是
_______
反应;
(2)根据游戏规则,乙可能是
___________
(填物质名称),写出能代表乙与丙反应的一个化学方程式
_____________________
.
四、实验题
23.氧气是我们身边无法离开的物质。某兴趣小组对氧气的研究如下:
I.氧气的制备:
(1)该装置中棉花团的作用是________,图中装置一处明显的错误是________。
II.氧气的收集:
[实验1]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
[实验2]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
[实验3]用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1
实验2
实验3
氧气的体积分数(%)
79.7
79.6
79.9
88.4
89.0
87.9
90.0
89.8
89.3
氧气的平均体积分数(%)
79.7
88.4
89.7
数据分析:
(2)由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是________。
(3)不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是___。
Ⅲ.铁丝在氧气中燃烧
(4)铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是________(填化学式)。将燃烧后的黑色固体粉碎后,滴加稀硫酸,若产生气泡,则原因是__________(用化学反应方程式表示)。
24.某化学兴趣小组根据右图所示进行模拟炼铁的实验,并对产物成分进行探究。
经初步分析:无色气体A不含有单质气体,黑色粉末B含有两种单质中的一种或者两种。
高炉炼铁的原理为:Fe2O3+3CO2Fe+3CO2,请写出反应器中一氧化碳是如何产生的化学方程式:_________________________________________________。
兴趣小组又分成甲乙两组分别对无色气体A和黑色粉末B的成分进行探究。
(猜想与假设)
甲组在分析了炼铁的原理后,认为无色气体A中可能有CO2,也可能有未反应的_____。
乙组认为黑色粉末的成分中存在以下三种情况:
假设一:只含有铁。
假设二:只含有_______。
假设三:以上两种物质都含有。
(实验探究)
(1)为验证甲组的猜想,大家按下图示进行实验(箭头表示气体流向):
当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中灼热的氧化铜变红,可以确定无色气体A的成分为:_____________________,Ⅱ中浓硫酸的作用是:____________________________。
(2)为验证乙组中假设三成立,大家用物理和化学两种方法来进行探究
实验方法
实验操作
实验现象
实验结果
物理方法
_____________________
_______
假设三成立
化学方法
取少量黑色粉末B于试管中,加入过量的稀盐酸
______
假设三成立
写出黑色粉末B中加入过量的稀盐酸反应的化学方程式:______________________。
(交流反思)
在做甲组的实验中发现其存在一个很不环保的缺陷,请指出来_____________________。
五、计算题
25.工业上可利用“铝热反应”焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将某些金属从其氧化物中置换出来。若用铝与氧化铁反应来制取11.2
kg铁。请计算:
(1)氧化铁中铁元素的质量分数_____。
(2)理论上需要消耗铝的质量_____。
26.分别用两种方法测定10g铜锌合金中锌的含量。
加入的试剂
测得数据
方法1
足量稀硫酸
气体0.2
g
方法2
足量硫酸铜溶液
固体质量减少0.1
g
请任选1种方法的数据,计算合金中锌的质量分数(写出计算过程及结果)。
_______
参考答案
1.C
2.C
3.D
4.A
5.B
6.C
7.C
8.B
9.C
10.D
11.D
12.D
13.A
14.D
15.C
16.②
④
①
③
17.
硫酸亚铁
将铁丝伸入盛有滤液的试管中,若铁丝表面有红色固体出现,证明有硫酸铜;反之,没有
18.导电性、导热性、延展性
C
19.生铁
C
>
A
B
复分解
20.抗腐蚀性能变好(强度或硬度更高)
将钛放入硫酸铜(氯化铜)溶液中(将铜放入氯化钛溶液中或将钛和铜分别放入稀盐酸/稀硫酸中等)
最外层电子数相同(最外层电子数都是4
个)
质子数不同(电子层数不同/第二层电子数不同
2C
+
SiO2
2CO
+
Si
置换反应
化学变化中,分子可分(或原子不可分或分子种类改变或原子重新组合或原子种类、数量不变等)
21.H2O
冶炼金属
分解反应
22.C+O2CO2
置换
氧化铜或氧化铁
CO+CuOCu+CO2或Fe2O3+3CO2Fe+3CO2
23.防止高锰酸钾粉末进入导管
试管口向上倾斜(或试管口没有略向下倾斜或试管口不应向上倾斜等合理答案)
延长收集时间
集气瓶中含水蒸气
CO2
24.【猜想与假设】C+O2点燃
CO2
、CO2+C2CO
CO;
C
【实验探究】(1)CO2
、CO;干燥作用
(2)
实验方法
实验操作
实验现象
实验结果
物理方法
取少量黑色粉末B,用磁铁吸引
部分黑色粉末被吸引上来
化学方法
部分黑色粉末溶解,产生气泡
Fe+2HCl=
FeCl2+H2↑
没有进行尾气处理
25.(1)70%(2)5.4kg
26.65%
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
