(10)海水“制碱”—2021-2022学年化学鲁教版(五四制)九年级全一册同步课时作业(含解析)
文档属性
| 名称 | (10)海水“制碱”—2021-2022学年化学鲁教版(五四制)九年级全一册同步课时作业(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 293.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-03 00:00:00 | ||
图片预览



文档简介
(10)海水“制碱”—2021-2022学年化学鲁教版(五四制)
九年级全一册同步课时作业
1.氯碱工业是以电解食盐水为基础的基本化学工业。电解食盐水不可能生成的是( )
A.
B.
C.
D.
2.下列不属于氨碱法制纯碱所需原料的是( )
A.石灰石 B.氯化钠 C.氢氧化钠 D.水
3.蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )。
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
4.下列反应属于复分解反应的是( )
A. B.
C. D.
5.下列物质不能与碳酸钠溶液反应的是( )
A.盐酸
B.氯化钡溶液
C.氢氧化钙溶液
D.氢氧化钾溶液
6.下列关于碳酸钠与碳酸氢钠的说法错误的是( )
A.溶液呈碱性
B.固体难溶于水
C.“纯碱”是碳酸钠的俗名
D.可用于烘焙糕点
7.根据氨碱法生产纯碱的反应原理,下列有关理解中,错误的是( )
A.用食盐制纯碱需要含碳、氧元素的物质
B.因为小苏打不溶于水以沉淀析出,化学反应才能发生
C.某些物质的循环利用,既节约了资金,又保护了环境
D.氨气的使用促进了二氧化碳的反应,保证生产的顺利进行
8.“”是著名的“侯氏制碱法”的重要反应。下列有关叙述正确的是( )。
A.是纯碱
B.析出晶体后剩余溶液中溶质只有
C.配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D.向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
9.我国著名化工专家侯德榜先生发明了“侯氏制碱法”,为我国民族工业的发展作出了杰出贡献。是侯氏制碱法的重要反应之一。下列有关说法错误的是( )
A.向饱和食盐水中先通入氨气,使溶液呈碱性,更易吸收酸性的气体
B.反应后,首先结晶析出,过滤即可将其分离出来
C.结晶析出后,剩余溶液中的溶质只有
D.结晶析出后,剩余溶液还能继续溶解固体
10.下列关于复分解反应的说法中,正确的是( )
A.若反应物和生成物都是化合物,则一定属于复分解反应
B.反应前各物质质量之和等于反应后生成的各物质质量之和
C.中和反应也属于复分解反应,在生成物中可能有不溶于稀硝酸的沉淀产生
D.在复分解反应中,生成物不可能同时出现水、沉淀和气体
11.爱国科学家侯德榜先生发明了侯氏制碱法,为我国民族工业的发展做出了杰出的贡献,该方法是将通入饱和的溶液中充分反应,其中的一步反应是,下列叙述错误的是( )。
A.该反应不符合复分解反应发生的条件
B.该反应中四种物质都是盐
C.反应后可用过滤的方法分离出
D.反应后的溶液中还能继续溶解
12.下列各组离子在溶液中能大量共存的是( )
A.
B.
C.
D.
13.某探究小组的同学用四种溶液进行“复分解反应发生条件及应用”的实验探究:将四种溶液两两混合,若将溶液分别混合:
(1)实验中,能直接观察到说明溶液发生化学反应的证据是_____________。
(2)实验中混合“无明显现象”,但实际上二者发生了化学反应,其反应的实质是结合生成。同理,发生了化学反应,其反应的实质是_____________。由此,同学们总结得出结论:复分解反应发生的条件是有沉淀、气体或水生成。
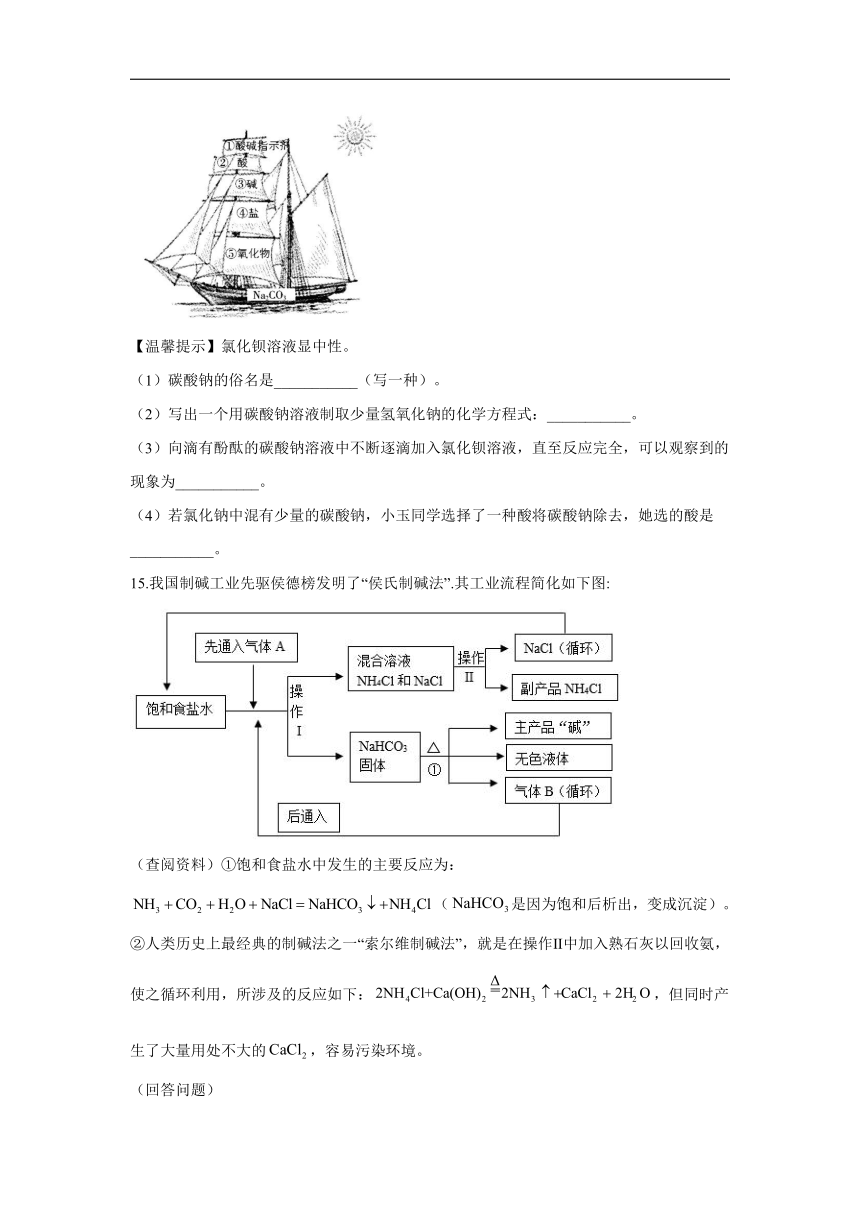
14.酷爱化学和卡通的小玉同学在复习碳酸钠时,发现碳酸钠“神通广大”,它竟然与酸碱指示剂、酸、碱、盐都应!如画出的卡通图如图所示。
【温馨提示】氯化钡溶液显中性。
(1)碳酸钠的俗名是___________(写一种)。
(2)写出一个用碳酸钠溶液制取少量氢氧化钠的化学方程式:___________。
(3)向滴有酚酞的碳酸钠溶液中不断逐滴加入氯化钡溶液,直至反应完全,可以观察到的现象为___________。
(4)若氯化钠中混有少量的碳酸钠,小玉同学选择了一种酸将碳酸钠除去,她选的酸是___________。
15.我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其工业流程简化如下图:
(查阅资料)①饱和食盐水中发生的主要反应为:(是因为饱和后析出,变成沉淀)。
②人类历史上最经典的制碱法之一“索尔维制碱法”,就是在操作Ⅱ中加入熟石灰以回收氨,使之循环利用,所涉及的反应如下:,但同时产生了大量用处不大的,容易污染环境。
(回答问题)
(1)“侯氏制碱法”所得的主产品“碱”,其俗名是__________(写其中一个即可)。
(2)气体A具有刺激性气味,它是______(填化学式);气体B能使石蕊试液变________(填“红”或“蓝”),操作I的名称是_______。
(3)写出反应①的化学方程式________,该反应属于_______反应(填基本反应类型)。
(4)副产品是一种________肥(选择“氮”、“磷”“钾”或“复合”)。
(5)针对“索尔维制碱法”的缺点,侯德榜先生在操作Ⅱ中加入的却是氯化钠,使单独结晶。相比较而言,“侯氏制碱法”的优点在于__________。
答案以及解析
1.答案:D
解析:食盐的主要成分是氯化钠,食盐水的组成元素有氢元素、氧元素、钠元素和氯元素四种,根据化学反应前后元素的种类不变,所以生成物中不可能含有氮元素,即电解食盐水不可能生成硝酸钠。
2.答案:C
解析:根据氨碱法制纯碱的流程可知,需要的原料为氯化钠、水、氨气和二氧化碳,其中二氧化碳可由石灰石高温分解得到。
3.答案:A
解析:能加入食物的,首先要能食用,生石灰和氢氧化钠都有强烈的腐蚀性,不能食用。氯化钠不能除酸,而碳酸氢钠能和酸反应生成二氧化碳气体,既能除酸又能让面团发软。
4.答案:A
解析:A、,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项正确。
B、,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故选项错误。
C、,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误。
D、,该反应符合“一变多”的形式,符合分解反应的特征,属于分解反应,故选项错误。
故选:A。
5.答案:D
解析:本题考查复分解反应发生的条件。碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,符合复分解反应发生的条件,反应能够发生,A项错误;氯化钡与碳酸钠反应会生成碳酸钡沉淀,符合复分解反应发生的条件,反应能够发生,B项错误;碳酸钠与氢氧化钙反应会生成碳酸钙沉淀,符合复分解反应发生的条件,反应能够发生,C项错误;氢氧化钾与碳酸钠混合不能产生沉淀,也没有气体和水生成,不符合复分解反应发生的条件,不能发生反应,D项正确。
6.答案:B
解析:固体易溶于水,故B错误。
7.答案:B
解析:用食盐制纯碱,根据质量守恒定律,反应前后元素种类不变,则该过程需要含碳、氧元素的物质,A正确;氨碱法生产纯碱的反应原理之一是用氨气和二氧化碳与氯化钠和水反应生成碳酸氢钠和氯化铵,碳酸氢钠俗称小苏打,小苏打能溶于水,B错误;二氧化碳能循环利用,既节约了资金,又保护了环境,C正确;氨气溶于水所得的氨水呈碱性,比水更易吸收二氧化碳,保证生产的顺利进行,D正确。
8.答案:D
解析:碳酸氢钠的俗名是小苏打,纯碱是碳酸钠,A错误;在相同条件下,由于碳酸氢钠的溶解度比氯化铵的溶解度小,所以碳酸氢钠先结晶析出,过滤后的滤液中一定有碳酸氢钠和氯化铵,B错误;配制溶液的过程中玻璃棒的作用是搅拌加速溶解,不能提高物质的溶解度,C错误;向饱和食盐水中通入氨气,制成饱和氨盐水,饱和氨盐水显碱性,更易于吸收二氧化碳,D正确。
9.答案:C
解析:向饱和食盐水中先通入氨气,使溶液呈碱性,更易吸收酸性的气体,A正确;反应后,碳酸氢钠溶解度较小,首先结晶析出,过滤即可将其分离出来,B正确;结晶析出后,剩余溶液仍为的饱和溶液,其中的溶质至少有两种,即和,C错误;反应中氯化钠被消耗,剩余溶液是氯化钠的不饱和溶液,还能继续溶解固体,D正确。
10.答案:C
解析:本题考查复分解反应的相关知识。复分解反应是两种化合物互相交换成分,生成另外两种化合物的反应,中反应物和生成物都是化合物,但不属于复分解反应,A错误;反应前各物质的质量总和不一定等于反应后生成的各物质质量之和,因为反应物可能剩余,B错误;由中和反应的概念,可知中和反应是复分解反应的一种,属于复分解反应,既是中和反应也属于复分解反应,且生成的硫酸钡不溶于稀硝酸,C正确;属于复分解反应,且生成物同时出现水、沉淀和气体,D错误。
11.答案:A
解析:由反应的化学方程式:可知,该反应生成物碳酸氢钠是沉淀,符合复分解反应发生的条件,A错误;该反应中四种物质均是由金属离子(或铵根离子)和酸根离子构成的,均属于盐,B正确;过滤是把不溶于液体的固体与液体分离的一种方法,反应后可用过滤的方法分离出,C正确;氯化钠是反应物,反应后氯化钠的质量减少,反应后的溶液中还能继续溶解,D正确。
12.答案:A
解析:本题考查离子的共存。硫酸钾、硝酸钾都能够溶于水,钾离子、硫酸根离子、硝酸根离子能够共存;铵根离子和氢氧根离子作用生成水,则铵根离子、氢氧根离子不能共存;铜离子与氢氧根离子作用形成氢氧化铜沉淀,则铜离子、氢氧根离子不能共存;钙离子与碳酸根离子作用形成碳酸钙沉淀,则钙离子、碳酸根离子不能共存。故选择A。
13.答案:(1)混合后溶液中产生气泡
(2)结合生成白色沉淀
解析:(1)能与溶液反应生成硫酸钠、水和二氧化碳,能直接观察到说明二者发生化学反应的证据是混合后溶液中产生气泡。
(2)发生化学反应生成硫酸钡白色沉淀和盐酸,反应的实质是结合生成白色沉淀。
14.答案:(1)纯碱(或苏打)
(2)(合理即可)
(3)出现白色沉淀,溶液逐渐由红色变为无色
(4)盐酸
解析:(1)碳酸钠俗称纯碱或苏打。
(2)碳酸钠和氢氧化钙反应生成氢氧化钠和碳酸钙,据此书写化学方程式。
(3)碳酸钠溶液显碱性,滴有酚酞的碳酸钠溶液呈红色碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,氯化钠溶液呈中性,所以向滴有酚酞的碳酸钠溶液中不断逐滴加入氯化钡溶液,直至反应完全,可以观察到的现象为出现白色沉淀,溶液逐渐由红色变为无色。
(4)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,所以可用盐酸除去氯化钠中混有的少量碳酸钠。
15.答案:(1)纯碱(或苏打)(2);红;过滤(3);分解(4)氮 (5)可回收利用氯化铵,同时及减少环境污染
九年级全一册同步课时作业
1.氯碱工业是以电解食盐水为基础的基本化学工业。电解食盐水不可能生成的是( )
A.
B.
C.
D.
2.下列不属于氨碱法制纯碱所需原料的是( )
A.石灰石 B.氯化钠 C.氢氧化钠 D.水
3.蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )。
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
4.下列反应属于复分解反应的是( )
A. B.
C. D.
5.下列物质不能与碳酸钠溶液反应的是( )
A.盐酸
B.氯化钡溶液
C.氢氧化钙溶液
D.氢氧化钾溶液
6.下列关于碳酸钠与碳酸氢钠的说法错误的是( )
A.溶液呈碱性
B.固体难溶于水
C.“纯碱”是碳酸钠的俗名
D.可用于烘焙糕点
7.根据氨碱法生产纯碱的反应原理,下列有关理解中,错误的是( )
A.用食盐制纯碱需要含碳、氧元素的物质
B.因为小苏打不溶于水以沉淀析出,化学反应才能发生
C.某些物质的循环利用,既节约了资金,又保护了环境
D.氨气的使用促进了二氧化碳的反应,保证生产的顺利进行
8.“”是著名的“侯氏制碱法”的重要反应。下列有关叙述正确的是( )。
A.是纯碱
B.析出晶体后剩余溶液中溶质只有
C.配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D.向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
9.我国著名化工专家侯德榜先生发明了“侯氏制碱法”,为我国民族工业的发展作出了杰出贡献。是侯氏制碱法的重要反应之一。下列有关说法错误的是( )
A.向饱和食盐水中先通入氨气,使溶液呈碱性,更易吸收酸性的气体
B.反应后,首先结晶析出,过滤即可将其分离出来
C.结晶析出后,剩余溶液中的溶质只有
D.结晶析出后,剩余溶液还能继续溶解固体
10.下列关于复分解反应的说法中,正确的是( )
A.若反应物和生成物都是化合物,则一定属于复分解反应
B.反应前各物质质量之和等于反应后生成的各物质质量之和
C.中和反应也属于复分解反应,在生成物中可能有不溶于稀硝酸的沉淀产生
D.在复分解反应中,生成物不可能同时出现水、沉淀和气体
11.爱国科学家侯德榜先生发明了侯氏制碱法,为我国民族工业的发展做出了杰出的贡献,该方法是将通入饱和的溶液中充分反应,其中的一步反应是,下列叙述错误的是( )。
A.该反应不符合复分解反应发生的条件
B.该反应中四种物质都是盐
C.反应后可用过滤的方法分离出
D.反应后的溶液中还能继续溶解
12.下列各组离子在溶液中能大量共存的是( )
A.
B.
C.
D.
13.某探究小组的同学用四种溶液进行“复分解反应发生条件及应用”的实验探究:将四种溶液两两混合,若将溶液分别混合:
(1)实验中,能直接观察到说明溶液发生化学反应的证据是_____________。
(2)实验中混合“无明显现象”,但实际上二者发生了化学反应,其反应的实质是结合生成。同理,发生了化学反应,其反应的实质是_____________。由此,同学们总结得出结论:复分解反应发生的条件是有沉淀、气体或水生成。
14.酷爱化学和卡通的小玉同学在复习碳酸钠时,发现碳酸钠“神通广大”,它竟然与酸碱指示剂、酸、碱、盐都应!如画出的卡通图如图所示。
【温馨提示】氯化钡溶液显中性。
(1)碳酸钠的俗名是___________(写一种)。
(2)写出一个用碳酸钠溶液制取少量氢氧化钠的化学方程式:___________。
(3)向滴有酚酞的碳酸钠溶液中不断逐滴加入氯化钡溶液,直至反应完全,可以观察到的现象为___________。
(4)若氯化钠中混有少量的碳酸钠,小玉同学选择了一种酸将碳酸钠除去,她选的酸是___________。
15.我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其工业流程简化如下图:
(查阅资料)①饱和食盐水中发生的主要反应为:(是因为饱和后析出,变成沉淀)。
②人类历史上最经典的制碱法之一“索尔维制碱法”,就是在操作Ⅱ中加入熟石灰以回收氨,使之循环利用,所涉及的反应如下:,但同时产生了大量用处不大的,容易污染环境。
(回答问题)
(1)“侯氏制碱法”所得的主产品“碱”,其俗名是__________(写其中一个即可)。
(2)气体A具有刺激性气味,它是______(填化学式);气体B能使石蕊试液变________(填“红”或“蓝”),操作I的名称是_______。
(3)写出反应①的化学方程式________,该反应属于_______反应(填基本反应类型)。
(4)副产品是一种________肥(选择“氮”、“磷”“钾”或“复合”)。
(5)针对“索尔维制碱法”的缺点,侯德榜先生在操作Ⅱ中加入的却是氯化钠,使单独结晶。相比较而言,“侯氏制碱法”的优点在于__________。
答案以及解析
1.答案:D
解析:食盐的主要成分是氯化钠,食盐水的组成元素有氢元素、氧元素、钠元素和氯元素四种,根据化学反应前后元素的种类不变,所以生成物中不可能含有氮元素,即电解食盐水不可能生成硝酸钠。
2.答案:C
解析:根据氨碱法制纯碱的流程可知,需要的原料为氯化钠、水、氨气和二氧化碳,其中二氧化碳可由石灰石高温分解得到。
3.答案:A
解析:能加入食物的,首先要能食用,生石灰和氢氧化钠都有强烈的腐蚀性,不能食用。氯化钠不能除酸,而碳酸氢钠能和酸反应生成二氧化碳气体,既能除酸又能让面团发软。
4.答案:A
解析:A、,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项正确。
B、,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故选项错误。
C、,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误。
D、,该反应符合“一变多”的形式,符合分解反应的特征,属于分解反应,故选项错误。
故选:A。
5.答案:D
解析:本题考查复分解反应发生的条件。碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,符合复分解反应发生的条件,反应能够发生,A项错误;氯化钡与碳酸钠反应会生成碳酸钡沉淀,符合复分解反应发生的条件,反应能够发生,B项错误;碳酸钠与氢氧化钙反应会生成碳酸钙沉淀,符合复分解反应发生的条件,反应能够发生,C项错误;氢氧化钾与碳酸钠混合不能产生沉淀,也没有气体和水生成,不符合复分解反应发生的条件,不能发生反应,D项正确。
6.答案:B
解析:固体易溶于水,故B错误。
7.答案:B
解析:用食盐制纯碱,根据质量守恒定律,反应前后元素种类不变,则该过程需要含碳、氧元素的物质,A正确;氨碱法生产纯碱的反应原理之一是用氨气和二氧化碳与氯化钠和水反应生成碳酸氢钠和氯化铵,碳酸氢钠俗称小苏打,小苏打能溶于水,B错误;二氧化碳能循环利用,既节约了资金,又保护了环境,C正确;氨气溶于水所得的氨水呈碱性,比水更易吸收二氧化碳,保证生产的顺利进行,D正确。
8.答案:D
解析:碳酸氢钠的俗名是小苏打,纯碱是碳酸钠,A错误;在相同条件下,由于碳酸氢钠的溶解度比氯化铵的溶解度小,所以碳酸氢钠先结晶析出,过滤后的滤液中一定有碳酸氢钠和氯化铵,B错误;配制溶液的过程中玻璃棒的作用是搅拌加速溶解,不能提高物质的溶解度,C错误;向饱和食盐水中通入氨气,制成饱和氨盐水,饱和氨盐水显碱性,更易于吸收二氧化碳,D正确。
9.答案:C
解析:向饱和食盐水中先通入氨气,使溶液呈碱性,更易吸收酸性的气体,A正确;反应后,碳酸氢钠溶解度较小,首先结晶析出,过滤即可将其分离出来,B正确;结晶析出后,剩余溶液仍为的饱和溶液,其中的溶质至少有两种,即和,C错误;反应中氯化钠被消耗,剩余溶液是氯化钠的不饱和溶液,还能继续溶解固体,D正确。
10.答案:C
解析:本题考查复分解反应的相关知识。复分解反应是两种化合物互相交换成分,生成另外两种化合物的反应,中反应物和生成物都是化合物,但不属于复分解反应,A错误;反应前各物质的质量总和不一定等于反应后生成的各物质质量之和,因为反应物可能剩余,B错误;由中和反应的概念,可知中和反应是复分解反应的一种,属于复分解反应,既是中和反应也属于复分解反应,且生成的硫酸钡不溶于稀硝酸,C正确;属于复分解反应,且生成物同时出现水、沉淀和气体,D错误。
11.答案:A
解析:由反应的化学方程式:可知,该反应生成物碳酸氢钠是沉淀,符合复分解反应发生的条件,A错误;该反应中四种物质均是由金属离子(或铵根离子)和酸根离子构成的,均属于盐,B正确;过滤是把不溶于液体的固体与液体分离的一种方法,反应后可用过滤的方法分离出,C正确;氯化钠是反应物,反应后氯化钠的质量减少,反应后的溶液中还能继续溶解,D正确。
12.答案:A
解析:本题考查离子的共存。硫酸钾、硝酸钾都能够溶于水,钾离子、硫酸根离子、硝酸根离子能够共存;铵根离子和氢氧根离子作用生成水,则铵根离子、氢氧根离子不能共存;铜离子与氢氧根离子作用形成氢氧化铜沉淀,则铜离子、氢氧根离子不能共存;钙离子与碳酸根离子作用形成碳酸钙沉淀,则钙离子、碳酸根离子不能共存。故选择A。
13.答案:(1)混合后溶液中产生气泡
(2)结合生成白色沉淀
解析:(1)能与溶液反应生成硫酸钠、水和二氧化碳,能直接观察到说明二者发生化学反应的证据是混合后溶液中产生气泡。
(2)发生化学反应生成硫酸钡白色沉淀和盐酸,反应的实质是结合生成白色沉淀。
14.答案:(1)纯碱(或苏打)
(2)(合理即可)
(3)出现白色沉淀,溶液逐渐由红色变为无色
(4)盐酸
解析:(1)碳酸钠俗称纯碱或苏打。
(2)碳酸钠和氢氧化钙反应生成氢氧化钠和碳酸钙,据此书写化学方程式。
(3)碳酸钠溶液显碱性,滴有酚酞的碳酸钠溶液呈红色碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,氯化钠溶液呈中性,所以向滴有酚酞的碳酸钠溶液中不断逐滴加入氯化钡溶液,直至反应完全,可以观察到的现象为出现白色沉淀,溶液逐渐由红色变为无色。
(4)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,所以可用盐酸除去氯化钠中混有的少量碳酸钠。
15.答案:(1)纯碱(或苏打)(2);红;过滤(3);分解(4)氮 (5)可回收利用氯化铵,同时及减少环境污染
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
