第三单元 溶液 单元测试题(含答案)—2021-2022学年九年级化学鲁教版上册(word版)
文档属性
| 名称 | 第三单元 溶液 单元测试题(含答案)—2021-2022学年九年级化学鲁教版上册(word版) |  | |
| 格式 | docx | ||
| 文件大小 | 93.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-07 07:20:45 | ||
图片预览


文档简介
本卷由系统自动生成,请仔细校对后使用,答案仅供参考。
第三单元《溶液》测试题
一、单选题
1.把少量下列物质分别放入水中,充分搅拌,不能得到溶液的是
A.蔗糖
B.汽油
C.氯化钾
D.碳酸氢铵
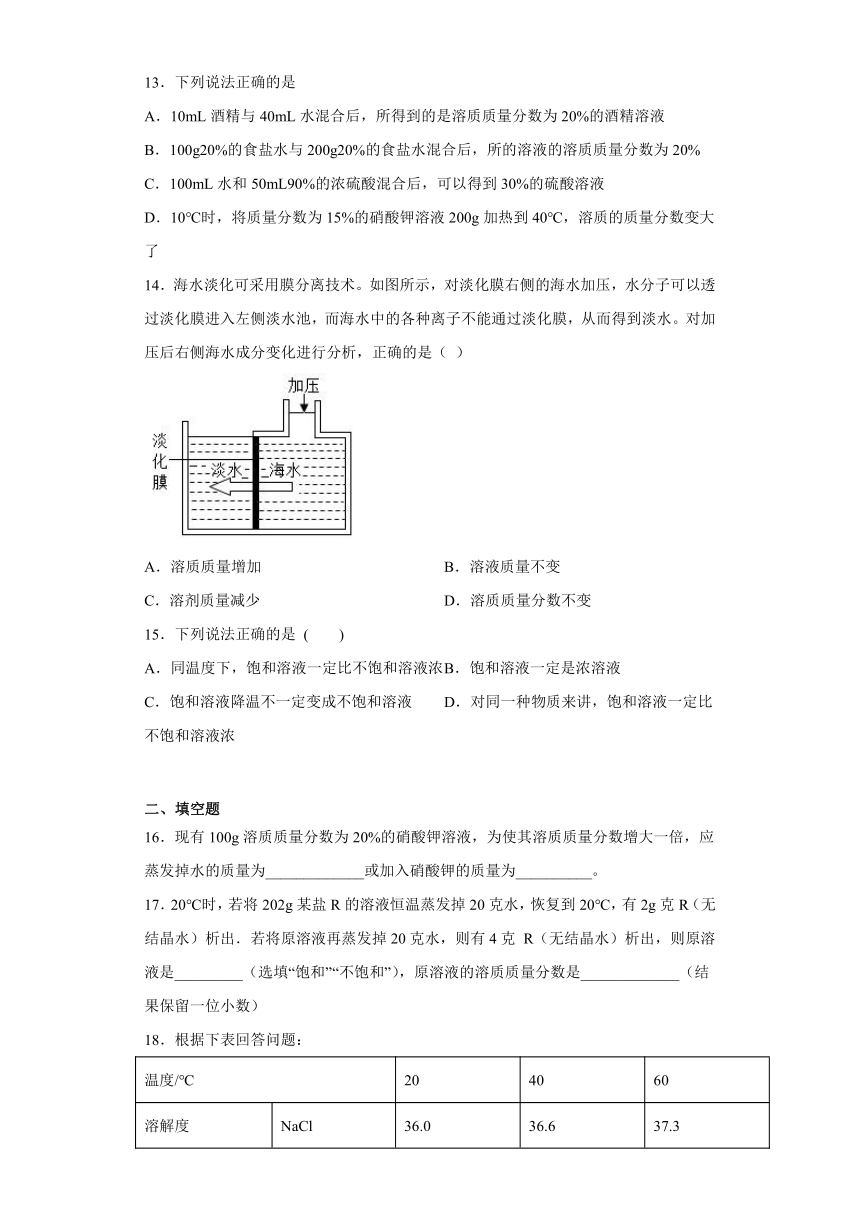
2.配制70克16%的
NaCl溶液,下列操作会使所配溶液溶质质量分数大于16%的是
A.称取氯化钠
B.转移氯化钠
C.量取水
D.配好后装瓶
3.实验室用蔗糖固体配制
50g
溶质质量分数为
5%的蔗糖溶液(1g
以下用游码),以下有关做法正确的是( )
A.选择的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、广口瓶
B.用规格为
500mL
的量筒准确量取
47.5mL
水
C.称量时,发现砝码与药品的位置放反,导致所配制溶液的溶质质量分数偏大
D.操作步骤为计算、称取、量取、溶解、装瓶存放
4.现有60℃的硝酸钾溶液500g,保持温度不变,蒸发掉10g水,则溶液中一定保持不变的是
A.溶质的质量
B.溶剂的质量
C.溶液的质量
D.硝酸钾的溶解度
5.2020年世界水日的主题是“水与气候变化”。下列有关水和溶液的说法正确的是
A.洗洁精除去油污的原理是油污能溶解洗洁精
B.物质的溶解过程通常会伴随着热量的变化
C.溶液中的溶质以分子或离子的形式均匀分散在溶剂中并保持静止不动
D.用滤纸过滤后的河水为纯净水
6.打开汽水瓶盖后,瓶内迅速出现大量气泡,对瓶盖打开后分析正确的是( )
A.瓶内压强增大
B.气体溶解度增大
C.溶液为饱和溶液
D.溶液中气体浓度变大
7.下列关于溶液的说法中,正确的是
A.溶液是由溶质和溶剂组成的
B.溶液是一种纯净物
C.溶液都是无色的
D.溶液中只能含有一种溶质
8.
下列实验操作,能达到预期目的的是
A.用100
mL量筒量取8.2
mL水
B.用托盘天平称取5.6
g氧化铜粉末
C.用内壁有水的烧杯配制一定溶质质量分数的溶液
D.用过滤的方法可以除去水中所有的杂质
9.如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是
A.氯化钠
B.硝酸钾
C.硝酸铵
D.氢氧化钾
10.实验室用氯化钠配制50克质量分数为6%的氯化钠溶液,下列说法正确的是
A.所需氯化钠的质量为6克
B.溶解氯化钠时用玻璃棒搅拌
C.俯视量筒读数会使所配溶液偏稀
D.所需玻璃仪器有烧杯、托盘天平等
11.下列有关溶液的说法中正确的是
A.均一、稳定的液体都是溶液
B.物质溶于水后,水的导电性都会增强
C.溶液一定是无色、透明的混合物
D.溶液里的各部分的性质是相同的
12.对于下列事实的解释正确的是(
)
选项
事
实
解
释
A
氯化钠是咸的,葡萄糖是甜的
不同种物质的分子性质不同
B
纯水不导电
水分子中不含电子
C
搜救犬通过闻气味找到搜寻的目标
分子在不断运动
D
25m3的氧气加压后可以装入0.024m3的钢瓶中
氧分子的体积变小
A.A
B.B
C.C
D.D
13.下列说法正确的是
A.10mL酒精与40mL水混合后,所得到的是溶质质量分数为20%的酒精溶液
B.100g20%的食盐水与200g20%的食盐水混合后,所的溶液的溶质质量分数为20%
C.100mL水和50mL90%的浓硫酸混合后,可以得到30%的硫酸溶液
D.10℃时,将质量分数为15%的硝酸钾溶液200g加热到40℃,溶质的质量分数变大了
14.海水淡化可采用膜分离技术。如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是(
)
A.溶质质量增加
B.溶液质量不变
C.溶剂质量减少
D.溶质质量分数不变
15.下列说法正确的是
(
)
A.同温度下,饱和溶液一定比不饱和溶液浓
B.饱和溶液一定是浓溶液
C.饱和溶液降温不一定变成不饱和溶液
D.对同一种物质来讲,饱和溶液一定比不饱和溶液浓
二、填空题
16.现有100g溶质质量分数为20%的硝酸钾溶液,为使其溶质质量分数增大一倍,应蒸发掉水的质量为_____________或加入硝酸钾的质量为__________。
17.20℃时,若将202g某盐R的溶液恒温蒸发掉20克水,恢复到20℃,有2g克R(无结晶水)析出.若将原溶液再蒸发掉20克水,则有4克
R(无结晶水)析出,则原溶液是_________(选填“饱和”“不饱和”),原溶液的溶质质量分数是_____________(结果保留一位小数)
18.根据下表回答问题:
温度/℃
20
40
60
溶解度
NaCl
36.0
36.6
37.3
KNO3
31.6
63.9
110
(1)60℃,100g水中最多能溶解KNO3的质量为_____。
(2)下列说法正确的是_____(填序号)
A
20℃时,KNO3饱和溶液的质量分数为31.6%
B
40℃时,136.6gNaCl溶液中一定含有36.6gNaCl
C
将40℃时KNO3的饱和溶液降温到20℃,析出32.3gKNO3固体
D
将40℃时NaCl和KNO3的饱和溶液分别降温至20℃,降温后两溶液质量分数的大小关系为NaCl>KNO3
(3)20℃时,按下列图示操作:
①在溶液A、B、C中,KNO3溶解达到饱和状态的有_____(填字母)
②比较溶液A、B中KNO3的质量分数:A_____B(填“>“或”<”或“=”)
19.下图是A、B两种固体物质的溶解度曲线。
(1)当温度为_____℃时,A物质与B物质的溶解度相等;
(2)40℃将40gB物质放入200g水中充分溶解后所得溶液是(选填“饱和”或“不饱和”)_______溶液;
(3)若将B物质从溶液中结晶析出,最好采用的方法是____________。
20.20℃时A物质的饱和溶液中溶质的质量分数为20%,那么20℃A物质的溶解度是_______g;20℃时,2.2gA物质投入10g水中,充分溶解后所得的溶液质量是_______g.。
三、推断题
21.如图所示,A是金属氧化物,B是金属单质,C是黄色溶液,D是浅绿色溶液,E是红褐色沉淀,反应③是物质F与氧气、水发生的化合反应,请回答下列问题:
(1)写出C的化学式_____。
(2)化学反应①的基本类型是_____。
(3)写出反应②和③的化学方程式:②_____;③_____。
四、实验题
22.20℃时,小明要配制100g质量分数为10%的硝酸钾溶液,如图所示是他配制硝酸钾溶液的实验操作示意图。
(1)量取所需要的水应选择____________(选填“10mL”“50mL”或“100mL”)的量筒。
(2)指出图①中的操作错误_________。
(3)该实验正确操作顺序是__________(选填序号)。
A④⑤①③②
B④①③⑤②
C④⑤③②①
D④①③②⑤
(4)如果其他操作均正确,按③所示操作取水,则所配制溶液的溶质质量分数__________(选填“>”“<”或“=”)10%。
23.下表是KNO3和NaCl在不同温度下的溶解度。
温度/℃
10
20
30
40
50
60
70
80
90
溶解度/g
KNO3
20.9
32
45.8
64
85.5
110
138
168
202
NaCl
35.8
36
36.3
36.6
37
37.7
37.8
38.4
39
(1)从表中得出,40℃时,KNO3的溶解度为___。
(2)将69gKNO3和18gNaCl完全溶解在50g水中,改变温度,使KNO3析出而NaCl不析出,则温度t应控制在的范围是_______(KNO3和NaCl溶解度互不影响)。
(3)KNO3溶液中含有少量的NaCl时,可通过________的方法提纯KNO3,对析出的晶体和剩余溶液的分析正确的是___(填字母)。
A剩余溶液一定是KNO3的饱和溶液
B剩余溶液一定是NaCl的不饱和溶液
C上述方法不能将两者完全分离
D析出的晶体中一定只含有硝酸钾
五、计算题
24.现有6.5克的锌与100g的稀硫酸恰好完全反应
(1)生成氢气的质量;_______
(2)求所用稀硫酸的溶质质量分数;_______
(3)求所得溶液的溶质质量分数;(保留一位小数)_______
25.为测定某生铁样品中铁的含量,现将5.8
g生铁样品置于烧杯中,加入一定质量的稀硫酸。所加稀硫酸与生成气体的质量关系如右图所示。
(1)据报道,每年因锈蚀而损失的钢铁相当于年产量的20%一40%,铁制品锈蚀的主要原因是_____________________________________________:。
(2)若该生铁样品中杂质不与稀硫酸反应,计算该样品中铁的含量(精确到0.1%)。
参考答案
1.B
2.C
3.D
4.D
5.B
6.C
7.A
8.B
9.D
10.B
11.D
12.C
13.B
14.C
15.C
16.50g
33.3g
17.不饱和
15.8%
18.110g
D
AB
>
19.40
不饱和
蒸发结晶
20.25
12.2
21. FeCl3
复分解反应
Fe+2HCl=FeCl2+H2↑
4Fe(OH)2+O2+2H2O=4Fe(OH)3
22.100mL
将砝码与称量物放反了(合理即可)
B
<
23.64g
20℃≤t<70℃
降温结晶
AC
24.(1)0.2g(2)9.8%(3)15.1%
25.(1)铁与空气中的氧气和水蒸气发生反应
(2)96.6%
答案第2页,总2页
第三单元《溶液》测试题
一、单选题
1.把少量下列物质分别放入水中,充分搅拌,不能得到溶液的是
A.蔗糖
B.汽油
C.氯化钾
D.碳酸氢铵
2.配制70克16%的
NaCl溶液,下列操作会使所配溶液溶质质量分数大于16%的是
A.称取氯化钠
B.转移氯化钠
C.量取水
D.配好后装瓶
3.实验室用蔗糖固体配制
50g
溶质质量分数为
5%的蔗糖溶液(1g
以下用游码),以下有关做法正确的是( )
A.选择的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、广口瓶
B.用规格为
500mL
的量筒准确量取
47.5mL
水
C.称量时,发现砝码与药品的位置放反,导致所配制溶液的溶质质量分数偏大
D.操作步骤为计算、称取、量取、溶解、装瓶存放
4.现有60℃的硝酸钾溶液500g,保持温度不变,蒸发掉10g水,则溶液中一定保持不变的是
A.溶质的质量
B.溶剂的质量
C.溶液的质量
D.硝酸钾的溶解度
5.2020年世界水日的主题是“水与气候变化”。下列有关水和溶液的说法正确的是
A.洗洁精除去油污的原理是油污能溶解洗洁精
B.物质的溶解过程通常会伴随着热量的变化
C.溶液中的溶质以分子或离子的形式均匀分散在溶剂中并保持静止不动
D.用滤纸过滤后的河水为纯净水
6.打开汽水瓶盖后,瓶内迅速出现大量气泡,对瓶盖打开后分析正确的是( )
A.瓶内压强增大
B.气体溶解度增大
C.溶液为饱和溶液
D.溶液中气体浓度变大
7.下列关于溶液的说法中,正确的是
A.溶液是由溶质和溶剂组成的
B.溶液是一种纯净物
C.溶液都是无色的
D.溶液中只能含有一种溶质
8.
下列实验操作,能达到预期目的的是
A.用100
mL量筒量取8.2
mL水
B.用托盘天平称取5.6
g氧化铜粉末
C.用内壁有水的烧杯配制一定溶质质量分数的溶液
D.用过滤的方法可以除去水中所有的杂质
9.如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是
A.氯化钠
B.硝酸钾
C.硝酸铵
D.氢氧化钾
10.实验室用氯化钠配制50克质量分数为6%的氯化钠溶液,下列说法正确的是
A.所需氯化钠的质量为6克
B.溶解氯化钠时用玻璃棒搅拌
C.俯视量筒读数会使所配溶液偏稀
D.所需玻璃仪器有烧杯、托盘天平等
11.下列有关溶液的说法中正确的是
A.均一、稳定的液体都是溶液
B.物质溶于水后,水的导电性都会增强
C.溶液一定是无色、透明的混合物
D.溶液里的各部分的性质是相同的
12.对于下列事实的解释正确的是(
)
选项
事
实
解
释
A
氯化钠是咸的,葡萄糖是甜的
不同种物质的分子性质不同
B
纯水不导电
水分子中不含电子
C
搜救犬通过闻气味找到搜寻的目标
分子在不断运动
D
25m3的氧气加压后可以装入0.024m3的钢瓶中
氧分子的体积变小
A.A
B.B
C.C
D.D
13.下列说法正确的是
A.10mL酒精与40mL水混合后,所得到的是溶质质量分数为20%的酒精溶液
B.100g20%的食盐水与200g20%的食盐水混合后,所的溶液的溶质质量分数为20%
C.100mL水和50mL90%的浓硫酸混合后,可以得到30%的硫酸溶液
D.10℃时,将质量分数为15%的硝酸钾溶液200g加热到40℃,溶质的质量分数变大了
14.海水淡化可采用膜分离技术。如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是(
)
A.溶质质量增加
B.溶液质量不变
C.溶剂质量减少
D.溶质质量分数不变
15.下列说法正确的是
(
)
A.同温度下,饱和溶液一定比不饱和溶液浓
B.饱和溶液一定是浓溶液
C.饱和溶液降温不一定变成不饱和溶液
D.对同一种物质来讲,饱和溶液一定比不饱和溶液浓
二、填空题
16.现有100g溶质质量分数为20%的硝酸钾溶液,为使其溶质质量分数增大一倍,应蒸发掉水的质量为_____________或加入硝酸钾的质量为__________。
17.20℃时,若将202g某盐R的溶液恒温蒸发掉20克水,恢复到20℃,有2g克R(无结晶水)析出.若将原溶液再蒸发掉20克水,则有4克
R(无结晶水)析出,则原溶液是_________(选填“饱和”“不饱和”),原溶液的溶质质量分数是_____________(结果保留一位小数)
18.根据下表回答问题:
温度/℃
20
40
60
溶解度
NaCl
36.0
36.6
37.3
KNO3
31.6
63.9
110
(1)60℃,100g水中最多能溶解KNO3的质量为_____。
(2)下列说法正确的是_____(填序号)
A
20℃时,KNO3饱和溶液的质量分数为31.6%
B
40℃时,136.6gNaCl溶液中一定含有36.6gNaCl
C
将40℃时KNO3的饱和溶液降温到20℃,析出32.3gKNO3固体
D
将40℃时NaCl和KNO3的饱和溶液分别降温至20℃,降温后两溶液质量分数的大小关系为NaCl>KNO3
(3)20℃时,按下列图示操作:
①在溶液A、B、C中,KNO3溶解达到饱和状态的有_____(填字母)
②比较溶液A、B中KNO3的质量分数:A_____B(填“>“或”<”或“=”)
19.下图是A、B两种固体物质的溶解度曲线。
(1)当温度为_____℃时,A物质与B物质的溶解度相等;
(2)40℃将40gB物质放入200g水中充分溶解后所得溶液是(选填“饱和”或“不饱和”)_______溶液;
(3)若将B物质从溶液中结晶析出,最好采用的方法是____________。
20.20℃时A物质的饱和溶液中溶质的质量分数为20%,那么20℃A物质的溶解度是_______g;20℃时,2.2gA物质投入10g水中,充分溶解后所得的溶液质量是_______g.。
三、推断题
21.如图所示,A是金属氧化物,B是金属单质,C是黄色溶液,D是浅绿色溶液,E是红褐色沉淀,反应③是物质F与氧气、水发生的化合反应,请回答下列问题:
(1)写出C的化学式_____。
(2)化学反应①的基本类型是_____。
(3)写出反应②和③的化学方程式:②_____;③_____。
四、实验题
22.20℃时,小明要配制100g质量分数为10%的硝酸钾溶液,如图所示是他配制硝酸钾溶液的实验操作示意图。
(1)量取所需要的水应选择____________(选填“10mL”“50mL”或“100mL”)的量筒。
(2)指出图①中的操作错误_________。
(3)该实验正确操作顺序是__________(选填序号)。
A④⑤①③②
B④①③⑤②
C④⑤③②①
D④①③②⑤
(4)如果其他操作均正确,按③所示操作取水,则所配制溶液的溶质质量分数__________(选填“>”“<”或“=”)10%。
23.下表是KNO3和NaCl在不同温度下的溶解度。
温度/℃
10
20
30
40
50
60
70
80
90
溶解度/g
KNO3
20.9
32
45.8
64
85.5
110
138
168
202
NaCl
35.8
36
36.3
36.6
37
37.7
37.8
38.4
39
(1)从表中得出,40℃时,KNO3的溶解度为___。
(2)将69gKNO3和18gNaCl完全溶解在50g水中,改变温度,使KNO3析出而NaCl不析出,则温度t应控制在的范围是_______(KNO3和NaCl溶解度互不影响)。
(3)KNO3溶液中含有少量的NaCl时,可通过________的方法提纯KNO3,对析出的晶体和剩余溶液的分析正确的是___(填字母)。
A剩余溶液一定是KNO3的饱和溶液
B剩余溶液一定是NaCl的不饱和溶液
C上述方法不能将两者完全分离
D析出的晶体中一定只含有硝酸钾
五、计算题
24.现有6.5克的锌与100g的稀硫酸恰好完全反应
(1)生成氢气的质量;_______
(2)求所用稀硫酸的溶质质量分数;_______
(3)求所得溶液的溶质质量分数;(保留一位小数)_______
25.为测定某生铁样品中铁的含量,现将5.8
g生铁样品置于烧杯中,加入一定质量的稀硫酸。所加稀硫酸与生成气体的质量关系如右图所示。
(1)据报道,每年因锈蚀而损失的钢铁相当于年产量的20%一40%,铁制品锈蚀的主要原因是_____________________________________________:。
(2)若该生铁样品中杂质不与稀硫酸反应,计算该样品中铁的含量(精确到0.1%)。
参考答案
1.B
2.C
3.D
4.D
5.B
6.C
7.A
8.B
9.D
10.B
11.D
12.C
13.B
14.C
15.C
16.50g
33.3g
17.不饱和
15.8%
18.110g
D
AB
>
19.40
不饱和
蒸发结晶
20.25
12.2
21. FeCl3
复分解反应
Fe+2HCl=FeCl2+H2↑
4Fe(OH)2+O2+2H2O=4Fe(OH)3
22.100mL
将砝码与称量物放反了(合理即可)
B
<
23.64g
20℃≤t<70℃
降温结晶
AC
24.(1)0.2g(2)9.8%(3)15.1%
25.(1)铁与空气中的氧气和水蒸气发生反应
(2)96.6%
答案第2页,总2页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
