第七单元《燃料及其利用》单元测试题(含答案)--2021-2022学年九年级化学人教版上册
文档属性
| 名称 | 第七单元《燃料及其利用》单元测试题(含答案)--2021-2022学年九年级化学人教版上册 |  | |
| 格式 | docx | ||
| 文件大小 | 223.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-07 14:54:10 | ||
图片预览


文档简介
第七单元《燃料及其利用》测试题
一、单选题
1.不能用于扑灭石油油井起火的方法是
A.降低石油的着火点
B.使火焰与空气隔绝
C.设法阻止石油喷射
D.降低油井井口的温度
2.如图所示的“火立熄”是一种新型的家用灭火用品。“火立熄”接触到火焰3~5秒后炸开,释放的粉末覆盖在可燃物上,同时放出不可燃气体,使火焰熄灭。其灭火原理是
A.清除可燃物
B.使可燃物与氧气隔绝
C.降低了可燃物的着火点
D.使温度降低到着火点以下
3.氢气运输车上应张贴的标志是( )
A.
B.
C.
D.
4.下列气体中,对空气有污染的是
A.N2
B.O2
C.CO
D.CO2
5.使燃料充分燃烧的方法,错误的是
A.提供足量的氧气
B.降低燃料的着火点
C.固体燃料粉碎
D.液体燃料喷成雾状
6.以下判断正确的是( )
A.煤、石油、乙醇是三种重要的化石燃料
B.空气中氧气的质量分数为21%
C.只有含碳元素的物质才能燃烧
D.扑灭图书档案火灾最适宜用液态二氧化碳灭火器
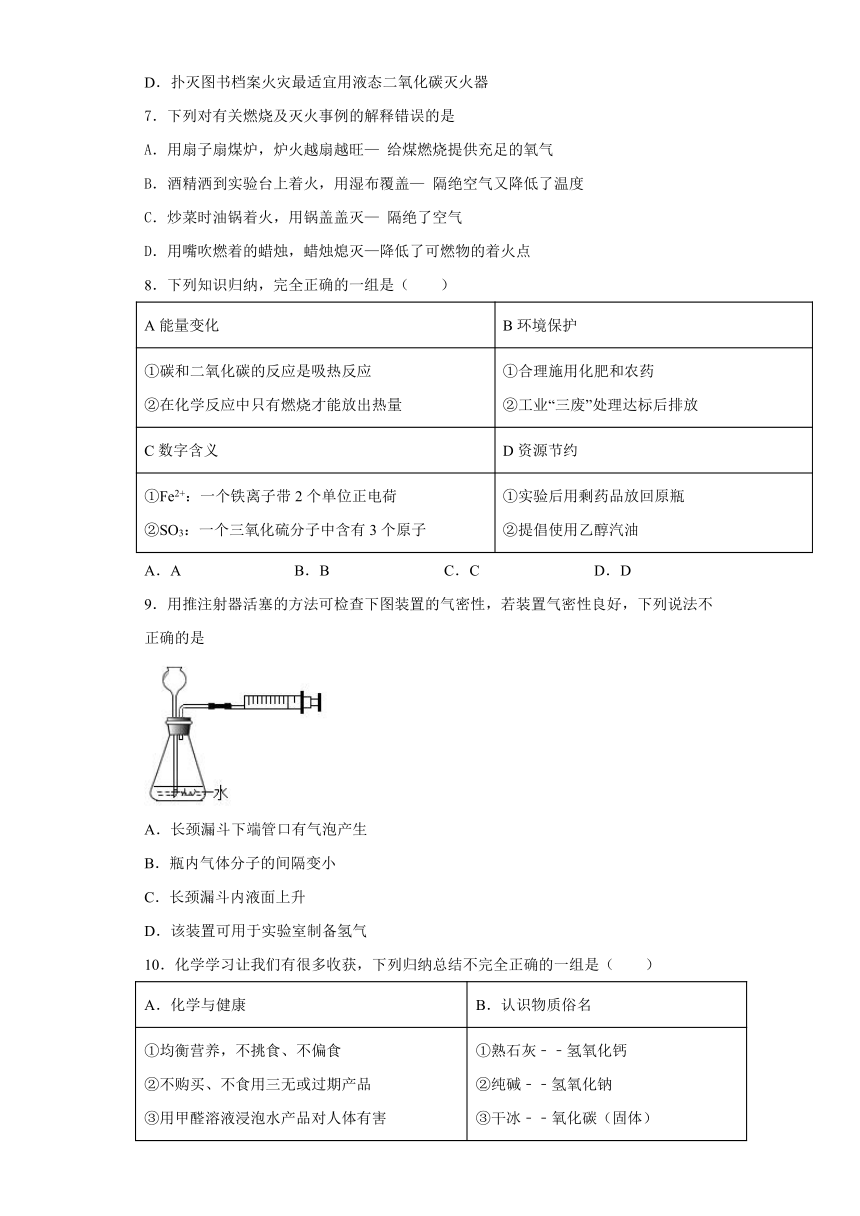
7.下列对有关燃烧及灭火事例的解释错误的是
A.用扇子扇煤炉,炉火越扇越旺—
给煤燃烧提供充足的氧气
B.酒精洒到实验台上着火,用湿布覆盖—
隔绝空气又降低了温度
C.炒菜时油锅着火,用锅盖盖灭—
隔绝了空气
D.用嘴吹燃着的蜡烛,蜡烛熄灭—降低了可燃物的着火点
8.下列知识归纳,完全正确的一组是( )
A能量变化
B环境保护
①碳和二氧化碳的反应是吸热反应
②在化学反应中只有燃烧才能放出热量
①合理施用化肥和农药
②工业“三废”处理达标后排放
C数字含义
D资源节约
①Fe2+:一个铁离子带2个单位正电荷
②SO3:一个三氧化硫分子中含有3个原子
①实验后用剩药品放回原瓶
②提倡使用乙醇汽油
A.A
B.B
C.C
D.D
9.用推注射器活塞的方法可检查下图装置的气密性,若装置气密性良好,下列说法不正确的是
A.长颈漏斗下端管口有气泡产生
B.瓶内气体分子的间隔变小
C.长颈漏斗内液面上升
D.该装置可用于实验室制备氢气
10.化学学习让我们有很多收获,下列归纳总结不完全正确的一组是( )
A.化学与健康
B.认识物质俗名
①均衡营养,不挑食、不偏食
②不购买、不食用三无或过期产品
③用甲醛溶液浸泡水产品对人体有害
①熟石灰﹣﹣氢氧化钙
②纯碱﹣﹣氢氧化钠
③干冰﹣﹣氧化碳(固体)
C.安全与自救
D.化学与资源
①在通风不畅的环境用煤取暖易导CO中毒
②身上着火后就地打滚是利用隔绝空气的灭火原理
③火灾发生后要用湿毛巾捂住口鼻迅速逃离并拨打火警电话119
①煤、石油、天然气是三大化石燃料
②合理使用农药化肥提高农业产量
③塑料、合成纤谁和合成橡胶属于三大有机合成材料
A.A
B.B
C.C
D.D
11.戊二醛(C5H8O2)是一种预防“禽流感”的高效消毒剂。下列说法错误的是
A.戊二醛属于有机化合物
B.戊二醛由碳、氢、氧三种元素组成
C.戊二醛中碳、氢、氧元素质量比为5:8:2
D.戊二醛中碳元素的质量分数最高
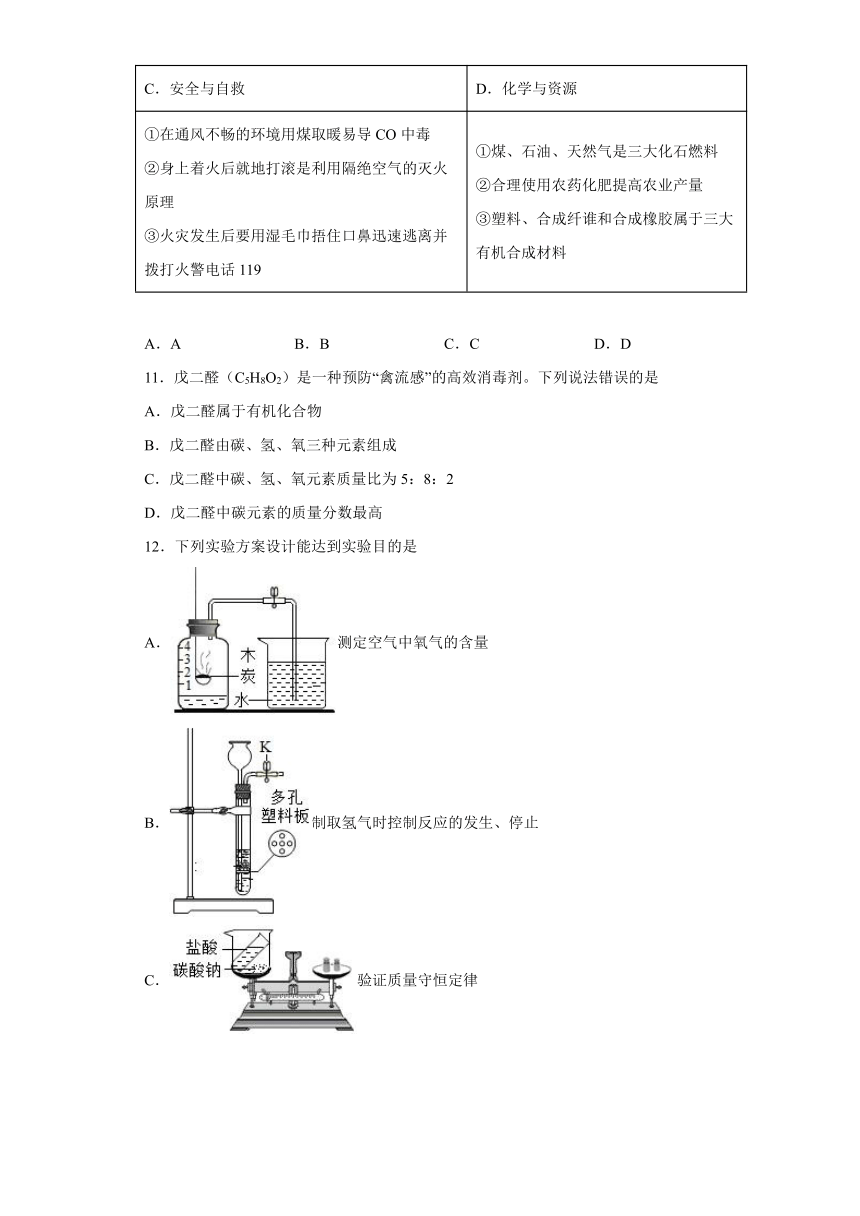
12.下列实验方案设计能达到实验目的是
A.测定空气中氧气的含量
B.制取氢气时控制反应的发生、停止
C.验证质量守恒定律
D.验证燃烧需要温度达到着火点
13.下列有关说法错误的是
A.验证质量守恒定律实验时,有气体参加或生成的反应应该在密闭仪器中进行
B.消防队员用水降低可燃物的温度来灭火
C.不锈钢具有很好的抗腐蚀性能,但也不是绝对不会生锈
D.合金的硬度一般比组成它们的纯金属的硬度大,熔点一般也比纯金属的熔点高
14.近年来,我国煤矿事故大多数是由于瓦斯爆炸所致.瓦斯中含有甲烷和一氧化碳等气体,当矿井中瓦斯浓度达到一定范围时遇明火即燃烧爆炸.为避免灾难发生,下列措施切实可行的是( )
①加强安全管理,杜绝明火源
②降低瓦斯气体的着火点
③提高通风能力
④将矿井中的氧气除去.
A.①③
B.②③
C.②④
D.①④
15.分类和归纳是学习化学的重要方法,下列分类归纳正确的是
A.最外层电子数相同的粒子一定是同种元素
B.pH<7的雨水一定是酸雨
C.生成盐和水的反应一定是中和反应
D.有机物一定含有碳元素
二、填空题
16.按要求回答下列问题:
(1)推广沼气使用既节能又环保,沼气主要成分是____________(填写化学式),其燃烧的化学方程式是_________________________________。
(2)化石燃料属于___________资源。人们生活中用煤作燃料一般是做成蜂窝状,目的是___________。
(3)Fe、Fe2+和Fe3+具有相同的___________数,都属于________元素,又因为它们的核外具有不同的_________数,故化学性质__________(填写“相同”或“不相同”)。
(4)金刚石与石墨物理性质不同的微观原因是?______;而铝化学性质活性但抗腐蚀能力好的原因是_________________(用化学方程式)。
17.我们的生活中处处有化学,下列生活中的问题用化学知识解答。
(1)“低碳生活”
方式中的”“
碳”指的是碳_____(填
“单质”
“原子”或“元素”)
(2)生活中用篮子沥水,该操作的原理类似化学实验中的_____操作
(3)用扇子扇煤炉,火焰越扇越旺是因为_____;
(4)日常生活中你的“绿色”做法_____(举一例)
18.能源与环境已经成为人们日益关注的问题:
(1)目前人类以化石燃料为主要能源,常见的化石燃料包括煤、天然气和___________。
(2)工业上常把煤块粉碎后使其充分燃烧,其目的是___________。
A.减少煤的浪费
B.减少氧气的消耗
C.减少一氧化碳的排放
D.减少酸雨的形成
(3)天然气的主要成分是甲烷,其完仝燃烧的化学方程式为_______,甲烷的燃烧对环境___________(填“会”或“不会”)产生影啊。
19.实验二中课外活动小组的同学针对家庭燃料的变迁,提出相关问题,请你参与讨论。
(1)20世纪60年代以前,我国城市家庭是以“煤球”为燃料,在冬天,时有煤气中毒事件发生,其原因可能是_____________________。
(2)到了70年代,已用“蜂窝煤”取代了“煤球”,你认为这种变化的好处是____________________。
(3)到了80年代,液化石油气和管道煤气取代了“蜂窝煤”。煤气中的主要成分CO燃烧的化学方程式是____。
(4)到了21世纪初,由于“西气东输”,天然气又取代了管道煤气,天然气中主要成分完全燃烧的化学方程式是_________________________________。
(5)已知同温同压下,相同体积的任何气体中含有的分子数目相同,燃气灶是由灶体、进气管、进风管和电子开关等组成的,若将燃烧煤气改为天然气,则更换的灶具与原来的灶具相比,构造上最大的区别是_______。
20.煤、石油和天然气是重要的、不可再生的能源,它们燃烧产生过多的二氧化碳等物质会对环境造成严重的影响。我国政府高度重视“节能减排”,确定我国今年“世界环境日”的主题和标识。
(1)下列措施符合我国“世界环境日”主题的是____________。(填字母)
A.限制发展高耗能的产业
B.推广使用“乙醇汽油”,减少有害气体排放
C.为了减少废气对本地区空气的污染,
化工厂加高烟囱
D.将污染严重的工厂迁到农村去
(2)天然气的主要成分是_______(填名称),其完全燃烧的化学方程式为_____________。
(3)图2中的信息告诫人类:二氧化碳等气体过多的排放,使_______________加剧,导致全球变暖。为减少二氧化碳过多的排放对环境的影响,你能做的一件事____________________;科学家采取“组分转化”技术,将二氧化碳和氢气以一定比例混和,在一定条件下反应,生成一种重要的化工原料乙烯(C2H4?)和水。该反应的化学方程式为_____________________________。
(4)为解决能源短缺和环境污染的问题,目前有待开发、利用的新能源有_______________。(写一种)
(5)“绿箱子环保计划——废弃手机及配件回收联合行动”已在全国许多重点城市中相继开展,废弃手机中的金属材料回收利用的意义,你认为有_______________(举出一个方面)。
三、推断题
21.A~G是初中化学常见的物质,它们之间的转化关系如图甲所示,部分反应条件、反应物及生成物已略去。A、C、F、G都为单质,B、D、E都为氧化物。C是世界年产量最高的金属,F是紫红色金属。回答下列问题:
⑴D的化学式为____________;
⑵写出B→A的化学方程式______________。
22.A~E均为初中化学中常见的物质.它们有如图所示的转化关系.
(1)若D为亮红色金属,C、E为无色气体且组成元素相同,则C的化学式为
_____
,反应①的化学方程式为
_____
.
(2)若通常状况下,A、B、D为气体,且B为单质,C、E为无色液体,则A的化学式为
_____
,反应②的化学方程式为
_____
.
四、实验题
23.请根据下列各图中有关信息,回答下列问题:
(1)仪器a、b的名称:a________,b________,取用粉末状药品使用的仪器是________。
(2)若用装置A制取氧气,其反应的文字表达式为________,若要收集到较纯净的氧气,其收集装置应选________(填序号)。
(3)实验用锌粒与稀硫酸反应制取氢气,为了控制反应的发生与停止,选择最佳的发生装置是________(填字母)。
(4)通常情况下,NH3是一种无色、有刺激性气味的气体,极易溶于水且水溶液显碱性,密度比空气小。实验室里用氯化铵固体和氢氧化钙固体混合加热制取NH3。实验室制取NH3应选择的发生装置是________(填字母),若选择G装置利用排空气法收集NH3,气体应该从________口(填“c”或“d”)进入。将NH3溶于水中可配制成氨水溶液,氨水能使无色酚酞变________色。
24.结合下图回答问题:
(1)仪器名称:①_____,②_____。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置_____(选填序号)和D组合,化学方程式为_____,二氧化锰的作用是_____。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有_____。用E装置收集H2,气体应从_____(选填“a”或“b”)端通入。
(4)F为简易净水装置,相当于化学实验中的_____装置。向该装置处理过的水中,加入少量肥皂水振荡,产生较多浮渣,说明是_____水(填“硬”或“软”),若要得到纯水,还需要进行_____(填操作名称)。
五、计算题
25.已知天然气的主要成份是甲烷,化学式为:CH4,求算:
(1)
碳元素和氢元素的质量比是:________
(2)32
g的甲烷完全燃烧的话,可以生成二氧化碳多少g________?
26.在海底和冻土层存在着储量巨大的“天然气水合物”,具有良好开发和应用前景。有科学家开采得到一种天然气水合物样品,取95.6g样品放置在一密闭弃器内,该样品迅速转化为甲烧气体(CH4)和水,将甲烷气体分离并完全燃烧,得到35.2g二氧化碳。求该天然气水合物样品中甲烷的质量分数。(精确到0.1%)
参考答案
1.A
2.B
3.B
4.C
5.B
6.D
7.D
8.B
9.A
10.B
11.C
12.B
13.D
14.A
15.D
16.CH4
;CH4+2O2CO2+2H2O不可再生;增大与氧气接触面;核电荷数(或质子数);铁;核外电子数(或最外层电子数);不相同。原子排列方式不同;4Al+3O2
=
2Al2O3
17.元素
过滤
增加了氧气
骑车出行等
18.石油
A
会
19.通风不好,煤燃烧不充分,产生的CO使人中毒
增大煤与空气的接触面积,使煤燃烧更充分
2CO+O22CO2
CH4+2O2CO2+2H2O
进气管减小(或进风管增大)
20.A
、B
甲烷(CH4)
CH4
+
2O2
CO2
+
2H2O
温室效应
植树造林(合理答案均可)
2CO2+6H2C2H4?
+4H2O
氢能(合理答案均可)
可以节约金属资源;可以节约冶炼相关金属所消耗的能源;可以减少对环境的污染。(任写一点)
21.CO
2H2O2H2↑+O2↑
22.CO
C+2CuO2Cu+CO2↑
CH4
C2H5OH+3O22CO2+3H2O
23.铁架台
长颈漏斗
药匙
D
C
A
d
红
24.铁架台
长颈漏斗
A
2KClO32KCl+3O2↑
催化
控制反应的发生与停止(或随开随停)
a
过滤
硬
蒸馏
25.(1)3:1(2)88g
26.13.4%
一、单选题
1.不能用于扑灭石油油井起火的方法是
A.降低石油的着火点
B.使火焰与空气隔绝
C.设法阻止石油喷射
D.降低油井井口的温度
2.如图所示的“火立熄”是一种新型的家用灭火用品。“火立熄”接触到火焰3~5秒后炸开,释放的粉末覆盖在可燃物上,同时放出不可燃气体,使火焰熄灭。其灭火原理是
A.清除可燃物
B.使可燃物与氧气隔绝
C.降低了可燃物的着火点
D.使温度降低到着火点以下
3.氢气运输车上应张贴的标志是( )
A.
B.
C.
D.
4.下列气体中,对空气有污染的是
A.N2
B.O2
C.CO
D.CO2
5.使燃料充分燃烧的方法,错误的是
A.提供足量的氧气
B.降低燃料的着火点
C.固体燃料粉碎
D.液体燃料喷成雾状
6.以下判断正确的是( )
A.煤、石油、乙醇是三种重要的化石燃料
B.空气中氧气的质量分数为21%
C.只有含碳元素的物质才能燃烧
D.扑灭图书档案火灾最适宜用液态二氧化碳灭火器
7.下列对有关燃烧及灭火事例的解释错误的是
A.用扇子扇煤炉,炉火越扇越旺—
给煤燃烧提供充足的氧气
B.酒精洒到实验台上着火,用湿布覆盖—
隔绝空气又降低了温度
C.炒菜时油锅着火,用锅盖盖灭—
隔绝了空气
D.用嘴吹燃着的蜡烛,蜡烛熄灭—降低了可燃物的着火点
8.下列知识归纳,完全正确的一组是( )
A能量变化
B环境保护
①碳和二氧化碳的反应是吸热反应
②在化学反应中只有燃烧才能放出热量
①合理施用化肥和农药
②工业“三废”处理达标后排放
C数字含义
D资源节约
①Fe2+:一个铁离子带2个单位正电荷
②SO3:一个三氧化硫分子中含有3个原子
①实验后用剩药品放回原瓶
②提倡使用乙醇汽油
A.A
B.B
C.C
D.D
9.用推注射器活塞的方法可检查下图装置的气密性,若装置气密性良好,下列说法不正确的是
A.长颈漏斗下端管口有气泡产生
B.瓶内气体分子的间隔变小
C.长颈漏斗内液面上升
D.该装置可用于实验室制备氢气
10.化学学习让我们有很多收获,下列归纳总结不完全正确的一组是( )
A.化学与健康
B.认识物质俗名
①均衡营养,不挑食、不偏食
②不购买、不食用三无或过期产品
③用甲醛溶液浸泡水产品对人体有害
①熟石灰﹣﹣氢氧化钙
②纯碱﹣﹣氢氧化钠
③干冰﹣﹣氧化碳(固体)
C.安全与自救
D.化学与资源
①在通风不畅的环境用煤取暖易导CO中毒
②身上着火后就地打滚是利用隔绝空气的灭火原理
③火灾发生后要用湿毛巾捂住口鼻迅速逃离并拨打火警电话119
①煤、石油、天然气是三大化石燃料
②合理使用农药化肥提高农业产量
③塑料、合成纤谁和合成橡胶属于三大有机合成材料
A.A
B.B
C.C
D.D
11.戊二醛(C5H8O2)是一种预防“禽流感”的高效消毒剂。下列说法错误的是
A.戊二醛属于有机化合物
B.戊二醛由碳、氢、氧三种元素组成
C.戊二醛中碳、氢、氧元素质量比为5:8:2
D.戊二醛中碳元素的质量分数最高
12.下列实验方案设计能达到实验目的是
A.测定空气中氧气的含量
B.制取氢气时控制反应的发生、停止
C.验证质量守恒定律
D.验证燃烧需要温度达到着火点
13.下列有关说法错误的是
A.验证质量守恒定律实验时,有气体参加或生成的反应应该在密闭仪器中进行
B.消防队员用水降低可燃物的温度来灭火
C.不锈钢具有很好的抗腐蚀性能,但也不是绝对不会生锈
D.合金的硬度一般比组成它们的纯金属的硬度大,熔点一般也比纯金属的熔点高
14.近年来,我国煤矿事故大多数是由于瓦斯爆炸所致.瓦斯中含有甲烷和一氧化碳等气体,当矿井中瓦斯浓度达到一定范围时遇明火即燃烧爆炸.为避免灾难发生,下列措施切实可行的是( )
①加强安全管理,杜绝明火源
②降低瓦斯气体的着火点
③提高通风能力
④将矿井中的氧气除去.
A.①③
B.②③
C.②④
D.①④
15.分类和归纳是学习化学的重要方法,下列分类归纳正确的是
A.最外层电子数相同的粒子一定是同种元素
B.pH<7的雨水一定是酸雨
C.生成盐和水的反应一定是中和反应
D.有机物一定含有碳元素
二、填空题
16.按要求回答下列问题:
(1)推广沼气使用既节能又环保,沼气主要成分是____________(填写化学式),其燃烧的化学方程式是_________________________________。
(2)化石燃料属于___________资源。人们生活中用煤作燃料一般是做成蜂窝状,目的是___________。
(3)Fe、Fe2+和Fe3+具有相同的___________数,都属于________元素,又因为它们的核外具有不同的_________数,故化学性质__________(填写“相同”或“不相同”)。
(4)金刚石与石墨物理性质不同的微观原因是?______;而铝化学性质活性但抗腐蚀能力好的原因是_________________(用化学方程式)。
17.我们的生活中处处有化学,下列生活中的问题用化学知识解答。
(1)“低碳生活”
方式中的”“
碳”指的是碳_____(填
“单质”
“原子”或“元素”)
(2)生活中用篮子沥水,该操作的原理类似化学实验中的_____操作
(3)用扇子扇煤炉,火焰越扇越旺是因为_____;
(4)日常生活中你的“绿色”做法_____(举一例)
18.能源与环境已经成为人们日益关注的问题:
(1)目前人类以化石燃料为主要能源,常见的化石燃料包括煤、天然气和___________。
(2)工业上常把煤块粉碎后使其充分燃烧,其目的是___________。
A.减少煤的浪费
B.减少氧气的消耗
C.减少一氧化碳的排放
D.减少酸雨的形成
(3)天然气的主要成分是甲烷,其完仝燃烧的化学方程式为_______,甲烷的燃烧对环境___________(填“会”或“不会”)产生影啊。
19.实验二中课外活动小组的同学针对家庭燃料的变迁,提出相关问题,请你参与讨论。
(1)20世纪60年代以前,我国城市家庭是以“煤球”为燃料,在冬天,时有煤气中毒事件发生,其原因可能是_____________________。
(2)到了70年代,已用“蜂窝煤”取代了“煤球”,你认为这种变化的好处是____________________。
(3)到了80年代,液化石油气和管道煤气取代了“蜂窝煤”。煤气中的主要成分CO燃烧的化学方程式是____。
(4)到了21世纪初,由于“西气东输”,天然气又取代了管道煤气,天然气中主要成分完全燃烧的化学方程式是_________________________________。
(5)已知同温同压下,相同体积的任何气体中含有的分子数目相同,燃气灶是由灶体、进气管、进风管和电子开关等组成的,若将燃烧煤气改为天然气,则更换的灶具与原来的灶具相比,构造上最大的区别是_______。
20.煤、石油和天然气是重要的、不可再生的能源,它们燃烧产生过多的二氧化碳等物质会对环境造成严重的影响。我国政府高度重视“节能减排”,确定我国今年“世界环境日”的主题和标识。
(1)下列措施符合我国“世界环境日”主题的是____________。(填字母)
A.限制发展高耗能的产业
B.推广使用“乙醇汽油”,减少有害气体排放
C.为了减少废气对本地区空气的污染,
化工厂加高烟囱
D.将污染严重的工厂迁到农村去
(2)天然气的主要成分是_______(填名称),其完全燃烧的化学方程式为_____________。
(3)图2中的信息告诫人类:二氧化碳等气体过多的排放,使_______________加剧,导致全球变暖。为减少二氧化碳过多的排放对环境的影响,你能做的一件事____________________;科学家采取“组分转化”技术,将二氧化碳和氢气以一定比例混和,在一定条件下反应,生成一种重要的化工原料乙烯(C2H4?)和水。该反应的化学方程式为_____________________________。
(4)为解决能源短缺和环境污染的问题,目前有待开发、利用的新能源有_______________。(写一种)
(5)“绿箱子环保计划——废弃手机及配件回收联合行动”已在全国许多重点城市中相继开展,废弃手机中的金属材料回收利用的意义,你认为有_______________(举出一个方面)。
三、推断题
21.A~G是初中化学常见的物质,它们之间的转化关系如图甲所示,部分反应条件、反应物及生成物已略去。A、C、F、G都为单质,B、D、E都为氧化物。C是世界年产量最高的金属,F是紫红色金属。回答下列问题:
⑴D的化学式为____________;
⑵写出B→A的化学方程式______________。
22.A~E均为初中化学中常见的物质.它们有如图所示的转化关系.
(1)若D为亮红色金属,C、E为无色气体且组成元素相同,则C的化学式为
_____
,反应①的化学方程式为
_____
.
(2)若通常状况下,A、B、D为气体,且B为单质,C、E为无色液体,则A的化学式为
_____
,反应②的化学方程式为
_____
.
四、实验题
23.请根据下列各图中有关信息,回答下列问题:
(1)仪器a、b的名称:a________,b________,取用粉末状药品使用的仪器是________。
(2)若用装置A制取氧气,其反应的文字表达式为________,若要收集到较纯净的氧气,其收集装置应选________(填序号)。
(3)实验用锌粒与稀硫酸反应制取氢气,为了控制反应的发生与停止,选择最佳的发生装置是________(填字母)。
(4)通常情况下,NH3是一种无色、有刺激性气味的气体,极易溶于水且水溶液显碱性,密度比空气小。实验室里用氯化铵固体和氢氧化钙固体混合加热制取NH3。实验室制取NH3应选择的发生装置是________(填字母),若选择G装置利用排空气法收集NH3,气体应该从________口(填“c”或“d”)进入。将NH3溶于水中可配制成氨水溶液,氨水能使无色酚酞变________色。
24.结合下图回答问题:
(1)仪器名称:①_____,②_____。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置_____(选填序号)和D组合,化学方程式为_____,二氧化锰的作用是_____。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有_____。用E装置收集H2,气体应从_____(选填“a”或“b”)端通入。
(4)F为简易净水装置,相当于化学实验中的_____装置。向该装置处理过的水中,加入少量肥皂水振荡,产生较多浮渣,说明是_____水(填“硬”或“软”),若要得到纯水,还需要进行_____(填操作名称)。
五、计算题
25.已知天然气的主要成份是甲烷,化学式为:CH4,求算:
(1)
碳元素和氢元素的质量比是:________
(2)32
g的甲烷完全燃烧的话,可以生成二氧化碳多少g________?
26.在海底和冻土层存在着储量巨大的“天然气水合物”,具有良好开发和应用前景。有科学家开采得到一种天然气水合物样品,取95.6g样品放置在一密闭弃器内,该样品迅速转化为甲烧气体(CH4)和水,将甲烷气体分离并完全燃烧,得到35.2g二氧化碳。求该天然气水合物样品中甲烷的质量分数。(精确到0.1%)
参考答案
1.A
2.B
3.B
4.C
5.B
6.D
7.D
8.B
9.A
10.B
11.C
12.B
13.D
14.A
15.D
16.CH4
;CH4+2O2CO2+2H2O不可再生;增大与氧气接触面;核电荷数(或质子数);铁;核外电子数(或最外层电子数);不相同。原子排列方式不同;4Al+3O2
=
2Al2O3
17.元素
过滤
增加了氧气
骑车出行等
18.石油
A
会
19.通风不好,煤燃烧不充分,产生的CO使人中毒
增大煤与空气的接触面积,使煤燃烧更充分
2CO+O22CO2
CH4+2O2CO2+2H2O
进气管减小(或进风管增大)
20.A
、B
甲烷(CH4)
CH4
+
2O2
CO2
+
2H2O
温室效应
植树造林(合理答案均可)
2CO2+6H2C2H4?
+4H2O
氢能(合理答案均可)
可以节约金属资源;可以节约冶炼相关金属所消耗的能源;可以减少对环境的污染。(任写一点)
21.CO
2H2O2H2↑+O2↑
22.CO
C+2CuO2Cu+CO2↑
CH4
C2H5OH+3O22CO2+3H2O
23.铁架台
长颈漏斗
药匙
D
C
A
d
红
24.铁架台
长颈漏斗
A
2KClO32KCl+3O2↑
催化
控制反应的发生与停止(或随开随停)
a
过滤
硬
蒸馏
25.(1)3:1(2)88g
26.13.4%
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
