黑龙江省虎林市高级中学化学课件2.1 钠及其化合物
文档属性
| 名称 | 黑龙江省虎林市高级中学化学课件2.1 钠及其化合物 |

|
|
| 格式 | zip | ||
| 文件大小 | 257.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 其它版本 | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-05-29 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
钠及其化合物
【知识梳理】
1.钠的物理性质
(1)颜色: ,熔点: ,硬度: ,
导电、导热性: 。
(2)钠、水与煤油的密度大小为: 。
银白色
低
小
良好
ρ水>ρ钠>ρ煤油
探究点一 钠
2.钠的化学性质
(1)主要化学性质
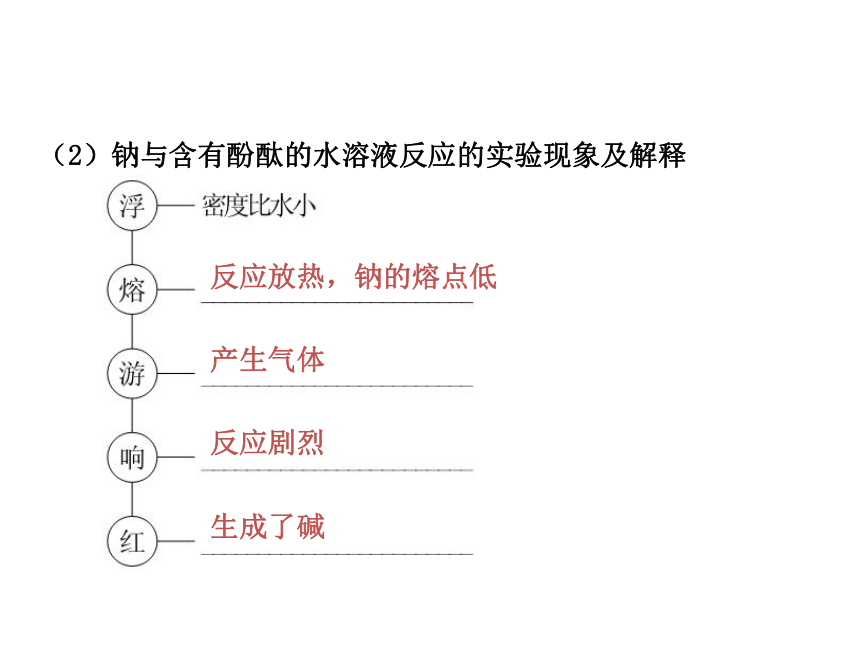
(2)钠与含有酚酞的水溶液反应的实验现象及解释
反应放热,钠的熔点低
产生气体
反应剧烈
生成了碱
3.钠的保存
实验室通常将少量金属钠保存在煤油中,目的是
。 d
防止钠与空气中的氧气和水发生反应
例1 将Na、Mg、Al各0.3 mol分别加入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积比是( )
A.1∶2∶3 B.6∶3∶2
C.3∶1∶1 D.1∶1∶1
【典例精析】
c
[2011·龙岩模拟]在一定温度下将一定量的金属
钠放入一定物质的量浓度的NaOH溶液中,反应完成后,NaOH溶液的物质的量浓度( )
A.增大 B.不能确定
C.减少 D.不变
B
【知识梳理】
氧化钠和过氧化钠的比较
名称 氧化钠 过氧化钠
化学式
阳、阴离子数比 Na+和O2-之比为____ Na+和O之比为2∶1
氧的化合价 -2 -1
类别 ____________
(不属于碱性氧化物)
与H2O反应
与CO2反应
与盐酸反应
稳定性 不稳定 较稳定
用途 供氧剂
转化关系
Na2O
Na2O2
2∶1
碱性氧化物
过氧化物
Na2O+H2O===2NaOH
2Na2O2+2H2O===4NaOH+O2↑
Na2O+CO2===Na2CO3
2Na2O2+2CO2===2Na2CO3+O2
Na2O+2HCl===2NaCl+H2O
2Na2O2+4HCl===4NaCl+2H2O+O2↑
探究点二 氧化钠与过氧化钠
例2 下列关于过氧化钠的叙述中,正确的是( )
A.过氧化钠能与酸反应生成盐和水,所以过氧化钠是
碱性氧化物
B.将过量Na2O2投入紫色石蕊试液中,溶液变蓝
C.过氧化钠与水反应时,过氧化钠既是氧化剂又是还
原剂
D.过氧化钠的电子式是Na+[? ?? ?]2-Na+
【典例精析】
C
CO2与H2的混合气体5 g在150 ℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4 g,则原混合气体中CO2的物质的量分数为( )
A.25% B.75%
C.88% D.32%
A
【知识梳理】
1.Na2CO3与NaHCO3(写出相关反应的离子方程式)
化学式 Na2CO3 NaHCO3
俗名
颜色、状态 ________(Na2CO3·
10H2O为晶体)
与过量
盐酸反应
与Ca(OH)2
反应(足量)
与BaCl2反应 不反应
加热 不易分解 2NaHCO3===Na2CO3+H2O↑+CO2↑
转化
纯碱
小苏打
白色粉末
白色晶体
探究点三 碳酸钠和碳酸氢钠及焰色反应
2.焰色反应
(1)概念
某些金属或它们的化合物在灼烧时会使火焰呈现出特殊的颜色,是 (填“化学”或“物理”)变化。
物理
(2)实验操作
洗——用__________洗净铂丝。
↓
烧——在无色火焰上灼烧至________________。
↓
蘸——用洁净的铂丝蘸取待测样品(固体或溶液)。
↓
烧——再次在火焰上灼烧,观察火焰的颜色。
↓
洗——将铂丝用__________洗净,再次灼烧至与火焰颜
色一致。
稀盐酸
与火焰颜色一致
稀盐酸
(3)常见金属元素焰色反应的颜色
黄色
紫色
蓝色钴玻璃
金属或金属离子 钠 钾
焰色反应的颜色 _____(透过____________ _观察)
【要点深化】
1.Na2CO3与NaHCO3的鉴别
2.Na2CO3、NaHCO3和盐酸的反应
Na2CO3溶液和稀盐酸反应可理解为分步反应:
Na2CO3+HCl===NaHCO3+NaCl
NaHCO3+HCl===NaCl+H2O+CO2↑
NaHCO3溶液和稀盐酸反应的化学方程式为:
NaHCO3+HCl===NaCl+H2O+CO2↑
(1)反应速率:NaHCO3快。
(2)CO2的生成量
①等物质的量的Na2CO3、NaHCO3分别与足量的盐
酸反应,产生的CO2相等;
②等质量的Na2CO3、NaHCO3分别与足量的盐酸反
应,NaHCO3产生的CO2多。
(3)Na2CO3溶液与盐酸的互滴鉴别
向Na2CO3溶液中逐滴加入盐酸,开始无气泡产生,
而向盐酸中滴加Na2CO3溶液,立即有气泡产生。
[2011·汕头模拟]可以用来断定碳酸氢钠粉末中是否混有碳酸钠的实验方法是( )
A.加热时有无色气体放出
B.滴加盐酸时有无气泡放出
C.溶于水后,滴加稀的氯化镁溶液,看有无白色沉淀生成
D.溶于水后,滴加澄清石灰水,看有无白色沉淀生成
C
钠及其化合物
【知识梳理】
1.钠的物理性质
(1)颜色: ,熔点: ,硬度: ,
导电、导热性: 。
(2)钠、水与煤油的密度大小为: 。
银白色
低
小
良好
ρ水>ρ钠>ρ煤油
探究点一 钠
2.钠的化学性质
(1)主要化学性质
(2)钠与含有酚酞的水溶液反应的实验现象及解释
反应放热,钠的熔点低
产生气体
反应剧烈
生成了碱
3.钠的保存
实验室通常将少量金属钠保存在煤油中,目的是
。 d
防止钠与空气中的氧气和水发生反应
例1 将Na、Mg、Al各0.3 mol分别加入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积比是( )
A.1∶2∶3 B.6∶3∶2
C.3∶1∶1 D.1∶1∶1
【典例精析】
c
[2011·龙岩模拟]在一定温度下将一定量的金属
钠放入一定物质的量浓度的NaOH溶液中,反应完成后,NaOH溶液的物质的量浓度( )
A.增大 B.不能确定
C.减少 D.不变
B
【知识梳理】
氧化钠和过氧化钠的比较
名称 氧化钠 过氧化钠
化学式
阳、阴离子数比 Na+和O2-之比为____ Na+和O之比为2∶1
氧的化合价 -2 -1
类别 ____________
(不属于碱性氧化物)
与H2O反应
与CO2反应
与盐酸反应
稳定性 不稳定 较稳定
用途 供氧剂
转化关系
Na2O
Na2O2
2∶1
碱性氧化物
过氧化物
Na2O+H2O===2NaOH
2Na2O2+2H2O===4NaOH+O2↑
Na2O+CO2===Na2CO3
2Na2O2+2CO2===2Na2CO3+O2
Na2O+2HCl===2NaCl+H2O
2Na2O2+4HCl===4NaCl+2H2O+O2↑
探究点二 氧化钠与过氧化钠
例2 下列关于过氧化钠的叙述中,正确的是( )
A.过氧化钠能与酸反应生成盐和水,所以过氧化钠是
碱性氧化物
B.将过量Na2O2投入紫色石蕊试液中,溶液变蓝
C.过氧化钠与水反应时,过氧化钠既是氧化剂又是还
原剂
D.过氧化钠的电子式是Na+[? ?? ?]2-Na+
【典例精析】
C
CO2与H2的混合气体5 g在150 ℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4 g,则原混合气体中CO2的物质的量分数为( )
A.25% B.75%
C.88% D.32%
A
【知识梳理】
1.Na2CO3与NaHCO3(写出相关反应的离子方程式)
化学式 Na2CO3 NaHCO3
俗名
颜色、状态 ________(Na2CO3·
10H2O为晶体)
与过量
盐酸反应
与Ca(OH)2
反应(足量)
与BaCl2反应 不反应
加热 不易分解 2NaHCO3===Na2CO3+H2O↑+CO2↑
转化
纯碱
小苏打
白色粉末
白色晶体
探究点三 碳酸钠和碳酸氢钠及焰色反应
2.焰色反应
(1)概念
某些金属或它们的化合物在灼烧时会使火焰呈现出特殊的颜色,是 (填“化学”或“物理”)变化。
物理
(2)实验操作
洗——用__________洗净铂丝。
↓
烧——在无色火焰上灼烧至________________。
↓
蘸——用洁净的铂丝蘸取待测样品(固体或溶液)。
↓
烧——再次在火焰上灼烧,观察火焰的颜色。
↓
洗——将铂丝用__________洗净,再次灼烧至与火焰颜
色一致。
稀盐酸
与火焰颜色一致
稀盐酸
(3)常见金属元素焰色反应的颜色
黄色
紫色
蓝色钴玻璃
金属或金属离子 钠 钾
焰色反应的颜色 _____(透过____________ _观察)
【要点深化】
1.Na2CO3与NaHCO3的鉴别
2.Na2CO3、NaHCO3和盐酸的反应
Na2CO3溶液和稀盐酸反应可理解为分步反应:
Na2CO3+HCl===NaHCO3+NaCl
NaHCO3+HCl===NaCl+H2O+CO2↑
NaHCO3溶液和稀盐酸反应的化学方程式为:
NaHCO3+HCl===NaCl+H2O+CO2↑
(1)反应速率:NaHCO3快。
(2)CO2的生成量
①等物质的量的Na2CO3、NaHCO3分别与足量的盐
酸反应,产生的CO2相等;
②等质量的Na2CO3、NaHCO3分别与足量的盐酸反
应,NaHCO3产生的CO2多。
(3)Na2CO3溶液与盐酸的互滴鉴别
向Na2CO3溶液中逐滴加入盐酸,开始无气泡产生,
而向盐酸中滴加Na2CO3溶液,立即有气泡产生。
[2011·汕头模拟]可以用来断定碳酸氢钠粉末中是否混有碳酸钠的实验方法是( )
A.加热时有无色气体放出
B.滴加盐酸时有无气泡放出
C.溶于水后,滴加稀的氯化镁溶液,看有无白色沉淀生成
D.溶于水后,滴加澄清石灰水,看有无白色沉淀生成
C
同课章节目录
