第2单元常见的酸和碱单元过关检测(二)(含解析)--2021-2022学年九年级化学鲁教版(五四学制)全一册
文档属性
| 名称 | 第2单元常见的酸和碱单元过关检测(二)(含解析)--2021-2022学年九年级化学鲁教版(五四学制)全一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 187.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-09 00:00:00 | ||
图片预览



文档简介
单元过关检测(二)第2单元常见的酸和碱2021~2022学年九年级化学同步练习(鲁教版五四学制)
一.选择题(共20小题)
1.下列实验操作正确的是( )
A.pH试纸的使用
B.检验氧气
C.点燃酒精灯
D.过滤
2.如图示实验操作正确的是( )
A.由试管底部套上试管夹
B.添加酒精
C.加入固体
D.测定溶液pH
3.能使无色酚酞试液变红色的溶液是( )
A.氯化钠溶液
B.盐酸
C.氯化铵溶液
D.氢氧化钠溶液
4.下列能使紫色石蕊溶液变红色的物质是( )
A.盐酸
B.氢氧化钠
C.石灰水
D.氨水
5.下列实验现象描述正确的是( )
A.硬水中滴加肥皂水,产生大量泡沫
B.铁丝在氧气中燃烧,火星四射
C.打开浓盐酸瓶盖,瓶口产生大量白烟
D.镁条在空气中燃烧,生成白色氧化镁
6.下列关于实验现象的描述,正确的是( )
A.固体硝酸铵溶于水,溶液温度降低
B.硫在空气中燃烧,产生有刺激性气味二氧化硫气体
C.打开盛浓盐酸的试剂瓶瓶盖,瓶口出现白烟
D.木炭在氧气中燃烧生成黑色固体
7.稀硫酸中能使紫色石蕊试液变红色的微粒是( )
A.硫酸分子
B.氢离子
C.硫酸根离子
D.水分子
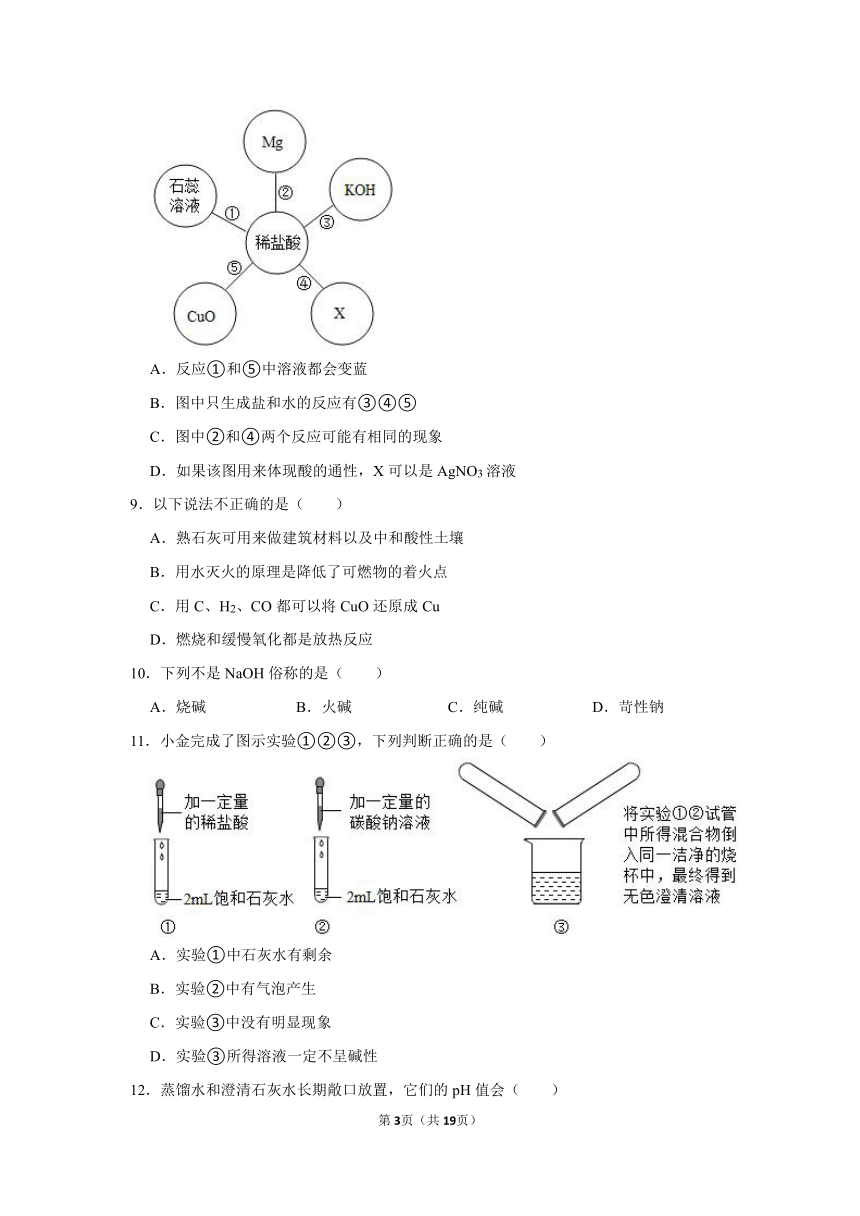
8.如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同。下列分析正确的是( )
A.反应①和⑤中溶液都会变蓝
B.图中只生成盐和水的反应有③④⑤
C.图中②和④两个反应可能有相同的现象
D.如果该图用来体现酸的通性,X可以是AgNO3溶液
9.以下说法不正确的是( )
A.熟石灰可用来做建筑材料以及中和酸性土壤
B.用水灭火的原理是降低了可燃物的着火点
C.用C、H2、CO都可以将CuO还原成Cu
D.燃烧和缓慢氧化都是放热反应
10.下列不是NaOH俗称的是( )
A.烧碱
B.火碱
C.纯碱
D.苛性钠
11.小金完成了图示实验①②③,下列判断正确的是( )
A.实验①中石灰水有剩余
B.实验②中有气泡产生
C.实验③中没有明显现象
D.实验③所得溶液一定不呈碱性
12.蒸馏水和澄清石灰水长期敞口放置,它们的pH值会( )
A.前者不变
后者变大
B.前者变小
后者变大
C.两者都变小
D.两者都变大
13.下列生活经验没有应用酸碱反应原理的是( )
A.用熟石灰改良酸性土壤
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸
C.用氢氧化铝治疗胃酸过多
D.用生石灰作干燥剂
14.小明同学在复习阶段在笔记本上对化学知识进行了归纳整理:
①用广泛pH试纸测得某地下水的pH为5.2
②粗盐提纯时需把蒸发皿中的水蒸干才能停止加热
③煤燃烧生成的有害气体二氧化硫溶于雨水会形成酸雨
④配制6%的氯化钠溶液,量取水时,仰视量筒刻度使所配氯化钠溶液的质量分数偏低
⑤氢氧化铝能治疗胃酸过多,所以氢氧化钠也可以治疗胃酸过多
⑥能使无色酚酞溶液变红的一定是碱溶液
⑦生成盐和水的反应一定是中和反应。
其中正确的个数是( )
A.2个
B.3个
C.4个
D.5个
15.如图是生活中常见洗涤用品的pH,显酸性的是( )
A.洁厕灵
B.消毒液
C.肥皂水
D.炉具清洁剂
16.如图是生活中一些物质的pH,下列说法中不正确的是( )
A.蚊虫叮咬可涂抹牙膏或肥皂水
B.肥皂水能使紫色石蕊溶液变红
C.胃酸过多的人适宜多喝玉米粥
D.西瓜汁的酸性比苹果汁的酸性弱
17.下列物质呈酸性的是( )
A.食醋
B.肥皂水
C.石灰水
D.浓氨水
18.某同学用月季花自制酸碱指示剂,并用于检验白醋的酸碱性,部分操作如下,其中错误的是( )
A.研磨花瓣
B.浸取色素
C.取用白醋
D.检验白醋
19.下列叙述正确的是( )
A.正常胃液的pH范围是0.5﹣1.9
B.酸有相似的化学性质,是因为不同的酸中都含氢离子
C.浓盐酸和浓硫酸敞口放置在空气中,一段时间后都变稀
D.饱和溶液一定比它的不饱和溶液浓
20.“关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A.扑灭因电线老化短路引起的失火,应在断电后使用干粉灭火器
B.用铁锅炒菜可以为人体补充铁元素,使用铁锅后应保持洁净、干燥
C.去除餐具上的油污,可利用洗涤剂、炉具清洁剂等碱性物质
D.健康人的体液必须维持在一定的酸碱度范围内,如血浆的PH在7.35?7.45
单元过关检测(二)第2单元常见的酸和碱2021~2022学年九年级化学同步练习(鲁教版五四学制)
参考答案与试题解析
一.选择题(共20小题)
1.下列实验操作正确的是( )
A.pH试纸的使用
B.检验氧气
C.点燃酒精灯
D.过滤
【分析】A、根据用pH试纸测定溶液的pH的方法进行分析判断。
B、根据氧气的检验方法进行分析判断。
C、使用酒精灯时要注意“两查、两禁、一不可”。
D、过滤液体时,注意“一贴、二低、三靠”的原则。
【解答】解:A、用pH试纸测定溶液的pH时,正确的操作方法为取一片pH试纸放在玻璃片或白瓷板上,用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,把试纸显示的颜色与标准比色卡对比来确定pH.不能将pH试纸伸入待测液中,以免污染待测液,图中所示操作错误。
B、检验是否是氧气时,将带火星的木条伸入集气瓶中,若木条复燃,说明是氧气,图中所示操作正确。
C、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所示操作错误。
D、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图中所示操作错误。
故选:B。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
2.如图示实验操作正确的是( )
A.由试管底部套上试管夹
B.添加酒精
C.加入固体
D.测定溶液pH
【分析】A、根据用试管夹夹持试管的方法,进行分析判断。
B、使用酒精灯时要注意“两查、两禁、一不可”。
C、根据向试管中装块状或颗粒状固体药品的方法(“一横、二放、三慢竖”)进行分析判断。
D、根据用pH试纸测定溶液的pH的方法进行分析判断。
【解答】解:A、用试管夹夹持试管时,试管夹应该从试管底部往上套,夹持在试管的中上部,图中所示操作正确。
B、使用酒精灯时要注意“两查、两禁、一不可”,禁止向燃着的酒精灯内添加酒精灯,图中所示操作错误。
C、向试管中装块状固体药品时,先将试管横放,用镊子把块状固体放在试管口,再慢慢将试管竖立起来,图中所示操作错误。
D、用pH试纸测定溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,把试纸显示的颜色与标准比色卡对比来确定pH.不能用水湿润pH试纸,溶液显酸性,则稀释了待测溶液,使溶液的酸性减弱,测定结果偏大,图中所示操作错误。
故选:A。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
3.能使无色酚酞试液变红色的溶液是( )
A.氯化钠溶液
B.盐酸
C.氯化铵溶液
D.氢氧化钠溶液
【分析】根据已有的酚酞遇碱性溶液变红的知识进行分析解答即可.
【解答】解:A、氯化钠溶液呈中性,不能使酚酞试液变色,错误;
B、盐酸呈酸性,不能使酚酞试液变色,错误;
C、氯化铵溶液呈中性,不能使酚酞试液变色,错误;
D、氢氧化钠溶液呈碱性,能使酚酞试液变色,正确;
故选:D。
【点评】本题考查的是溶液的酸碱性与指示剂变色的知识,完成此题,可以依据已有的知识进行.
4.下列能使紫色石蕊溶液变红色的物质是( )
A.盐酸
B.氢氧化钠
C.石灰水
D.氨水
【分析】紫色石蕊溶液遇酸性溶液变红,遇中性溶液不变色,遇碱性溶液变蓝,进行分析判断。
【解答】解:A、盐酸显酸性,能使紫色石蕊溶液变红色,故选项正确。
B、氢氧化钠显碱性,能使紫色石蕊溶液变蓝色,故选项错误。
C、石灰水显碱性,能使紫色石蕊溶液变蓝色,故选项错误。
D、氨水显碱性,能使紫色石蕊溶液变蓝色,故选项错误。
故选:A。
【点评】本题难度不大,掌握紫色石蕊溶液遇酸碱性溶液的变色情况、常见物质的酸碱性是正确解答本题的关键。
5.下列实验现象描述正确的是( )
A.硬水中滴加肥皂水,产生大量泡沫
B.铁丝在氧气中燃烧,火星四射
C.打开浓盐酸瓶盖,瓶口产生大量白烟
D.镁条在空气中燃烧,生成白色氧化镁
【分析】A、根据硬水的检验方法,进行分析判断。
B、根据铁丝在氧气中燃烧的现象进行分析判断.
C、根据浓盐酸具有挥发性,进行分析判断。
D、根据镁条在空气中燃烧的现象,进行分析判断。
【解答】解:A、硬水中滴加肥皂水,产生较少的泡沫,故选项说法错误。
B、铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故选项说法正确。
C、浓盐酸具有挥发性,打开装有浓盐酸试剂瓶的瓶塞,从浓盐酸中挥发出来的氯化氢气体与空气中的水蒸气接触形成盐酸小液滴,瓶口上方有白雾产生,故选项说法错误。
D、镁条在空气中燃烧,生成白色氧化镁是实验结论而不是实验现象,故选项说法错误。
故选:B。
【点评】本题难度不大,掌握浓盐酸具有挥发性、常见物质燃烧的现象等即可正确解答,在描述实验现象时,需要注意烟和雾的区别、实验结论和实验现象的区别。
6.下列关于实验现象的描述,正确的是( )
A.固体硝酸铵溶于水,溶液温度降低
B.硫在空气中燃烧,产生有刺激性气味二氧化硫气体
C.打开盛浓盐酸的试剂瓶瓶盖,瓶口出现白烟
D.木炭在氧气中燃烧生成黑色固体
【分析】A、根据硝酸铵溶于水吸热,进行分析判断。
B、根据硫在空气中燃烧的现象,进行分析判断。
C、根据浓盐酸具有挥发性,进行分析判断。
D、根据木炭在氧气中燃烧的现象,进行分析判断。
【解答】解:A、硝酸铵溶于水吸热,溶液温度降低,故选项说法正确。
B、硫在空气中燃烧,产生有刺激性气味二氧化硫气体是实验结论而不是实验现象,故选项说法错误。
C、浓盐酸具有挥发性,打开装有浓盐酸试剂瓶的瓶塞,从浓盐酸中挥发出来的氯化氢气体与空气中的水蒸气接触形成盐酸小液滴,瓶口上方有白雾产生,故选项说法错误。
D、木炭在氧气中燃烧,发出白光,生成能使澄清石灰水变浑浊的气体,故选项说法错误。
故选:A。
【点评】本题难度不大,掌握浓盐酸具有挥发性、硝酸铵溶于水吸热、常见物质燃烧的现象等即可正确解答,在描述实验现象时,需要注意烟和雾的区别、实验结论和实验现象的区别。
7.稀硫酸中能使紫色石蕊试液变红色的微粒是( )
A.硫酸分子
B.氢离子
C.硫酸根离子
D.水分子
【分析】根据酸的化学性质,进行分析判断。
【解答】解:酸是指在电离时产生的阳离子全部是氢离子的化合物,稀硫酸中能使紫色石蕊试液变红色的微粒是氢离子。
故选:B。
【点评】本题难度不大,掌握酸的化学性质、酸具有相似化学性质的原因是正确解答本题的关键。
8.如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同。下列分析正确的是( )
A.反应①和⑤中溶液都会变蓝
B.图中只生成盐和水的反应有③④⑤
C.图中②和④两个反应可能有相同的现象
D.如果该图用来体现酸的通性,X可以是AgNO3溶液
【分析】A、稀盐酸显酸性,能使石蕊溶液变红色;
B、硝酸银和盐酸反应生成氯化银沉淀和硝酸;
C、镁和盐酸反应生成氯化镁和氢气,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
D、盐酸能和硝酸银反应生成白色沉淀氯化银和硝酸。
【解答】解:A、稀盐酸显酸性,能使石蕊溶液变红色,该选项说法不正确;
B、如果X是硝酸银,则硝酸银和盐酸反应生成氯化银沉淀和硝酸,不能生成水,该选项说法不正确;
C、镁和盐酸反应生成氯化镁和氢气,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,实验现象都是固体溶解,产生气泡,该选项说法正确;
D、AgNO3溶液与盐酸反应体现的是盐酸中氯离子的性质,而不是酸电离的氢离子的性质,所以AgNO3溶液不能体现酸的通性,该选项说法不正确。
故选:C。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。
9.以下说法不正确的是( )
A.熟石灰可用来做建筑材料以及中和酸性土壤
B.用水灭火的原理是降低了可燃物的着火点
C.用C、H2、CO都可以将CuO还原成Cu
D.燃烧和缓慢氧化都是放热反应
【分析】A、根据熟石灰的性质解答;
B、根据水灭火的原理解答;
C、根据这三种物质的性质解答;
D、根据氧化反应的特点解答.
【解答】解:A、熟石灰能与二氧化碳反应生成坚硬额块状固体碳酸钙,可以用作建筑材料,氢氧化钙具有碱性,能与酸性物质反应,可以用于改良酸性土壤,正确;
B、用水灭火的原理是降低温度到可燃物的着火点以下,不是降低了着火点,错误;
C、碳、氢气和一氧化碳都具有还原性,可以用于还原氧化铜,正确;
D、燃烧和缓慢氧化都有热量放出,正确;
故选:B。
【点评】本题考查的是常见的物质的性质以及化学反应中能量的变化,完成此题,可以依据已有的知识进行.
10.下列不是NaOH俗称的是( )
A.烧碱
B.火碱
C.纯碱
D.苛性钠
【分析】根据所学知识可以知道,氢氧化钠俗称烧碱、火碱、苛性钠。
【解答】解:氢氧化钠俗称烧碱、火碱、苛性钠,而纯碱是碳酸钠的俗称;
故选:C。
【点评】本题考查了氢氧化钠的俗称,完成此题,可以依据已有的知识进行。要求同学们在平时的学习中加强基础知识的储备。
11.小金完成了图示实验①②③,下列判断正确的是( )
A.实验①中石灰水有剩余
B.实验②中有气泡产生
C.实验③中没有明显现象
D.实验③所得溶液一定不呈碱性
【分析】A.依据盐酸与石灰水的实验现象分析;
B.依据碳酸钠与石灰水反应原理分析;
C.依据实验①和②的生成物分析,再依据实验③的现象分析;
D.依据实验③的现象分析。
【解答】解:A.实验①反应后试管中一定含有氯化钙,可能含有HCl或Ca(OH)2,实验②反应后的试管中一定含有CaCO3和NaOH,可能含有Na2CO3,或Ca(OH)2,将实验①②反应后的物质混合,最终得无色溶液,则说明实验①反应后试管中一定含有CaCl2和HCl,则实验①中石灰水无剩余,故A错误;
B.碳酸钠与石灰水反应生成白色碳酸钙沉淀和氢氧化钠,则实验②的实验现象为产生白色沉淀,故B错误;
C.综合分析实验①②③可知,实验①中一定是盐酸有剩余,则实验①反应后盐酸与实验②中碳酸钙反应生成CaCl2、水和二氧化碳,所以实验③的现象是固体溶解,有气泡产生,故C错误;
D.①反应后试管中HCl,先与②反应后的NaOH(或NaOH和Ca(OH)2)反应,再与CaCO3反应,最终得无色溶液,则实验③所得溶液一定不呈碱性,故D正确;
故选:D。
【点评】此题主要考查常见物质的性质,主要利用实验图示及物质的性质来分析和解决有关问题,结合各方面的条件得出正确结论。
12.蒸馏水和澄清石灰水长期敞口放置,它们的pH值会( )
A.前者不变
后者变大
B.前者变小
后者变大
C.两者都变小
D.两者都变大
【分析】二氧化碳能够溶于水,和水反应能生成碳酸;石灰水能够吸收空气中的二氧化碳,二氧化碳和氢氧化钙反应能生成碳酸钙和水.
【解答】解:蒸馏水显中性,pH等于7,二氧化碳溶于水后生成的碳酸显酸性,溶液的pH减小;
石灰水显碱性,pH大于7,吸收二氧化碳后,二氧化碳和氢氧化钙反应生成碳酸钙和水,溶液的碱性减弱,pH减小。
故选:C。
【点评】解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论.
13.下列生活经验没有应用酸碱反应原理的是( )
A.用熟石灰改良酸性土壤
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸
C.用氢氧化铝治疗胃酸过多
D.用生石灰作干燥剂
【分析】中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,据此进行分析判断。
【解答】解:A、用熟石灰改良酸性土壤,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,应用了酸碱反应原理,故选项错误.
B、用氢氧化钠溶液洗涤石油产品中的残留硫酸,该反应的反应物是酸和碱,属于中和反应,应用了酸碱反应原理,故选项错误.
C、用氢氧化铝治疗胃酸过多,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,应用了酸碱反应原理,故选项错误.
D、用生石灰作干燥剂,该反应的反应物是金属氧化物和水,不是酸与碱的反应,不属于中和反应,没有应用酸碱反应原理,故选项正确.
故选:D。
【点评】本题难度不大,掌握中和反应的特征(反应物是酸和碱,生成物是盐和水)是正确解答此类题的关键。
14.小明同学在复习阶段在笔记本上对化学知识进行了归纳整理:
①用广泛pH试纸测得某地下水的pH为5.2
②粗盐提纯时需把蒸发皿中的水蒸干才能停止加热
③煤燃烧生成的有害气体二氧化硫溶于雨水会形成酸雨
④配制6%的氯化钠溶液,量取水时,仰视量筒刻度使所配氯化钠溶液的质量分数偏低
⑤氢氧化铝能治疗胃酸过多,所以氢氧化钠也可以治疗胃酸过多
⑥能使无色酚酞溶液变红的一定是碱溶液
⑦生成盐和水的反应一定是中和反应。
其中正确的个数是( )
A.2个
B.3个
C.4个
D.5个
【分析】①pH试纸上的标准比色卡上的数字只有整数,即使用pH试纸所测得的溶液酸碱度为整数。
②根据蒸发操作中停止加热的时机,进行分析判断。
③根据二氧化硫对环境的影响,进行分析判断。
④用量筒量取水时,仰视液面,读数比实际液体体积小,进行分析判断。
⑤根据氢氧化钠具有腐蚀性,进行分析判断。
⑥根据显碱性的不一定是碱溶液,进行分析判断。
⑦中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,进行分析判断。
【解答】解:①由于标准比色卡上的数字只有整数,用广泛pH试纸测得某地下水的pH不可能精确为5.2,故说法错误。
②蒸发时,待蒸发皿中出现较多固体时,应停止加热,利用余热将剩余液体蒸干,故说法错误。
③煤燃烧生成的有害气体二氧化硫溶于雨水,会形成酸雨,故说法正确。
④配制6%的氯化钠溶液,量取水时,仰视量筒刻度,读数比实际液体体积小,会造成实际量取的水的体积偏大,使所配氯化钠溶液的质量分数偏低,故说法正确。
⑤氢氧化铝能治疗胃酸过多,氢氧化钠具有腐蚀性,不能用于治疗胃酸过多,故说法错误。
⑥能使无色酚酞溶液变红的不一定是碱溶液,也可能是碳酸钠等盐溶液,故说法错误。
⑦中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故说法错误。
故正确的个数是2个。
故选:A。
【点评】本题难度不大,掌握中和反应的特征、氢氧化钠具有腐蚀性、显碱性的不一定是碱溶液等是正确解答本题的关键。
15.如图是生活中常见洗涤用品的pH,显酸性的是( )
A.洁厕灵
B.消毒液
C.肥皂水
D.炉具清洁剂
【分析】当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性,且pH越大,碱性越强。据此分析判断即可。
【解答】解:A、洁厕灵pH为1~2,pH小于7,显酸性,故正确;
B、消毒液pH为8~9,pH大于7,显碱性,故错误;
C、肥皂水pH为9~11,pH大于7,显碱性,故错误;
D、炉具清洁剂pH为12~13,pH大于7,显碱性,故错误;
故选:A。
【点评】本题难度不大,掌握溶液的酸碱性和溶液pH大小之间的关系是顺利解题的关键。
16.如图是生活中一些物质的pH,下列说法中不正确的是( )
A.蚊虫叮咬可涂抹牙膏或肥皂水
B.肥皂水能使紫色石蕊溶液变红
C.胃酸过多的人适宜多喝玉米粥
D.西瓜汁的酸性比苹果汁的酸性弱
【分析】当溶液的pH等于7时,呈中性。当溶液的pH大于7时,呈碱性。当溶液的pH小于7时,呈酸性。当溶液的pH<7时,随着pH的减小酸性增强。当溶液的pH>7时,随着pH的增大碱性增强。石蕊试液遇酸性溶液变红色,遇碱性溶液变蓝色,遇中性溶液不变色。
【解答】解:A.蚊虫的毒液显酸性,牙膏和肥皂水的pH大于7,显碱性,所以蚊虫叮咬可涂抹牙膏或肥皂水,选项说法正确;
B.肥皂水的pH大于7,显碱性,能使紫色石蕊溶液变蓝色,选项说法错误;
C.玉米粥显弱碱性,所以胃酸过多的人适宜多喝玉米粥,选项说法正确;
D.西瓜汁的pH大于苹果汁的pH,所以西瓜汁的酸性比苹果汁的酸性弱,选项说法正确。
故选:B。
【点评】解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论。
17.下列物质呈酸性的是( )
A.食醋
B.肥皂水
C.石灰水
D.浓氨水
【分析】根据常见物质的酸碱性,进行分析判断。
【解答】解:A、食醋中含有醋酸,显酸性,故选项正确。
B、肥皂水显碱性,故选项错误。
C、石灰水是氢氧化钙的水溶液,显碱性,故选项错误。
D、浓氨水属于碱溶液,显碱性,故选项错误。
故选:A。
【点评】本题难度不大,了解常见化学物质的酸碱性是正确解答本题的关键。
18.某同学用月季花自制酸碱指示剂,并用于检验白醋的酸碱性,部分操作如下,其中错误的是( )
A.研磨花瓣
B.浸取色素
C.取用白醋
D.检验白醋
【分析】A、根据研磨的方法,进行分析判断。
B、根据浸取色素的方法,进行分析判断。
C、根据向试管中倾倒液体药品的方法进行分析判断。
D、根据使用胶头滴管滴加少量液体的方法进行分析判断。
【解答】解:A、研磨花瓣,可在研钵中进行,图中所示操作正确。
B、将研磨后的花瓣放入烧杯中,加入水浸泡,可用玻璃棒进行搅拌,图中所示操作正确。
C、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨试管口,图中所示操作正确。
D、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误。
故选:D。
【点评】本题难度不大,熟悉检验白醋的酸碱性的实验步骤、各操作的注意事项是解答本题的关键。
19.下列叙述正确的是( )
A.正常胃液的pH范围是0.5﹣1.9
B.酸有相似的化学性质,是因为不同的酸中都含氢离子
C.浓盐酸和浓硫酸敞口放置在空气中,一段时间后都变稀
D.饱和溶液一定比它的不饱和溶液浓
【分析】A.根据胃液的pH来分析;
B.根据酸具有通性的原因来分析;
C.根据浓盐酸的挥发性以及浓硫酸的吸水性来分析;
D.根据溶液的浓度大小来分析。
【解答】解:A.正常胃液的pH范围:0.9~1.5,故错误;
B.酸有相似的化学性质,是因为不同的酸中的阳离子都全部是氢离子,故错误;
C.浓盐酸具有挥发性,溶质减少,溶质质量分数减小,浓硫酸具有吸水性,溶剂增多,溶质质量分数减小,故正确;
D.因为不知道温度,因此无法判断饱和溶液是否比它的不饱和溶液浓,故错误。
故选:C。
【点评】本题考查的知识点较多,掌握胃酸的范围、酸具有共性的原因、浓盐酸与浓硫酸的性质、溶液浓度的比较等,难度不大。
20.“关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A.扑灭因电线老化短路引起的失火,应在断电后使用干粉灭火器
B.用铁锅炒菜可以为人体补充铁元素,使用铁锅后应保持洁净、干燥
C.去除餐具上的油污,可利用洗涤剂、炉具清洁剂等碱性物质
D.健康人的体液必须维持在一定的酸碱度范围内,如血浆的PH在7.35?7.45
【分析】A、根据灭火的原理进行解答;
B、根据铁锅后应保持洁净、干燥可以防止铁生锈进行解答;
C、根据炉具清洁剂中含有氢氧化钠,氢氧化钠具有强烈的腐蚀性进行解答;
D、根据健康人的体液必须维持在一定的酸碱度范围内进行解答。
【解答】解:A、扑灭因电线老化短路引起的失火,应在断电后使用干粉灭火器,故A正确;
B、用铁锅炒菜可以为人体补充铁元素,使用铁锅后应保持洁净、干燥可以防止铁生锈,故B正确;
C、炉具清洁剂中含有氢氧化钠,氢氧化钠具有强烈的腐蚀性,不能用于餐具去除餐具上的油污,故C错误;
D、健康人的体液必须维持在一定的酸碱度范围内,如血浆的pH在7.35?7.45,故D正确。
故选:C。
【点评】本题难度不大,了解化学元素与人体健康的关系、灭火的原理等是正确解答本题的关键。
第2页(共3页)
一.选择题(共20小题)
1.下列实验操作正确的是( )
A.pH试纸的使用
B.检验氧气
C.点燃酒精灯
D.过滤
2.如图示实验操作正确的是( )
A.由试管底部套上试管夹
B.添加酒精
C.加入固体
D.测定溶液pH
3.能使无色酚酞试液变红色的溶液是( )
A.氯化钠溶液
B.盐酸
C.氯化铵溶液
D.氢氧化钠溶液
4.下列能使紫色石蕊溶液变红色的物质是( )
A.盐酸
B.氢氧化钠
C.石灰水
D.氨水
5.下列实验现象描述正确的是( )
A.硬水中滴加肥皂水,产生大量泡沫
B.铁丝在氧气中燃烧,火星四射
C.打开浓盐酸瓶盖,瓶口产生大量白烟
D.镁条在空气中燃烧,生成白色氧化镁
6.下列关于实验现象的描述,正确的是( )
A.固体硝酸铵溶于水,溶液温度降低
B.硫在空气中燃烧,产生有刺激性气味二氧化硫气体
C.打开盛浓盐酸的试剂瓶瓶盖,瓶口出现白烟
D.木炭在氧气中燃烧生成黑色固体
7.稀硫酸中能使紫色石蕊试液变红色的微粒是( )
A.硫酸分子
B.氢离子
C.硫酸根离子
D.水分子
8.如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同。下列分析正确的是( )
A.反应①和⑤中溶液都会变蓝
B.图中只生成盐和水的反应有③④⑤
C.图中②和④两个反应可能有相同的现象
D.如果该图用来体现酸的通性,X可以是AgNO3溶液
9.以下说法不正确的是( )
A.熟石灰可用来做建筑材料以及中和酸性土壤
B.用水灭火的原理是降低了可燃物的着火点
C.用C、H2、CO都可以将CuO还原成Cu
D.燃烧和缓慢氧化都是放热反应
10.下列不是NaOH俗称的是( )
A.烧碱
B.火碱
C.纯碱
D.苛性钠
11.小金完成了图示实验①②③,下列判断正确的是( )
A.实验①中石灰水有剩余
B.实验②中有气泡产生
C.实验③中没有明显现象
D.实验③所得溶液一定不呈碱性
12.蒸馏水和澄清石灰水长期敞口放置,它们的pH值会( )
A.前者不变
后者变大
B.前者变小
后者变大
C.两者都变小
D.两者都变大
13.下列生活经验没有应用酸碱反应原理的是( )
A.用熟石灰改良酸性土壤
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸
C.用氢氧化铝治疗胃酸过多
D.用生石灰作干燥剂
14.小明同学在复习阶段在笔记本上对化学知识进行了归纳整理:
①用广泛pH试纸测得某地下水的pH为5.2
②粗盐提纯时需把蒸发皿中的水蒸干才能停止加热
③煤燃烧生成的有害气体二氧化硫溶于雨水会形成酸雨
④配制6%的氯化钠溶液,量取水时,仰视量筒刻度使所配氯化钠溶液的质量分数偏低
⑤氢氧化铝能治疗胃酸过多,所以氢氧化钠也可以治疗胃酸过多
⑥能使无色酚酞溶液变红的一定是碱溶液
⑦生成盐和水的反应一定是中和反应。
其中正确的个数是( )
A.2个
B.3个
C.4个
D.5个
15.如图是生活中常见洗涤用品的pH,显酸性的是( )
A.洁厕灵
B.消毒液
C.肥皂水
D.炉具清洁剂
16.如图是生活中一些物质的pH,下列说法中不正确的是( )
A.蚊虫叮咬可涂抹牙膏或肥皂水
B.肥皂水能使紫色石蕊溶液变红
C.胃酸过多的人适宜多喝玉米粥
D.西瓜汁的酸性比苹果汁的酸性弱
17.下列物质呈酸性的是( )
A.食醋
B.肥皂水
C.石灰水
D.浓氨水
18.某同学用月季花自制酸碱指示剂,并用于检验白醋的酸碱性,部分操作如下,其中错误的是( )
A.研磨花瓣
B.浸取色素
C.取用白醋
D.检验白醋
19.下列叙述正确的是( )
A.正常胃液的pH范围是0.5﹣1.9
B.酸有相似的化学性质,是因为不同的酸中都含氢离子
C.浓盐酸和浓硫酸敞口放置在空气中,一段时间后都变稀
D.饱和溶液一定比它的不饱和溶液浓
20.“关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A.扑灭因电线老化短路引起的失火,应在断电后使用干粉灭火器
B.用铁锅炒菜可以为人体补充铁元素,使用铁锅后应保持洁净、干燥
C.去除餐具上的油污,可利用洗涤剂、炉具清洁剂等碱性物质
D.健康人的体液必须维持在一定的酸碱度范围内,如血浆的PH在7.35?7.45
单元过关检测(二)第2单元常见的酸和碱2021~2022学年九年级化学同步练习(鲁教版五四学制)
参考答案与试题解析
一.选择题(共20小题)
1.下列实验操作正确的是( )
A.pH试纸的使用
B.检验氧气
C.点燃酒精灯
D.过滤
【分析】A、根据用pH试纸测定溶液的pH的方法进行分析判断。
B、根据氧气的检验方法进行分析判断。
C、使用酒精灯时要注意“两查、两禁、一不可”。
D、过滤液体时,注意“一贴、二低、三靠”的原则。
【解答】解:A、用pH试纸测定溶液的pH时,正确的操作方法为取一片pH试纸放在玻璃片或白瓷板上,用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,把试纸显示的颜色与标准比色卡对比来确定pH.不能将pH试纸伸入待测液中,以免污染待测液,图中所示操作错误。
B、检验是否是氧气时,将带火星的木条伸入集气瓶中,若木条复燃,说明是氧气,图中所示操作正确。
C、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所示操作错误。
D、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图中所示操作错误。
故选:B。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
2.如图示实验操作正确的是( )
A.由试管底部套上试管夹
B.添加酒精
C.加入固体
D.测定溶液pH
【分析】A、根据用试管夹夹持试管的方法,进行分析判断。
B、使用酒精灯时要注意“两查、两禁、一不可”。
C、根据向试管中装块状或颗粒状固体药品的方法(“一横、二放、三慢竖”)进行分析判断。
D、根据用pH试纸测定溶液的pH的方法进行分析判断。
【解答】解:A、用试管夹夹持试管时,试管夹应该从试管底部往上套,夹持在试管的中上部,图中所示操作正确。
B、使用酒精灯时要注意“两查、两禁、一不可”,禁止向燃着的酒精灯内添加酒精灯,图中所示操作错误。
C、向试管中装块状固体药品时,先将试管横放,用镊子把块状固体放在试管口,再慢慢将试管竖立起来,图中所示操作错误。
D、用pH试纸测定溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,把试纸显示的颜色与标准比色卡对比来确定pH.不能用水湿润pH试纸,溶液显酸性,则稀释了待测溶液,使溶液的酸性减弱,测定结果偏大,图中所示操作错误。
故选:A。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
3.能使无色酚酞试液变红色的溶液是( )
A.氯化钠溶液
B.盐酸
C.氯化铵溶液
D.氢氧化钠溶液
【分析】根据已有的酚酞遇碱性溶液变红的知识进行分析解答即可.
【解答】解:A、氯化钠溶液呈中性,不能使酚酞试液变色,错误;
B、盐酸呈酸性,不能使酚酞试液变色,错误;
C、氯化铵溶液呈中性,不能使酚酞试液变色,错误;
D、氢氧化钠溶液呈碱性,能使酚酞试液变色,正确;
故选:D。
【点评】本题考查的是溶液的酸碱性与指示剂变色的知识,完成此题,可以依据已有的知识进行.
4.下列能使紫色石蕊溶液变红色的物质是( )
A.盐酸
B.氢氧化钠
C.石灰水
D.氨水
【分析】紫色石蕊溶液遇酸性溶液变红,遇中性溶液不变色,遇碱性溶液变蓝,进行分析判断。
【解答】解:A、盐酸显酸性,能使紫色石蕊溶液变红色,故选项正确。
B、氢氧化钠显碱性,能使紫色石蕊溶液变蓝色,故选项错误。
C、石灰水显碱性,能使紫色石蕊溶液变蓝色,故选项错误。
D、氨水显碱性,能使紫色石蕊溶液变蓝色,故选项错误。
故选:A。
【点评】本题难度不大,掌握紫色石蕊溶液遇酸碱性溶液的变色情况、常见物质的酸碱性是正确解答本题的关键。
5.下列实验现象描述正确的是( )
A.硬水中滴加肥皂水,产生大量泡沫
B.铁丝在氧气中燃烧,火星四射
C.打开浓盐酸瓶盖,瓶口产生大量白烟
D.镁条在空气中燃烧,生成白色氧化镁
【分析】A、根据硬水的检验方法,进行分析判断。
B、根据铁丝在氧气中燃烧的现象进行分析判断.
C、根据浓盐酸具有挥发性,进行分析判断。
D、根据镁条在空气中燃烧的现象,进行分析判断。
【解答】解:A、硬水中滴加肥皂水,产生较少的泡沫,故选项说法错误。
B、铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故选项说法正确。
C、浓盐酸具有挥发性,打开装有浓盐酸试剂瓶的瓶塞,从浓盐酸中挥发出来的氯化氢气体与空气中的水蒸气接触形成盐酸小液滴,瓶口上方有白雾产生,故选项说法错误。
D、镁条在空气中燃烧,生成白色氧化镁是实验结论而不是实验现象,故选项说法错误。
故选:B。
【点评】本题难度不大,掌握浓盐酸具有挥发性、常见物质燃烧的现象等即可正确解答,在描述实验现象时,需要注意烟和雾的区别、实验结论和实验现象的区别。
6.下列关于实验现象的描述,正确的是( )
A.固体硝酸铵溶于水,溶液温度降低
B.硫在空气中燃烧,产生有刺激性气味二氧化硫气体
C.打开盛浓盐酸的试剂瓶瓶盖,瓶口出现白烟
D.木炭在氧气中燃烧生成黑色固体
【分析】A、根据硝酸铵溶于水吸热,进行分析判断。
B、根据硫在空气中燃烧的现象,进行分析判断。
C、根据浓盐酸具有挥发性,进行分析判断。
D、根据木炭在氧气中燃烧的现象,进行分析判断。
【解答】解:A、硝酸铵溶于水吸热,溶液温度降低,故选项说法正确。
B、硫在空气中燃烧,产生有刺激性气味二氧化硫气体是实验结论而不是实验现象,故选项说法错误。
C、浓盐酸具有挥发性,打开装有浓盐酸试剂瓶的瓶塞,从浓盐酸中挥发出来的氯化氢气体与空气中的水蒸气接触形成盐酸小液滴,瓶口上方有白雾产生,故选项说法错误。
D、木炭在氧气中燃烧,发出白光,生成能使澄清石灰水变浑浊的气体,故选项说法错误。
故选:A。
【点评】本题难度不大,掌握浓盐酸具有挥发性、硝酸铵溶于水吸热、常见物质燃烧的现象等即可正确解答,在描述实验现象时,需要注意烟和雾的区别、实验结论和实验现象的区别。
7.稀硫酸中能使紫色石蕊试液变红色的微粒是( )
A.硫酸分子
B.氢离子
C.硫酸根离子
D.水分子
【分析】根据酸的化学性质,进行分析判断。
【解答】解:酸是指在电离时产生的阳离子全部是氢离子的化合物,稀硫酸中能使紫色石蕊试液变红色的微粒是氢离子。
故选:B。
【点评】本题难度不大,掌握酸的化学性质、酸具有相似化学性质的原因是正确解答本题的关键。
8.如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同。下列分析正确的是( )
A.反应①和⑤中溶液都会变蓝
B.图中只生成盐和水的反应有③④⑤
C.图中②和④两个反应可能有相同的现象
D.如果该图用来体现酸的通性,X可以是AgNO3溶液
【分析】A、稀盐酸显酸性,能使石蕊溶液变红色;
B、硝酸银和盐酸反应生成氯化银沉淀和硝酸;
C、镁和盐酸反应生成氯化镁和氢气,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
D、盐酸能和硝酸银反应生成白色沉淀氯化银和硝酸。
【解答】解:A、稀盐酸显酸性,能使石蕊溶液变红色,该选项说法不正确;
B、如果X是硝酸银,则硝酸银和盐酸反应生成氯化银沉淀和硝酸,不能生成水,该选项说法不正确;
C、镁和盐酸反应生成氯化镁和氢气,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,实验现象都是固体溶解,产生气泡,该选项说法正确;
D、AgNO3溶液与盐酸反应体现的是盐酸中氯离子的性质,而不是酸电离的氢离子的性质,所以AgNO3溶液不能体现酸的通性,该选项说法不正确。
故选:C。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。
9.以下说法不正确的是( )
A.熟石灰可用来做建筑材料以及中和酸性土壤
B.用水灭火的原理是降低了可燃物的着火点
C.用C、H2、CO都可以将CuO还原成Cu
D.燃烧和缓慢氧化都是放热反应
【分析】A、根据熟石灰的性质解答;
B、根据水灭火的原理解答;
C、根据这三种物质的性质解答;
D、根据氧化反应的特点解答.
【解答】解:A、熟石灰能与二氧化碳反应生成坚硬额块状固体碳酸钙,可以用作建筑材料,氢氧化钙具有碱性,能与酸性物质反应,可以用于改良酸性土壤,正确;
B、用水灭火的原理是降低温度到可燃物的着火点以下,不是降低了着火点,错误;
C、碳、氢气和一氧化碳都具有还原性,可以用于还原氧化铜,正确;
D、燃烧和缓慢氧化都有热量放出,正确;
故选:B。
【点评】本题考查的是常见的物质的性质以及化学反应中能量的变化,完成此题,可以依据已有的知识进行.
10.下列不是NaOH俗称的是( )
A.烧碱
B.火碱
C.纯碱
D.苛性钠
【分析】根据所学知识可以知道,氢氧化钠俗称烧碱、火碱、苛性钠。
【解答】解:氢氧化钠俗称烧碱、火碱、苛性钠,而纯碱是碳酸钠的俗称;
故选:C。
【点评】本题考查了氢氧化钠的俗称,完成此题,可以依据已有的知识进行。要求同学们在平时的学习中加强基础知识的储备。
11.小金完成了图示实验①②③,下列判断正确的是( )
A.实验①中石灰水有剩余
B.实验②中有气泡产生
C.实验③中没有明显现象
D.实验③所得溶液一定不呈碱性
【分析】A.依据盐酸与石灰水的实验现象分析;
B.依据碳酸钠与石灰水反应原理分析;
C.依据实验①和②的生成物分析,再依据实验③的现象分析;
D.依据实验③的现象分析。
【解答】解:A.实验①反应后试管中一定含有氯化钙,可能含有HCl或Ca(OH)2,实验②反应后的试管中一定含有CaCO3和NaOH,可能含有Na2CO3,或Ca(OH)2,将实验①②反应后的物质混合,最终得无色溶液,则说明实验①反应后试管中一定含有CaCl2和HCl,则实验①中石灰水无剩余,故A错误;
B.碳酸钠与石灰水反应生成白色碳酸钙沉淀和氢氧化钠,则实验②的实验现象为产生白色沉淀,故B错误;
C.综合分析实验①②③可知,实验①中一定是盐酸有剩余,则实验①反应后盐酸与实验②中碳酸钙反应生成CaCl2、水和二氧化碳,所以实验③的现象是固体溶解,有气泡产生,故C错误;
D.①反应后试管中HCl,先与②反应后的NaOH(或NaOH和Ca(OH)2)反应,再与CaCO3反应,最终得无色溶液,则实验③所得溶液一定不呈碱性,故D正确;
故选:D。
【点评】此题主要考查常见物质的性质,主要利用实验图示及物质的性质来分析和解决有关问题,结合各方面的条件得出正确结论。
12.蒸馏水和澄清石灰水长期敞口放置,它们的pH值会( )
A.前者不变
后者变大
B.前者变小
后者变大
C.两者都变小
D.两者都变大
【分析】二氧化碳能够溶于水,和水反应能生成碳酸;石灰水能够吸收空气中的二氧化碳,二氧化碳和氢氧化钙反应能生成碳酸钙和水.
【解答】解:蒸馏水显中性,pH等于7,二氧化碳溶于水后生成的碳酸显酸性,溶液的pH减小;
石灰水显碱性,pH大于7,吸收二氧化碳后,二氧化碳和氢氧化钙反应生成碳酸钙和水,溶液的碱性减弱,pH减小。
故选:C。
【点评】解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论.
13.下列生活经验没有应用酸碱反应原理的是( )
A.用熟石灰改良酸性土壤
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸
C.用氢氧化铝治疗胃酸过多
D.用生石灰作干燥剂
【分析】中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,据此进行分析判断。
【解答】解:A、用熟石灰改良酸性土壤,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,应用了酸碱反应原理,故选项错误.
B、用氢氧化钠溶液洗涤石油产品中的残留硫酸,该反应的反应物是酸和碱,属于中和反应,应用了酸碱反应原理,故选项错误.
C、用氢氧化铝治疗胃酸过多,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,应用了酸碱反应原理,故选项错误.
D、用生石灰作干燥剂,该反应的反应物是金属氧化物和水,不是酸与碱的反应,不属于中和反应,没有应用酸碱反应原理,故选项正确.
故选:D。
【点评】本题难度不大,掌握中和反应的特征(反应物是酸和碱,生成物是盐和水)是正确解答此类题的关键。
14.小明同学在复习阶段在笔记本上对化学知识进行了归纳整理:
①用广泛pH试纸测得某地下水的pH为5.2
②粗盐提纯时需把蒸发皿中的水蒸干才能停止加热
③煤燃烧生成的有害气体二氧化硫溶于雨水会形成酸雨
④配制6%的氯化钠溶液,量取水时,仰视量筒刻度使所配氯化钠溶液的质量分数偏低
⑤氢氧化铝能治疗胃酸过多,所以氢氧化钠也可以治疗胃酸过多
⑥能使无色酚酞溶液变红的一定是碱溶液
⑦生成盐和水的反应一定是中和反应。
其中正确的个数是( )
A.2个
B.3个
C.4个
D.5个
【分析】①pH试纸上的标准比色卡上的数字只有整数,即使用pH试纸所测得的溶液酸碱度为整数。
②根据蒸发操作中停止加热的时机,进行分析判断。
③根据二氧化硫对环境的影响,进行分析判断。
④用量筒量取水时,仰视液面,读数比实际液体体积小,进行分析判断。
⑤根据氢氧化钠具有腐蚀性,进行分析判断。
⑥根据显碱性的不一定是碱溶液,进行分析判断。
⑦中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,进行分析判断。
【解答】解:①由于标准比色卡上的数字只有整数,用广泛pH试纸测得某地下水的pH不可能精确为5.2,故说法错误。
②蒸发时,待蒸发皿中出现较多固体时,应停止加热,利用余热将剩余液体蒸干,故说法错误。
③煤燃烧生成的有害气体二氧化硫溶于雨水,会形成酸雨,故说法正确。
④配制6%的氯化钠溶液,量取水时,仰视量筒刻度,读数比实际液体体积小,会造成实际量取的水的体积偏大,使所配氯化钠溶液的质量分数偏低,故说法正确。
⑤氢氧化铝能治疗胃酸过多,氢氧化钠具有腐蚀性,不能用于治疗胃酸过多,故说法错误。
⑥能使无色酚酞溶液变红的不一定是碱溶液,也可能是碳酸钠等盐溶液,故说法错误。
⑦中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故说法错误。
故正确的个数是2个。
故选:A。
【点评】本题难度不大,掌握中和反应的特征、氢氧化钠具有腐蚀性、显碱性的不一定是碱溶液等是正确解答本题的关键。
15.如图是生活中常见洗涤用品的pH,显酸性的是( )
A.洁厕灵
B.消毒液
C.肥皂水
D.炉具清洁剂
【分析】当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性,且pH越大,碱性越强。据此分析判断即可。
【解答】解:A、洁厕灵pH为1~2,pH小于7,显酸性,故正确;
B、消毒液pH为8~9,pH大于7,显碱性,故错误;
C、肥皂水pH为9~11,pH大于7,显碱性,故错误;
D、炉具清洁剂pH为12~13,pH大于7,显碱性,故错误;
故选:A。
【点评】本题难度不大,掌握溶液的酸碱性和溶液pH大小之间的关系是顺利解题的关键。
16.如图是生活中一些物质的pH,下列说法中不正确的是( )
A.蚊虫叮咬可涂抹牙膏或肥皂水
B.肥皂水能使紫色石蕊溶液变红
C.胃酸过多的人适宜多喝玉米粥
D.西瓜汁的酸性比苹果汁的酸性弱
【分析】当溶液的pH等于7时,呈中性。当溶液的pH大于7时,呈碱性。当溶液的pH小于7时,呈酸性。当溶液的pH<7时,随着pH的减小酸性增强。当溶液的pH>7时,随着pH的增大碱性增强。石蕊试液遇酸性溶液变红色,遇碱性溶液变蓝色,遇中性溶液不变色。
【解答】解:A.蚊虫的毒液显酸性,牙膏和肥皂水的pH大于7,显碱性,所以蚊虫叮咬可涂抹牙膏或肥皂水,选项说法正确;
B.肥皂水的pH大于7,显碱性,能使紫色石蕊溶液变蓝色,选项说法错误;
C.玉米粥显弱碱性,所以胃酸过多的人适宜多喝玉米粥,选项说法正确;
D.西瓜汁的pH大于苹果汁的pH,所以西瓜汁的酸性比苹果汁的酸性弱,选项说法正确。
故选:B。
【点评】解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论。
17.下列物质呈酸性的是( )
A.食醋
B.肥皂水
C.石灰水
D.浓氨水
【分析】根据常见物质的酸碱性,进行分析判断。
【解答】解:A、食醋中含有醋酸,显酸性,故选项正确。
B、肥皂水显碱性,故选项错误。
C、石灰水是氢氧化钙的水溶液,显碱性,故选项错误。
D、浓氨水属于碱溶液,显碱性,故选项错误。
故选:A。
【点评】本题难度不大,了解常见化学物质的酸碱性是正确解答本题的关键。
18.某同学用月季花自制酸碱指示剂,并用于检验白醋的酸碱性,部分操作如下,其中错误的是( )
A.研磨花瓣
B.浸取色素
C.取用白醋
D.检验白醋
【分析】A、根据研磨的方法,进行分析判断。
B、根据浸取色素的方法,进行分析判断。
C、根据向试管中倾倒液体药品的方法进行分析判断。
D、根据使用胶头滴管滴加少量液体的方法进行分析判断。
【解答】解:A、研磨花瓣,可在研钵中进行,图中所示操作正确。
B、将研磨后的花瓣放入烧杯中,加入水浸泡,可用玻璃棒进行搅拌,图中所示操作正确。
C、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨试管口,图中所示操作正确。
D、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误。
故选:D。
【点评】本题难度不大,熟悉检验白醋的酸碱性的实验步骤、各操作的注意事项是解答本题的关键。
19.下列叙述正确的是( )
A.正常胃液的pH范围是0.5﹣1.9
B.酸有相似的化学性质,是因为不同的酸中都含氢离子
C.浓盐酸和浓硫酸敞口放置在空气中,一段时间后都变稀
D.饱和溶液一定比它的不饱和溶液浓
【分析】A.根据胃液的pH来分析;
B.根据酸具有通性的原因来分析;
C.根据浓盐酸的挥发性以及浓硫酸的吸水性来分析;
D.根据溶液的浓度大小来分析。
【解答】解:A.正常胃液的pH范围:0.9~1.5,故错误;
B.酸有相似的化学性质,是因为不同的酸中的阳离子都全部是氢离子,故错误;
C.浓盐酸具有挥发性,溶质减少,溶质质量分数减小,浓硫酸具有吸水性,溶剂增多,溶质质量分数减小,故正确;
D.因为不知道温度,因此无法判断饱和溶液是否比它的不饱和溶液浓,故错误。
故选:C。
【点评】本题考查的知识点较多,掌握胃酸的范围、酸具有共性的原因、浓盐酸与浓硫酸的性质、溶液浓度的比较等,难度不大。
20.“关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A.扑灭因电线老化短路引起的失火,应在断电后使用干粉灭火器
B.用铁锅炒菜可以为人体补充铁元素,使用铁锅后应保持洁净、干燥
C.去除餐具上的油污,可利用洗涤剂、炉具清洁剂等碱性物质
D.健康人的体液必须维持在一定的酸碱度范围内,如血浆的PH在7.35?7.45
【分析】A、根据灭火的原理进行解答;
B、根据铁锅后应保持洁净、干燥可以防止铁生锈进行解答;
C、根据炉具清洁剂中含有氢氧化钠,氢氧化钠具有强烈的腐蚀性进行解答;
D、根据健康人的体液必须维持在一定的酸碱度范围内进行解答。
【解答】解:A、扑灭因电线老化短路引起的失火,应在断电后使用干粉灭火器,故A正确;
B、用铁锅炒菜可以为人体补充铁元素,使用铁锅后应保持洁净、干燥可以防止铁生锈,故B正确;
C、炉具清洁剂中含有氢氧化钠,氢氧化钠具有强烈的腐蚀性,不能用于餐具去除餐具上的油污,故C错误;
D、健康人的体液必须维持在一定的酸碱度范围内,如血浆的pH在7.35?7.45,故D正确。
故选:C。
【点评】本题难度不大,了解化学元素与人体健康的关系、灭火的原理等是正确解答本题的关键。
第2页(共3页)
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
