第三单元课题2原子的构成同步练习(二)(含解析)-2021~2022学年八年级化学人教版五四制全一册
文档属性
| 名称 | 第三单元课题2原子的构成同步练习(二)(含解析)-2021~2022学年八年级化学人教版五四制全一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 110.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-11 00:00:00 | ||
图片预览




文档简介
课题二原子的构成(二)第三单元物质构成的奥秘2021~2022学年八年级化学同步练习(人教五四版)
一.选择题(共15小题)
1.如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构。根据他的实验可知下列对原子结构的认识不正确的是( )
A.原子内部有一个带正电的原子核
B.卢瑟福提出原子核式模型结构是一个得出结论的过程
C.α粒子可能是某原子的原子核
D.原子内部有很大的空间
2.第118号元素名为oganesson,元素符号为Og,源于俄罗斯核物理学家尤里?奥加涅相,已知该元素原子的相对原子质量为293,核电荷数为118,其核外电子数为( )
A.411
B.293
C.175
D.118
3.中国新一代人造“小太阳”﹣﹣可控核聚变发电成功。在核聚变的过程中,导致原子种类发生变化的粒子是( )
A.电子
B.中子
C.质子
D.离子
4.磁冰箱的工作效率比普通冰箱高30%以上,生产磁冰箱所用的材料中含稀土元素钆(Gd),钆元素的某种原子的相对原子质量为157,核电荷数为64,中子数为93,则钆原子的核外电子数为( )
A.64
B.93
C.157
D.221
5.疫情期间,同学们由于上网课用眼增多,容易引发近视。科学家通过研究发现青少年近视还可能与体内缺少微量元素铬有关。铬原子的相对原子质量是52,核电荷数是24,则铬原子的核外电子数为( )
A.24
B.28
C.52
D.76
6.2020年12月初,考古发掘队在三星堆遗址5号祭祀坑中出土了举世绝美的黄金面具。已知金(Au)原子的相对原子质量是197,质子数是79,以下说法正确的是( )
A.金(Au)属于非金属元素
B.该原子的核电荷数是79
C.该原子的核外有118个电子
D.该原子的核内有79个中子
7.我国第一艘自主建造的航母“山东舰”在建造时用到了大量钛合金,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为( )
A.22
B.26
C.48
D.70
8.2021年4月,日本政府计划将核废水排入海里,其中含有大量的氚。氚一旦进入人体可能从人体内部对人造成辐射损害,如果人类持续暴露在氚的辐射下,可能会导致细脑死亡,DNA遗传损伤。下列说法正确的是( )
A.氚原子与氢原子的最外层电子数相同
B.氚原子与氢原子都有中子,只是数目不同
C.氚与氢元素不属于同种元素
D.氚原子与氢原子相对原子质量相同
9.碳﹣14在考古学中可用以测定生物死亡年代。其原子核中含有6个质子和8个中子,则碳﹣14原子的核外电子数是( )
A.6
B.8
C.14
D.12
10.核泄漏的放射性物质中,存在原子序数是53,相对原子质量为131的元素碘。碘的质子数为( )
A.53
B.131
C.184
D.78
11.科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法不正确的是( )
A.在元素周期表中排在氢的前面
B.由于没有质子,被称为“零号元素”
C.质量大约是一个氢分子质量的2倍
D.不显电性
12.丹麦物理学家阿格?玻尔与莫特森及雷恩沃特共同提出了关于原子核的集体模型而共同获得了1975年诺贝尔物理学奖。关于原子核的下列叙述中正确的是( )
①原子的质量主要集中在原子核上
②原子核居于原子中心,带正电,所占体积很小
③构成原子核的质子、中子是不能再分的粒子
④原子核的核电荷数等于核内中子数
⑤所有的原子都是由质子、中子和电子构成的
⑥原子核具有很高的密度
A.①②⑤
B.①②⑥
C.③④⑤
D.③⑤⑥
13.原子是化学变化中的最小粒子。下列对原子的认识正确的是( )
A.汤姆森通过实验发现了原子核很小
B.电子质量很小且带正电荷
C.多电子原子中,电子具有的能量和运动速率几乎完全相同
D.电子在原子里有“广阔”的运动空间
14.某元素原子核内有174个中子,相对原子质量为291,则该元素的中子数与电子数之差( )
A.50
B.61
C.72
D.57
15.2021年3月,三星堆遗址又新出土重要文物500多件,科学家使用碳14年代检测印证了三星堆遗址属于商代晚期,碳14原子的原子核内含有6个质子和8个中子,则其原子最外层电子数为( )
A.4
B.6
C.8
D.14
二.填空题(共5小题)
16.近日,日本政府宣布将福岛核废水排放入海,引发全世界关注。核废水中含有氚、锶、铯等放射性核素。其中氚被称作超重氢,它的相对原子质量为3,核内质子数为1,则它原子核内的中子数为
。
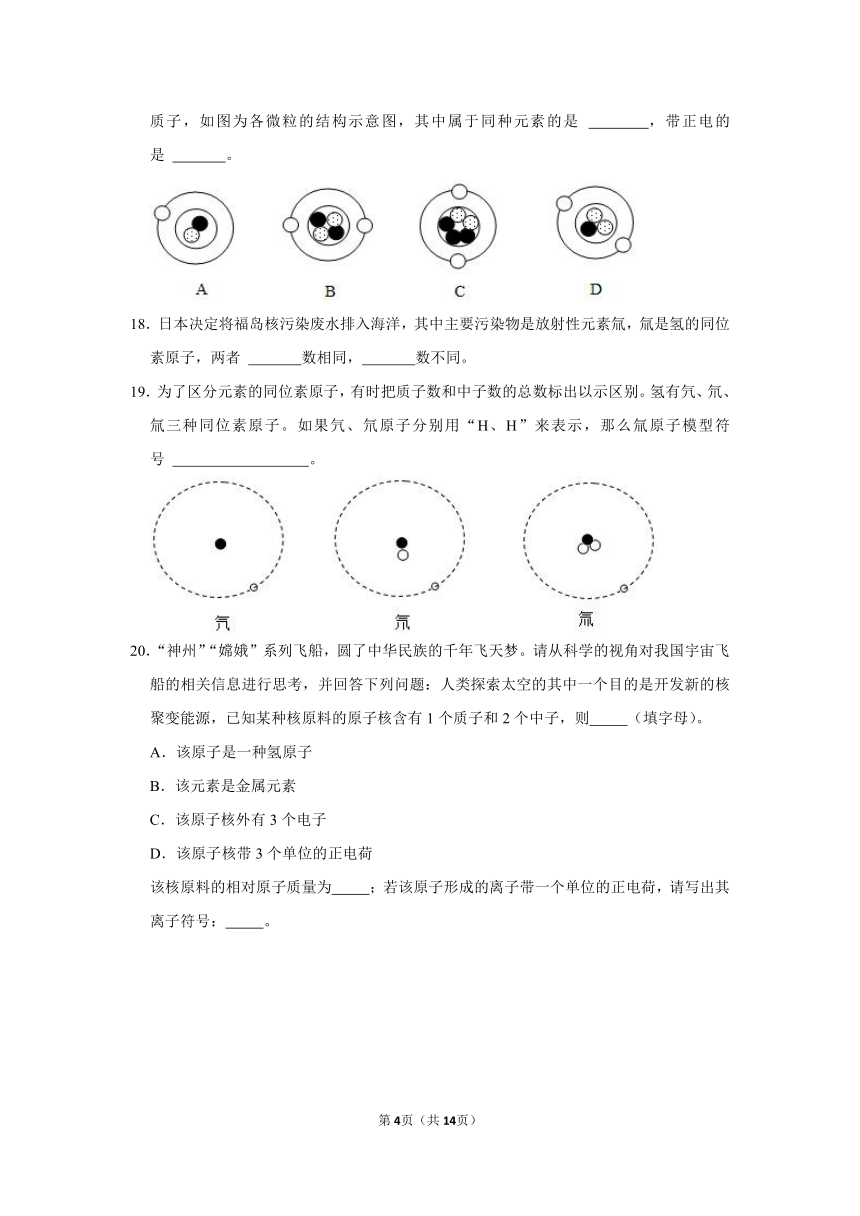
17.原子由质子、中子、电子等粒子构成,若以“〇”“”“”分别代表电子、中子、质子,如图为各微粒的结构示意图,其中属于同种元素的是
,带正电的是
。
18.日本决定将福岛核污染废水排入海洋,其中主要污染物是放射性元素氚,氚是氢的同位素原子,两者
数相同,
数不同。
19.为了区分元素的同位素原子,有时把质子数和中子数的总数标出以示区别。氢有氕、氘、氚三种同位素原子。如果氕、氘原子分别用“H、H”来表示,那么氚原子模型符号
。
20.“神州”“嫦娥”系列飞船,圆了中华民族的千年飞天梦。请从科学的视角对我国宇宙飞船的相关信息进行思考,并回答下列问题:人类探索太空的其中一个目的是开发新的核聚变能源,已知某种核原料的原子核含有1个质子和2个中子,则
(填字母)。
A.该原子是一种氢原子
B.该元素是金属元素
C.该原子核外有3个电子
D.该原子核带3个单位的正电荷
该核原料的相对原子质量为
;若该原子形成的离子带一个单位的正电荷,请写出其离子符号:
。
课题二原子的构成(二)第三单元物质构成的奥秘2021~2022学年八年级化学同步练习(人教五四版)
参考答案与试题解析
一.选择题(共15小题)
1.如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构。根据他的实验可知下列对原子结构的认识不正确的是( )
A.原子内部有一个带正电的原子核
B.卢瑟福提出原子核式模型结构是一个得出结论的过程
C.α粒子可能是某原子的原子核
D.原子内部有很大的空间
【分析】根据(1)由图甲用a粒子轰击原子而产生散射的实验,大多数α粒子能穿透原子而不改变原来的运动方向;说明原子中有一个很大的空间,原子不是实心球体;
(2)一小部分α粒子改变了原来的运动方向;说明原子核内有带正电的微粒;
(3)有极少部分α粒子被弹了回来,说明原子核体积很小,质量大;进行分析解答本题。
【解答】解:根据图甲用a粒子轰击原子而产生散射的实验,可知大多数α粒子能穿透原子而不改变原来的运动方向;说明原子中有一个很大的空间,原子不是实心球体;
一小部分α粒子改变了原来的运动方向;说明原子核内有带正电的微粒;
有极少部分α粒子被弹了回来,说明原子核体积很小,质量大;
由此可知:
A、原子内部有一个带正电的原子核,故A正确;
B、卢瑟福提出原子核式模型结构是一个提出猜想的过程,故B错误。
C、α粒子带正电荷,且质量较大,所以α粒子可能是某原子的原子核,故C正确;
D、因为大多数α粒子能穿透原子而不改变原来的运动方向,说明原子内部有很大的空间,故D正确。
故选:B。
【点评】此题主要考查学生对于原子的理解和掌握,属于基础性问题。
2.第118号元素名为oganesson,元素符号为Og,源于俄罗斯核物理学家尤里?奥加涅相,已知该元素原子的相对原子质量为293,核电荷数为118,其核外电子数为( )
A.411
B.293
C.175
D.118
【分析】根据原子中:核电荷数=质子数=电子数,相对原子质量=质子数+中子数,进行分析解答.
【解答】解:因为在原子中:核电荷数=质子数=电子数,由题意该原子的核电荷数为118,故其核外电子数均为118。
故选:D。
【点评】掌握原子中的两个等量关系:核电荷数=质子数=电子数、相对原子质量=质子数+中子数,并能够熟练的应用.
3.中国新一代人造“小太阳”﹣﹣可控核聚变发电成功。在核聚变的过程中,导致原子种类发生变化的粒子是( )
A.电子
B.中子
C.质子
D.离子
【分析】根据决定原子种类的核内质子数,进行分析判断。
【解答】解:决定原子种类的核内质子数,不同种的原子核内质子数不同,则在核聚变的过程中,导致原子种类发生变化的粒子是质子。
故选:C。
【点评】本题难度不大,明确决定原子种类的核内质子数是正确解答本题的关键。
4.磁冰箱的工作效率比普通冰箱高30%以上,生产磁冰箱所用的材料中含稀土元素钆(Gd),钆元素的某种原子的相对原子质量为157,核电荷数为64,中子数为93,则钆原子的核外电子数为( )
A.64
B.93
C.157
D.221
【分析】根据原子中核电荷数=核内质子数=核外电子数,结合题意进行分析解答。
【解答】解:因为原子中核电荷数=核内质子数=核外电子数,由题意该原子的核电荷数为64,故钆原子的核外电子数为64。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数,相对原子质量为157、中子数为93是干扰信息。
5.疫情期间,同学们由于上网课用眼增多,容易引发近视。科学家通过研究发现青少年近视还可能与体内缺少微量元素铬有关。铬原子的相对原子质量是52,核电荷数是24,则铬原子的核外电子数为( )
A.24
B.28
C.52
D.76
【分析】根据原子中核电荷数=核内质子数=核外电子数,结合题意进行分析解答。
【解答】解:因为原子中核电荷数=核内质子数=核外电子数,由题意核电荷数是24,故其核外电子数为24。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数,铬原子的相对原子质量是52是干扰信息。
6.2020年12月初,考古发掘队在三星堆遗址5号祭祀坑中出土了举世绝美的黄金面具。已知金(Au)原子的相对原子质量是197,质子数是79,以下说法正确的是( )
A.金(Au)属于非金属元素
B.该原子的核电荷数是79
C.该原子的核外有118个电子
D.该原子的核内有79个中子
【分析】根据金属元素名称一般有“钅”字旁,原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数,结合题意进行分析解答。
【解答】解:A、金属于金属元素,故选项说法错误。
B、因为原子中核电荷数=核内质子数=核外电子数,由题意金原子的质子数是79,故该原子的核电荷数是79,故选项说法正确。
C、因为原子中核电荷数=核内质子数=核外电子数,由题意金原子的质子数是79,该原子的核外有79个电子,故选项说法错误。
D、根据相对原子质量=质子数+中子数,由题意该原子的相对原子质量为197,则中子数=197﹣79=118,故选项说法错误。
故选:B。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数。
7.我国第一艘自主建造的航母“山东舰”在建造时用到了大量钛合金,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为( )
A.22
B.26
C.48
D.70
【分析】根据原子中核电荷数=核内质子数=核外电子数,结合题意进行分析解答。
【解答】解:因为原子中核电荷数=核内质子数=核外电子数,由题意钛原子的质子数为22,则钛原子的核外电子数为22。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数,要注意相对原子质量为48是干扰信息。
8.2021年4月,日本政府计划将核废水排入海里,其中含有大量的氚。氚一旦进入人体可能从人体内部对人造成辐射损害,如果人类持续暴露在氚的辐射下,可能会导致细脑死亡,DNA遗传损伤。下列说法正确的是( )
A.氚原子与氢原子的最外层电子数相同
B.氚原子与氢原子都有中子,只是数目不同
C.氚与氢元素不属于同种元素
D.氚原子与氢原子相对原子质量相同
【分析】根据图中氢原子和氚原子的构成,结合题意,进行分析判断。
【解答】解:A、氚原子与氢原子的最外层电子数均为1,最外层电子数相同,故选项说法正确。
B、氚原子中有中子,氢原子中没有中子,故选项说法错误。
C、氚与氢元素的核内质子数相同,属于同种元素,故选项说法错误。
D、相对原子质量=质子数+中子数,氚原子与氢原子的质子数相同,中子数不同,相对原子质量不同,故选项说法错误。
故选:A。
【点评】本题难度不大,了解图示的含义、相对原子质量=质子数+中子数、元素的特征等是正确解答本题的关键。
9.碳﹣14在考古学中可用以测定生物死亡年代。其原子核中含有6个质子和8个中子,则碳﹣14原子的核外电子数是( )
A.6
B.8
C.14
D.12
【分析】根据原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数,结合题意进行分析解答。
【解答】解:因为原子中核电荷数=核内质子数=核外电子数,由题意该原子的原子核中含有6个质子,故碳﹣14原子的核外电子数是6。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数,要注意原子核中含有8个中子是干扰信息。
10.核泄漏的放射性物质中,存在原子序数是53,相对原子质量为131的元素碘。碘的质子数为( )
A.53
B.131
C.184
D.78
【分析】根据原子中原子序数=核电荷数=核内质子数=核外电子数,结合题意进行分析解答。
【解答】解:原子中原子序数=核电荷数=核内质子数=核外电子数,由题意碘原子的原子序数是53,故碘的质子数为53。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中原子序数=核电荷数=核内质子数=核外电子数,相对原子质量为131是干扰信息。
11.科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法不正确的是( )
A.在元素周期表中排在氢的前面
B.由于没有质子,被称为“零号元素”
C.质量大约是一个氢分子质量的2倍
D.不显电性
【分析】根据题意,科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”,结合中子不带电,进行分析判断。
【解答】解:A、元素周期表是按原子序数递增的顺序排列的,由于该粒子没有质子,在现有的周期表中不可能有它的位置,故选项说法错误。
B、由于没有质子,被称为“零号元素”,故选项说法正确。
C、根据1个质子和1个中子的质量大约相等,1个质子的相对质量为1,其相对质量为,1个氢原子中含有1个质子,1个氢分子由2个氢原子构成,则质量大约是一个氢分子质量的2倍,故选项说法正确。
D、由题意,该粒子由四个中子构成,中子不带电,则该粒子不显电性,故选项说法正确。
故选:A。
【点评】本题难度不大,明确“四中子”的构成、中子不带电等是正确解答本题的关键。
12.丹麦物理学家阿格?玻尔与莫特森及雷恩沃特共同提出了关于原子核的集体模型而共同获得了1975年诺贝尔物理学奖。关于原子核的下列叙述中正确的是( )
①原子的质量主要集中在原子核上
②原子核居于原子中心,带正电,所占体积很小
③构成原子核的质子、中子是不能再分的粒子
④原子核的核电荷数等于核内中子数
⑤所有的原子都是由质子、中子和电子构成的
⑥原子核具有很高的密度
A.①②⑤
B.①②⑥
C.③④⑤
D.③⑤⑥
【分析】根据原子核的带电情况、原子核的结构来分析。
【解答】解:①原子是由原子核和电子构成的,电子的质量微乎其微,所以原子的质量主要集中在原子核上,说法正确;
②原子核居于原子中心,带正电,所占体积很小,说法正确;
③构成原子核的质子、中子并不是最小的粒子,还可以分成更小的粒子,说法错误;
④原子核的核电荷数等于核内质子数,与中子数无关,说法错误;
⑤原子是由质子、中子和电子构成的,但并不是所有的原子中都含有中子,如氢原子中没有中子,说法错误;
⑥原子核很小,但集中了原子的大部分质量,原子核具有很高的密度,说法正确。
故选:B。
【点评】本题考查的是原子结构的知识,完成此题,可以依据已有的知识进行.记住课本基础知识,对于解决此类识记性的基础题非常方便,熟悉原子的结构和微粒带电情况.
13.原子是化学变化中的最小粒子。下列对原子的认识正确的是( )
A.汤姆森通过实验发现了原子核很小
B.电子质量很小且带正电荷
C.多电子原子中,电子具有的能量和运动速率几乎完全相同
D.电子在原子里有“广阔”的运动空间
【分析】根据原子的构成、原子的发现史,进行分析判断。
【解答】解:A、汤姆森通过实验发现了电子,后来卢瑟福发现了原子核,故选项说法错误,
B、电子质量很小且带负电荷,故选项说法错误。
C、多电子原子中,电子具有的能量是不同的,能量较低的,在离核近的区域内运动,能量较高的,在离核远的区域内运动,故选项说法错误。
D、原子核的体积很小很小,电子在原子里有“广阔”的运动空间,故选项说法错误。
故选:D。
【点评】本题难度不大,了解原子的构成、发现史是正确解答本题的关键。
14.某元素原子核内有174个中子,相对原子质量为291,则该元素的中子数与电子数之差( )
A.50
B.61
C.72
D.57
【分析】根据原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数,结合题意进行分析解答。
【解答】解:因为相对原子质量=质子数+中子数,某元素原子核内有174个中子,相对原子质量为291,则质子数=291﹣174=117;原子中核电荷数=核内质子数=核外电子数,则该原子的电子数为57,则该元素的中子数与电子数之差是174﹣117=57。
故选:D。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数。
15.2021年3月,三星堆遗址又新出土重要文物500多件,科学家使用碳14年代检测印证了三星堆遗址属于商代晚期,碳14原子的原子核内含有6个质子和8个中子,则其原子最外层电子数为( )
A.4
B.6
C.8
D.14
【分析】根据在原子中,原子序数=质子数=核电荷数=核外电子数,进行解答。
【解答】解:在原子中,原子序数=质子数=核电荷数=核外电子数,碳14的原子中,原子核内含有6个质子,因此原子核外电子数为6,第一层排两个,第二次(最外层)排4个电子。
故选:A。
【点评】本体难度不大,注意:原子序数=质子数=核电荷数=核外电子数的前提条件是在原子中。
二.填空题(共5小题)
16.近日,日本政府宣布将福岛核废水排放入海,引发全世界关注。核废水中含有氚、锶、铯等放射性核素。其中氚被称作超重氢,它的相对原子质量为3,核内质子数为1,则它原子核内的中子数为
2 。
【分析】根据相对原子质量=质子数+中子数,结合题意进行分析解答。
【解答】解:由题意相对原子质量为3,核内质子数为1,根据相对原子质量=质子数+中子数,则中子数=3﹣1=2。
故答案为:
2。
【点评】本题难度不大,解题的关键是掌握并灵活运用相对原子质量=质子数+中子数。
17.原子由质子、中子、电子等粒子构成,若以“〇”“”“”分别代表电子、中子、质子,如图为各微粒的结构示意图,其中属于同种元素的是
AD ,带正电的是
C 。
【分析】根据元素是质子数(即核电荷数)相同的一类原子的总称,结合质子带正电,中子不带电,电子带负电,进行分析解答。
【解答】解:元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,AD的质子数相同,属于同种元素。
C中微粒的质子数为3,电子数为2,带1个单位的正电荷。
故答案为:
AD;C。
【点评】本题难度不大,明确同种元素的粒子是质子数相同、原子中各粒子的带电情况是正确解答本题的关键。
18.日本决定将福岛核污染废水排入海洋,其中主要污染物是放射性元素氚,氚是氢的同位素原子,两者
质子 数相同, 中子 数不同。
【分析】根据题意,氚是氢的同位素原子,结合同位素的特征,进行分析解答。
【解答】解:同位素是质子数相同,中子数不同的同种原子,氚是氢的同位素原子,两者质子数相同,中子数不同。
故答案为:
质子;中子。
【点评】本题难度不大,了解同位素的特征等是正确解答本题的关键。
19.为了区分元素的同位素原子,有时把质子数和中子数的总数标出以示区别。氢有氕、氘、氚三种同位素原子。如果氕、氘原子分别用“H、H”来表示,那么氚原子模型符号
H 。
【分析】根据氚原子属于氢元素,其原子核内有1个质子,2个中子,核外只有1个电子来分析。
【解答】解:根据题意知,氚原子属于氢元素,其原子核内有1个质子,2个中子,核外只有1个电子,所以“H”来表示氚原子模型符号。
故答案是:H。
【点评】本题主要考查了原子结构的基础知识,需要在平时加强训练即可完成。
20.“神州”“嫦娥”系列飞船,圆了中华民族的千年飞天梦。请从科学的视角对我国宇宙飞船的相关信息进行思考,并回答下列问题:人类探索太空的其中一个目的是开发新的核聚变能源,已知某种核原料的原子核含有1个质子和2个中子,则 A (填字母)。
A.该原子是一种氢原子
B.该元素是金属元素
C.该原子核外有3个电子
D.该原子核带3个单位的正电荷
该核原料的相对原子质量为 3 ;若该原子形成的离子带一个单位的正电荷,请写出其离子符号: H+ 。
【分析】由题意“已知某种核原料的原子核中含有1个质子和2个中子”,结合“相对原子质量≈质子数+中子数(近似整数值)”和“核内质子数=核外电子数=核电荷数”,根据质子数决定元素种类,推断其原子种类。
【解答】解:已知某种核原料的原子核中含有1个质子和2个中子。
A、根据质子数为1,可知该原子是一种氢原子,说法正确;
B、根据质子数为1,可知该元素为氢元素,为非金属元素,说法错误;
C、根据原子中核内质子数=核外电子数可知,该原子核外有1个电子,说法错误;
D、根据某种核原料的原子核含有1个质子,故该原子核带1个单位的正电荷,说法错误。
由于相对原子质量≈质子数+中子数,该核原料的相对原子质量为1+2=3;若该原子形成的离子带一个单位的正电荷,请写出其离子符号:H+。
故答案为:A;3;H+。
【点评】了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的;掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称。
第2页(共3页)
一.选择题(共15小题)
1.如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构。根据他的实验可知下列对原子结构的认识不正确的是( )
A.原子内部有一个带正电的原子核
B.卢瑟福提出原子核式模型结构是一个得出结论的过程
C.α粒子可能是某原子的原子核
D.原子内部有很大的空间
2.第118号元素名为oganesson,元素符号为Og,源于俄罗斯核物理学家尤里?奥加涅相,已知该元素原子的相对原子质量为293,核电荷数为118,其核外电子数为( )
A.411
B.293
C.175
D.118
3.中国新一代人造“小太阳”﹣﹣可控核聚变发电成功。在核聚变的过程中,导致原子种类发生变化的粒子是( )
A.电子
B.中子
C.质子
D.离子
4.磁冰箱的工作效率比普通冰箱高30%以上,生产磁冰箱所用的材料中含稀土元素钆(Gd),钆元素的某种原子的相对原子质量为157,核电荷数为64,中子数为93,则钆原子的核外电子数为( )
A.64
B.93
C.157
D.221
5.疫情期间,同学们由于上网课用眼增多,容易引发近视。科学家通过研究发现青少年近视还可能与体内缺少微量元素铬有关。铬原子的相对原子质量是52,核电荷数是24,则铬原子的核外电子数为( )
A.24
B.28
C.52
D.76
6.2020年12月初,考古发掘队在三星堆遗址5号祭祀坑中出土了举世绝美的黄金面具。已知金(Au)原子的相对原子质量是197,质子数是79,以下说法正确的是( )
A.金(Au)属于非金属元素
B.该原子的核电荷数是79
C.该原子的核外有118个电子
D.该原子的核内有79个中子
7.我国第一艘自主建造的航母“山东舰”在建造时用到了大量钛合金,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为( )
A.22
B.26
C.48
D.70
8.2021年4月,日本政府计划将核废水排入海里,其中含有大量的氚。氚一旦进入人体可能从人体内部对人造成辐射损害,如果人类持续暴露在氚的辐射下,可能会导致细脑死亡,DNA遗传损伤。下列说法正确的是( )
A.氚原子与氢原子的最外层电子数相同
B.氚原子与氢原子都有中子,只是数目不同
C.氚与氢元素不属于同种元素
D.氚原子与氢原子相对原子质量相同
9.碳﹣14在考古学中可用以测定生物死亡年代。其原子核中含有6个质子和8个中子,则碳﹣14原子的核外电子数是( )
A.6
B.8
C.14
D.12
10.核泄漏的放射性物质中,存在原子序数是53,相对原子质量为131的元素碘。碘的质子数为( )
A.53
B.131
C.184
D.78
11.科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法不正确的是( )
A.在元素周期表中排在氢的前面
B.由于没有质子,被称为“零号元素”
C.质量大约是一个氢分子质量的2倍
D.不显电性
12.丹麦物理学家阿格?玻尔与莫特森及雷恩沃特共同提出了关于原子核的集体模型而共同获得了1975年诺贝尔物理学奖。关于原子核的下列叙述中正确的是( )
①原子的质量主要集中在原子核上
②原子核居于原子中心,带正电,所占体积很小
③构成原子核的质子、中子是不能再分的粒子
④原子核的核电荷数等于核内中子数
⑤所有的原子都是由质子、中子和电子构成的
⑥原子核具有很高的密度
A.①②⑤
B.①②⑥
C.③④⑤
D.③⑤⑥
13.原子是化学变化中的最小粒子。下列对原子的认识正确的是( )
A.汤姆森通过实验发现了原子核很小
B.电子质量很小且带正电荷
C.多电子原子中,电子具有的能量和运动速率几乎完全相同
D.电子在原子里有“广阔”的运动空间
14.某元素原子核内有174个中子,相对原子质量为291,则该元素的中子数与电子数之差( )
A.50
B.61
C.72
D.57
15.2021年3月,三星堆遗址又新出土重要文物500多件,科学家使用碳14年代检测印证了三星堆遗址属于商代晚期,碳14原子的原子核内含有6个质子和8个中子,则其原子最外层电子数为( )
A.4
B.6
C.8
D.14
二.填空题(共5小题)
16.近日,日本政府宣布将福岛核废水排放入海,引发全世界关注。核废水中含有氚、锶、铯等放射性核素。其中氚被称作超重氢,它的相对原子质量为3,核内质子数为1,则它原子核内的中子数为
。
17.原子由质子、中子、电子等粒子构成,若以“〇”“”“”分别代表电子、中子、质子,如图为各微粒的结构示意图,其中属于同种元素的是
,带正电的是
。
18.日本决定将福岛核污染废水排入海洋,其中主要污染物是放射性元素氚,氚是氢的同位素原子,两者
数相同,
数不同。
19.为了区分元素的同位素原子,有时把质子数和中子数的总数标出以示区别。氢有氕、氘、氚三种同位素原子。如果氕、氘原子分别用“H、H”来表示,那么氚原子模型符号
。
20.“神州”“嫦娥”系列飞船,圆了中华民族的千年飞天梦。请从科学的视角对我国宇宙飞船的相关信息进行思考,并回答下列问题:人类探索太空的其中一个目的是开发新的核聚变能源,已知某种核原料的原子核含有1个质子和2个中子,则
(填字母)。
A.该原子是一种氢原子
B.该元素是金属元素
C.该原子核外有3个电子
D.该原子核带3个单位的正电荷
该核原料的相对原子质量为
;若该原子形成的离子带一个单位的正电荷,请写出其离子符号:
。
课题二原子的构成(二)第三单元物质构成的奥秘2021~2022学年八年级化学同步练习(人教五四版)
参考答案与试题解析
一.选择题(共15小题)
1.如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构。根据他的实验可知下列对原子结构的认识不正确的是( )
A.原子内部有一个带正电的原子核
B.卢瑟福提出原子核式模型结构是一个得出结论的过程
C.α粒子可能是某原子的原子核
D.原子内部有很大的空间
【分析】根据(1)由图甲用a粒子轰击原子而产生散射的实验,大多数α粒子能穿透原子而不改变原来的运动方向;说明原子中有一个很大的空间,原子不是实心球体;
(2)一小部分α粒子改变了原来的运动方向;说明原子核内有带正电的微粒;
(3)有极少部分α粒子被弹了回来,说明原子核体积很小,质量大;进行分析解答本题。
【解答】解:根据图甲用a粒子轰击原子而产生散射的实验,可知大多数α粒子能穿透原子而不改变原来的运动方向;说明原子中有一个很大的空间,原子不是实心球体;
一小部分α粒子改变了原来的运动方向;说明原子核内有带正电的微粒;
有极少部分α粒子被弹了回来,说明原子核体积很小,质量大;
由此可知:
A、原子内部有一个带正电的原子核,故A正确;
B、卢瑟福提出原子核式模型结构是一个提出猜想的过程,故B错误。
C、α粒子带正电荷,且质量较大,所以α粒子可能是某原子的原子核,故C正确;
D、因为大多数α粒子能穿透原子而不改变原来的运动方向,说明原子内部有很大的空间,故D正确。
故选:B。
【点评】此题主要考查学生对于原子的理解和掌握,属于基础性问题。
2.第118号元素名为oganesson,元素符号为Og,源于俄罗斯核物理学家尤里?奥加涅相,已知该元素原子的相对原子质量为293,核电荷数为118,其核外电子数为( )
A.411
B.293
C.175
D.118
【分析】根据原子中:核电荷数=质子数=电子数,相对原子质量=质子数+中子数,进行分析解答.
【解答】解:因为在原子中:核电荷数=质子数=电子数,由题意该原子的核电荷数为118,故其核外电子数均为118。
故选:D。
【点评】掌握原子中的两个等量关系:核电荷数=质子数=电子数、相对原子质量=质子数+中子数,并能够熟练的应用.
3.中国新一代人造“小太阳”﹣﹣可控核聚变发电成功。在核聚变的过程中,导致原子种类发生变化的粒子是( )
A.电子
B.中子
C.质子
D.离子
【分析】根据决定原子种类的核内质子数,进行分析判断。
【解答】解:决定原子种类的核内质子数,不同种的原子核内质子数不同,则在核聚变的过程中,导致原子种类发生变化的粒子是质子。
故选:C。
【点评】本题难度不大,明确决定原子种类的核内质子数是正确解答本题的关键。
4.磁冰箱的工作效率比普通冰箱高30%以上,生产磁冰箱所用的材料中含稀土元素钆(Gd),钆元素的某种原子的相对原子质量为157,核电荷数为64,中子数为93,则钆原子的核外电子数为( )
A.64
B.93
C.157
D.221
【分析】根据原子中核电荷数=核内质子数=核外电子数,结合题意进行分析解答。
【解答】解:因为原子中核电荷数=核内质子数=核外电子数,由题意该原子的核电荷数为64,故钆原子的核外电子数为64。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数,相对原子质量为157、中子数为93是干扰信息。
5.疫情期间,同学们由于上网课用眼增多,容易引发近视。科学家通过研究发现青少年近视还可能与体内缺少微量元素铬有关。铬原子的相对原子质量是52,核电荷数是24,则铬原子的核外电子数为( )
A.24
B.28
C.52
D.76
【分析】根据原子中核电荷数=核内质子数=核外电子数,结合题意进行分析解答。
【解答】解:因为原子中核电荷数=核内质子数=核外电子数,由题意核电荷数是24,故其核外电子数为24。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数,铬原子的相对原子质量是52是干扰信息。
6.2020年12月初,考古发掘队在三星堆遗址5号祭祀坑中出土了举世绝美的黄金面具。已知金(Au)原子的相对原子质量是197,质子数是79,以下说法正确的是( )
A.金(Au)属于非金属元素
B.该原子的核电荷数是79
C.该原子的核外有118个电子
D.该原子的核内有79个中子
【分析】根据金属元素名称一般有“钅”字旁,原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数,结合题意进行分析解答。
【解答】解:A、金属于金属元素,故选项说法错误。
B、因为原子中核电荷数=核内质子数=核外电子数,由题意金原子的质子数是79,故该原子的核电荷数是79,故选项说法正确。
C、因为原子中核电荷数=核内质子数=核外电子数,由题意金原子的质子数是79,该原子的核外有79个电子,故选项说法错误。
D、根据相对原子质量=质子数+中子数,由题意该原子的相对原子质量为197,则中子数=197﹣79=118,故选项说法错误。
故选:B。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数。
7.我国第一艘自主建造的航母“山东舰”在建造时用到了大量钛合金,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为( )
A.22
B.26
C.48
D.70
【分析】根据原子中核电荷数=核内质子数=核外电子数,结合题意进行分析解答。
【解答】解:因为原子中核电荷数=核内质子数=核外电子数,由题意钛原子的质子数为22,则钛原子的核外电子数为22。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数,要注意相对原子质量为48是干扰信息。
8.2021年4月,日本政府计划将核废水排入海里,其中含有大量的氚。氚一旦进入人体可能从人体内部对人造成辐射损害,如果人类持续暴露在氚的辐射下,可能会导致细脑死亡,DNA遗传损伤。下列说法正确的是( )
A.氚原子与氢原子的最外层电子数相同
B.氚原子与氢原子都有中子,只是数目不同
C.氚与氢元素不属于同种元素
D.氚原子与氢原子相对原子质量相同
【分析】根据图中氢原子和氚原子的构成,结合题意,进行分析判断。
【解答】解:A、氚原子与氢原子的最外层电子数均为1,最外层电子数相同,故选项说法正确。
B、氚原子中有中子,氢原子中没有中子,故选项说法错误。
C、氚与氢元素的核内质子数相同,属于同种元素,故选项说法错误。
D、相对原子质量=质子数+中子数,氚原子与氢原子的质子数相同,中子数不同,相对原子质量不同,故选项说法错误。
故选:A。
【点评】本题难度不大,了解图示的含义、相对原子质量=质子数+中子数、元素的特征等是正确解答本题的关键。
9.碳﹣14在考古学中可用以测定生物死亡年代。其原子核中含有6个质子和8个中子,则碳﹣14原子的核外电子数是( )
A.6
B.8
C.14
D.12
【分析】根据原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数,结合题意进行分析解答。
【解答】解:因为原子中核电荷数=核内质子数=核外电子数,由题意该原子的原子核中含有6个质子,故碳﹣14原子的核外电子数是6。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数,要注意原子核中含有8个中子是干扰信息。
10.核泄漏的放射性物质中,存在原子序数是53,相对原子质量为131的元素碘。碘的质子数为( )
A.53
B.131
C.184
D.78
【分析】根据原子中原子序数=核电荷数=核内质子数=核外电子数,结合题意进行分析解答。
【解答】解:原子中原子序数=核电荷数=核内质子数=核外电子数,由题意碘原子的原子序数是53,故碘的质子数为53。
故选:A。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中原子序数=核电荷数=核内质子数=核外电子数,相对原子质量为131是干扰信息。
11.科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法不正确的是( )
A.在元素周期表中排在氢的前面
B.由于没有质子,被称为“零号元素”
C.质量大约是一个氢分子质量的2倍
D.不显电性
【分析】根据题意,科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”,结合中子不带电,进行分析判断。
【解答】解:A、元素周期表是按原子序数递增的顺序排列的,由于该粒子没有质子,在现有的周期表中不可能有它的位置,故选项说法错误。
B、由于没有质子,被称为“零号元素”,故选项说法正确。
C、根据1个质子和1个中子的质量大约相等,1个质子的相对质量为1,其相对质量为,1个氢原子中含有1个质子,1个氢分子由2个氢原子构成,则质量大约是一个氢分子质量的2倍,故选项说法正确。
D、由题意,该粒子由四个中子构成,中子不带电,则该粒子不显电性,故选项说法正确。
故选:A。
【点评】本题难度不大,明确“四中子”的构成、中子不带电等是正确解答本题的关键。
12.丹麦物理学家阿格?玻尔与莫特森及雷恩沃特共同提出了关于原子核的集体模型而共同获得了1975年诺贝尔物理学奖。关于原子核的下列叙述中正确的是( )
①原子的质量主要集中在原子核上
②原子核居于原子中心,带正电,所占体积很小
③构成原子核的质子、中子是不能再分的粒子
④原子核的核电荷数等于核内中子数
⑤所有的原子都是由质子、中子和电子构成的
⑥原子核具有很高的密度
A.①②⑤
B.①②⑥
C.③④⑤
D.③⑤⑥
【分析】根据原子核的带电情况、原子核的结构来分析。
【解答】解:①原子是由原子核和电子构成的,电子的质量微乎其微,所以原子的质量主要集中在原子核上,说法正确;
②原子核居于原子中心,带正电,所占体积很小,说法正确;
③构成原子核的质子、中子并不是最小的粒子,还可以分成更小的粒子,说法错误;
④原子核的核电荷数等于核内质子数,与中子数无关,说法错误;
⑤原子是由质子、中子和电子构成的,但并不是所有的原子中都含有中子,如氢原子中没有中子,说法错误;
⑥原子核很小,但集中了原子的大部分质量,原子核具有很高的密度,说法正确。
故选:B。
【点评】本题考查的是原子结构的知识,完成此题,可以依据已有的知识进行.记住课本基础知识,对于解决此类识记性的基础题非常方便,熟悉原子的结构和微粒带电情况.
13.原子是化学变化中的最小粒子。下列对原子的认识正确的是( )
A.汤姆森通过实验发现了原子核很小
B.电子质量很小且带正电荷
C.多电子原子中,电子具有的能量和运动速率几乎完全相同
D.电子在原子里有“广阔”的运动空间
【分析】根据原子的构成、原子的发现史,进行分析判断。
【解答】解:A、汤姆森通过实验发现了电子,后来卢瑟福发现了原子核,故选项说法错误,
B、电子质量很小且带负电荷,故选项说法错误。
C、多电子原子中,电子具有的能量是不同的,能量较低的,在离核近的区域内运动,能量较高的,在离核远的区域内运动,故选项说法错误。
D、原子核的体积很小很小,电子在原子里有“广阔”的运动空间,故选项说法错误。
故选:D。
【点评】本题难度不大,了解原子的构成、发现史是正确解答本题的关键。
14.某元素原子核内有174个中子,相对原子质量为291,则该元素的中子数与电子数之差( )
A.50
B.61
C.72
D.57
【分析】根据原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数,结合题意进行分析解答。
【解答】解:因为相对原子质量=质子数+中子数,某元素原子核内有174个中子,相对原子质量为291,则质子数=291﹣174=117;原子中核电荷数=核内质子数=核外电子数,则该原子的电子数为57,则该元素的中子数与电子数之差是174﹣117=57。
故选:D。
【点评】本题难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数、相对原子质量=质子数+中子数。
15.2021年3月,三星堆遗址又新出土重要文物500多件,科学家使用碳14年代检测印证了三星堆遗址属于商代晚期,碳14原子的原子核内含有6个质子和8个中子,则其原子最外层电子数为( )
A.4
B.6
C.8
D.14
【分析】根据在原子中,原子序数=质子数=核电荷数=核外电子数,进行解答。
【解答】解:在原子中,原子序数=质子数=核电荷数=核外电子数,碳14的原子中,原子核内含有6个质子,因此原子核外电子数为6,第一层排两个,第二次(最外层)排4个电子。
故选:A。
【点评】本体难度不大,注意:原子序数=质子数=核电荷数=核外电子数的前提条件是在原子中。
二.填空题(共5小题)
16.近日,日本政府宣布将福岛核废水排放入海,引发全世界关注。核废水中含有氚、锶、铯等放射性核素。其中氚被称作超重氢,它的相对原子质量为3,核内质子数为1,则它原子核内的中子数为
2 。
【分析】根据相对原子质量=质子数+中子数,结合题意进行分析解答。
【解答】解:由题意相对原子质量为3,核内质子数为1,根据相对原子质量=质子数+中子数,则中子数=3﹣1=2。
故答案为:
2。
【点评】本题难度不大,解题的关键是掌握并灵活运用相对原子质量=质子数+中子数。
17.原子由质子、中子、电子等粒子构成,若以“〇”“”“”分别代表电子、中子、质子,如图为各微粒的结构示意图,其中属于同种元素的是
AD ,带正电的是
C 。
【分析】根据元素是质子数(即核电荷数)相同的一类原子的总称,结合质子带正电,中子不带电,电子带负电,进行分析解答。
【解答】解:元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,AD的质子数相同,属于同种元素。
C中微粒的质子数为3,电子数为2,带1个单位的正电荷。
故答案为:
AD;C。
【点评】本题难度不大,明确同种元素的粒子是质子数相同、原子中各粒子的带电情况是正确解答本题的关键。
18.日本决定将福岛核污染废水排入海洋,其中主要污染物是放射性元素氚,氚是氢的同位素原子,两者
质子 数相同, 中子 数不同。
【分析】根据题意,氚是氢的同位素原子,结合同位素的特征,进行分析解答。
【解答】解:同位素是质子数相同,中子数不同的同种原子,氚是氢的同位素原子,两者质子数相同,中子数不同。
故答案为:
质子;中子。
【点评】本题难度不大,了解同位素的特征等是正确解答本题的关键。
19.为了区分元素的同位素原子,有时把质子数和中子数的总数标出以示区别。氢有氕、氘、氚三种同位素原子。如果氕、氘原子分别用“H、H”来表示,那么氚原子模型符号
H 。
【分析】根据氚原子属于氢元素,其原子核内有1个质子,2个中子,核外只有1个电子来分析。
【解答】解:根据题意知,氚原子属于氢元素,其原子核内有1个质子,2个中子,核外只有1个电子,所以“H”来表示氚原子模型符号。
故答案是:H。
【点评】本题主要考查了原子结构的基础知识,需要在平时加强训练即可完成。
20.“神州”“嫦娥”系列飞船,圆了中华民族的千年飞天梦。请从科学的视角对我国宇宙飞船的相关信息进行思考,并回答下列问题:人类探索太空的其中一个目的是开发新的核聚变能源,已知某种核原料的原子核含有1个质子和2个中子,则 A (填字母)。
A.该原子是一种氢原子
B.该元素是金属元素
C.该原子核外有3个电子
D.该原子核带3个单位的正电荷
该核原料的相对原子质量为 3 ;若该原子形成的离子带一个单位的正电荷,请写出其离子符号: H+ 。
【分析】由题意“已知某种核原料的原子核中含有1个质子和2个中子”,结合“相对原子质量≈质子数+中子数(近似整数值)”和“核内质子数=核外电子数=核电荷数”,根据质子数决定元素种类,推断其原子种类。
【解答】解:已知某种核原料的原子核中含有1个质子和2个中子。
A、根据质子数为1,可知该原子是一种氢原子,说法正确;
B、根据质子数为1,可知该元素为氢元素,为非金属元素,说法错误;
C、根据原子中核内质子数=核外电子数可知,该原子核外有1个电子,说法错误;
D、根据某种核原料的原子核含有1个质子,故该原子核带1个单位的正电荷,说法错误。
由于相对原子质量≈质子数+中子数,该核原料的相对原子质量为1+2=3;若该原子形成的离子带一个单位的正电荷,请写出其离子符号:H+。
故答案为:A;3;H+。
【点评】了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的;掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称。
第2页(共3页)
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
