实验十六 粗盐中难溶性杂质的去除——初中化学实验知识归纳及同步训练汇编(含解析)
文档属性
| 名称 | 实验十六 粗盐中难溶性杂质的去除——初中化学实验知识归纳及同步训练汇编(含解析) |
|
|
| 格式 | doc | ||
| 文件大小 | 184.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-08-13 00:00:00 | ||
图片预览

文档简介
实验十六 粗盐中难溶性杂质的去除——初中化学实验汇编
*知识点归纳
实验步骤:
(1)溶解:用托盘天平称取5.0 g粗盐,用量筒量取10 mL水,用药匙将粗盐逐渐加入盛有10 ml水的烧杯中,边加边用玻璃棒搅拌,直到不再溶解为止。
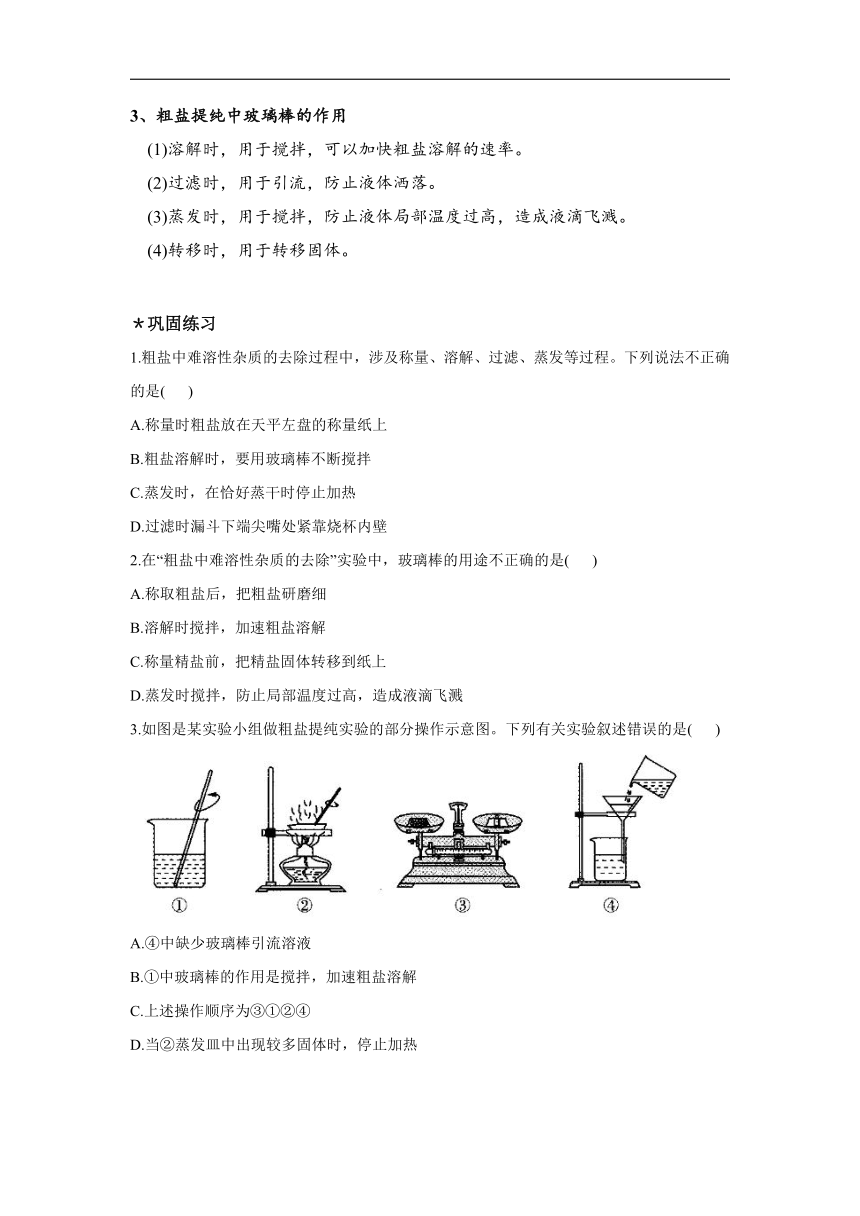
(2)过滤:过滤食盐水,观察滤液是否澄清,若滤液浑浊,需再过滤或检查装置,并找出原因。
(3)蒸发:把所得澄清滤液倒入蒸发皿,如图所示,把蒸发皿放在铁架台的铁圈上,用酒精灯加热,同时用玻璃棒不断搅拌滤液,以防液滴飞溅。待蒸发皿中出现较多固体时,停止加热。利用蒸发皿的余热使滤液蒸干。
(4)计算产率:用玻璃棒把固体转移到纸上,称量,将提纯过后的氯化钠与粗盐作比较,并计算精盐的产率。
2、注意事项
(1)待蒸发皿中出现较多固体时,停止加热,利用余热使剩余水分蒸干,不能将滤液完全蒸干再停止加热。
(2)蒸发皿是可以直接加热的仪器,蒸发时,倒入液体的体积不超过蒸发皿容积的2/3。
(3)加热时,不断用玻璃棒搅拌。
(4)热的蒸发皿不能直接放在实验台上,以免烫坏实验台,如需取下可使用坩埚钳。
3、粗盐提纯中玻璃棒的作用
(1)溶解时,用于搅拌,可以加快粗盐溶解的速率。
(2)过滤时,用于引流,防止液体洒落。
(3)蒸发时,用于搅拌,防止液体局部温度过高,造成液滴飞溅。
(4)转移时,用于转移固体。
*巩固练习
1.粗盐中难溶性杂质的去除过程中,涉及称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
2.在“粗盐中难溶性杂质的去除”实验中,玻璃棒的用途不正确的是( )
A.称取粗盐后,把粗盐研磨细
B.溶解时搅拌,加速粗盐溶解
C.称量精盐前,把精盐固体转移到纸上
D.蒸发时搅拌,防止局部温度过高,造成液滴飞溅
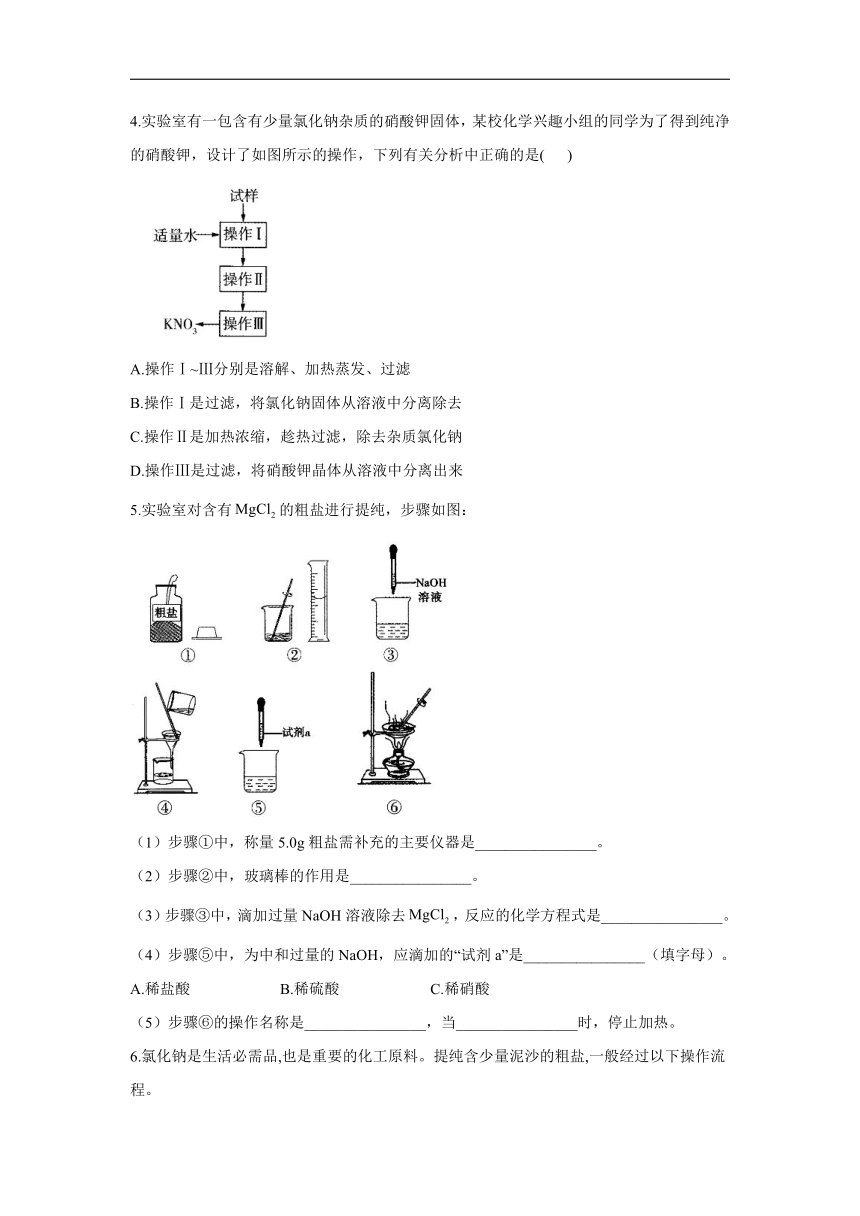
3.如图是某实验小组做粗盐提纯实验的部分操作示意图。下列有关实验叙述错误的是( )
A.④中缺少玻璃棒引流溶液
B.①中玻璃棒的作用是搅拌,加速粗盐溶解
C.上述操作顺序为③①②④
D.当②蒸发皿中出现较多固体时,停止加热
4.实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作,下列有关分析中正确的是( )
A.操作Ⅰ~Ⅲ分别是溶解、加热蒸发、过滤
B.操作Ⅰ是过滤,将氯化钠固体从溶液中分离除去
C.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
D.操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来
5.实验室对含有的粗盐进行提纯,步骤如图:
(1)步骤①中,称量5.0g粗盐需补充的主要仪器是________________。
(2)步骤②中,玻璃棒的作用是________________。
(3)步骤③中,滴加过量NaOH溶液除去,反应的化学方程式是________________。
(4)步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是________________(填字母)。
A.稀盐酸 B.稀硫酸 C.稀硝酸
(5)步骤⑥的操作名称是________________,当________________时,停止加热。
6.氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程。
(1)操作③中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是_________(填序号)。?
(2)操作④中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到的仪器是 ,该操作中玻璃棒的作用是 。
(3)实验结束后称量获得的精盐,计算发现精盐制得率较低,其可能原因是 (填序号)。?
A.食盐没有全部溶解即过滤 B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿 D.器皿上沾有的精盐没全部转移到称量纸上
(4)为了除去粗盐中的等可溶性杂质,先后加入过量的氯化钡溶液、氢氧化钠溶液、碳酸钠溶液,能否先加碳酸钠溶液后加氯化钡溶液,为什么?
。
答案以及解析
1.答案:C
解析:称量时粗盐放在天平左盘的称量纸上,故A正确;粗盐溶解时,要用玻璃棒不断搅拌,故B正确;蒸发时,待蒸发皿中出现较多固体时,应停止加热,利用余热将剩余液体蒸干,故C错误;过滤液体时,要注意“一贴、二低、三靠”的原则,过滤时漏斗下端尖嘴处紧靠烧杯内壁,故D正确。
2.答案:A
解析:称取粗盐后,把粗盐硏磨细,应用研钵和研杵进行,A错误。溶解时玻璃棒的作用是搅拌,加速粗盐溶解,B正确。称量精盐前,可用玻璃棒把精盐固体转移到纸上,C正确。蒸发时搅拌,防止因局部温度过高,造成液滴飞溅,D正确。
3.答案:C
解析:
选项 正误 分析
A √ 过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流溶液
B √ 溶解时玻璃棒的作用是搅拌,加快溶解速率
C × 粗盐的主要成分是氯化钠,粗盐提纯是通过粗盐溶解(称量,溶解粗盐,把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来),从而得到精盐的过程,蒸发应在过滤之后
D √ 蒸发时,待蒸发皿中出现较多固体时,应停止加热,利用余热将剩余液体蒸干
4.答案:D
解析:提纯含少量氯化钠杂质的硝酸钾,应采用冷却结晶法。结合流程可知,操作Ⅰ为溶解,操作Ⅱ为蒸发浓缩,冷却结晶,操作Ⅲ是过滤,故A、B、C不正确,D正确。
5.答案:(1)天平(托盘天平或电子天平均可)
(2)搅拌,加速溶解
(3)
(4)A
(5)蒸发;蒸发皿中出现较多固体
解析:(4)步骤⑤中,为了中和过量的NaOH,应该滴加稀盐酸,若滴加稀硫酸或稀硝酸会生成新杂质。
6.答案:(1)D
(2)蒸发皿、搅拌使受热均匀,防止液体飞溅
(3)ABD
(4)过量的氯化钡要用碳酸钠除去
*知识点归纳
实验步骤:
(1)溶解:用托盘天平称取5.0 g粗盐,用量筒量取10 mL水,用药匙将粗盐逐渐加入盛有10 ml水的烧杯中,边加边用玻璃棒搅拌,直到不再溶解为止。
(2)过滤:过滤食盐水,观察滤液是否澄清,若滤液浑浊,需再过滤或检查装置,并找出原因。
(3)蒸发:把所得澄清滤液倒入蒸发皿,如图所示,把蒸发皿放在铁架台的铁圈上,用酒精灯加热,同时用玻璃棒不断搅拌滤液,以防液滴飞溅。待蒸发皿中出现较多固体时,停止加热。利用蒸发皿的余热使滤液蒸干。
(4)计算产率:用玻璃棒把固体转移到纸上,称量,将提纯过后的氯化钠与粗盐作比较,并计算精盐的产率。
2、注意事项
(1)待蒸发皿中出现较多固体时,停止加热,利用余热使剩余水分蒸干,不能将滤液完全蒸干再停止加热。
(2)蒸发皿是可以直接加热的仪器,蒸发时,倒入液体的体积不超过蒸发皿容积的2/3。
(3)加热时,不断用玻璃棒搅拌。
(4)热的蒸发皿不能直接放在实验台上,以免烫坏实验台,如需取下可使用坩埚钳。
3、粗盐提纯中玻璃棒的作用
(1)溶解时,用于搅拌,可以加快粗盐溶解的速率。
(2)过滤时,用于引流,防止液体洒落。
(3)蒸发时,用于搅拌,防止液体局部温度过高,造成液滴飞溅。
(4)转移时,用于转移固体。
*巩固练习
1.粗盐中难溶性杂质的去除过程中,涉及称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
2.在“粗盐中难溶性杂质的去除”实验中,玻璃棒的用途不正确的是( )
A.称取粗盐后,把粗盐研磨细
B.溶解时搅拌,加速粗盐溶解
C.称量精盐前,把精盐固体转移到纸上
D.蒸发时搅拌,防止局部温度过高,造成液滴飞溅
3.如图是某实验小组做粗盐提纯实验的部分操作示意图。下列有关实验叙述错误的是( )
A.④中缺少玻璃棒引流溶液
B.①中玻璃棒的作用是搅拌,加速粗盐溶解
C.上述操作顺序为③①②④
D.当②蒸发皿中出现较多固体时,停止加热
4.实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作,下列有关分析中正确的是( )
A.操作Ⅰ~Ⅲ分别是溶解、加热蒸发、过滤
B.操作Ⅰ是过滤,将氯化钠固体从溶液中分离除去
C.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
D.操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来
5.实验室对含有的粗盐进行提纯,步骤如图:
(1)步骤①中,称量5.0g粗盐需补充的主要仪器是________________。
(2)步骤②中,玻璃棒的作用是________________。
(3)步骤③中,滴加过量NaOH溶液除去,反应的化学方程式是________________。
(4)步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是________________(填字母)。
A.稀盐酸 B.稀硫酸 C.稀硝酸
(5)步骤⑥的操作名称是________________,当________________时,停止加热。
6.氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程。
(1)操作③中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是_________(填序号)。?
(2)操作④中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到的仪器是 ,该操作中玻璃棒的作用是 。
(3)实验结束后称量获得的精盐,计算发现精盐制得率较低,其可能原因是 (填序号)。?
A.食盐没有全部溶解即过滤 B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿 D.器皿上沾有的精盐没全部转移到称量纸上
(4)为了除去粗盐中的等可溶性杂质,先后加入过量的氯化钡溶液、氢氧化钠溶液、碳酸钠溶液,能否先加碳酸钠溶液后加氯化钡溶液,为什么?
。
答案以及解析
1.答案:C
解析:称量时粗盐放在天平左盘的称量纸上,故A正确;粗盐溶解时,要用玻璃棒不断搅拌,故B正确;蒸发时,待蒸发皿中出现较多固体时,应停止加热,利用余热将剩余液体蒸干,故C错误;过滤液体时,要注意“一贴、二低、三靠”的原则,过滤时漏斗下端尖嘴处紧靠烧杯内壁,故D正确。
2.答案:A
解析:称取粗盐后,把粗盐硏磨细,应用研钵和研杵进行,A错误。溶解时玻璃棒的作用是搅拌,加速粗盐溶解,B正确。称量精盐前,可用玻璃棒把精盐固体转移到纸上,C正确。蒸发时搅拌,防止因局部温度过高,造成液滴飞溅,D正确。
3.答案:C
解析:
选项 正误 分析
A √ 过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流溶液
B √ 溶解时玻璃棒的作用是搅拌,加快溶解速率
C × 粗盐的主要成分是氯化钠,粗盐提纯是通过粗盐溶解(称量,溶解粗盐,把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来),从而得到精盐的过程,蒸发应在过滤之后
D √ 蒸发时,待蒸发皿中出现较多固体时,应停止加热,利用余热将剩余液体蒸干
4.答案:D
解析:提纯含少量氯化钠杂质的硝酸钾,应采用冷却结晶法。结合流程可知,操作Ⅰ为溶解,操作Ⅱ为蒸发浓缩,冷却结晶,操作Ⅲ是过滤,故A、B、C不正确,D正确。
5.答案:(1)天平(托盘天平或电子天平均可)
(2)搅拌,加速溶解
(3)
(4)A
(5)蒸发;蒸发皿中出现较多固体
解析:(4)步骤⑤中,为了中和过量的NaOH,应该滴加稀盐酸,若滴加稀硫酸或稀硝酸会生成新杂质。
6.答案:(1)D
(2)蒸发皿、搅拌使受热均匀,防止液体飞溅
(3)ABD
(4)过量的氯化钡要用碳酸钠除去
同课章节目录
