第3章 第1节 2 有机化合物的结构特点
文档属性
| 名称 | 第3章 第1节 2 有机化合物的结构特点 |

|
|
| 格式 | zip | ||
| 文件大小 | 426.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-09-19 00:00:00 | ||
图片预览







文档简介
(共34张PPT)
2
有机化合物的结构特点
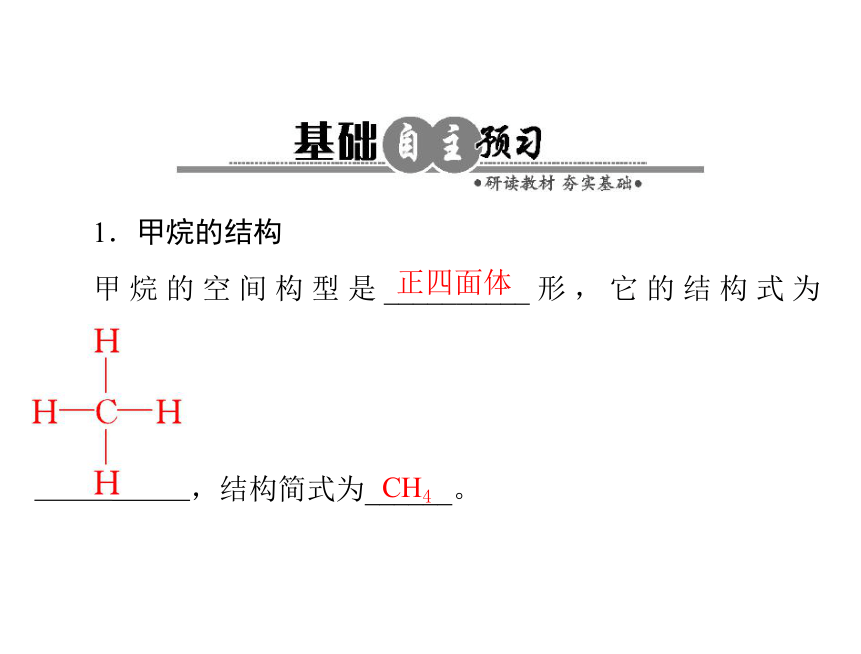
1.甲烷的结构
正四面体
甲 烷 的 空 间 构 型 是 __________ 形 , 它 的 结 构 式 为
,结构简式为______。
CH4
如何证明甲烷的结构不是平面正方形,而是正四面体形?
代物均只有 1 种。假设甲烷是平面正方形结构
,四个
氢原子的位置虽然也相同,但是相互间存在相邻和相间的关系,
则其分子里的 2 个氢原子被氯原子取代得到的 CH2Cl2 应该有 2
答案:甲烷分子中有4个等同的C—H 键,在空间可能有
两种对称分布:正四面体结构和平面正方形结构。甲烷无论是
正四面体结构还是平面正方形,其一氯代物、三氯代物和四氯
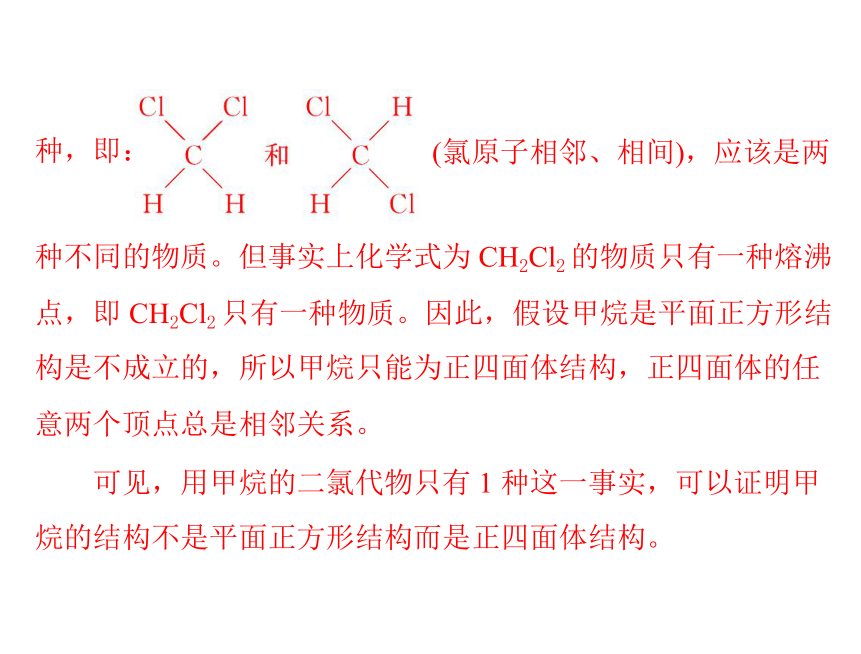
种,即:
(氯原子相邻、相间),应该是两
种不同的物质。但事实上化学式为 CH2Cl2 的物质只有一种熔沸
点,即 CH2Cl2 只有一种物质。因此,假设甲烷是平面正方形结
构是不成立的,所以甲烷只能为正四面体结构,正四面体的任
意两个顶点总是相邻关系。
可见,用甲烷的二氯代物只有 1 种这一事实,可以证明甲
烷的结构不是平面正方形结构而是正四面体结构。
2.有机化合物结构的多样性
碳
4
共价键
单
有机化合物分子里都含有____原子。由于碳原子的最外层
有___个电子,碳原子不仅可以通过_______与其他原子结合形
成分子,还可以彼此间以共价键构成_____________,再结合其
他原子形成分子;碳原子之间可以是___键,也可以是___键或
___键。这些是有机化合物结构多样性的一种表现。
3.烷烃
碳链或碳环
双
叁
C
H
烃:仅含___和___两种元素的有机物,称为___________,
也称为烃。
碳氢化合物
C—C 单键
全部
饱和
烷烃是指碳原子跟碳原子都以共价键结合成___________,
碳原子剩余的价键______跟氢原子相结合的_____烃。
4.同分异构现象和同分异构体
(1)定义
化学式
结构
化合物具有相同的_______,但具有不同的______的现象,
叫做同分异构现象。具有同分异构现象的化合物互称同分异构
体,如正丁烷与异丁烷就是丁烷的两种同分异构体,属于两种
化合物。
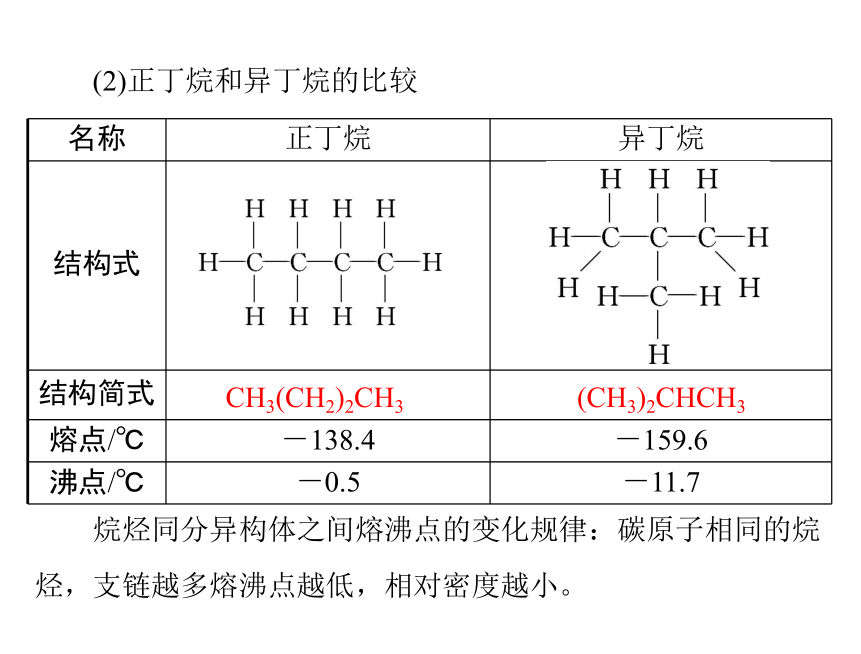
名称 正丁烷 异丁烷
结构式
结构简式
熔点/℃ -138.4 -159.6
沸点/℃ -0.5 -11.7
(2)正丁烷和异丁烷的比较
烷烃同分异构体之间熔沸点的变化规律:碳原子相同的烷
烃,支链越多熔沸点越低,相对密度越小。
(CH3)2CHCH3
CH3(CH2)2CH3
(1)一般说来,有机化合物分子中的碳原子数越多,它的同
分异构体数目就越多。例如:戊烷(C5H12)有 3 种同分异构体,
己烷(C6H14)有 5 种同分异构体。
(2)在有机化合物中,同分异构现象非常普遍,这是有机化
合物结构多样性的又一表现。
1.甲烷分子的结构
甲烷分子中,碳原子最外层上的 4 个电子分别与 4 个氢原
子上的电子形成 4 个共价键。构成正四面体结构,碳原子位于
正四面体的中心,4 个氢原子分别位于正四面体的 4 个顶点上。
表示方法如下:
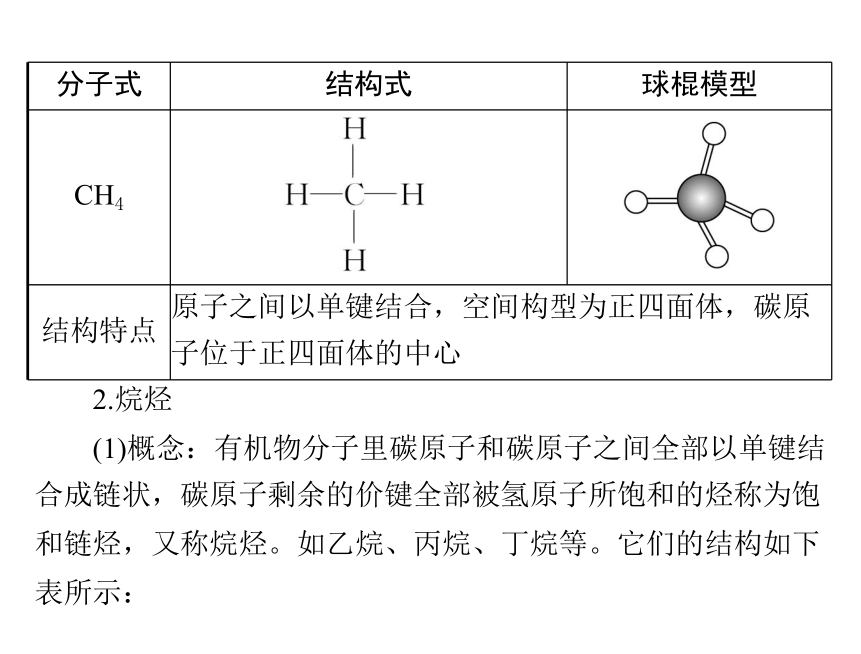
分子式 结构式 球棍模型
CH4
结构特点 原子之间以单键结合,空间构型为正四面体,碳原
子位于正四面体的中心
2.烷烃
(1)概念:有机物分子里碳原子和碳原子之间全部以单键结
合成链状,碳原子剩余的价键全部被氢原子所饱和的烃称为饱
和链烃,又称烷烃。如乙烷、丙烷、丁烷等。它们的结构如下
表所示:
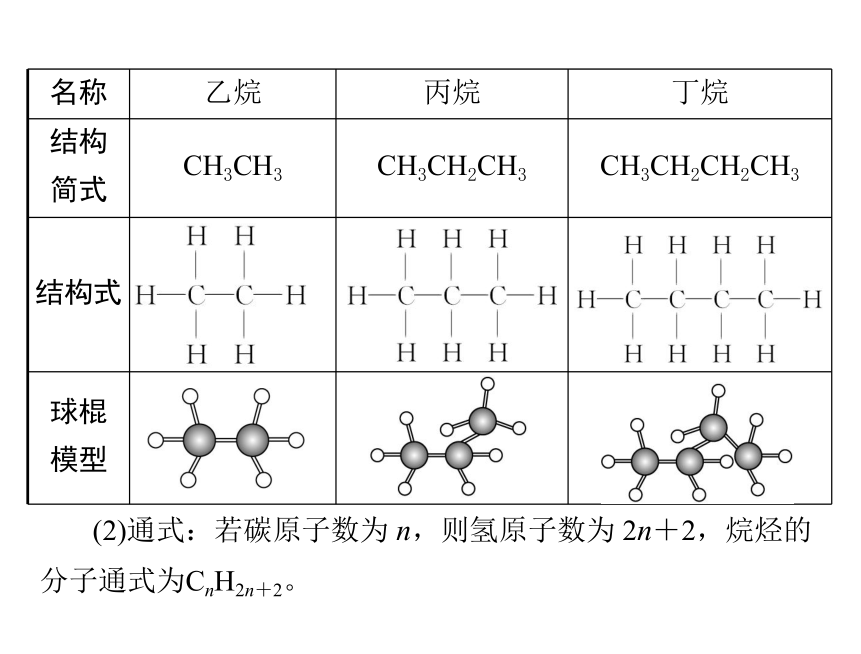
名称 乙烷 丙烷 丁烷
结构
简式 CH3CH3 CH3CH2CH3 CH3CH2CH2CH3
结构式
球棍
模型
(2)通式:若碳原子数为 n,则氢原子数为 2n+2,烷烃的
分子通式为CnH2n+2。
CnH2n+2+
(3)烷烃的性质:
①物理性质:烷烃的熔沸点都较低,密度较小,但随着分
子中碳原子数的增加,呈现出规律性的变化:状态由气态到液
态再到固态,熔沸点逐渐升高,密度逐渐增大;分子里碳原子
数小于等于 4 的烷烃,在常温常压下都是气体;烷烃不溶于水,
但易溶于有机溶剂。液态烷烃本身就是有机溶剂,如己烷。
②化学性质:烷烃的化学性质和甲烷相似,如通常不与强
酸、强碱或强氧化剂反应,都不能使酸性高锰酸钾溶液或溴水
退色;都能发生取代反应,取代反应是烷烃的特征反应;都具
有可燃性,烷烃完全燃烧的通式为
3n+1
2
O2
点燃
nCO2+(n+1)H2O
(4)烷烃的命名
①在分子内的碳原子数后加一个“烷”字,称为“某烷”。
②分子中碳原子数在十个以内时,用天干表示,即用甲、
乙、丙、丁、戊、己、庚、辛、壬、癸表示,如甲烷、丁烷等。
③分子中碳原子数在十个以上时,直接用大写数字来表示,
如十二烷、十八烷等。
④对于碳原子数相同而结构不同的烷烃,一般在烷烃名称
之前再加“正”“异”“新”等字加以区别,如正丁烷、异丁
烷等。
3.同分异构现象和同分异构体
(1)同分异构体概念的内涵有两点:一是分子式相同,二是
结构不同,二者缺一不可。分子式相同必然相对分子质量相同,
但相对分子质量相同不一定分子式相同,如CO和C2H4、C2H6O
和 CH2O2 均是相对分子质量相同,但分子式不相同。
(2)同分异构现象广泛存在于有机化合物中,不仅存在于同
类物质中,也存在于不同类物质之间,例如,CH3CH2OH 和
CH3—O—CH3(二甲醚)等。
(3)烷烃的同分异构体数目随分子中碳原子数的增多而增
多。如 CH4、CH3CH3、CH3CH2CH3 均不存在同分异构体,而
丁烷、戊烷的同分异构体的种数分别为 2 种、3 种。
(4)烷烃同分异构体的写法
烷烃的同分异构体的书写规律可概括为:主链由长到短,
支链由整到散,位置由心到边,排列对、邻、间。
以戊烷(C5H12)为例的同分异构体的写法:
①先写出最长的碳链作为主链:C—C—C—C—C—C(氢原
子及其个数省略)
②从主链的一端取下一个碳原子,依次连在主链中心对称
线一侧的碳原子上:
注意不能加在两端,否则会和前面重复,同时注意对称的
位置也会有重复。
③从主链的一端取下两个碳原子:
a.把取下的两个碳原子当作一个支链加在主链上:
b.把两个碳原子作为两个支链加在主链上:
从主链上取下的碳原子,不得多于主链上剩余的碳原子,
否则一定会重复。
例 1.下列事实中能证明甲烷分子是以碳原子为中心的正四
面体结构的是(
)。
A.CH3Cl 只代表一种物质
B.CH2Cl2 只代表一种物质
C.CHCl3 只代表一种物质
D.CCl4 只代表一种物质
答案:B
解析:对于甲烷的正四面体结构,因为其4个顶点的位置完全相同,所以它的一氯代物(CH3Cl)、二氯代物(CH2Cl2)、三氯代物(CHCl3)、四氯代物(CCl4)都只有一种。而如果甲烷是平面正方形结构,虽然4个C—H键都完全相同,但4个顶点的氢原子的位置关系却不同,可能相邻,也可能相间,所以虽然CH3Cl、CHCl3、CCl4都只有一种,但CH2Cl2却有两种,一种是两个氯原子相邻,另一种是两个氯原子相间。由CH2Cl2只有一种这一点可以判断出CH4为正四面体结构,而不是平面正方形结构。
例2.下列有关烷烃的叙述中,不正确的是(
)。
C
A.在烷烃分子中,所有的化学键都为单键
B.所有的烷烃在光照条件下都能与 Cl2 发生取代反应
C.烷烃的分子通式为 CnH2n+2,符合该通式的烃不一定是
烷烃
D.随着碳原子数的增加,烷烃的熔沸点逐渐升高
解析:烷烃中的碳碳键、碳氢键均为单键,且烷烃在光照
条件下都能与Cl2 发生取代反应,这是烷烃的结构特征和反应
特征,故 A、B 正确;由于烷烃分子的通式CnH2n+2 中的 C 原子
已达饱和,所以符合 CnH2n+2 的有机物只可能为烷烃,故 C 错
误;由于随着 C 原子数的增加,烷烃的相对分子质量增大,其
熔沸点升高,故 D 正确。
变式训练1. 下列不属于烷烃性质的是(
)。
B
A.它们燃烧时生成二氧化碳和水
B.它们都溶于水
C.它们都能跟卤素发生取代反应
D.通常情况下,它们跟酸、碱和氧化剂都不反应
烷烃的结构和甲烷相似,分子内原子间都以单键相连,结
构相似,性质也相似。
例 3.(2010 湖南师大附中高一检测)正丁烷与异丁烷互为同
分异构体的依据是(
)。
D
A.具有相似的化学性质
B.具有相同的物理性质
C.分子具有相同的空间结构
D.分子式相同,但分子内碳原子的连接方式不同
解析:分子式相同,结构不同的物质互称同分异构体,同
分异构体空间结构不同,化学性质也不一定相似,物理性质不
相同。
物质 沸点/℃
正丁烷 CH3(CH2)2CH3 -0.5
正戊烷 CH3(CH2)3CH3 36.1
异戊烷
27.8
新戊烷
9.5
正己烷 CH3(CH2)4CH3 69.0
变式训练 2 在1.01×105 Pa 下,测得的某些烷烃的沸点见
下表。
据表分析,下列选项正确的是(
)。
D
A.在标准状况下,新戊烷是气体
B.在 1.01×105 Pa、20 ℃时,C5H12 都是液体
C.烷烃随碳原子数增加,沸点降低
D.C5H12 随支链增加,沸点降低
解析:新戊烷的沸点是9.5 ℃,标准状况下是液体,20 ℃
时是气体,A、B 均错误;烷烃随碳原子数的增加,沸点升高,
C 错误;C5H12的三种同分异构体中,随支链数增加,沸点降低,
D 正确。
例 4.(2010 吉林长春高一检测)已知丙烷的二氯代物有 4 种
)。
C
同分异构体,则其六氯代物的同分异构体的数目为(
A.2 种
B.3 种
C.4 种
D.5 种
解析:二氯丙烷:丙烷(C3H8)分子主链上有两个氢原子被
氯原子取代→氯原子有 4 种位置关系→二氯丙烷的同分异构体
有 4 种;六氯丙烷:全氯丙烷(C3Cl8)分子主链上有两个氯原子
被氢原子取代→氢原子有 4 种位置关系→六氯丙烷的同分异构
体有 4 种,故选 C 项。
例5.有下列几组物质:
C.红磷和白磷
B.甲烷和己烷
D.正丁烷和异丁烷
其中,①属于同分异构体的是______;②属于同位素的是
___;③属于同素异形体的是___;④属于同一种物质的是___。
D、F
A
C
E
概念即可解答。
解析:利用同位素、同素异形体、同系物及同分异构体的
1.(双选)下列分子中与甲烷分子空间构型相同的是(
)。
BD
A.CHCl3
C.CFCl3
B.CCl4
D.CF4
解析:只有甲烷的四个氢原子被同一原子取代时,产物才
是正四面体。
2 同分异构体现象是有机化学中的一种普遍现象,下列有
关同分异构体的叙述中正确的是(
)。
A
A.分子式相同而结构式不同的化合物互称同分异构体
B.组成成分相同而结构式不同的物质互称同分异构体
C.互为同分异构体的物质性质相同
D.互为同分异构体的物质物理性质相同
解析:互为同分异构体的物质必须是化合物,故B 项错误;
同分异构体的化学性质相似,物理性质不同,故C、D 项错误。
3.下列烷烃分子中进行一氯取代反应后,只能生成三种沸
点不同产物的是(
)。
D
解析:生成三种沸点不同的一氯产物,说明上述烷烃的一
氯代物只有三种同分异构体。
A.(CH3)2CHCH2CH2CH3
B.(CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2
D.(CH3)3CCH2CH3
4.(2010 山东青岛高一检测)下列说法正确的是(
)。
B
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结
合的烃一定是饱和链烃
B.分子组成符合 CnH2n+2 的烃一定是烷烃
C.正戊烷分子中所有碳原子均在一条直线上
D.新戊烷的一氯取代物有 2 种
解析:A 项符合条件的烃为饱和烃,可为烷烃,也可为环
烷烃,但分子组成符合CnH2n+2 的烃一定为烷烃,故 A 错误,
B 正确;在烷烃分子中与碳原子紧邻的四个原子构成四面体形,
所以正戊烷分子中所有碳原子呈锯齿形,而非直线形,故 C 错
误;新戊烷分子完全对称,分子中只有一种氢原子,故一氯取
代物只有一种,故 D 错误。
内容特点
本节是在学生初中已有的个别有机化合物的概念的基础
上,进一步了解有机化学的发展过程、研究范畴以及对生产、
生活、环境的重要作用。从碳的原子结构和成键方式入手,以
甲烷、乙烷、丙烷和丁烷等同系列及丁烷的同分异构现象为例,
说明有机化合物结构的多样性是导致有机物种类繁多的原因。
取代反应是烷烃的特征反应,因此甲烷的取代反应是本节的重
点内容之一。教材在实验的基础上使学生了解取代反应,然后
以球棍模型形象地说明取代反应的本质,帮助学生建立取代反
应的概念。
本节的知识框架为:
教学指要
首先以初中已有的化学知识为基础,引导学生对有机化合
物与无机化合物进行比较,然后进行本节的教学。本节内容可
以安排成两个知识模块:甲烷的结构和性质、同分异构现象。
具体建议如下:
通过“观察·思考”让学生观察实验,引导学生思考、讨论,
得出实验结论,然后引出取代反应的概念,并与无机化学中的
置换反应加以比较,进一步认识有机化合物、有机反应的特殊
性。
在有机化合物的结构特点的教学中,结合学生已有的原子
结构和共价键的知识,引导他们分析碳原子的成键特点,并以
球棍模型和比例模型形象地展示甲烷及其取代反应的各级取代
产物的立体结构。对于同分异构现象,可以从丁烷的球棍模型
入手,分析碳原子的不同连接方式,引出同分异构体的概念,
并让学生认识到:同分异构现象是有机化合物种类繁多的原因
之一。
2
有机化合物的结构特点
1.甲烷的结构
正四面体
甲 烷 的 空 间 构 型 是 __________ 形 , 它 的 结 构 式 为
,结构简式为______。
CH4
如何证明甲烷的结构不是平面正方形,而是正四面体形?
代物均只有 1 种。假设甲烷是平面正方形结构
,四个
氢原子的位置虽然也相同,但是相互间存在相邻和相间的关系,
则其分子里的 2 个氢原子被氯原子取代得到的 CH2Cl2 应该有 2
答案:甲烷分子中有4个等同的C—H 键,在空间可能有
两种对称分布:正四面体结构和平面正方形结构。甲烷无论是
正四面体结构还是平面正方形,其一氯代物、三氯代物和四氯
种,即:
(氯原子相邻、相间),应该是两
种不同的物质。但事实上化学式为 CH2Cl2 的物质只有一种熔沸
点,即 CH2Cl2 只有一种物质。因此,假设甲烷是平面正方形结
构是不成立的,所以甲烷只能为正四面体结构,正四面体的任
意两个顶点总是相邻关系。
可见,用甲烷的二氯代物只有 1 种这一事实,可以证明甲
烷的结构不是平面正方形结构而是正四面体结构。
2.有机化合物结构的多样性
碳
4
共价键
单
有机化合物分子里都含有____原子。由于碳原子的最外层
有___个电子,碳原子不仅可以通过_______与其他原子结合形
成分子,还可以彼此间以共价键构成_____________,再结合其
他原子形成分子;碳原子之间可以是___键,也可以是___键或
___键。这些是有机化合物结构多样性的一种表现。
3.烷烃
碳链或碳环
双
叁
C
H
烃:仅含___和___两种元素的有机物,称为___________,
也称为烃。
碳氢化合物
C—C 单键
全部
饱和
烷烃是指碳原子跟碳原子都以共价键结合成___________,
碳原子剩余的价键______跟氢原子相结合的_____烃。
4.同分异构现象和同分异构体
(1)定义
化学式
结构
化合物具有相同的_______,但具有不同的______的现象,
叫做同分异构现象。具有同分异构现象的化合物互称同分异构
体,如正丁烷与异丁烷就是丁烷的两种同分异构体,属于两种
化合物。
名称 正丁烷 异丁烷
结构式
结构简式
熔点/℃ -138.4 -159.6
沸点/℃ -0.5 -11.7
(2)正丁烷和异丁烷的比较
烷烃同分异构体之间熔沸点的变化规律:碳原子相同的烷
烃,支链越多熔沸点越低,相对密度越小。
(CH3)2CHCH3
CH3(CH2)2CH3
(1)一般说来,有机化合物分子中的碳原子数越多,它的同
分异构体数目就越多。例如:戊烷(C5H12)有 3 种同分异构体,
己烷(C6H14)有 5 种同分异构体。
(2)在有机化合物中,同分异构现象非常普遍,这是有机化
合物结构多样性的又一表现。
1.甲烷分子的结构
甲烷分子中,碳原子最外层上的 4 个电子分别与 4 个氢原
子上的电子形成 4 个共价键。构成正四面体结构,碳原子位于
正四面体的中心,4 个氢原子分别位于正四面体的 4 个顶点上。
表示方法如下:
分子式 结构式 球棍模型
CH4
结构特点 原子之间以单键结合,空间构型为正四面体,碳原
子位于正四面体的中心
2.烷烃
(1)概念:有机物分子里碳原子和碳原子之间全部以单键结
合成链状,碳原子剩余的价键全部被氢原子所饱和的烃称为饱
和链烃,又称烷烃。如乙烷、丙烷、丁烷等。它们的结构如下
表所示:
名称 乙烷 丙烷 丁烷
结构
简式 CH3CH3 CH3CH2CH3 CH3CH2CH2CH3
结构式
球棍
模型
(2)通式:若碳原子数为 n,则氢原子数为 2n+2,烷烃的
分子通式为CnH2n+2。
CnH2n+2+
(3)烷烃的性质:
①物理性质:烷烃的熔沸点都较低,密度较小,但随着分
子中碳原子数的增加,呈现出规律性的变化:状态由气态到液
态再到固态,熔沸点逐渐升高,密度逐渐增大;分子里碳原子
数小于等于 4 的烷烃,在常温常压下都是气体;烷烃不溶于水,
但易溶于有机溶剂。液态烷烃本身就是有机溶剂,如己烷。
②化学性质:烷烃的化学性质和甲烷相似,如通常不与强
酸、强碱或强氧化剂反应,都不能使酸性高锰酸钾溶液或溴水
退色;都能发生取代反应,取代反应是烷烃的特征反应;都具
有可燃性,烷烃完全燃烧的通式为
3n+1
2
O2
点燃
nCO2+(n+1)H2O
(4)烷烃的命名
①在分子内的碳原子数后加一个“烷”字,称为“某烷”。
②分子中碳原子数在十个以内时,用天干表示,即用甲、
乙、丙、丁、戊、己、庚、辛、壬、癸表示,如甲烷、丁烷等。
③分子中碳原子数在十个以上时,直接用大写数字来表示,
如十二烷、十八烷等。
④对于碳原子数相同而结构不同的烷烃,一般在烷烃名称
之前再加“正”“异”“新”等字加以区别,如正丁烷、异丁
烷等。
3.同分异构现象和同分异构体
(1)同分异构体概念的内涵有两点:一是分子式相同,二是
结构不同,二者缺一不可。分子式相同必然相对分子质量相同,
但相对分子质量相同不一定分子式相同,如CO和C2H4、C2H6O
和 CH2O2 均是相对分子质量相同,但分子式不相同。
(2)同分异构现象广泛存在于有机化合物中,不仅存在于同
类物质中,也存在于不同类物质之间,例如,CH3CH2OH 和
CH3—O—CH3(二甲醚)等。
(3)烷烃的同分异构体数目随分子中碳原子数的增多而增
多。如 CH4、CH3CH3、CH3CH2CH3 均不存在同分异构体,而
丁烷、戊烷的同分异构体的种数分别为 2 种、3 种。
(4)烷烃同分异构体的写法
烷烃的同分异构体的书写规律可概括为:主链由长到短,
支链由整到散,位置由心到边,排列对、邻、间。
以戊烷(C5H12)为例的同分异构体的写法:
①先写出最长的碳链作为主链:C—C—C—C—C—C(氢原
子及其个数省略)
②从主链的一端取下一个碳原子,依次连在主链中心对称
线一侧的碳原子上:
注意不能加在两端,否则会和前面重复,同时注意对称的
位置也会有重复。
③从主链的一端取下两个碳原子:
a.把取下的两个碳原子当作一个支链加在主链上:
b.把两个碳原子作为两个支链加在主链上:
从主链上取下的碳原子,不得多于主链上剩余的碳原子,
否则一定会重复。
例 1.下列事实中能证明甲烷分子是以碳原子为中心的正四
面体结构的是(
)。
A.CH3Cl 只代表一种物质
B.CH2Cl2 只代表一种物质
C.CHCl3 只代表一种物质
D.CCl4 只代表一种物质
答案:B
解析:对于甲烷的正四面体结构,因为其4个顶点的位置完全相同,所以它的一氯代物(CH3Cl)、二氯代物(CH2Cl2)、三氯代物(CHCl3)、四氯代物(CCl4)都只有一种。而如果甲烷是平面正方形结构,虽然4个C—H键都完全相同,但4个顶点的氢原子的位置关系却不同,可能相邻,也可能相间,所以虽然CH3Cl、CHCl3、CCl4都只有一种,但CH2Cl2却有两种,一种是两个氯原子相邻,另一种是两个氯原子相间。由CH2Cl2只有一种这一点可以判断出CH4为正四面体结构,而不是平面正方形结构。
例2.下列有关烷烃的叙述中,不正确的是(
)。
C
A.在烷烃分子中,所有的化学键都为单键
B.所有的烷烃在光照条件下都能与 Cl2 发生取代反应
C.烷烃的分子通式为 CnH2n+2,符合该通式的烃不一定是
烷烃
D.随着碳原子数的增加,烷烃的熔沸点逐渐升高
解析:烷烃中的碳碳键、碳氢键均为单键,且烷烃在光照
条件下都能与Cl2 发生取代反应,这是烷烃的结构特征和反应
特征,故 A、B 正确;由于烷烃分子的通式CnH2n+2 中的 C 原子
已达饱和,所以符合 CnH2n+2 的有机物只可能为烷烃,故 C 错
误;由于随着 C 原子数的增加,烷烃的相对分子质量增大,其
熔沸点升高,故 D 正确。
变式训练1. 下列不属于烷烃性质的是(
)。
B
A.它们燃烧时生成二氧化碳和水
B.它们都溶于水
C.它们都能跟卤素发生取代反应
D.通常情况下,它们跟酸、碱和氧化剂都不反应
烷烃的结构和甲烷相似,分子内原子间都以单键相连,结
构相似,性质也相似。
例 3.(2010 湖南师大附中高一检测)正丁烷与异丁烷互为同
分异构体的依据是(
)。
D
A.具有相似的化学性质
B.具有相同的物理性质
C.分子具有相同的空间结构
D.分子式相同,但分子内碳原子的连接方式不同
解析:分子式相同,结构不同的物质互称同分异构体,同
分异构体空间结构不同,化学性质也不一定相似,物理性质不
相同。
物质 沸点/℃
正丁烷 CH3(CH2)2CH3 -0.5
正戊烷 CH3(CH2)3CH3 36.1
异戊烷
27.8
新戊烷
9.5
正己烷 CH3(CH2)4CH3 69.0
变式训练 2 在1.01×105 Pa 下,测得的某些烷烃的沸点见
下表。
据表分析,下列选项正确的是(
)。
D
A.在标准状况下,新戊烷是气体
B.在 1.01×105 Pa、20 ℃时,C5H12 都是液体
C.烷烃随碳原子数增加,沸点降低
D.C5H12 随支链增加,沸点降低
解析:新戊烷的沸点是9.5 ℃,标准状况下是液体,20 ℃
时是气体,A、B 均错误;烷烃随碳原子数的增加,沸点升高,
C 错误;C5H12的三种同分异构体中,随支链数增加,沸点降低,
D 正确。
例 4.(2010 吉林长春高一检测)已知丙烷的二氯代物有 4 种
)。
C
同分异构体,则其六氯代物的同分异构体的数目为(
A.2 种
B.3 种
C.4 种
D.5 种
解析:二氯丙烷:丙烷(C3H8)分子主链上有两个氢原子被
氯原子取代→氯原子有 4 种位置关系→二氯丙烷的同分异构体
有 4 种;六氯丙烷:全氯丙烷(C3Cl8)分子主链上有两个氯原子
被氢原子取代→氢原子有 4 种位置关系→六氯丙烷的同分异构
体有 4 种,故选 C 项。
例5.有下列几组物质:
C.红磷和白磷
B.甲烷和己烷
D.正丁烷和异丁烷
其中,①属于同分异构体的是______;②属于同位素的是
___;③属于同素异形体的是___;④属于同一种物质的是___。
D、F
A
C
E
概念即可解答。
解析:利用同位素、同素异形体、同系物及同分异构体的
1.(双选)下列分子中与甲烷分子空间构型相同的是(
)。
BD
A.CHCl3
C.CFCl3
B.CCl4
D.CF4
解析:只有甲烷的四个氢原子被同一原子取代时,产物才
是正四面体。
2 同分异构体现象是有机化学中的一种普遍现象,下列有
关同分异构体的叙述中正确的是(
)。
A
A.分子式相同而结构式不同的化合物互称同分异构体
B.组成成分相同而结构式不同的物质互称同分异构体
C.互为同分异构体的物质性质相同
D.互为同分异构体的物质物理性质相同
解析:互为同分异构体的物质必须是化合物,故B 项错误;
同分异构体的化学性质相似,物理性质不同,故C、D 项错误。
3.下列烷烃分子中进行一氯取代反应后,只能生成三种沸
点不同产物的是(
)。
D
解析:生成三种沸点不同的一氯产物,说明上述烷烃的一
氯代物只有三种同分异构体。
A.(CH3)2CHCH2CH2CH3
B.(CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2
D.(CH3)3CCH2CH3
4.(2010 山东青岛高一检测)下列说法正确的是(
)。
B
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结
合的烃一定是饱和链烃
B.分子组成符合 CnH2n+2 的烃一定是烷烃
C.正戊烷分子中所有碳原子均在一条直线上
D.新戊烷的一氯取代物有 2 种
解析:A 项符合条件的烃为饱和烃,可为烷烃,也可为环
烷烃,但分子组成符合CnH2n+2 的烃一定为烷烃,故 A 错误,
B 正确;在烷烃分子中与碳原子紧邻的四个原子构成四面体形,
所以正戊烷分子中所有碳原子呈锯齿形,而非直线形,故 C 错
误;新戊烷分子完全对称,分子中只有一种氢原子,故一氯取
代物只有一种,故 D 错误。
内容特点
本节是在学生初中已有的个别有机化合物的概念的基础
上,进一步了解有机化学的发展过程、研究范畴以及对生产、
生活、环境的重要作用。从碳的原子结构和成键方式入手,以
甲烷、乙烷、丙烷和丁烷等同系列及丁烷的同分异构现象为例,
说明有机化合物结构的多样性是导致有机物种类繁多的原因。
取代反应是烷烃的特征反应,因此甲烷的取代反应是本节的重
点内容之一。教材在实验的基础上使学生了解取代反应,然后
以球棍模型形象地说明取代反应的本质,帮助学生建立取代反
应的概念。
本节的知识框架为:
教学指要
首先以初中已有的化学知识为基础,引导学生对有机化合
物与无机化合物进行比较,然后进行本节的教学。本节内容可
以安排成两个知识模块:甲烷的结构和性质、同分异构现象。
具体建议如下:
通过“观察·思考”让学生观察实验,引导学生思考、讨论,
得出实验结论,然后引出取代反应的概念,并与无机化学中的
置换反应加以比较,进一步认识有机化合物、有机反应的特殊
性。
在有机化合物的结构特点的教学中,结合学生已有的原子
结构和共价键的知识,引导他们分析碳原子的成键特点,并以
球棍模型和比例模型形象地展示甲烷及其取代反应的各级取代
产物的立体结构。对于同分异构现象,可以从丁烷的球棍模型
入手,分析碳原子的不同连接方式,引出同分异构体的概念,
并让学生认识到:同分异构现象是有机化合物种类繁多的原因
之一。
