第3章 第2节 1 石油的炼制 乙烯
图片预览







文档简介
(共27张PPT)
第 2 节
石油和煤
重要的烃
“一骑红尘妃子笑,无人知是荔枝来。”该诗句描述了作
为一国之君的唐玄宗为了讨好杨贵妃,不惜代价命人远道从广
东等地乘驿马日夜兼程运送荔枝。现在,人们把青橘子和熟苹
果放在同一个塑料袋里,系紧袋口,这样一段时间后青橘子就
可以变黄、成熟,而且散发出诱人的清香。人们在运输水果的
时候有时会放入浸泡过酸性高锰酸钾溶液的硅藻土,目的是什
么呢?通过本节课的学习你就可以解释这个问题。
提示:浸泡过酸性高锰酸钾溶液
的硅藻土能够吸收水果产生的乙烯,
从而防止运输途中水果早熟。
1
石油的炼制
乙烯
1.石油的炼制
烃
碳
氧
(1)石油的成分:主要是由不同数目碳原子的____组成的复
杂混合物,石油中____ 和____ 质量分数之和平均可达 97%~
98%。
(2)石油的炼制方法
加热
冷凝
沸点
①分馏:用_____和_____的方法把石油分成不同_____范围
的产物,主要产品是石油气、汽油、煤油、柴油及重油等。
②裂化:在催化剂存在下通过加热把相对分子质量____、
沸点___的烃断裂为相对分子质量_____、沸点____的烃,主要
产品是高质量的____。
大
高
较小
较低
汽油
典型反应:C16H34
催化剂
△
____________
③裂解:常用石油分馏产品做原料,采用比裂化更高的温
度(700~1 000 ℃以上),使其中的____________________断裂
成乙烯、丙烯等________烃,主要产品是_____、丙烯等。
相对分子质量较大的烃
小分子
乙烯
C8H18+C8H16
体,标准状况下的密度为 1.25 g·L-1。
2.乙烯
无
难
(1)物理性质:乙烯是____色、稍有气味、____溶于水的气
2
双
(2)分子结构:乙烯的分子式为_____。从分子式可以看出,
一个乙烯分子比一个乙烷分子少___个氢原子。乙烯分子里碳原
,结构简式
子间的共价键是____键,结构式为
为___________。
C2H4
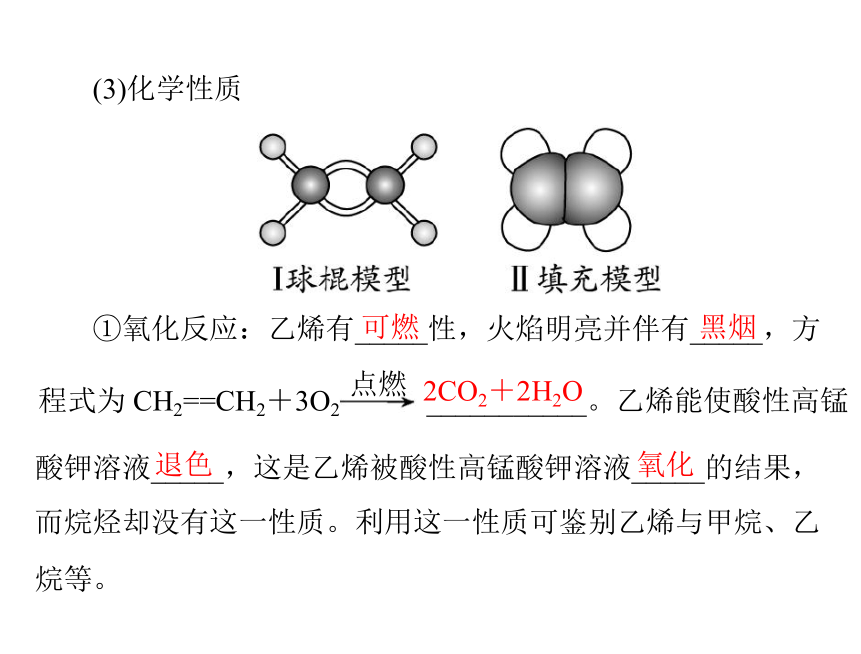
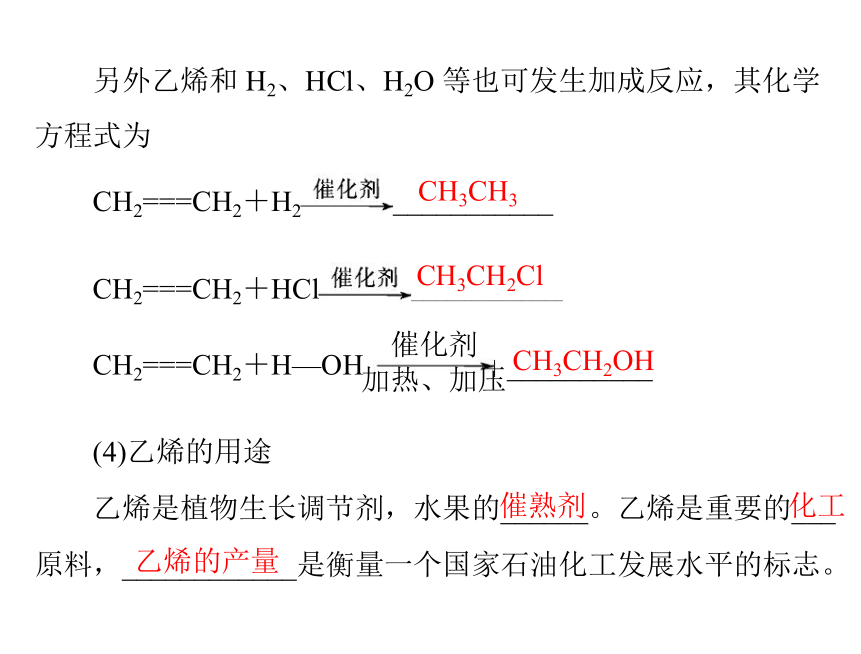
(3)化学性质
①氧化反应:乙烯有_____性,火焰明亮并伴有_____,方
程式为 CH2==CH2+3O2
点燃
___________。乙烯能使酸性高锰
酸钾溶液_____,这是乙烯被酸性高锰酸钾溶液_____的结果,
而烷烃却没有这一性质。利用这一性质可鉴别乙烯与甲烷、乙
烷等。
可燃
黑烟
2CO2+2H2O
退色
氧化
②加成反应:有机物分子中______上的碳原子与其他原子
(或原子团)直接结合生成新的化合物分子的反应。
双键
乙烯能使溴的四氯化碳溶液_____,实质是乙烯分子中碳碳
双键中的_____键断裂,两个溴原子分别加在_____的两个碳原
子上,方程式为 CH2===CH2+Br2
CH2BrCH2Br。
退色
因此,可用溴水或溴的四氯化碳溶液鉴别乙烯与甲烷、乙
烷等,也可用于除去甲烷中混有的乙烯。
一个
断键
乙烯使溴的四氯化碳溶液退色与使酸性高锰酸钾溶液退色
在原理上有何不同?
答案:前者是加成反应,后者是氧化反应。
另外乙烯和 H2、HCl、H2O 等也可发生加成反应,其化学
方程式为
CH2===CH2+H2
CH2===CH2+HCl
___________
_________________________
CH3CH2Cl
CH2===CH2+H—OH
催化剂
加热、加压
__________
CH3CH2OH
(4)乙烯的用途
催熟剂
化工
乙烯的产量
乙烯是植物生长调节剂,水果的______。乙烯是重要的___
原料,____________是衡量一个国家石油化工发展水平的标志。
CH3CH3
1.石油的成分
按元素来看:碳、氢含量之和为 97%~98%。
按物质来看:烷烃、环烷烃、芳香烃的混合物。
过程 原理 产品及用途
脱水、
脱盐 除去原油中的盐和水,减少对设备的
腐蚀
分馏 利用加热和冷凝,把石油分成不同沸
点范围的产物 石油气、汽油、煤油、
柴油、蜡油、润滑油、
重油
裂化 在一定条件下加热,把相对分子质量
大、沸点高的烃断裂为相对分子质量
较小、沸点较低的烃 轻质液体燃料(裂化
汽油)
催化
裂化 在一定条件下使用催化剂并加热,把
相对分子质量大、沸点高的烃断裂为
相对分子质量较小、沸点较低的烃 轻质液体燃料(裂化
汽油)
裂解 以石油分馏产品为原料,采用比裂化
更高的温度,使其中相对分子质量较
大的烃断裂成乙烯、丙烯等小分子 乙烯(有机化工的原
料)
2.石油的炼制
3.乙烯的氧化反应和加成反应
氧化反应
(1)空气中若含 3.4%~34%的乙烯,遇火极易发生爆炸,所
以点燃乙烯时要验纯。
(2)当温度高于 100 ℃时,乙烯燃烧前后的混合气体体积相等。
(3)乙烯完全燃烧生成的 CO2 和 H2O 的物质的量之比为 1∶1。
(4)乙烯使酸性 KMnO4 溶液退色,可用于区别 CH4(烷烃)
和 C2H4(烯烃)。
(5)酸性 KMnO4 溶液可将 CH2===CH2 最终氧化为 CO2,因此
当 CH4 中混有 CH2===CH2 时,不能用通过酸性 KMnO4 溶液的办
法除去乙烯,因为有新杂质 CO2 生成,不能达到提纯的目的。
加成反应
(1)当乙烯与 Br2 反应时,一般用溴水或溴的四氯化碳溶液,
生成的 1,2 二溴乙烷是无色液体,反应的化学方程式为
,通常简写为
CH2===CH2+Br2
CH2Br—CH2Br。
(2) 利用乙烯能使溴水退色而甲烷( 或烷烃) 不能使溴水退
色,既可以区别乙烯和甲烷(或烷烃),也可以除去甲烷(或烷烃)
中混有的乙烯气体以提纯甲烷(或烷烃)。
(3)为制得纯净的氯乙烷,应用乙烯和 HCl 的加成反应而不
宜用乙烷与 Cl2 的取代反应。因为乙烯与 HCl 的加成产物只有
一种,而乙烷与 Cl2 的取代产物是多种氯代烷的混合物。
(4)通常条件下,烯烃不和水反应(可用排水法收集乙烯),
但在一定条件下烯烃可以和水反应生成醇(工业上水化法制乙
醇的原理)。
(5)乙烯的自身加聚反应可以得到聚乙烯。
以上现象经常用作烯烃和其他物质的鉴别或除杂,在高考
中经常考查。在应用时要注意溴水和溴的四氯化碳溶液的区别。
名称
比较 取代反应 加成反应
概念 有机物分子里的某些原子或原
子团被其他原子或原子团所替
代的反应 有机物分子中不饱和碳
原子和其他原子或原子
团直接结合生成新的化
合物的反应
键的变化 一般是 C—H、O—H 或 C—O
键断裂,结合一个原子或原子
团,另一原子或原子团同替代
下来的基团结合成另一种物质 不饱和键中的不稳定键
断裂,不饱和原子直接和
其他原子或原子团结合
反应特点 ①可发生分步取代反应
②一上一下 ①有时只有一种加成方
式,有时有多种加成方式
②断一加二
产物 两种或多种物质 一种新有机物
4.取代反应和加成反应的比较
例 1.下列说法错误的是(
)。
A.石油中含有 C5~C11 的烷烃,可以通过石油的分馏得到
汽油
B.含 C18 以上烷烃的重油经过催化裂化可以得到汽油
C.石油裂解是为了获得更多的汽油
D.汽油、煤油、柴油都是由烃构成的混合物
解析:A 项中石油主要由液态烃构成,也溶有少量气态烃
和固态烃。石油中肯定含有C5~C11 的烷烃,因此通过石油的
分馏就可以得到汽油、煤油等分馏产品;B 项中含C18 以上的固
态烃利用率低,交通运输业需要更多的燃料油,使重油长链烃
分子断裂就可以得到汽油,使长链烃分子断裂为C5~C11 的烷
烃的过程是采用催化裂化的方法;C 项中石油裂解属于深度裂
化,采用的温度比裂化更高,长链烃分子断裂程度大。裂解的
目的不是为了生产更多的汽油,而是为了获得大量的石油化工
产品;D 项中石油是烃的混合物,石油的分馏产品汽油、煤油、
柴油等仍是烃的混合物,所不同的只是这些分馏产品沸点范围
小,是含碳原子数接近的烃的混合物。
答案:C
例2.既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中
混有的少量乙烯的操作方法是(
)。
B
A.混合气通过盛酸性高锰酸钾溶液的洗气瓶
B.混合气通过盛足量溴水的洗气瓶
C.混合气通过盛蒸馏水的洗气瓶
D.混合气跟适量氯化氢混合
生成液体物质
,而乙烯被酸性KMnO4 溶液氧化的生
成物可能是CO2,若有CO2 生成,则使CH4 中混入了新的杂质。
解析:鉴别这两种气体,酸性高锰酸钾溶液和溴水均有明
显的现象,但要除去甲烷中的乙烯,不是仅凭现象就能达到目
的,还要考虑反应产物的影响。乙烯与溴水反应是加成反应,
B.H2+Cl2=====2HCl
变式训练.下列各反应属于加成反应的是(
)。
A
CH3CH2OH
A.CH2===CH2+H—OH
光照
C.CH2===CH2+3O2
点燃
2CO2+2H2O
D.CH3—CH3+2Cl2
CH2ClCH2Cl+2HCl
解析:A 项符合加成反应的概念;B 项是无机的化合反应;
C 项乙烯发生了氧化反应;D 项发生了取代反应。
例 3.体育比赛中当运动员肌肉挫伤或扭伤时,队医随即对
准运动员的受伤部位喷射药剂——氯乙烷(沸点为 12.27 ℃),进
行局部冷冻麻醉应急处理。
(1)制取氯乙烷(CH3CH2Cl)的最好的方法是(
)。
A.乙烷与氯气发生取代反应
B.乙烯与氯气发生加成反应
C.乙烷与氯化氢反应
D.乙烯与氯化氢发生加成反应
(2)写出所选反应的化学方程式:_____________________。
(3)决定氯乙烷能用于冷冻麻醉应急处理的理由是_______
__________________________。
解析:(1)乙烷与氯气发生取代反应的产物为各种氯代乙烷
的混合物;乙烯与氯气发生加成反应的产物为 1,2 二氯乙烷;
只有乙烯和氯化氢的加成反应才能得到较纯的一氯乙烷,产物
为CH3CH2Cl;乙烷与氯化氢不反应。
(2)加成反应发生在不饱和碳原子上,所以化学方程式 为
CH2===CH2+HCl
CH3CH2Cl。
(3)氯乙烷的沸点低,为 12.27 ℃,易汽化而吸收能量,使
局部冷冻麻醉
答案:(1)D
(2)CH2===CH2+HCl―→CH3CH2Cl
例 4.下列反应中前者属于取代反应,后者属于加成反应的
是(
)。
A.甲烷与氯气混合后在光照条件下的反应;乙烯使酸性
高锰酸钾溶液退色
B.乙烯与溴的四氯化碳溶液反应;乙烯与水在一定条件
下的反应
C.乙烷与氯气混合后在光照条件下的反应;乙烯与水生
成乙醇的反应
D.乙烯与溴水反应;乙烯在空气中点燃
解析:A 项中甲烷与Cl2 发生取代反应,乙烯被酸性高锰酸钾
氧化发生氧化反应;B 项中的两个反应都是加成反应;D 项中乙
烯与溴水发生加成反应,乙烯在空气中点燃发生了氧化反应。
答案:C
取代反应和加成反应是两类重要的有机反应,饱和烃的特
征反应是取代反应,不饱和烃的特征反应是加成反应。
1.下列关于乙烯的说法,不正确的是(
)。
B
A.是无色气体,比空气略轻,难溶于水
B.与溴水发生取代反应而使溴水退色
C.乙烯的产量标志着一个国家的石油化工水平
D.可用点燃法鉴别乙烯和甲烷
解析:乙烯与溴水发生加成反应而使溴水退色;点燃乙烯
会产生黑烟,但点燃甲烷不会产生黑烟,因此可用点燃法鉴别
乙烯和甲烷。
2.能证明乙烯分子里含有一个碳碳双键的事实是(
)。
A.乙烯分子里碳氢原子的个数比为 1∶2
C
B.乙烯完全燃烧生成 CO2 和 H2O 的物质的量相等
C.乙烯易与溴水发生加成反应,且 1 mol 乙烯完全加成需
消耗 1 mol 溴单质
D.乙烯能使酸性 KMnO4 溶液退色
解析:乙烯结构上的特点是含有碳碳双键,特征化学反应
是加成反应。
3.衡量一个国家石油化工发展水平的标志是(
)。
A.乙烯产量
C.天然气产量
B.石油产量
D.汽油产量
4.(双选)下列物质的制取应选用加成反应的是(
)。
AC
A.一氯丙烷
C.CH2BrCH2Br
B.三氯甲烷
D.CH2Br2
A
5.某烯烃的结构简式为 CH2==CH—CH==CH—CH3,若它
在一定条件下能与氯气发生加成反应,那么 1 mol 该烯烃完全
)。
加成需要消耗的氯气的物质的量是(
A.1 mol
C.3 mol
B.2 mol
D.4 mol
解析:1 mol 碳碳双键能与 1 mol Cl2 发生加成反应。
B
第 2 节
石油和煤
重要的烃
“一骑红尘妃子笑,无人知是荔枝来。”该诗句描述了作
为一国之君的唐玄宗为了讨好杨贵妃,不惜代价命人远道从广
东等地乘驿马日夜兼程运送荔枝。现在,人们把青橘子和熟苹
果放在同一个塑料袋里,系紧袋口,这样一段时间后青橘子就
可以变黄、成熟,而且散发出诱人的清香。人们在运输水果的
时候有时会放入浸泡过酸性高锰酸钾溶液的硅藻土,目的是什
么呢?通过本节课的学习你就可以解释这个问题。
提示:浸泡过酸性高锰酸钾溶液
的硅藻土能够吸收水果产生的乙烯,
从而防止运输途中水果早熟。
1
石油的炼制
乙烯
1.石油的炼制
烃
碳
氧
(1)石油的成分:主要是由不同数目碳原子的____组成的复
杂混合物,石油中____ 和____ 质量分数之和平均可达 97%~
98%。
(2)石油的炼制方法
加热
冷凝
沸点
①分馏:用_____和_____的方法把石油分成不同_____范围
的产物,主要产品是石油气、汽油、煤油、柴油及重油等。
②裂化:在催化剂存在下通过加热把相对分子质量____、
沸点___的烃断裂为相对分子质量_____、沸点____的烃,主要
产品是高质量的____。
大
高
较小
较低
汽油
典型反应:C16H34
催化剂
△
____________
③裂解:常用石油分馏产品做原料,采用比裂化更高的温
度(700~1 000 ℃以上),使其中的____________________断裂
成乙烯、丙烯等________烃,主要产品是_____、丙烯等。
相对分子质量较大的烃
小分子
乙烯
C8H18+C8H16
体,标准状况下的密度为 1.25 g·L-1。
2.乙烯
无
难
(1)物理性质:乙烯是____色、稍有气味、____溶于水的气
2
双
(2)分子结构:乙烯的分子式为_____。从分子式可以看出,
一个乙烯分子比一个乙烷分子少___个氢原子。乙烯分子里碳原
,结构简式
子间的共价键是____键,结构式为
为___________。
C2H4
(3)化学性质
①氧化反应:乙烯有_____性,火焰明亮并伴有_____,方
程式为 CH2==CH2+3O2
点燃
___________。乙烯能使酸性高锰
酸钾溶液_____,这是乙烯被酸性高锰酸钾溶液_____的结果,
而烷烃却没有这一性质。利用这一性质可鉴别乙烯与甲烷、乙
烷等。
可燃
黑烟
2CO2+2H2O
退色
氧化
②加成反应:有机物分子中______上的碳原子与其他原子
(或原子团)直接结合生成新的化合物分子的反应。
双键
乙烯能使溴的四氯化碳溶液_____,实质是乙烯分子中碳碳
双键中的_____键断裂,两个溴原子分别加在_____的两个碳原
子上,方程式为 CH2===CH2+Br2
CH2BrCH2Br。
退色
因此,可用溴水或溴的四氯化碳溶液鉴别乙烯与甲烷、乙
烷等,也可用于除去甲烷中混有的乙烯。
一个
断键
乙烯使溴的四氯化碳溶液退色与使酸性高锰酸钾溶液退色
在原理上有何不同?
答案:前者是加成反应,后者是氧化反应。
另外乙烯和 H2、HCl、H2O 等也可发生加成反应,其化学
方程式为
CH2===CH2+H2
CH2===CH2+HCl
___________
_________________________
CH3CH2Cl
CH2===CH2+H—OH
催化剂
加热、加压
__________
CH3CH2OH
(4)乙烯的用途
催熟剂
化工
乙烯的产量
乙烯是植物生长调节剂,水果的______。乙烯是重要的___
原料,____________是衡量一个国家石油化工发展水平的标志。
CH3CH3
1.石油的成分
按元素来看:碳、氢含量之和为 97%~98%。
按物质来看:烷烃、环烷烃、芳香烃的混合物。
过程 原理 产品及用途
脱水、
脱盐 除去原油中的盐和水,减少对设备的
腐蚀
分馏 利用加热和冷凝,把石油分成不同沸
点范围的产物 石油气、汽油、煤油、
柴油、蜡油、润滑油、
重油
裂化 在一定条件下加热,把相对分子质量
大、沸点高的烃断裂为相对分子质量
较小、沸点较低的烃 轻质液体燃料(裂化
汽油)
催化
裂化 在一定条件下使用催化剂并加热,把
相对分子质量大、沸点高的烃断裂为
相对分子质量较小、沸点较低的烃 轻质液体燃料(裂化
汽油)
裂解 以石油分馏产品为原料,采用比裂化
更高的温度,使其中相对分子质量较
大的烃断裂成乙烯、丙烯等小分子 乙烯(有机化工的原
料)
2.石油的炼制
3.乙烯的氧化反应和加成反应
氧化反应
(1)空气中若含 3.4%~34%的乙烯,遇火极易发生爆炸,所
以点燃乙烯时要验纯。
(2)当温度高于 100 ℃时,乙烯燃烧前后的混合气体体积相等。
(3)乙烯完全燃烧生成的 CO2 和 H2O 的物质的量之比为 1∶1。
(4)乙烯使酸性 KMnO4 溶液退色,可用于区别 CH4(烷烃)
和 C2H4(烯烃)。
(5)酸性 KMnO4 溶液可将 CH2===CH2 最终氧化为 CO2,因此
当 CH4 中混有 CH2===CH2 时,不能用通过酸性 KMnO4 溶液的办
法除去乙烯,因为有新杂质 CO2 生成,不能达到提纯的目的。
加成反应
(1)当乙烯与 Br2 反应时,一般用溴水或溴的四氯化碳溶液,
生成的 1,2 二溴乙烷是无色液体,反应的化学方程式为
,通常简写为
CH2===CH2+Br2
CH2Br—CH2Br。
(2) 利用乙烯能使溴水退色而甲烷( 或烷烃) 不能使溴水退
色,既可以区别乙烯和甲烷(或烷烃),也可以除去甲烷(或烷烃)
中混有的乙烯气体以提纯甲烷(或烷烃)。
(3)为制得纯净的氯乙烷,应用乙烯和 HCl 的加成反应而不
宜用乙烷与 Cl2 的取代反应。因为乙烯与 HCl 的加成产物只有
一种,而乙烷与 Cl2 的取代产物是多种氯代烷的混合物。
(4)通常条件下,烯烃不和水反应(可用排水法收集乙烯),
但在一定条件下烯烃可以和水反应生成醇(工业上水化法制乙
醇的原理)。
(5)乙烯的自身加聚反应可以得到聚乙烯。
以上现象经常用作烯烃和其他物质的鉴别或除杂,在高考
中经常考查。在应用时要注意溴水和溴的四氯化碳溶液的区别。
名称
比较 取代反应 加成反应
概念 有机物分子里的某些原子或原
子团被其他原子或原子团所替
代的反应 有机物分子中不饱和碳
原子和其他原子或原子
团直接结合生成新的化
合物的反应
键的变化 一般是 C—H、O—H 或 C—O
键断裂,结合一个原子或原子
团,另一原子或原子团同替代
下来的基团结合成另一种物质 不饱和键中的不稳定键
断裂,不饱和原子直接和
其他原子或原子团结合
反应特点 ①可发生分步取代反应
②一上一下 ①有时只有一种加成方
式,有时有多种加成方式
②断一加二
产物 两种或多种物质 一种新有机物
4.取代反应和加成反应的比较
例 1.下列说法错误的是(
)。
A.石油中含有 C5~C11 的烷烃,可以通过石油的分馏得到
汽油
B.含 C18 以上烷烃的重油经过催化裂化可以得到汽油
C.石油裂解是为了获得更多的汽油
D.汽油、煤油、柴油都是由烃构成的混合物
解析:A 项中石油主要由液态烃构成,也溶有少量气态烃
和固态烃。石油中肯定含有C5~C11 的烷烃,因此通过石油的
分馏就可以得到汽油、煤油等分馏产品;B 项中含C18 以上的固
态烃利用率低,交通运输业需要更多的燃料油,使重油长链烃
分子断裂就可以得到汽油,使长链烃分子断裂为C5~C11 的烷
烃的过程是采用催化裂化的方法;C 项中石油裂解属于深度裂
化,采用的温度比裂化更高,长链烃分子断裂程度大。裂解的
目的不是为了生产更多的汽油,而是为了获得大量的石油化工
产品;D 项中石油是烃的混合物,石油的分馏产品汽油、煤油、
柴油等仍是烃的混合物,所不同的只是这些分馏产品沸点范围
小,是含碳原子数接近的烃的混合物。
答案:C
例2.既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中
混有的少量乙烯的操作方法是(
)。
B
A.混合气通过盛酸性高锰酸钾溶液的洗气瓶
B.混合气通过盛足量溴水的洗气瓶
C.混合气通过盛蒸馏水的洗气瓶
D.混合气跟适量氯化氢混合
生成液体物质
,而乙烯被酸性KMnO4 溶液氧化的生
成物可能是CO2,若有CO2 生成,则使CH4 中混入了新的杂质。
解析:鉴别这两种气体,酸性高锰酸钾溶液和溴水均有明
显的现象,但要除去甲烷中的乙烯,不是仅凭现象就能达到目
的,还要考虑反应产物的影响。乙烯与溴水反应是加成反应,
B.H2+Cl2=====2HCl
变式训练.下列各反应属于加成反应的是(
)。
A
CH3CH2OH
A.CH2===CH2+H—OH
光照
C.CH2===CH2+3O2
点燃
2CO2+2H2O
D.CH3—CH3+2Cl2
CH2ClCH2Cl+2HCl
解析:A 项符合加成反应的概念;B 项是无机的化合反应;
C 项乙烯发生了氧化反应;D 项发生了取代反应。
例 3.体育比赛中当运动员肌肉挫伤或扭伤时,队医随即对
准运动员的受伤部位喷射药剂——氯乙烷(沸点为 12.27 ℃),进
行局部冷冻麻醉应急处理。
(1)制取氯乙烷(CH3CH2Cl)的最好的方法是(
)。
A.乙烷与氯气发生取代反应
B.乙烯与氯气发生加成反应
C.乙烷与氯化氢反应
D.乙烯与氯化氢发生加成反应
(2)写出所选反应的化学方程式:_____________________。
(3)决定氯乙烷能用于冷冻麻醉应急处理的理由是_______
__________________________。
解析:(1)乙烷与氯气发生取代反应的产物为各种氯代乙烷
的混合物;乙烯与氯气发生加成反应的产物为 1,2 二氯乙烷;
只有乙烯和氯化氢的加成反应才能得到较纯的一氯乙烷,产物
为CH3CH2Cl;乙烷与氯化氢不反应。
(2)加成反应发生在不饱和碳原子上,所以化学方程式 为
CH2===CH2+HCl
CH3CH2Cl。
(3)氯乙烷的沸点低,为 12.27 ℃,易汽化而吸收能量,使
局部冷冻麻醉
答案:(1)D
(2)CH2===CH2+HCl―→CH3CH2Cl
例 4.下列反应中前者属于取代反应,后者属于加成反应的
是(
)。
A.甲烷与氯气混合后在光照条件下的反应;乙烯使酸性
高锰酸钾溶液退色
B.乙烯与溴的四氯化碳溶液反应;乙烯与水在一定条件
下的反应
C.乙烷与氯气混合后在光照条件下的反应;乙烯与水生
成乙醇的反应
D.乙烯与溴水反应;乙烯在空气中点燃
解析:A 项中甲烷与Cl2 发生取代反应,乙烯被酸性高锰酸钾
氧化发生氧化反应;B 项中的两个反应都是加成反应;D 项中乙
烯与溴水发生加成反应,乙烯在空气中点燃发生了氧化反应。
答案:C
取代反应和加成反应是两类重要的有机反应,饱和烃的特
征反应是取代反应,不饱和烃的特征反应是加成反应。
1.下列关于乙烯的说法,不正确的是(
)。
B
A.是无色气体,比空气略轻,难溶于水
B.与溴水发生取代反应而使溴水退色
C.乙烯的产量标志着一个国家的石油化工水平
D.可用点燃法鉴别乙烯和甲烷
解析:乙烯与溴水发生加成反应而使溴水退色;点燃乙烯
会产生黑烟,但点燃甲烷不会产生黑烟,因此可用点燃法鉴别
乙烯和甲烷。
2.能证明乙烯分子里含有一个碳碳双键的事实是(
)。
A.乙烯分子里碳氢原子的个数比为 1∶2
C
B.乙烯完全燃烧生成 CO2 和 H2O 的物质的量相等
C.乙烯易与溴水发生加成反应,且 1 mol 乙烯完全加成需
消耗 1 mol 溴单质
D.乙烯能使酸性 KMnO4 溶液退色
解析:乙烯结构上的特点是含有碳碳双键,特征化学反应
是加成反应。
3.衡量一个国家石油化工发展水平的标志是(
)。
A.乙烯产量
C.天然气产量
B.石油产量
D.汽油产量
4.(双选)下列物质的制取应选用加成反应的是(
)。
AC
A.一氯丙烷
C.CH2BrCH2Br
B.三氯甲烷
D.CH2Br2
A
5.某烯烃的结构简式为 CH2==CH—CH==CH—CH3,若它
在一定条件下能与氯气发生加成反应,那么 1 mol 该烯烃完全
)。
加成需要消耗的氯气的物质的量是(
A.1 mol
C.3 mol
B.2 mol
D.4 mol
解析:1 mol 碳碳双键能与 1 mol Cl2 发生加成反应。
B
