(沪教版)6.3.2物质的溶解性(课件22页)
文档属性
| 名称 | (沪教版)6.3.2物质的溶解性(课件22页) |

|
|
| 格式 | ppt | ||
| 文件大小 | 50.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-29 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
第二课时
第3节 物质的溶解性
影响物质溶解性的因素有那些呢?
1、溶质的性质 不同的溶质在同一种溶剂溶解性不同
3、温度 绝大部份的物质温度越高,溶解能力越强
2、溶剂的性质 同种的溶质在不同的溶剂溶解性不同
氯化钠,也叫“食盐”
硝酸钾,是一种白色粉末
“溶解之王”争霸赛
定量的比较这两种物质溶解能力的大小
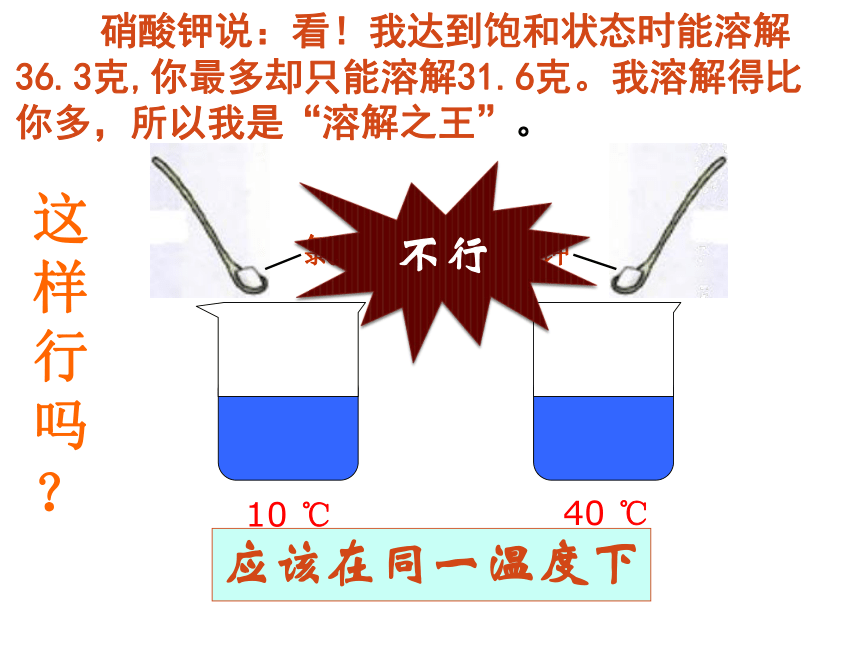
10 ℃
40 ℃
氯化钠
硝酸钾
不行
应该在同一温度下
这样行吗
?
硝酸钾说:看!我达到饱和状态时能溶解36.3克,你最多却只能溶解31.6克。我溶解得比你多,所以我是“溶解之王”。
硝酸钾
氯化钠
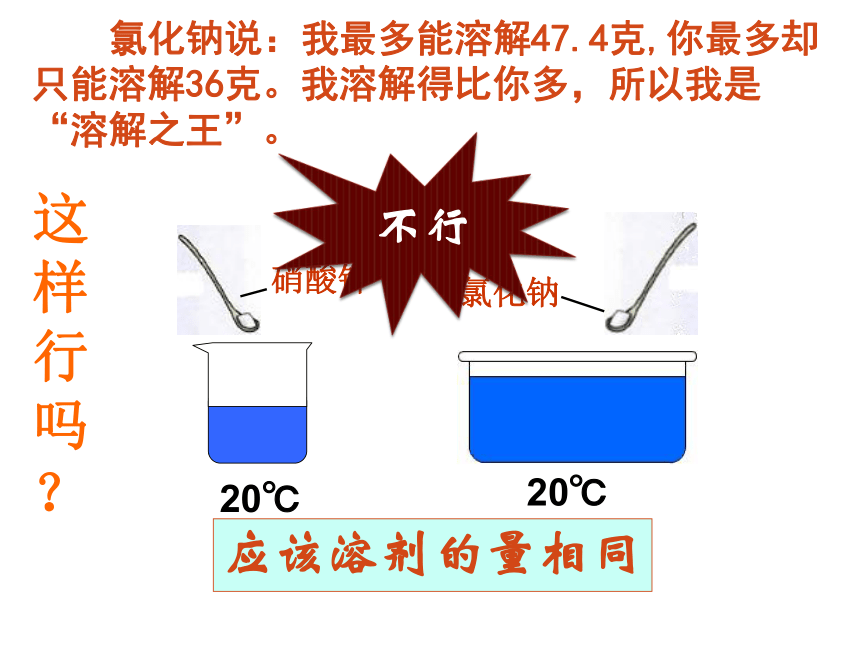
不行
应该溶剂的量相同
这样行吗
?
氯化钠说:我最多能溶解47.4克,你最多却只能溶解36克。我溶解得比你多,所以我是“溶解之王”。
20℃
20℃
1克氯化钠
1克硝酸钾
20克水
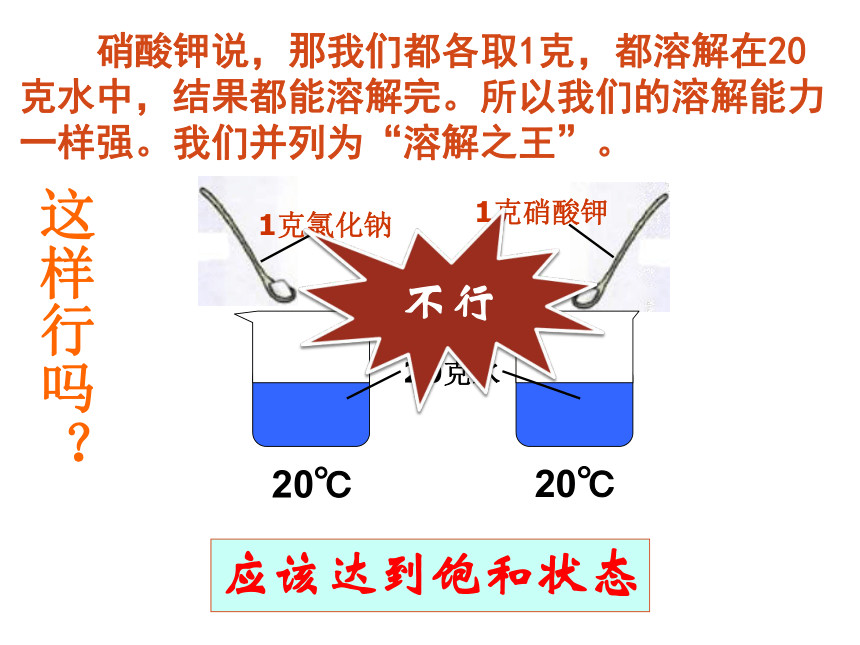
不行
应该达到饱和状态
这样行吗?
硝酸钾说,那我们都各取1克,都溶解在20克水中,结果都能溶解完。所以我们的溶解能力一样强。我们并列为“溶解之王”。
这样行吗?
20℃
20℃
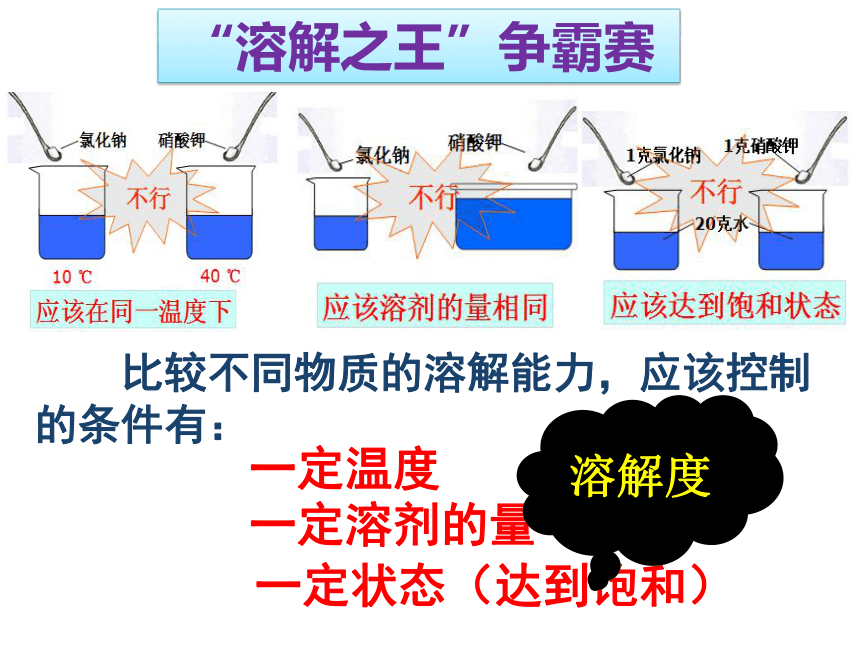
一定状态(达到饱和)
比较不同物质的溶解能力,应该控制的条件有:
一定温度
一定溶剂的量
“溶解之王”争霸赛
溶解度
1、定义:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
一定温度 (温度改变,溶解度也改变)
100克溶剂(一般指水)
饱和状态
条件:
标准:
溶液状态:
单位:
质量(克)
2、固体溶解度的四要素:
二、物质溶解性的定量表示
20 C,食盐的溶解度为36g,其含义是?
其含义是:在20 C时,食盐在100克水中达到
饱和状态时溶解的质量为36克。
或:在20 C时,100克水中最多能溶解36克食盐。
20 C时,向50g的水中加入20g的氯化钠固体,试计算所得溶液溶质的质量分数。 (只要求列出计算式)
(已知20 C时,氯化钠溶解度为36g)
注意:是否完全溶解!
溶解度与溶解性的关系
溶解性
溶解度g/100g 水 (20℃)
易溶
可溶
微溶
难(不)溶
.
.
.
0.01g
1g
10g
易溶
可溶
微溶
难溶
.
.
.
.
溶解度/
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
.
硝酸钾
.
.
.
.
温度/℃ 0 10 20 30 40 50 60 70 80 90
100
溶解度
硝酸钾在不同温度时的溶解度:
13.3
31.6
20.9
45.8
63.9
85.5
110
138
168
202
246
溶解度的表示方法
(1)列表法
(2)溶解度曲线
温度(t)
160
150
140
130
120
110
100
90
80
70
60
50
40
30
20
10
200
190
180
170
10
100
90
80
70
60
50
40
30
20
0
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钠
硼酸
6、固体溶解度曲线及意义
点:曲线上的点均表示某物质在该温度下的溶解度。
交点:曲线的交点表示这两种物质在该温度下的溶解度相同。
曲线:曲线越陡,该物质的溶解度受温度影响越大。
.a
.b
g/100g水
溶解度
溶解度/克
10
20
30
40
50
60
70
80
90
100
110
120
130
140
150
160
170
180
190
200
10
20
30
40
50
60
70
80
90
100
0
氯化钠
温度/℃
硝酸钾
判决:氯化钠和硝酸钾的溶解能力谁强?
23
温度<23℃时,氯化钠溶解能力较强;
温度=23℃时,两者溶解能力一样强;
温度>23℃时,硝酸钾溶解能力较强。
“溶解之王”争霸赛——终审判决
天气闷热时,鱼塘里的鱼为什么总是接近水面游动?
打开汽水盖时,汽水会自动喷出来。这说明气体在水中的溶解度与什么有关?
海水“晒盐”
原理:借助日光和风力使水分蒸发,得到食盐
一、蒸发结晶
蒸发操作要点
1.蒸发皿中的液体量不能超过蒸发皿容积的2/3;
2.加热时,用玻璃棒不断搅拌,防止局部温度过高造成液滴飞溅;
3.当蒸发皿中出现较多量固体时,停止加热,并用玻璃棒不断搅拌,利用余热将剩余水分蒸干;
4.热的蒸发皿用坩埚钳夹持放在石棉网上,以免烫坏实验桌。
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
①
②
90℃时,109g的某物质溶在100g水中得到溶液①
③
④
溶液①
降温至
60℃
溶液②
溶液③
降温至
40℃
溶液④
降温至
20℃
二、降温结晶
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
①
②
③
④
用“变大”“变小”“不变”填表
变化
过程 溶质质量 溶剂质量 溶液质量 溶质质量分数 溶解度
①→②
②→③
③→④
不变
不变
不变
不变
变小
变小
不变
变小
变小
变小
变小
不变
变小
变小
变小
二、降温结晶
硝酸钾(氯化钠) 硝酸钾
提纯
①配制热的饱和溶液
溶解度受温度影响大
溶解度受温度影响小
②降温结晶
③过滤
三、结晶的应用
2. 提纯某些可溶性固体混合物
氯化钠(硝酸钾) 氯化钠
提纯
①溶解
溶解度受温度影响大
溶解度受温度影响小
②蒸发溶剂(大部分固体析出)
③趁热过滤
三、结晶的应用
2. 提纯某些可溶性固体混合物
第二课时
第3节 物质的溶解性
影响物质溶解性的因素有那些呢?
1、溶质的性质 不同的溶质在同一种溶剂溶解性不同
3、温度 绝大部份的物质温度越高,溶解能力越强
2、溶剂的性质 同种的溶质在不同的溶剂溶解性不同
氯化钠,也叫“食盐”
硝酸钾,是一种白色粉末
“溶解之王”争霸赛
定量的比较这两种物质溶解能力的大小
10 ℃
40 ℃
氯化钠
硝酸钾
不行
应该在同一温度下
这样行吗
?
硝酸钾说:看!我达到饱和状态时能溶解36.3克,你最多却只能溶解31.6克。我溶解得比你多,所以我是“溶解之王”。
硝酸钾
氯化钠
不行
应该溶剂的量相同
这样行吗
?
氯化钠说:我最多能溶解47.4克,你最多却只能溶解36克。我溶解得比你多,所以我是“溶解之王”。
20℃
20℃
1克氯化钠
1克硝酸钾
20克水
不行
应该达到饱和状态
这样行吗?
硝酸钾说,那我们都各取1克,都溶解在20克水中,结果都能溶解完。所以我们的溶解能力一样强。我们并列为“溶解之王”。
这样行吗?
20℃
20℃
一定状态(达到饱和)
比较不同物质的溶解能力,应该控制的条件有:
一定温度
一定溶剂的量
“溶解之王”争霸赛
溶解度
1、定义:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
一定温度 (温度改变,溶解度也改变)
100克溶剂(一般指水)
饱和状态
条件:
标准:
溶液状态:
单位:
质量(克)
2、固体溶解度的四要素:
二、物质溶解性的定量表示
20 C,食盐的溶解度为36g,其含义是?
其含义是:在20 C时,食盐在100克水中达到
饱和状态时溶解的质量为36克。
或:在20 C时,100克水中最多能溶解36克食盐。
20 C时,向50g的水中加入20g的氯化钠固体,试计算所得溶液溶质的质量分数。 (只要求列出计算式)
(已知20 C时,氯化钠溶解度为36g)
注意:是否完全溶解!
溶解度与溶解性的关系
溶解性
溶解度g/100g 水 (20℃)
易溶
可溶
微溶
难(不)溶
.
.
.
0.01g
1g
10g
易溶
可溶
微溶
难溶
.
.
.
.
溶解度/
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
.
硝酸钾
.
.
.
.
温度/℃ 0 10 20 30 40 50 60 70 80 90
100
溶解度
硝酸钾在不同温度时的溶解度:
13.3
31.6
20.9
45.8
63.9
85.5
110
138
168
202
246
溶解度的表示方法
(1)列表法
(2)溶解度曲线
温度(t)
160
150
140
130
120
110
100
90
80
70
60
50
40
30
20
10
200
190
180
170
10
100
90
80
70
60
50
40
30
20
0
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钠
硼酸
6、固体溶解度曲线及意义
点:曲线上的点均表示某物质在该温度下的溶解度。
交点:曲线的交点表示这两种物质在该温度下的溶解度相同。
曲线:曲线越陡,该物质的溶解度受温度影响越大。
.a
.b
g/100g水
溶解度
溶解度/克
10
20
30
40
50
60
70
80
90
100
110
120
130
140
150
160
170
180
190
200
10
20
30
40
50
60
70
80
90
100
0
氯化钠
温度/℃
硝酸钾
判决:氯化钠和硝酸钾的溶解能力谁强?
23
温度<23℃时,氯化钠溶解能力较强;
温度=23℃时,两者溶解能力一样强;
温度>23℃时,硝酸钾溶解能力较强。
“溶解之王”争霸赛——终审判决
天气闷热时,鱼塘里的鱼为什么总是接近水面游动?
打开汽水盖时,汽水会自动喷出来。这说明气体在水中的溶解度与什么有关?
海水“晒盐”
原理:借助日光和风力使水分蒸发,得到食盐
一、蒸发结晶
蒸发操作要点
1.蒸发皿中的液体量不能超过蒸发皿容积的2/3;
2.加热时,用玻璃棒不断搅拌,防止局部温度过高造成液滴飞溅;
3.当蒸发皿中出现较多量固体时,停止加热,并用玻璃棒不断搅拌,利用余热将剩余水分蒸干;
4.热的蒸发皿用坩埚钳夹持放在石棉网上,以免烫坏实验桌。
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
①
②
90℃时,109g的某物质溶在100g水中得到溶液①
③
④
溶液①
降温至
60℃
溶液②
溶液③
降温至
40℃
溶液④
降温至
20℃
二、降温结晶
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
①
②
③
④
用“变大”“变小”“不变”填表
变化
过程 溶质质量 溶剂质量 溶液质量 溶质质量分数 溶解度
①→②
②→③
③→④
不变
不变
不变
不变
变小
变小
不变
变小
变小
变小
变小
不变
变小
变小
变小
二、降温结晶
硝酸钾(氯化钠) 硝酸钾
提纯
①配制热的饱和溶液
溶解度受温度影响大
溶解度受温度影响小
②降温结晶
③过滤
三、结晶的应用
2. 提纯某些可溶性固体混合物
氯化钠(硝酸钾) 氯化钠
提纯
①溶解
溶解度受温度影响大
溶解度受温度影响小
②蒸发溶剂(大部分固体析出)
③趁热过滤
三、结晶的应用
2. 提纯某些可溶性固体混合物
