(沪教版)2021-2022学年九年级化学下册同步课件6.3 物质的溶解性(第2课时)(课件20页)
文档属性
| 名称 | (沪教版)2021-2022学年九年级化学下册同步课件6.3 物质的溶解性(第2课时)(课件20页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-21 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
第6章 溶解现象
第3节 物质的溶解性
(第2课时)
硝酸钾
白色粉末
易溶于水
氯化钠
俗名“食盐”
易溶于水
“溶解之王”争霸赛
20℃
40℃
氯化钠
硝酸钾
不行
应该在同一温度下
硝酸钾:我达到饱和状态时能溶解36.3克,你最多却只能溶解31.6克。我溶解得比你多,所以我是“溶解之王”。
硝酸钾
氯化钠
氯化钠:我最多能溶解47.4克,你最多却只能溶解36克。我溶解得比你多,所以我是“溶解之王”。
20℃
20℃
应该溶剂的量相同
不行
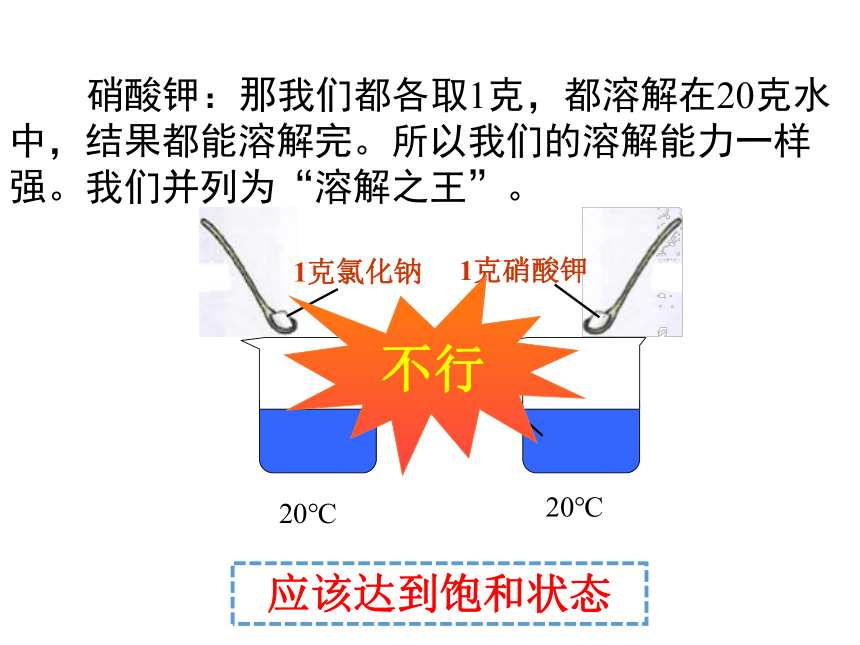
1克氯化钠
1克硝酸钾
20克水
硝酸钾:那我们都各取1克,都溶解在20克水中,结果都能溶解完。所以我们的溶解能力一样强。我们并列为“溶解之王”。
20℃
20℃
应该达到饱和状态
不行
一定状态(达到饱和)
定量地比较不同物质的溶解能力应该控制一定的条件:
一定温度
一定溶剂的量
溶解度
一、物质溶解性的定量表示
一、物质溶解性的定量表示
1. 固体物质的溶解度
(1)概念:在一定温度下,某固体物质在100g溶剂(通常溶剂为水)中达到饱和状态时所溶解的质量。
一定温度
(2)四要素:
①条件:一定温度 ②标准:100g溶剂
③状态:饱和状态 ④单位:克
S
一、物质溶解性的定量表示
1. 固体物质的溶解度
(3)含义:
一定温度
①指该物质在此温度下,在100g溶剂(通常溶剂为水)中达到饱和状态时所溶解的质量。
例:NaCl在20℃时的溶解度为36.0g。
指在20℃时,100g水中达到饱和状态时所溶解NaCl的质量为36.0g。(或在20℃时,100g水中最多溶解NaCl的质量为36.0g)。
一、物质溶解性的定量表示
1. 固体物质的溶解度
(3)含义:
一定温度
②指在此温度下,该物质的饱和溶液中,溶质、溶剂与饱和溶液三者之间的质量比=S:100g:(100g+S)。
例:NaCl在20℃时的溶解度为36.0g。
则在20℃时,任意质量的NaCl饱和状态中,NaCl、水、NaCl饱和溶液三者之间的质量比为36:100:136=9:25:34。
问题:20℃时氯化钠和硝酸钾的溶解能力谁强?
常见物质的溶解度(20℃)
物质名称 氯化钠 氢氧化钙 蔗 糖 氯酸钾 氯化铵
硝酸钾
溶解度/克 36.0 0.165 203.9 7.4 37.2
31.6
“溶解之王”争霸赛—初步较量
难溶
微溶
可溶
易溶
0.01g
10g
1g
(4)溶解度与溶解性的关系:
提 示:
难溶习惯上称“不溶”,绝对不溶的物质是没有的。
硝酸钾在不同温度时的溶解度
(1)固体物质溶解度的表示方法
温度/℃ 0 10 20 30 40 50
溶解度/g 13.3 20.9 31.6 45.8 63.9 85.5
2. 固体物质的溶解度曲线
一、物质溶解性的定量表示
①列表法:
.
.
.
.
溶解度/
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
.
硝酸钾
.
.
.
.
以温度为横坐标,溶解度为纵坐标,在坐标纸上先找出不同温度下相应溶解度的点,再用光滑的曲线将这些点连接起来,即为该物质的溶解度曲线。
2. 固体物质的溶解度曲线
②曲线法:
(1)固体物质溶解度的表示方法
点
线
面
曲线上的点
曲线交点
陡升型
下降型
缓升型
曲线下方的面上的点
曲线上方的面上的点
(2)固体物质溶解度曲线的意义
某物质在对应温度下的溶解度
两物质在该温度下的溶解度相等
大多数固体物质,如KNO3
极少数固体物质,如Ca(OH)2
少数固体物质,如NaCl
对应温度下该溶液是不饱和溶液
对应温度下该溶液是饱和溶液且有未溶固体
溶解度/克
10
20
30
40
50
60
70
80
90
100
110
120
130
140
150
160
170
180
190
200
10
20
30
40
50
60
70
80
90
100
0
氯化钠
温度/℃
硝酸钾
判决:氯化钠和硝酸钾的溶解能力谁强?
23
温度<23℃时,氯化钠溶解能力较强;
温度=23℃时,两者溶解能力一样强;
温度>23℃时,硝酸钾溶解能力较强。
“溶解之王”争霸赛—终审判决
打开可乐盖时有气体冒出
畅饮可乐后会打嗝
打开瓶塞,压强减小,CO2溶解性减弱,所以从水中逸出
温度升高CO2溶解性减弱,从体内逸出
随着压强的增大,气体的溶解度增大
随着温度的升高,气体的溶解度减小
影响气体
溶解度的因素
3. 气体物质的溶解度
1. 20℃时,氯酸钾的溶解度是7.4g,它表示( )
A.100g水溶解7.4g氯酸钾达到饱和状态
B.20℃时,100g氯酸钾溶液中溶解氯酸钾7.4g,溶液达到饱和状态
C.20℃时,100g水最多只能溶解氯酸钾7.4
D.20℃时,100g水中最多只能溶解7.4g氯酸钾
D
【课堂训练】
2. 下列关于固体物质的溶解度叙述正确的是( )
A.20℃时,100g水中溶解了30g某物质,则20℃时该物质的溶解度为30g
B.20℃时,100g水中正好溶解了30g某物质达到饱和状态,则该物质的溶解度为30g
C.20℃时,某100g饱和溶液中有30g溶质,则20℃时该物质的溶解度为30g
D.20℃时,30g某物质需要100g水才能恰好完全溶解,则20℃时该物质的溶解度为30g
D
3. 木糖醇是目前市场上的一种蔗糖替代品,在某些温度下其溶解度分别为:30℃时为70g,50℃时为84g,60℃时为90g。如图表示的是木糖醇等固体的溶解度曲线。根据曲线判断,下列说法不正确的是( )
A.X为木糖醇的溶解度曲线
B.随着温度的升高,Z物质的溶解度逐渐减小
C.可以采用冷却热饱和溶液的方法获得Z的晶体
D.50℃时,Y的饱和溶液和Z的饱和溶液溶质的质量分数相等
C
第6章 溶解现象
第3节 物质的溶解性
(第2课时)
硝酸钾
白色粉末
易溶于水
氯化钠
俗名“食盐”
易溶于水
“溶解之王”争霸赛
20℃
40℃
氯化钠
硝酸钾
不行
应该在同一温度下
硝酸钾:我达到饱和状态时能溶解36.3克,你最多却只能溶解31.6克。我溶解得比你多,所以我是“溶解之王”。
硝酸钾
氯化钠
氯化钠:我最多能溶解47.4克,你最多却只能溶解36克。我溶解得比你多,所以我是“溶解之王”。
20℃
20℃
应该溶剂的量相同
不行
1克氯化钠
1克硝酸钾
20克水
硝酸钾:那我们都各取1克,都溶解在20克水中,结果都能溶解完。所以我们的溶解能力一样强。我们并列为“溶解之王”。
20℃
20℃
应该达到饱和状态
不行
一定状态(达到饱和)
定量地比较不同物质的溶解能力应该控制一定的条件:
一定温度
一定溶剂的量
溶解度
一、物质溶解性的定量表示
一、物质溶解性的定量表示
1. 固体物质的溶解度
(1)概念:在一定温度下,某固体物质在100g溶剂(通常溶剂为水)中达到饱和状态时所溶解的质量。
一定温度
(2)四要素:
①条件:一定温度 ②标准:100g溶剂
③状态:饱和状态 ④单位:克
S
一、物质溶解性的定量表示
1. 固体物质的溶解度
(3)含义:
一定温度
①指该物质在此温度下,在100g溶剂(通常溶剂为水)中达到饱和状态时所溶解的质量。
例:NaCl在20℃时的溶解度为36.0g。
指在20℃时,100g水中达到饱和状态时所溶解NaCl的质量为36.0g。(或在20℃时,100g水中最多溶解NaCl的质量为36.0g)。
一、物质溶解性的定量表示
1. 固体物质的溶解度
(3)含义:
一定温度
②指在此温度下,该物质的饱和溶液中,溶质、溶剂与饱和溶液三者之间的质量比=S:100g:(100g+S)。
例:NaCl在20℃时的溶解度为36.0g。
则在20℃时,任意质量的NaCl饱和状态中,NaCl、水、NaCl饱和溶液三者之间的质量比为36:100:136=9:25:34。
问题:20℃时氯化钠和硝酸钾的溶解能力谁强?
常见物质的溶解度(20℃)
物质名称 氯化钠 氢氧化钙 蔗 糖 氯酸钾 氯化铵
硝酸钾
溶解度/克 36.0 0.165 203.9 7.4 37.2
31.6
“溶解之王”争霸赛—初步较量
难溶
微溶
可溶
易溶
0.01g
10g
1g
(4)溶解度与溶解性的关系:
提 示:
难溶习惯上称“不溶”,绝对不溶的物质是没有的。
硝酸钾在不同温度时的溶解度
(1)固体物质溶解度的表示方法
温度/℃ 0 10 20 30 40 50
溶解度/g 13.3 20.9 31.6 45.8 63.9 85.5
2. 固体物质的溶解度曲线
一、物质溶解性的定量表示
①列表法:
.
.
.
.
溶解度/
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
.
硝酸钾
.
.
.
.
以温度为横坐标,溶解度为纵坐标,在坐标纸上先找出不同温度下相应溶解度的点,再用光滑的曲线将这些点连接起来,即为该物质的溶解度曲线。
2. 固体物质的溶解度曲线
②曲线法:
(1)固体物质溶解度的表示方法
点
线
面
曲线上的点
曲线交点
陡升型
下降型
缓升型
曲线下方的面上的点
曲线上方的面上的点
(2)固体物质溶解度曲线的意义
某物质在对应温度下的溶解度
两物质在该温度下的溶解度相等
大多数固体物质,如KNO3
极少数固体物质,如Ca(OH)2
少数固体物质,如NaCl
对应温度下该溶液是不饱和溶液
对应温度下该溶液是饱和溶液且有未溶固体
溶解度/克
10
20
30
40
50
60
70
80
90
100
110
120
130
140
150
160
170
180
190
200
10
20
30
40
50
60
70
80
90
100
0
氯化钠
温度/℃
硝酸钾
判决:氯化钠和硝酸钾的溶解能力谁强?
23
温度<23℃时,氯化钠溶解能力较强;
温度=23℃时,两者溶解能力一样强;
温度>23℃时,硝酸钾溶解能力较强。
“溶解之王”争霸赛—终审判决
打开可乐盖时有气体冒出
畅饮可乐后会打嗝
打开瓶塞,压强减小,CO2溶解性减弱,所以从水中逸出
温度升高CO2溶解性减弱,从体内逸出
随着压强的增大,气体的溶解度增大
随着温度的升高,气体的溶解度减小
影响气体
溶解度的因素
3. 气体物质的溶解度
1. 20℃时,氯酸钾的溶解度是7.4g,它表示( )
A.100g水溶解7.4g氯酸钾达到饱和状态
B.20℃时,100g氯酸钾溶液中溶解氯酸钾7.4g,溶液达到饱和状态
C.20℃时,100g水最多只能溶解氯酸钾7.4
D.20℃时,100g水中最多只能溶解7.4g氯酸钾
D
【课堂训练】
2. 下列关于固体物质的溶解度叙述正确的是( )
A.20℃时,100g水中溶解了30g某物质,则20℃时该物质的溶解度为30g
B.20℃时,100g水中正好溶解了30g某物质达到饱和状态,则该物质的溶解度为30g
C.20℃时,某100g饱和溶液中有30g溶质,则20℃时该物质的溶解度为30g
D.20℃时,30g某物质需要100g水才能恰好完全溶解,则20℃时该物质的溶解度为30g
D
3. 木糖醇是目前市场上的一种蔗糖替代品,在某些温度下其溶解度分别为:30℃时为70g,50℃时为84g,60℃时为90g。如图表示的是木糖醇等固体的溶解度曲线。根据曲线判断,下列说法不正确的是( )
A.X为木糖醇的溶解度曲线
B.随着温度的升高,Z物质的溶解度逐渐减小
C.可以采用冷却热饱和溶液的方法获得Z的晶体
D.50℃时,Y的饱和溶液和Z的饱和溶液溶质的质量分数相等
C
