第6章第2节溶液组成的表示-2021-2022学年九年级化学沪教版(全国)下册 (1)(word版含解析)
文档属性
| 名称 | 第6章第2节溶液组成的表示-2021-2022学年九年级化学沪教版(全国)下册 (1)(word版含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 199.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-01-28 00:00:00 | ||
图片预览




文档简介
第二节溶液组成的表示第六章溶解现象2021_2022学年九年级化学同步练习(沪教版全国)
一.选择题(共13小题)
1.要配制100g溶质质量分数为10%的氯化钠溶液,下列操作或说法正确的是( )
A.将10g氯化钠固体直接放在天平的托盘上称量
B.为加快固体溶解,用温度计搅拌溶液
C.配制该溶液需要经过计算、称量、溶解、装瓶贴标签等步骤
D.配制该溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯等
2.现有一瓶溶质质量分数为10%的食盐水,关于该食盐水的说法正确的是( )
A.m质:m剂=1:10 B.m质:m液=1:10
C.m质:m液=1:11 D.m剂:m液=10:11
3.下列做法中,会使配制一定溶质质量分数的氢氧化钠溶液浓度偏高的是( )
A.用量筒量取水时俯视读数
B.将氢氧化钠放在托盘天平的右盘称量
C.用蒸馏水润洗过的烧杯溶解氢氧化钠
D.用敞口放置的氢氧化钠固体配制溶液
4.配制一定质量分数的溶液,一般不需要的步骤是( )
A.计算所需溶质和溶剂的质量
B.用天平称取所需溶质,放入烧杯中
C.用量筒量取所需溶剂,放入同一烧杯中并充分搅拌
D.将配得的溶液进行过滤
5.向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤.下列说法正确的是( )
资料:A的溶解度
温度/℃ 20 30 40 50 60
溶解度/g 37.2 41.4 45.8 50.4 55.2
25℃100g水①②③④⑤
A.②中A的质量分数最大 B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液 D.①③④⑤中没有固体存在
6.配制溶质质量分数为5%的下列溶液,能达到目的的是( )
A.称取5.0 g氯化钾,解在95 mL 水中,充分搅拌
B.称取5.0 g生石灰,放入95 mL水中充分搅拌
C.量取5.0 mL浓盐酸,倒入95 mL 水中,充分搅拌
D.称取5.0 g碳酸钙,放入95 mL水中,充分搅拌
7.饱和溶液用水稀释变成不饱和溶液的过程中,保持不变的是( )
A.溶质的质量 B.溶剂的质量
C.溶液的质量 D.溶质与溶剂的质量比
8.稀释质量分数为98%(密度为1.84g/mL)的浓硫酸配制500mL质量分数为20%的稀硫酸(密度为1.14g/mL),稀释时需用的水的体积约为( )
A.436.8 mL B.453.7 mL C.456.0 mL D.458.3 mL
9.下列条件下的氯化氢气体的溶液即为盐酸,其溶质的质量分数最大的是( )
A.20℃的饱和溶液 B.20℃的不饱和溶液
C.80℃的饱和溶液 D.80℃的不饱和溶液
10.20℃时硝酸钾的溶解度是31.6g,则在该温度下硝酸钾饱和溶液中溶质的质量分数( )
A.24.0% B.31.6% C.46.2% D.63.2%
11.实验室用密度为1.84g/cm3、质量分数为98%的浓硫酸和蒸馏水,配制500g质量分数为20%的稀硫酸.需要用多少mL的量筒量取多少mL的浓硫酸?( )
A.100 mL 54.35 mL B.100 mL 55.5 mL
C.250 mL 54.35 mL D.250 mL 55.5 mL
12.已知氢气可以在氯气中燃烧,其反应的化学方程式为:H2+Cl22HCl.在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11:5:1,用电火花点燃,使其充分反应,冷却后所得溶液的质量分数为( )
A.40.3% B.28.9% C.44.8% D.30.5%
13.兴趣小组在实验室要配制20%的稀硫酸,用来完成探究硫酸的化学性质实验.某成员负责准备实验仪器,他不需要选择的是( )
A.托盘天平 B.量筒 C.胶头滴管 D.烧杯
二.填空题(共5小题)
14.水是重要的物质,在实验室中常用于溶解物质、配制溶液.根据下列仪器,欲配制一定质量分数的食盐溶液,回答下列问题.
(1)上面的仪器中除D、E外,还必须选用的仪器有 ;(填字母)
(2) E的作用是 ;
(3)配制的步骤可以概括为计算、 和量取、 、装瓶贴标签.
15.小盘同学配制质量分数为5%的氯化钠溶液100g,以备实验.
(1)通过计算,需称取氯化钠的质量为 g.
(2)配制该溶液所需要的玻璃仪器有:烧杯、量筒、胶头滴管和 (写仪器名称).
(3)量取水的体积时,小盘同学仰视读数,则配制的氯化钠溶液的质量分数将 (填“偏小”、“不变”或“偏大”).
16.溶质分数是表示 的一种方法,溶质质量分数= .
17.“84”消毒液是预防新冠肺炎经常使用的消杀用品。回答下列问题:
(1)其有效成分次氯酸钠(NaClO)中氯元素的化合价为 。
(2)“84”消毒液的消毒原理为2NaClO+CO2+X═Na2CO3+2HClO,生成的HClO(次氯酸)具有较强的杀菌作用。化学方程式中X的化学式为 。
(3)探究发现,暴露在空气中(阳光充足)的“84”消毒液的消毒效果随时间的推移而减弱。据此,你认为“84”消毒液应 保存。
(4)“84”消毒液有一定的刺激性与腐蚀性,必须稀释以后才能使用。将50g含NaClO 5%的“84”消毒液稀释至1%,需向原溶液中加入水的质量为 g。
18.固体物质的溶解性与溶解度之间的关系如下表所示:
20℃时溶解度/g >10 10﹣1 1﹣0.01 <0.01
溶解性 易溶 可溶 微溶 难溶
M、N两种固体物质的溶解度曲线如图所示,试完成下列问题:
(1)M物质的溶解性属于 。
(2)在20℃时,M、N两种物质的 相等。
(3)在30℃时,将20gM物质(不含结晶水)完全溶于100g水中,得到不饱和溶液,若要将其转化成饱和溶液,下列措施可采取的是 。
A.再加入30gM物质B.将温度降低到10℃.倒掉溶液30g。
三.实验探究题(共1小题)
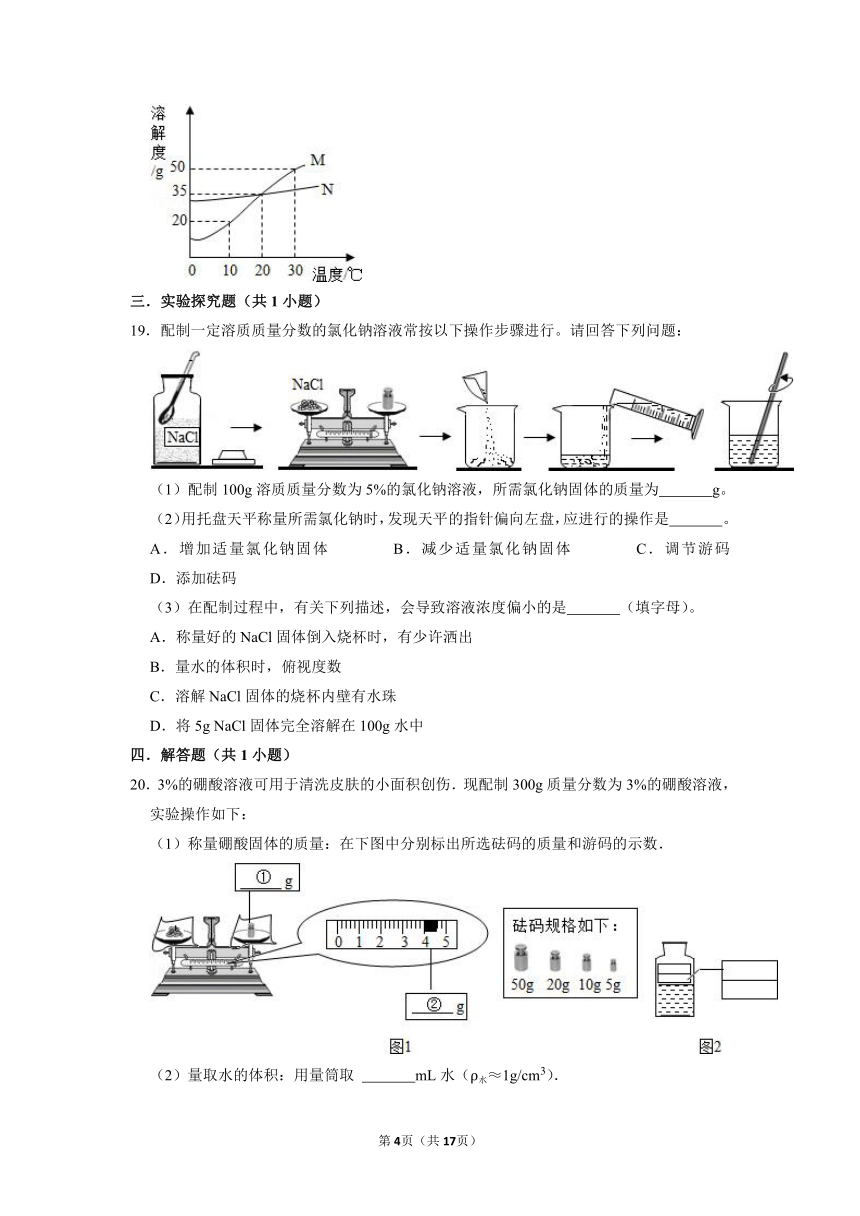
19.配制一定溶质质量分数的氯化钠溶液常按以下操作步骤进行。请回答下列问题:
(1)配制100g溶质质量分数为5%的氯化钠溶液,所需氯化钠固体的质量为 g。
(2)用托盘天平称量所需氯化钠时,发现天平的指针偏向左盘,应进行的操作是 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码
(3)在配制过程中,有关下列描述,会导致溶液浓度偏小的是 (填字母)。
A.称量好的NaCl固体倒入烧杯时,有少许洒出
B.量水的体积时,俯视度数
C.溶解NaCl固体的烧杯内壁有水珠
D.将5g NaCl固体完全溶解在100g水中
四.解答题(共1小题)
20.3%的硼酸溶液可用于清洗皮肤的小面积创伤.现配制300g质量分数为3%的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数.
(2)量取水的体积:用量筒取 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 .
(4)装瓶、贴标签:在右图的标签中填上相应的内容.
第二节溶液组成的表示第六章溶解现象2021_2022学年九年级化学同步练习(沪教版全国)
参考答案与试题解析
一.选择题(共13小题)
1.要配制100g溶质质量分数为10%的氯化钠溶液,下列操作或说法正确的是( )
A.将10g氯化钠固体直接放在天平的托盘上称量
B.为加快固体溶解,用温度计搅拌溶液
C.配制该溶液需要经过计算、称量、溶解、装瓶贴标签等步骤
D.配制该溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯等
【分析】根据溶液配制的知识进行分析,称量氯化钠固体需要放在纸上进行,使用量筒量取水的体积,溶解时使用玻璃棒进行搅拌。
【解答】解:A、称量固体时要将食盐放在纸上进行,故A错误;
B、进行搅拌时需要使用玻璃棒进行,不能使用温度计,故C错误;
C、配制该溶液需要经过计算、称量、溶解,配好的氯化钠溶液需要倒进细口瓶中贴标签备用,故C正确;
D、托盘天平用于称取固体氯化钠,量筒用于量取水,烧杯用于完成溶解操作,无需使用酒精灯,故D错误。
故选:C。
【点评】本题考查了溶液的配制,完成此题,可以依据已有的知识进行。
2.现有一瓶溶质质量分数为10%的食盐水,关于该食盐水的说法正确的是( )
A.m质:m剂=1:10 B.m质:m液=1:10
C.m质:m液=1:11 D.m剂:m液=10:11
【分析】根据溶液中的组成(即溶质和溶剂)判断和溶质的质量分数的概念及其含义,便可推算出正确的答案。
【解答】解:根据溶液中的组成判断可知,食盐水的溶质是食盐,溶剂是水。
由题意可知,该食盐水中溶质的质量分数为10%.也就是,溶质质量与溶液质量之比是:10:100(即1:10)。因此,B选项是正确的;C选项不正确。
A.m质:m剂=1:9,所以该选项不对。
D.m剂:m液=9:10.所以该选项也不对。
故选:B。
【点评】本题主要考查了溶液中溶质质量分数的概念及其含义等;当然,也考查了溶液组成的判断。因此,这是一道比较简单的题目。解答时,只要抓住溶质质量分数的概念及其含义,结合溶液的组成,细心地推断即可。
3.下列做法中,会使配制一定溶质质量分数的氢氧化钠溶液浓度偏高的是( )
A.用量筒量取水时俯视读数
B.将氢氧化钠放在托盘天平的右盘称量
C.用蒸馏水润洗过的烧杯溶解氢氧化钠
D.用敞口放置的氢氧化钠固体配制溶液
【分析】根据溶质质量分数变大,则可能是溶质质量偏大或溶剂质量偏小,可以分析出可能造成这两个方面错误的原因进行分析解答。
【解答】解:A、用量筒量取水读数时,俯视读数,量取的水少了,所以溶质质量分数偏大,正确;
B、将氢氧化钠放在托盘天平的右盘称量,则会导致称量的氢氧化钠固体减小,则使溶质质量分数偏小,错误;
C、用刚洗涤的烧杯溶解氢氧化钠,溶剂多了,溶质的质量分数偏低,错误;
D、将固体氢氧化钠放在敞口容器中,固体NaOH已部分变质,生成碳酸钠,所以氢氧化钠质量减少,溶质质量分数会减少,错误;
故选:A。
【点评】本题考查了导致溶质质量分数偏高的因素,完成此题,可以依据溶质质量分数公式进行。
4.配制一定质量分数的溶液,一般不需要的步骤是( )
A.计算所需溶质和溶剂的质量
B.用天平称取所需溶质,放入烧杯中
C.用量筒量取所需溶剂,放入同一烧杯中并充分搅拌
D.将配得的溶液进行过滤
【分析】根据配制一定溶质质量分数的溶液时,先计算出需溶质的质量和所需水的体积,用托盘天平称量出溶质加入烧杯内,再用量筒量取水倒入烧杯内,用玻璃棒搅拌。即可配成溶液解答。
【解答】解:先计算出需溶质的质量和所需水的体积,用托盘天平称量出溶质加入烧杯内,再用量筒量取水倒入烧杯内,用玻璃棒搅拌至氢氧化钠完全溶解。
过滤是将不溶性固体和可溶性固体分离分方法,不需要将配得的溶液进行过滤。
故选:D。
【点评】熟记使用固体(液体)溶质配制溶液的基本步骤:计算、称量(量取)、溶解。
5.向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤.下列说法正确的是( )
资料:A的溶解度
温度/℃ 20 30 40 50 60
溶解度/g 37.2 41.4 45.8 50.4 55.2
25℃100g水①②③④⑤
A.②中A的质量分数最大 B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液 D.①③④⑤中没有固体存在
【分析】溶解度为一定温度下,100g水溶解溶质达到饱和状态时所溶解溶质的质量;结合A物质在不同温度下的溶解度,根据溶液变化流程中的条件,判断物质的溶解及所得溶液的状态或组成;由资料中物质A的溶解度可知,物质A的溶解度随温度升高而增大.
【解答】解:A、根据A物质在30℃的溶解度为41.4g、60℃的溶解度为55.2g,可判断41.4g物质A在25℃时不能完全溶解而在60℃时可以全部溶解且为不饱和溶液,则溶液②的溶质质量分数小于溶液③的溶质质量分数。故A不正确;
B、溶液③为60℃时100g水溶解41.4gA物质所形成的溶液,溶液中溶质的质量分数=×100%≈29.3%;
溶液⑤为50℃时100g水溶解50.4gA的饱和溶液,溶液中溶质的质量分数=×100%≈33.5%;故B不正确;
C、综合A、B项分析可知:溶液②⑤为饱和溶液;60℃A的溶解度为55.2g,溶液④为60℃时100g水溶解50.4gA,可判断此时溶液为不饱和溶液;故C不正确;
D、根据20℃A的溶解度为37.2g可判断,25℃时37.2gA溶解在100g水中形成不饱和溶液,没有固体存在;综合A、B、C项分析,溶液③④均为不饱和溶液,没有固体存在;而溶液⑤恰好饱和,没有固体存在。故D正确;
故选:D。
【点评】利用物质的溶解度判断溶液的状态时,要明确溶解度是在该温度下100g水所能溶解溶质的最大质量.
6.配制溶质质量分数为5%的下列溶液,能达到目的的是( )
A.称取5.0 g氯化钾,解在95 mL 水中,充分搅拌
B.称取5.0 g生石灰,放入95 mL水中充分搅拌
C.量取5.0 mL浓盐酸,倒入95 mL 水中,充分搅拌
D.称取5.0 g碳酸钙,放入95 mL水中,充分搅拌
【分析】本题应从溶质质量分数的计算和物质的溶解性等多方面考虑.
A、氯化钾溶解于水根据数据计算可确定;
B、生石灰于水反应生成熟石灰,熟石灰微溶于水;
C、5.0mL浓盐酸是溶液的体积;
D、碳酸钙不溶于水;
【解答】解:A、氯化钾能溶解于水,5.0g氯化钾,溶解在95mL.水中计算溶质质量分数为5g÷(5g+95g)═5%;
B、生石灰于水反应生成熟石灰,熟石灰微溶于水,故错;
C、5.0mL浓盐酸是溶液的体积不能得出溶质氯化氢的质量,故不能求得溶质质量分数,故错;
D、碳酸钙不溶于水;不能得到溶液,故错;
故选:A。
【点评】充分考虑溶质质量分数的计算和物质的溶解性,才能准确把握此题,得出一个正确的结果.
7.饱和溶液用水稀释变成不饱和溶液的过程中,保持不变的是( )
A.溶质的质量 B.溶剂的质量
C.溶液的质量 D.溶质与溶剂的质量比
【分析】根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答。
【解答】解:饱和溶液用水稀释变成不饱和溶液的过程中,溶质质量不变,溶剂质量增加,溶液的质量增加。
A、饱和溶液用水稀释变成不饱和溶液的过程中,溶质的质量不变,故选项正确。
B、饱和溶液用水稀释变成不饱和溶液的过程中,溶剂的质量增加,故选项错误。
C、饱和溶液用水稀释变成不饱和溶液的过程中,溶液的质量增加,故选项错误。
D、饱和溶液用水稀释变成不饱和溶液的过程中,溶质与溶剂的质量比发生改变,故选项错误。
故选:A。
【点评】本题难度不大,考查溶液的稀释问题,掌握溶液稀释前后溶质的质量不变是正确解答此类题的关键所在。
8.稀释质量分数为98%(密度为1.84g/mL)的浓硫酸配制500mL质量分数为20%的稀硫酸(密度为1.14g/mL),稀释时需用的水的体积约为( )
A.436.8 mL B.453.7 mL C.456.0 mL D.458.3 mL
【分析】根据m=ρV计算出溶液的质量、溶质的质量=溶液的质量×溶质的质量分数、浓溶液配制稀溶液的过程中溶质的质量不变列式计算,再根据稀溶液与浓溶液的质量差来计算水的质量,进一步得到需要水的体积.
【解答】解:根据稀释过程中溶质的质量不变,设需浓硫酸的体积为x,可得:
1.84g/mL×x×98%=1.14g/mL×500mL×20% x≈63.2mL
需要水的质量为:1.14g/mL×500mL﹣1.84g/mL×63.2mL≈453.7g(合453.7mL)。
故选:B。
【点评】本题难度不大,考查溶液的稀释问题,掌握溶液稀释前后溶质的质量不变是正确解答此类题的关键所在.
9.下列条件下的氯化氢气体的溶液即为盐酸,其溶质的质量分数最大的是( )
A.20℃的饱和溶液 B.20℃的不饱和溶液
C.80℃的饱和溶液 D.80℃的不饱和溶液
【分析】根据温度对氯化氢气体的溶解度的影响和溶质质量分数和溶解度的关系解答.
【解答】解:由于同一温度下饱和溶液和不饱和溶液的溶质质量分数肯定是饱和溶液的溶质质量分数大,故20℃时的饱和氯化氢气体的溶液比不饱和氯化氢气体的溶液的溶质质量分数大;由于氯化氢气体的溶解度随温度的升高而减少。所以,故20℃时的饱和氯化氢气体的溶液比80℃的饱和氯化氢气体的溶液的溶质质量分数大。可以上分析可知:
A、溶质的质量分数最大的是20℃的饱和溶液。故A符合题意;
B、20℃的不饱和溶液比20℃的饱和溶液溶质的质量分数最小。故B不符合题意;
C、80℃的饱和溶液比20℃的饱和溶液溶质的质量分数最小。故C不符合题意;
D、80℃的不饱和溶液溶质的质量分数较小。故D不符合题意。
故选:A。
【点评】解答本题的关键是了解同一温度下饱和溶液和不饱和溶液的溶质质量分数肯定是饱和溶液的溶质质量分数大,气体的溶解度图温度的关系.
10.20℃时硝酸钾的溶解度是31.6g,则在该温度下硝酸钾饱和溶液中溶质的质量分数( )
A.24.0% B.31.6% C.46.2% D.63.2%
【分析】根据溶解度的概念:每100克水中最多溶解溶质的质量进行解答。
【解答】解:20℃时硝酸钾的溶解度是31.6g,即20℃时100g水中最多溶解硝酸钾的质量是31.6g,所以该温度下硝酸钾饱和溶液中溶质的质量分数=×100%=24.0%。
故选:A。
【点评】题主要考查溶解度概念的理解与掌握和溶液中溶质的质量分数的计算方法及应用,并能灵活应用于解题。
11.实验室用密度为1.84g/cm3、质量分数为98%的浓硫酸和蒸馏水,配制500g质量分数为20%的稀硫酸.需要用多少mL的量筒量取多少mL的浓硫酸?( )
A.100 mL 54.35 mL B.100 mL 55.5 mL
C.250 mL 54.35 mL D.250 mL 55.5 mL
【分析】根据溶液稀释前后溶质的质量不变计算所需浓硫酸的质量,由密度计算公式计算所需浓硫酸的体积,从减小实验误差的角度去选择量筒的量程,据此进行分析解答.
【解答】解:稀释浓硫酸时,根据溶质的质量=溶液的质量×溶质的质量分数、稀释前后溶质质量不变,设所需98%的浓硫酸的质量为x,则500g×20%=x×98%,x≈102g,由密度公式求得浓硫酸体积为≈55.5mL。
量筒能保证量取一次,且量程与液体的取用量最接近,所以误差最小。故准确量取55.5mL的浓硫酸,选用的量筒规格是100mL。
故选:B。
【点评】本题难度不大,掌握稀释前后溶质质量不变、溶质的质量=溶液的质量×溶质的质量分数等是正确解答本题的关键.
12.已知氢气可以在氯气中燃烧,其反应的化学方程式为:H2+Cl22HCl.在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11:5:1,用电火花点燃,使其充分反应,冷却后所得溶液的质量分数为( )
A.40.3% B.28.9% C.44.8% D.30.5%
【分析】氢气在氯气中燃烧生成氯化氢,氢气在氧气中燃烧生成水,冷却后提得溶液为氯化氢溶液;
计算氯化氢溶液的溶质质量分数,需要氯化氢和水的质量,根据反应的化学方程式,由H2、O2、Cl2的混合气体分子数之比为11:5:1,通过拟定数据的方法,可推断出反应生成HCl与H2O的质量比,从而完成所得溶液的质量分数的计算。
【解答】解:假设密闭容器中氯气分子个数为1,根据题意,则氧气分子个数为5,氢气分子个数为11
根据化学方程式H2+Cl22HCl可知:1分子氯气消耗1分子的氢气生成2分子氯化氢;
根据化学方程式2H2+O22H2O可知:5分子氧气可支持10分子氢气完全燃烧生成10分子水;
H2、O2、Cl2的混合气体分子数之比为11:5:1,用电火花点燃,使其充分反应,恰好完全反应,生成HCl与H2O的分子个数比为2:10=1:5;则生成HCl与H2O的质量比=36.5:90;因此,所得溶液的质量分数=≈28.9%
故选:B。
【点评】解决本题时,需要通过相对分子质量把物质的分子个数比转换成物质的质量比。
13.兴趣小组在实验室要配制20%的稀硫酸,用来完成探究硫酸的化学性质实验.某成员负责准备实验仪器,他不需要选择的是( )
A.托盘天平 B.量筒 C.胶头滴管 D.烧杯
【分析】用浓硫酸配制质量分数为20%的稀硫酸溶液,步骤为计算、量取(量取浓硫酸和水)、溶解,根据各操作所需要使用的仪器,判断所列仪器是否需要.
【解答】解:用浓硫酸配制质量分数为20%的稀硫酸溶液,首先计算配制溶液所需浓硫酸和水的质量,再量取浓硫酸和水,最后进行溶解;在这些操作中需要的仪器:量筒、胶头滴管、烧杯和玻璃棒。故不需要使用托盘天平。
故选:A。
【点评】本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键.
二.填空题(共5小题)
14.水是重要的物质,在实验室中常用于溶解物质、配制溶液.根据下列仪器,欲配制一定质量分数的食盐溶液,回答下列问题.
(1)上面的仪器中除D、E外,还必须选用的仪器有 BG ;(填字母)
(2) E的作用是 搅拌,加快食盐的溶解速率 ;
(3)配制的步骤可以概括为计算、 称量 和量取、 溶解 、装瓶贴标签.
【分析】(1)配制一定溶质质量分数的食盐溶液的操作步骤分别是:计算、称量、溶解,根据各操作所需要使用的仪器,判断所列仪器是否需要.
(2)根据玻璃棒的作用,进行分析解答.
(3)根据配制一定溶质质量分数的食盐溶液的操作步骤进行分析解答.
【解答】解:(1)配制一定溶质质量分数的食盐溶液的操作步骤分别是:计算、称量、溶解;托盘天平用于称取固体食盐、量筒用于量取水、烧杯用于完成溶解操作、玻璃棒用于溶解时的搅拌,上面的仪器中除D、E外,还必须选用的仪器有BG.
(2)玻璃棒用于溶解时的搅拌,加快食盐的溶解速率.
(3)配制一定质量分数的食盐溶液,首先计算配制溶液所需食盐和水的质量,再称量所需的食盐和量取水,最后进行溶解、装瓶贴标签.
故答案为:(1)BG;(2)搅拌,加快食盐的溶解速率;(3)称量;溶解.
【点评】本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键.
15.小盘同学配制质量分数为5%的氯化钠溶液100g,以备实验.
(1)通过计算,需称取氯化钠的质量为 5 g.
(2)配制该溶液所需要的玻璃仪器有:烧杯、量筒、胶头滴管和 玻璃棒 (写仪器名称).
(3)量取水的体积时,小盘同学仰视读数,则配制的氯化钠溶液的质量分数将 偏小 (填“偏小”、“不变”或“偏大”).
【分析】(1)溶质质量=溶液质量×溶质的质量分数,据此进行分析解答.
(2)根据配制溶质质量分数一定的溶液的步骤分析解答需要的仪器,进行分析解答.
(3)仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,据此进行分析解答.
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制质量分数为5%的氯化钠溶液100g,需称取氯化钠的质量为100g×5%=5g.
(2)配制质量分数为5%的氯化钠溶液100g,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,其中属于玻璃仪器的是玻璃棒、烧杯、胶头滴管、量筒.
(3)仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小.
故答案为:(1)5;(2)玻璃棒;(3)偏小.
【点评】本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.
16.溶质分数是表示 溶液浓度 的一种方法,溶质质量分数= ×100% .
【分析】溶质的质量分数表示的是溶液的浓度的高低,是溶质质量与溶液的质量的比值.
【解答】解:溶液质量分数是表示溶液浓度的一种方法,其数学意义是溶质质量与溶液质量之比.
故答案是:溶液浓度;×100%.
【点评】本题难度不大,掌握溶质质量分数的概念、含义等即可正确解答本题.
17.“84”消毒液是预防新冠肺炎经常使用的消杀用品。回答下列问题:
(1)其有效成分次氯酸钠(NaClO)中氯元素的化合价为 +1 。
(2)“84”消毒液的消毒原理为2NaClO+CO2+X═Na2CO3+2HClO,生成的HClO(次氯酸)具有较强的杀菌作用。化学方程式中X的化学式为 H2O 。
(3)探究发现,暴露在空气中(阳光充足)的“84”消毒液的消毒效果随时间的推移而减弱。据此,你认为“84”消毒液应 避光密封 保存。
(4)“84”消毒液有一定的刺激性与腐蚀性,必须稀释以后才能使用。将50g含NaClO 5%的“84”消毒液稀释至1%,需向原溶液中加入水的质量为 200 g。
【分析】(1)根据化合物中元素的化合价的计算方法以及离子符号的写法来分析;
(2)根据质量守恒定律来分析;
(3)根据药品的性质与保存方法来分析;
(4)根据溶液加水稀释过程中,溶质的质量不变来分析。
【解答】解:(1)在NaClO中,钠元素的化合价是+1,氧元素的化合价是﹣2,设氯元素的化合价是x,则有(+1)+x+(﹣2)=0,解得x=+1;
(2)根据反应的化学方程式2NaClO+CO2+X═Na2CO3+2HClO,反应物中钠、氯、碳、氧原子个数分别为2、2、1、4,反应后的生成物中钠、氯、碳、氢、氧原子个数分别为2、2、1、2、5,根据反应前后原子种类、数目不变,则每个X分子由2个氢原子、1个氧原子构成,则物质X的化学式为H2O;
(3)曝露在空气中(阳光充足)的“84”消毒液的消毒效果随时间的推移而减弱,所以“84”消毒液应避光密封保存;
(4)设需要加水的质量为x,则:
50g×5%=(50g+x)×1%
x=200g。
故答案为:(1)+1;(2)H2O;(3)避光密封;(4)200。
【点评】本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学反应前后原子守恒、信息应用以及有关溶液的计算等并能灵活运用是正确解答本题的关键。
18.固体物质的溶解性与溶解度之间的关系如下表所示:
20℃时溶解度/g >10 10﹣1 1﹣0.01 <0.01
溶解性 易溶 可溶 微溶 难溶
M、N两种固体物质的溶解度曲线如图所示,试完成下列问题:
(1)M物质的溶解性属于 易溶 。
(2)在20℃时,M、N两种物质的 溶解度 相等。
(3)在30℃时,将20gM物质(不含结晶水)完全溶于100g水中,得到不饱和溶液,若要将其转化成饱和溶液,下列措施可采取的是 AB 。
A.再加入30gM物质B.将温度降低到10℃.倒掉溶液30g。
【分析】物质的溶解性的强弱,是根据在20℃时的溶解度来确定的,若溶解度大于10g,属于易溶物质。溶解度大于1g,属于可溶物质。溶解度大于0.01g的,属于微溶物质。
【解答】解:(1)由曲线图中查出20℃时,M的溶解度为35g,大于10g,属易溶。
(2)20℃时,M、N的溶解度曲线相交,说明它们的溶解度相等。
(3)由曲线图看出,30℃时,M溶液要变成饱和,需要再加入30gM,或将温度降低到10℃。
故答案为:(1)易溶。
(2)溶解度。
(3)AB。
【点评】对于溶解度受温度影响较大的固体物质来说,可以通过改变温度的方法,使不饱和溶液变为饱和溶液。
三.实验探究题(共1小题)
19.配制一定溶质质量分数的氯化钠溶液常按以下操作步骤进行。请回答下列问题:
(1)配制100g溶质质量分数为5%的氯化钠溶液,所需氯化钠固体的质量为 5 g。
(2)用托盘天平称量所需氯化钠时,发现天平的指针偏向左盘,应进行的操作是 B 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码
(3)在配制过程中,有关下列描述,会导致溶液浓度偏小的是 ACD (填字母)。
A.称量好的NaCl固体倒入烧杯时,有少许洒出
B.量水的体积时,俯视度数
C.溶解NaCl固体的烧杯内壁有水珠
D.将5g NaCl固体完全溶解在100g水中
【分析】(1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量。
(2)使用托盘天平称量药品时应遵循“左物右码”,称量过程中他发现指针偏左了,说明药品质量大于砝码质量,应减少药品。
(3)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答。
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;
(2)用托盘天平称量5g固体药品NaCl时,步骤是:调节天平平衡,在右盘上加砝码和拨动游码,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl。
(3)A、称量好的NaCl固体倒入烧杯时,有少许洒出,溶质偏少,则使溶质质量分数偏小,故选项正确。
B、用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,故选项不正确。
C、溶解NaCl固体的烧杯内壁有水珠,多取了水,则使溶质质量分数偏小,故选项正确。
D、将5g NaCl固体完全溶解在100g水中,溶液质量大于100g,溶质质量分数偏小,故选项正确。
故答案为:(1)5,95,100;(2)B;(3)ACD。
【点评】本题难度不大,明确一定溶质质量分数溶液的配制的步骤、所需仪器、注意事项等是正确解答此类题的关键。
四.解答题(共1小题)
20.3%的硼酸溶液可用于清洗皮肤的小面积创伤.现配制300g质量分数为3%的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数.
(2)量取水的体积:用量筒取 291 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 烧杯、玻璃棒 .
(4)装瓶、贴标签:在右图的标签中填上相应的内容.
【分析】(1)根据溶质质量=溶液质量×溶质的质量分数,计算出所需硼酸固体的质量,进而确定所选砝码的质量和游码的示数.
(2)溶剂质量=溶液质量﹣溶质质量,据此进行分析解答.
(3)根据溶解操作所需的仪器,进行分析判断.
(4)标签中填上相应的内容是溶液的名称、溶质的质量分数,进行分析解答.
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制300g质量分数为3%的硼酸溶液,所需硼酸固体的质量为300g×3%=9g;选用5g的砝码,游码拨到4g处即可.
(2)溶剂质量=溶液质量﹣溶质质量,则所需水的质量=300g﹣9g=291g(合291mL).
(3)溶解用到的玻璃仪器是烧杯、玻璃棒.
(4)标签中填上相应的内容是溶液的名称、溶质的质量分数,图2的标签中填上相应的内容是硼酸溶液,3%.
故答案为:(1)5g;4g;(2)291;(3)烧杯、玻璃棒;(4)硼酸溶液,3%.
【点评】本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.
声明:试题解析著作权属所有,未经书面同意,不得复制发布
日期:2022/1/27 20:15:00;用户:15877047552;邮箱:15877047552;学号:38945411第2页(共2页)
一.选择题(共13小题)
1.要配制100g溶质质量分数为10%的氯化钠溶液,下列操作或说法正确的是( )
A.将10g氯化钠固体直接放在天平的托盘上称量
B.为加快固体溶解,用温度计搅拌溶液
C.配制该溶液需要经过计算、称量、溶解、装瓶贴标签等步骤
D.配制该溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯等
2.现有一瓶溶质质量分数为10%的食盐水,关于该食盐水的说法正确的是( )
A.m质:m剂=1:10 B.m质:m液=1:10
C.m质:m液=1:11 D.m剂:m液=10:11
3.下列做法中,会使配制一定溶质质量分数的氢氧化钠溶液浓度偏高的是( )
A.用量筒量取水时俯视读数
B.将氢氧化钠放在托盘天平的右盘称量
C.用蒸馏水润洗过的烧杯溶解氢氧化钠
D.用敞口放置的氢氧化钠固体配制溶液
4.配制一定质量分数的溶液,一般不需要的步骤是( )
A.计算所需溶质和溶剂的质量
B.用天平称取所需溶质,放入烧杯中
C.用量筒量取所需溶剂,放入同一烧杯中并充分搅拌
D.将配得的溶液进行过滤
5.向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤.下列说法正确的是( )
资料:A的溶解度
温度/℃ 20 30 40 50 60
溶解度/g 37.2 41.4 45.8 50.4 55.2
25℃100g水①②③④⑤
A.②中A的质量分数最大 B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液 D.①③④⑤中没有固体存在
6.配制溶质质量分数为5%的下列溶液,能达到目的的是( )
A.称取5.0 g氯化钾,解在95 mL 水中,充分搅拌
B.称取5.0 g生石灰,放入95 mL水中充分搅拌
C.量取5.0 mL浓盐酸,倒入95 mL 水中,充分搅拌
D.称取5.0 g碳酸钙,放入95 mL水中,充分搅拌
7.饱和溶液用水稀释变成不饱和溶液的过程中,保持不变的是( )
A.溶质的质量 B.溶剂的质量
C.溶液的质量 D.溶质与溶剂的质量比
8.稀释质量分数为98%(密度为1.84g/mL)的浓硫酸配制500mL质量分数为20%的稀硫酸(密度为1.14g/mL),稀释时需用的水的体积约为( )
A.436.8 mL B.453.7 mL C.456.0 mL D.458.3 mL
9.下列条件下的氯化氢气体的溶液即为盐酸,其溶质的质量分数最大的是( )
A.20℃的饱和溶液 B.20℃的不饱和溶液
C.80℃的饱和溶液 D.80℃的不饱和溶液
10.20℃时硝酸钾的溶解度是31.6g,则在该温度下硝酸钾饱和溶液中溶质的质量分数( )
A.24.0% B.31.6% C.46.2% D.63.2%
11.实验室用密度为1.84g/cm3、质量分数为98%的浓硫酸和蒸馏水,配制500g质量分数为20%的稀硫酸.需要用多少mL的量筒量取多少mL的浓硫酸?( )
A.100 mL 54.35 mL B.100 mL 55.5 mL
C.250 mL 54.35 mL D.250 mL 55.5 mL
12.已知氢气可以在氯气中燃烧,其反应的化学方程式为:H2+Cl22HCl.在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11:5:1,用电火花点燃,使其充分反应,冷却后所得溶液的质量分数为( )
A.40.3% B.28.9% C.44.8% D.30.5%
13.兴趣小组在实验室要配制20%的稀硫酸,用来完成探究硫酸的化学性质实验.某成员负责准备实验仪器,他不需要选择的是( )
A.托盘天平 B.量筒 C.胶头滴管 D.烧杯
二.填空题(共5小题)
14.水是重要的物质,在实验室中常用于溶解物质、配制溶液.根据下列仪器,欲配制一定质量分数的食盐溶液,回答下列问题.
(1)上面的仪器中除D、E外,还必须选用的仪器有 ;(填字母)
(2) E的作用是 ;
(3)配制的步骤可以概括为计算、 和量取、 、装瓶贴标签.
15.小盘同学配制质量分数为5%的氯化钠溶液100g,以备实验.
(1)通过计算,需称取氯化钠的质量为 g.
(2)配制该溶液所需要的玻璃仪器有:烧杯、量筒、胶头滴管和 (写仪器名称).
(3)量取水的体积时,小盘同学仰视读数,则配制的氯化钠溶液的质量分数将 (填“偏小”、“不变”或“偏大”).
16.溶质分数是表示 的一种方法,溶质质量分数= .
17.“84”消毒液是预防新冠肺炎经常使用的消杀用品。回答下列问题:
(1)其有效成分次氯酸钠(NaClO)中氯元素的化合价为 。
(2)“84”消毒液的消毒原理为2NaClO+CO2+X═Na2CO3+2HClO,生成的HClO(次氯酸)具有较强的杀菌作用。化学方程式中X的化学式为 。
(3)探究发现,暴露在空气中(阳光充足)的“84”消毒液的消毒效果随时间的推移而减弱。据此,你认为“84”消毒液应 保存。
(4)“84”消毒液有一定的刺激性与腐蚀性,必须稀释以后才能使用。将50g含NaClO 5%的“84”消毒液稀释至1%,需向原溶液中加入水的质量为 g。
18.固体物质的溶解性与溶解度之间的关系如下表所示:
20℃时溶解度/g >10 10﹣1 1﹣0.01 <0.01
溶解性 易溶 可溶 微溶 难溶
M、N两种固体物质的溶解度曲线如图所示,试完成下列问题:
(1)M物质的溶解性属于 。
(2)在20℃时,M、N两种物质的 相等。
(3)在30℃时,将20gM物质(不含结晶水)完全溶于100g水中,得到不饱和溶液,若要将其转化成饱和溶液,下列措施可采取的是 。
A.再加入30gM物质B.将温度降低到10℃.倒掉溶液30g。
三.实验探究题(共1小题)
19.配制一定溶质质量分数的氯化钠溶液常按以下操作步骤进行。请回答下列问题:
(1)配制100g溶质质量分数为5%的氯化钠溶液,所需氯化钠固体的质量为 g。
(2)用托盘天平称量所需氯化钠时,发现天平的指针偏向左盘,应进行的操作是 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码
(3)在配制过程中,有关下列描述,会导致溶液浓度偏小的是 (填字母)。
A.称量好的NaCl固体倒入烧杯时,有少许洒出
B.量水的体积时,俯视度数
C.溶解NaCl固体的烧杯内壁有水珠
D.将5g NaCl固体完全溶解在100g水中
四.解答题(共1小题)
20.3%的硼酸溶液可用于清洗皮肤的小面积创伤.现配制300g质量分数为3%的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数.
(2)量取水的体积:用量筒取 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 .
(4)装瓶、贴标签:在右图的标签中填上相应的内容.
第二节溶液组成的表示第六章溶解现象2021_2022学年九年级化学同步练习(沪教版全国)
参考答案与试题解析
一.选择题(共13小题)
1.要配制100g溶质质量分数为10%的氯化钠溶液,下列操作或说法正确的是( )
A.将10g氯化钠固体直接放在天平的托盘上称量
B.为加快固体溶解,用温度计搅拌溶液
C.配制该溶液需要经过计算、称量、溶解、装瓶贴标签等步骤
D.配制该溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯等
【分析】根据溶液配制的知识进行分析,称量氯化钠固体需要放在纸上进行,使用量筒量取水的体积,溶解时使用玻璃棒进行搅拌。
【解答】解:A、称量固体时要将食盐放在纸上进行,故A错误;
B、进行搅拌时需要使用玻璃棒进行,不能使用温度计,故C错误;
C、配制该溶液需要经过计算、称量、溶解,配好的氯化钠溶液需要倒进细口瓶中贴标签备用,故C正确;
D、托盘天平用于称取固体氯化钠,量筒用于量取水,烧杯用于完成溶解操作,无需使用酒精灯,故D错误。
故选:C。
【点评】本题考查了溶液的配制,完成此题,可以依据已有的知识进行。
2.现有一瓶溶质质量分数为10%的食盐水,关于该食盐水的说法正确的是( )
A.m质:m剂=1:10 B.m质:m液=1:10
C.m质:m液=1:11 D.m剂:m液=10:11
【分析】根据溶液中的组成(即溶质和溶剂)判断和溶质的质量分数的概念及其含义,便可推算出正确的答案。
【解答】解:根据溶液中的组成判断可知,食盐水的溶质是食盐,溶剂是水。
由题意可知,该食盐水中溶质的质量分数为10%.也就是,溶质质量与溶液质量之比是:10:100(即1:10)。因此,B选项是正确的;C选项不正确。
A.m质:m剂=1:9,所以该选项不对。
D.m剂:m液=9:10.所以该选项也不对。
故选:B。
【点评】本题主要考查了溶液中溶质质量分数的概念及其含义等;当然,也考查了溶液组成的判断。因此,这是一道比较简单的题目。解答时,只要抓住溶质质量分数的概念及其含义,结合溶液的组成,细心地推断即可。
3.下列做法中,会使配制一定溶质质量分数的氢氧化钠溶液浓度偏高的是( )
A.用量筒量取水时俯视读数
B.将氢氧化钠放在托盘天平的右盘称量
C.用蒸馏水润洗过的烧杯溶解氢氧化钠
D.用敞口放置的氢氧化钠固体配制溶液
【分析】根据溶质质量分数变大,则可能是溶质质量偏大或溶剂质量偏小,可以分析出可能造成这两个方面错误的原因进行分析解答。
【解答】解:A、用量筒量取水读数时,俯视读数,量取的水少了,所以溶质质量分数偏大,正确;
B、将氢氧化钠放在托盘天平的右盘称量,则会导致称量的氢氧化钠固体减小,则使溶质质量分数偏小,错误;
C、用刚洗涤的烧杯溶解氢氧化钠,溶剂多了,溶质的质量分数偏低,错误;
D、将固体氢氧化钠放在敞口容器中,固体NaOH已部分变质,生成碳酸钠,所以氢氧化钠质量减少,溶质质量分数会减少,错误;
故选:A。
【点评】本题考查了导致溶质质量分数偏高的因素,完成此题,可以依据溶质质量分数公式进行。
4.配制一定质量分数的溶液,一般不需要的步骤是( )
A.计算所需溶质和溶剂的质量
B.用天平称取所需溶质,放入烧杯中
C.用量筒量取所需溶剂,放入同一烧杯中并充分搅拌
D.将配得的溶液进行过滤
【分析】根据配制一定溶质质量分数的溶液时,先计算出需溶质的质量和所需水的体积,用托盘天平称量出溶质加入烧杯内,再用量筒量取水倒入烧杯内,用玻璃棒搅拌。即可配成溶液解答。
【解答】解:先计算出需溶质的质量和所需水的体积,用托盘天平称量出溶质加入烧杯内,再用量筒量取水倒入烧杯内,用玻璃棒搅拌至氢氧化钠完全溶解。
过滤是将不溶性固体和可溶性固体分离分方法,不需要将配得的溶液进行过滤。
故选:D。
【点评】熟记使用固体(液体)溶质配制溶液的基本步骤:计算、称量(量取)、溶解。
5.向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤.下列说法正确的是( )
资料:A的溶解度
温度/℃ 20 30 40 50 60
溶解度/g 37.2 41.4 45.8 50.4 55.2
25℃100g水①②③④⑤
A.②中A的质量分数最大 B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液 D.①③④⑤中没有固体存在
【分析】溶解度为一定温度下,100g水溶解溶质达到饱和状态时所溶解溶质的质量;结合A物质在不同温度下的溶解度,根据溶液变化流程中的条件,判断物质的溶解及所得溶液的状态或组成;由资料中物质A的溶解度可知,物质A的溶解度随温度升高而增大.
【解答】解:A、根据A物质在30℃的溶解度为41.4g、60℃的溶解度为55.2g,可判断41.4g物质A在25℃时不能完全溶解而在60℃时可以全部溶解且为不饱和溶液,则溶液②的溶质质量分数小于溶液③的溶质质量分数。故A不正确;
B、溶液③为60℃时100g水溶解41.4gA物质所形成的溶液,溶液中溶质的质量分数=×100%≈29.3%;
溶液⑤为50℃时100g水溶解50.4gA的饱和溶液,溶液中溶质的质量分数=×100%≈33.5%;故B不正确;
C、综合A、B项分析可知:溶液②⑤为饱和溶液;60℃A的溶解度为55.2g,溶液④为60℃时100g水溶解50.4gA,可判断此时溶液为不饱和溶液;故C不正确;
D、根据20℃A的溶解度为37.2g可判断,25℃时37.2gA溶解在100g水中形成不饱和溶液,没有固体存在;综合A、B、C项分析,溶液③④均为不饱和溶液,没有固体存在;而溶液⑤恰好饱和,没有固体存在。故D正确;
故选:D。
【点评】利用物质的溶解度判断溶液的状态时,要明确溶解度是在该温度下100g水所能溶解溶质的最大质量.
6.配制溶质质量分数为5%的下列溶液,能达到目的的是( )
A.称取5.0 g氯化钾,解在95 mL 水中,充分搅拌
B.称取5.0 g生石灰,放入95 mL水中充分搅拌
C.量取5.0 mL浓盐酸,倒入95 mL 水中,充分搅拌
D.称取5.0 g碳酸钙,放入95 mL水中,充分搅拌
【分析】本题应从溶质质量分数的计算和物质的溶解性等多方面考虑.
A、氯化钾溶解于水根据数据计算可确定;
B、生石灰于水反应生成熟石灰,熟石灰微溶于水;
C、5.0mL浓盐酸是溶液的体积;
D、碳酸钙不溶于水;
【解答】解:A、氯化钾能溶解于水,5.0g氯化钾,溶解在95mL.水中计算溶质质量分数为5g÷(5g+95g)═5%;
B、生石灰于水反应生成熟石灰,熟石灰微溶于水,故错;
C、5.0mL浓盐酸是溶液的体积不能得出溶质氯化氢的质量,故不能求得溶质质量分数,故错;
D、碳酸钙不溶于水;不能得到溶液,故错;
故选:A。
【点评】充分考虑溶质质量分数的计算和物质的溶解性,才能准确把握此题,得出一个正确的结果.
7.饱和溶液用水稀释变成不饱和溶液的过程中,保持不变的是( )
A.溶质的质量 B.溶剂的质量
C.溶液的质量 D.溶质与溶剂的质量比
【分析】根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答。
【解答】解:饱和溶液用水稀释变成不饱和溶液的过程中,溶质质量不变,溶剂质量增加,溶液的质量增加。
A、饱和溶液用水稀释变成不饱和溶液的过程中,溶质的质量不变,故选项正确。
B、饱和溶液用水稀释变成不饱和溶液的过程中,溶剂的质量增加,故选项错误。
C、饱和溶液用水稀释变成不饱和溶液的过程中,溶液的质量增加,故选项错误。
D、饱和溶液用水稀释变成不饱和溶液的过程中,溶质与溶剂的质量比发生改变,故选项错误。
故选:A。
【点评】本题难度不大,考查溶液的稀释问题,掌握溶液稀释前后溶质的质量不变是正确解答此类题的关键所在。
8.稀释质量分数为98%(密度为1.84g/mL)的浓硫酸配制500mL质量分数为20%的稀硫酸(密度为1.14g/mL),稀释时需用的水的体积约为( )
A.436.8 mL B.453.7 mL C.456.0 mL D.458.3 mL
【分析】根据m=ρV计算出溶液的质量、溶质的质量=溶液的质量×溶质的质量分数、浓溶液配制稀溶液的过程中溶质的质量不变列式计算,再根据稀溶液与浓溶液的质量差来计算水的质量,进一步得到需要水的体积.
【解答】解:根据稀释过程中溶质的质量不变,设需浓硫酸的体积为x,可得:
1.84g/mL×x×98%=1.14g/mL×500mL×20% x≈63.2mL
需要水的质量为:1.14g/mL×500mL﹣1.84g/mL×63.2mL≈453.7g(合453.7mL)。
故选:B。
【点评】本题难度不大,考查溶液的稀释问题,掌握溶液稀释前后溶质的质量不变是正确解答此类题的关键所在.
9.下列条件下的氯化氢气体的溶液即为盐酸,其溶质的质量分数最大的是( )
A.20℃的饱和溶液 B.20℃的不饱和溶液
C.80℃的饱和溶液 D.80℃的不饱和溶液
【分析】根据温度对氯化氢气体的溶解度的影响和溶质质量分数和溶解度的关系解答.
【解答】解:由于同一温度下饱和溶液和不饱和溶液的溶质质量分数肯定是饱和溶液的溶质质量分数大,故20℃时的饱和氯化氢气体的溶液比不饱和氯化氢气体的溶液的溶质质量分数大;由于氯化氢气体的溶解度随温度的升高而减少。所以,故20℃时的饱和氯化氢气体的溶液比80℃的饱和氯化氢气体的溶液的溶质质量分数大。可以上分析可知:
A、溶质的质量分数最大的是20℃的饱和溶液。故A符合题意;
B、20℃的不饱和溶液比20℃的饱和溶液溶质的质量分数最小。故B不符合题意;
C、80℃的饱和溶液比20℃的饱和溶液溶质的质量分数最小。故C不符合题意;
D、80℃的不饱和溶液溶质的质量分数较小。故D不符合题意。
故选:A。
【点评】解答本题的关键是了解同一温度下饱和溶液和不饱和溶液的溶质质量分数肯定是饱和溶液的溶质质量分数大,气体的溶解度图温度的关系.
10.20℃时硝酸钾的溶解度是31.6g,则在该温度下硝酸钾饱和溶液中溶质的质量分数( )
A.24.0% B.31.6% C.46.2% D.63.2%
【分析】根据溶解度的概念:每100克水中最多溶解溶质的质量进行解答。
【解答】解:20℃时硝酸钾的溶解度是31.6g,即20℃时100g水中最多溶解硝酸钾的质量是31.6g,所以该温度下硝酸钾饱和溶液中溶质的质量分数=×100%=24.0%。
故选:A。
【点评】题主要考查溶解度概念的理解与掌握和溶液中溶质的质量分数的计算方法及应用,并能灵活应用于解题。
11.实验室用密度为1.84g/cm3、质量分数为98%的浓硫酸和蒸馏水,配制500g质量分数为20%的稀硫酸.需要用多少mL的量筒量取多少mL的浓硫酸?( )
A.100 mL 54.35 mL B.100 mL 55.5 mL
C.250 mL 54.35 mL D.250 mL 55.5 mL
【分析】根据溶液稀释前后溶质的质量不变计算所需浓硫酸的质量,由密度计算公式计算所需浓硫酸的体积,从减小实验误差的角度去选择量筒的量程,据此进行分析解答.
【解答】解:稀释浓硫酸时,根据溶质的质量=溶液的质量×溶质的质量分数、稀释前后溶质质量不变,设所需98%的浓硫酸的质量为x,则500g×20%=x×98%,x≈102g,由密度公式求得浓硫酸体积为≈55.5mL。
量筒能保证量取一次,且量程与液体的取用量最接近,所以误差最小。故准确量取55.5mL的浓硫酸,选用的量筒规格是100mL。
故选:B。
【点评】本题难度不大,掌握稀释前后溶质质量不变、溶质的质量=溶液的质量×溶质的质量分数等是正确解答本题的关键.
12.已知氢气可以在氯气中燃烧,其反应的化学方程式为:H2+Cl22HCl.在一密闭容器中盛有H2、O2、Cl2的混合气体,已知其分子数之比为11:5:1,用电火花点燃,使其充分反应,冷却后所得溶液的质量分数为( )
A.40.3% B.28.9% C.44.8% D.30.5%
【分析】氢气在氯气中燃烧生成氯化氢,氢气在氧气中燃烧生成水,冷却后提得溶液为氯化氢溶液;
计算氯化氢溶液的溶质质量分数,需要氯化氢和水的质量,根据反应的化学方程式,由H2、O2、Cl2的混合气体分子数之比为11:5:1,通过拟定数据的方法,可推断出反应生成HCl与H2O的质量比,从而完成所得溶液的质量分数的计算。
【解答】解:假设密闭容器中氯气分子个数为1,根据题意,则氧气分子个数为5,氢气分子个数为11
根据化学方程式H2+Cl22HCl可知:1分子氯气消耗1分子的氢气生成2分子氯化氢;
根据化学方程式2H2+O22H2O可知:5分子氧气可支持10分子氢气完全燃烧生成10分子水;
H2、O2、Cl2的混合气体分子数之比为11:5:1,用电火花点燃,使其充分反应,恰好完全反应,生成HCl与H2O的分子个数比为2:10=1:5;则生成HCl与H2O的质量比=36.5:90;因此,所得溶液的质量分数=≈28.9%
故选:B。
【点评】解决本题时,需要通过相对分子质量把物质的分子个数比转换成物质的质量比。
13.兴趣小组在实验室要配制20%的稀硫酸,用来完成探究硫酸的化学性质实验.某成员负责准备实验仪器,他不需要选择的是( )
A.托盘天平 B.量筒 C.胶头滴管 D.烧杯
【分析】用浓硫酸配制质量分数为20%的稀硫酸溶液,步骤为计算、量取(量取浓硫酸和水)、溶解,根据各操作所需要使用的仪器,判断所列仪器是否需要.
【解答】解:用浓硫酸配制质量分数为20%的稀硫酸溶液,首先计算配制溶液所需浓硫酸和水的质量,再量取浓硫酸和水,最后进行溶解;在这些操作中需要的仪器:量筒、胶头滴管、烧杯和玻璃棒。故不需要使用托盘天平。
故选:A。
【点评】本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键.
二.填空题(共5小题)
14.水是重要的物质,在实验室中常用于溶解物质、配制溶液.根据下列仪器,欲配制一定质量分数的食盐溶液,回答下列问题.
(1)上面的仪器中除D、E外,还必须选用的仪器有 BG ;(填字母)
(2) E的作用是 搅拌,加快食盐的溶解速率 ;
(3)配制的步骤可以概括为计算、 称量 和量取、 溶解 、装瓶贴标签.
【分析】(1)配制一定溶质质量分数的食盐溶液的操作步骤分别是:计算、称量、溶解,根据各操作所需要使用的仪器,判断所列仪器是否需要.
(2)根据玻璃棒的作用,进行分析解答.
(3)根据配制一定溶质质量分数的食盐溶液的操作步骤进行分析解答.
【解答】解:(1)配制一定溶质质量分数的食盐溶液的操作步骤分别是:计算、称量、溶解;托盘天平用于称取固体食盐、量筒用于量取水、烧杯用于完成溶解操作、玻璃棒用于溶解时的搅拌,上面的仪器中除D、E外,还必须选用的仪器有BG.
(2)玻璃棒用于溶解时的搅拌,加快食盐的溶解速率.
(3)配制一定质量分数的食盐溶液,首先计算配制溶液所需食盐和水的质量,再称量所需的食盐和量取水,最后进行溶解、装瓶贴标签.
故答案为:(1)BG;(2)搅拌,加快食盐的溶解速率;(3)称量;溶解.
【点评】本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键.
15.小盘同学配制质量分数为5%的氯化钠溶液100g,以备实验.
(1)通过计算,需称取氯化钠的质量为 5 g.
(2)配制该溶液所需要的玻璃仪器有:烧杯、量筒、胶头滴管和 玻璃棒 (写仪器名称).
(3)量取水的体积时,小盘同学仰视读数,则配制的氯化钠溶液的质量分数将 偏小 (填“偏小”、“不变”或“偏大”).
【分析】(1)溶质质量=溶液质量×溶质的质量分数,据此进行分析解答.
(2)根据配制溶质质量分数一定的溶液的步骤分析解答需要的仪器,进行分析解答.
(3)仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,据此进行分析解答.
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制质量分数为5%的氯化钠溶液100g,需称取氯化钠的质量为100g×5%=5g.
(2)配制质量分数为5%的氯化钠溶液100g,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,其中属于玻璃仪器的是玻璃棒、烧杯、胶头滴管、量筒.
(3)仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小.
故答案为:(1)5;(2)玻璃棒;(3)偏小.
【点评】本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.
16.溶质分数是表示 溶液浓度 的一种方法,溶质质量分数= ×100% .
【分析】溶质的质量分数表示的是溶液的浓度的高低,是溶质质量与溶液的质量的比值.
【解答】解:溶液质量分数是表示溶液浓度的一种方法,其数学意义是溶质质量与溶液质量之比.
故答案是:溶液浓度;×100%.
【点评】本题难度不大,掌握溶质质量分数的概念、含义等即可正确解答本题.
17.“84”消毒液是预防新冠肺炎经常使用的消杀用品。回答下列问题:
(1)其有效成分次氯酸钠(NaClO)中氯元素的化合价为 +1 。
(2)“84”消毒液的消毒原理为2NaClO+CO2+X═Na2CO3+2HClO,生成的HClO(次氯酸)具有较强的杀菌作用。化学方程式中X的化学式为 H2O 。
(3)探究发现,暴露在空气中(阳光充足)的“84”消毒液的消毒效果随时间的推移而减弱。据此,你认为“84”消毒液应 避光密封 保存。
(4)“84”消毒液有一定的刺激性与腐蚀性,必须稀释以后才能使用。将50g含NaClO 5%的“84”消毒液稀释至1%,需向原溶液中加入水的质量为 200 g。
【分析】(1)根据化合物中元素的化合价的计算方法以及离子符号的写法来分析;
(2)根据质量守恒定律来分析;
(3)根据药品的性质与保存方法来分析;
(4)根据溶液加水稀释过程中,溶质的质量不变来分析。
【解答】解:(1)在NaClO中,钠元素的化合价是+1,氧元素的化合价是﹣2,设氯元素的化合价是x,则有(+1)+x+(﹣2)=0,解得x=+1;
(2)根据反应的化学方程式2NaClO+CO2+X═Na2CO3+2HClO,反应物中钠、氯、碳、氧原子个数分别为2、2、1、4,反应后的生成物中钠、氯、碳、氢、氧原子个数分别为2、2、1、2、5,根据反应前后原子种类、数目不变,则每个X分子由2个氢原子、1个氧原子构成,则物质X的化学式为H2O;
(3)曝露在空气中(阳光充足)的“84”消毒液的消毒效果随时间的推移而减弱,所以“84”消毒液应避光密封保存;
(4)设需要加水的质量为x,则:
50g×5%=(50g+x)×1%
x=200g。
故答案为:(1)+1;(2)H2O;(3)避光密封;(4)200。
【点评】本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学反应前后原子守恒、信息应用以及有关溶液的计算等并能灵活运用是正确解答本题的关键。
18.固体物质的溶解性与溶解度之间的关系如下表所示:
20℃时溶解度/g >10 10﹣1 1﹣0.01 <0.01
溶解性 易溶 可溶 微溶 难溶
M、N两种固体物质的溶解度曲线如图所示,试完成下列问题:
(1)M物质的溶解性属于 易溶 。
(2)在20℃时,M、N两种物质的 溶解度 相等。
(3)在30℃时,将20gM物质(不含结晶水)完全溶于100g水中,得到不饱和溶液,若要将其转化成饱和溶液,下列措施可采取的是 AB 。
A.再加入30gM物质B.将温度降低到10℃.倒掉溶液30g。
【分析】物质的溶解性的强弱,是根据在20℃时的溶解度来确定的,若溶解度大于10g,属于易溶物质。溶解度大于1g,属于可溶物质。溶解度大于0.01g的,属于微溶物质。
【解答】解:(1)由曲线图中查出20℃时,M的溶解度为35g,大于10g,属易溶。
(2)20℃时,M、N的溶解度曲线相交,说明它们的溶解度相等。
(3)由曲线图看出,30℃时,M溶液要变成饱和,需要再加入30gM,或将温度降低到10℃。
故答案为:(1)易溶。
(2)溶解度。
(3)AB。
【点评】对于溶解度受温度影响较大的固体物质来说,可以通过改变温度的方法,使不饱和溶液变为饱和溶液。
三.实验探究题(共1小题)
19.配制一定溶质质量分数的氯化钠溶液常按以下操作步骤进行。请回答下列问题:
(1)配制100g溶质质量分数为5%的氯化钠溶液,所需氯化钠固体的质量为 5 g。
(2)用托盘天平称量所需氯化钠时,发现天平的指针偏向左盘,应进行的操作是 B 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节游码 D.添加砝码
(3)在配制过程中,有关下列描述,会导致溶液浓度偏小的是 ACD (填字母)。
A.称量好的NaCl固体倒入烧杯时,有少许洒出
B.量水的体积时,俯视度数
C.溶解NaCl固体的烧杯内壁有水珠
D.将5g NaCl固体完全溶解在100g水中
【分析】(1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量。
(2)使用托盘天平称量药品时应遵循“左物右码”,称量过程中他发现指针偏左了,说明药品质量大于砝码质量,应减少药品。
(3)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答。
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;
(2)用托盘天平称量5g固体药品NaCl时,步骤是:调节天平平衡,在右盘上加砝码和拨动游码,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl。
(3)A、称量好的NaCl固体倒入烧杯时,有少许洒出,溶质偏少,则使溶质质量分数偏小,故选项正确。
B、用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,故选项不正确。
C、溶解NaCl固体的烧杯内壁有水珠,多取了水,则使溶质质量分数偏小,故选项正确。
D、将5g NaCl固体完全溶解在100g水中,溶液质量大于100g,溶质质量分数偏小,故选项正确。
故答案为:(1)5,95,100;(2)B;(3)ACD。
【点评】本题难度不大,明确一定溶质质量分数溶液的配制的步骤、所需仪器、注意事项等是正确解答此类题的关键。
四.解答题(共1小题)
20.3%的硼酸溶液可用于清洗皮肤的小面积创伤.现配制300g质量分数为3%的硼酸溶液,实验操作如下:
(1)称量硼酸固体的质量:在下图中分别标出所选砝码的质量和游码的示数.
(2)量取水的体积:用量筒取 291 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 烧杯、玻璃棒 .
(4)装瓶、贴标签:在右图的标签中填上相应的内容.
【分析】(1)根据溶质质量=溶液质量×溶质的质量分数,计算出所需硼酸固体的质量,进而确定所选砝码的质量和游码的示数.
(2)溶剂质量=溶液质量﹣溶质质量,据此进行分析解答.
(3)根据溶解操作所需的仪器,进行分析判断.
(4)标签中填上相应的内容是溶液的名称、溶质的质量分数,进行分析解答.
【解答】解:(1)溶质质量=溶液质量×溶质的质量分数,配制300g质量分数为3%的硼酸溶液,所需硼酸固体的质量为300g×3%=9g;选用5g的砝码,游码拨到4g处即可.
(2)溶剂质量=溶液质量﹣溶质质量,则所需水的质量=300g﹣9g=291g(合291mL).
(3)溶解用到的玻璃仪器是烧杯、玻璃棒.
(4)标签中填上相应的内容是溶液的名称、溶质的质量分数,图2的标签中填上相应的内容是硼酸溶液,3%.
故答案为:(1)5g;4g;(2)291;(3)烧杯、玻璃棒;(4)硼酸溶液,3%.
【点评】本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.
声明:试题解析著作权属所有,未经书面同意,不得复制发布
日期:2022/1/27 20:15:00;用户:15877047552;邮箱:15877047552;学号:38945411第2页(共2页)
