第2节 氧化和燃烧 过关训练(含答案)
文档属性
| 名称 | 第2节 氧化和燃烧 过关训练(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 466.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-02-13 00:00:00 | ||
图片预览




文档简介
第2节 氧化与燃烧
一、选择题
1.遇到着火时,正确处理火情有利于保护生命财产安全,下列处理方式中正确的是( )
A.家用电器着火,应立即用水浇灭
B.厨房天然气泄漏,可打开脱排油烟机排气
C.不慎碰倒燃着的酒精灯而着火,应立刻用湿抹布扑盖
D.炒菜时油锅着火,应立即用大量水冲灭
2.下列实验不能达到目的是( )
A.检查装置气密性 B.比较物质着火点
C.监控O2流速 D.探究微粒运动
3.某校化学兴趣小组设计实验探究燃烧的条件。将三支试管同时放入盛有80oC热水的烧杯中,有关说法不正确的是( )
A.三支试管中只有b试管中有白烟产生
B.气球的作用是防止燃烧产物污染环境
C.对比a和b两试管说明CO2不支持燃烧
D.本实验设计能证明燃烧的三个条件
4.小科用研钵将约20克氢氧化钡[Ba(OH)2]晶体磨成粉末,倒入一小烧杯。在玻璃片上洒上少量水,并将小烧杯放在玻璃片上、再向小烧杯中加入约10克氯化铵[NHCl]晶体,并用玻璃棒迅速搅拌,烧杯中产生刺激性气味的气体,静止片刻,提起小烧杯,观察到如图所示现象。下列对现象的观察分析中正确的是( )
A.用手触摸烧杯外壁,能感觉到发热
B.化学反应中,不同形式的能之间可以相互转化
C.把氢氧化钡晶体磨成粉末可以增加最终产生气体的质量
D.该反应和燃烧一样,反应物总的化学能高于生成物总的化学能
5.某同学用一系列实验探究物质的燃烧,得到下列结论,其中不正确的是( )
A.镁条在氧气和二氧化碳中均能燃烧,说明二氧化碳分子中有氧气
B.玻璃棒不能燃烧而火柴棒可以燃烧,说明燃烧与物质本身性质有关
C.蜡烛在氧气中比在空中燃烧更旺,说明燃烧与氧气的浓度有关
D.燃烧是一种化学反应,需考虑两方面因素:反应物(内因)和反应条件(外因)
6.我们生活中充满了科学的身影,下面一些生活中的现象,科学原理解释错误的是( )
A.生活中铝制品比铁难锈蚀,这是由于铝的化学性质比铁不活泼
B.房屋失火用水扑灭主要是为了将燃烧物的温度降低到着火点以下,而达到灭火的效果
C.棒冰从冰箱拿出来后,棒冰周围有“白气”,是因为棒冰中的冰升华成的水蒸气
D.骑自行车时,脚蹬得越使劲,车就行驶的越快,因为物体的运动需要力
7.用图示装置实验,注射器中吸入足量5%的溶液,广口瓶中放入适量,烧杯中倒入足量80℃的热水,燃烧匙和烧杯中金属盖内分别放置一小块白磷(白磷的着火点为40℃),塞紧瓶塞,打开止水夹,注入适量5%的溶液。通过此实验可验证( )
A.白磷燃烧需要助燃气体
B.白磷的着火点为40℃
C.白磷燃烧的产物为
D.是分解的催化剂
8.在平时做实验的过程中,若发现酒精灯的火焰太小时,我们可以将灯芯拨得松散一些,这样就可使酒精灯的火焰变得更旺。其中涉及的原理是( )
A.降低可燃物的着火点 B.提高可燃物的着火点
C.增加空气中氧气含量 D.增大可燃物与空气的接触面积
9.有一种自动干粉灭火球简称“AFO”,它体积不大,质量也只有1.3千克左右,当发生火灾的时候,只要AFO的引线接触到火焰,内部的高压超细纳米干粉就会热膨胀破裂,起到灭火的效果,AFO的主要灭火原理是( )
A.将可燃物隔绝空气 B.降低可燃物的着火点
C.降低可燃物的温度 D.干粉的催化作用减缓了燃烧的剧烈反应
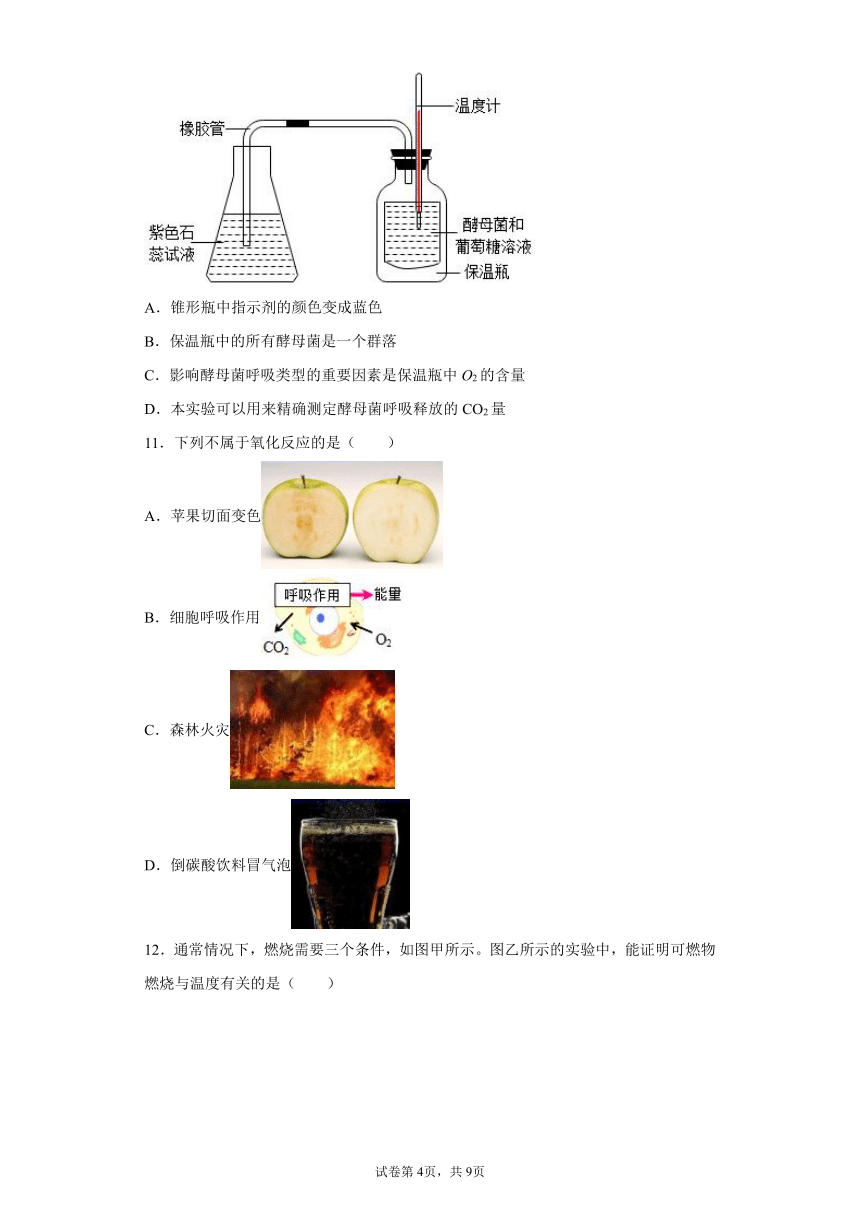
10.如图所示,某同学在一个保温瓶中放入葡萄糖和酵母菌溶液,用带有双孔的塞子封口,随着反应的进行,可以观察到锥形瓶中指示剂的颜色发生变化。下列有关实验的叙述中,正确的是( )
A.锥形瓶中指示剂的颜色变成蓝色
B.保温瓶中的所有酵母菌是一个群落
C.影响酵母菌呼吸类型的重要因素是保温瓶中O2的含量
D.本实验可以用来精确测定酵母菌呼吸释放的CO2量
11.下列不属于氧化反应的是( )
A.苹果切面变色
B.细胞呼吸作用
C.森林火灾
D.倒碳酸饮料冒气泡
12.通常情况下,燃烧需要三个条件,如图甲所示。图乙所示的实验中,能证明可燃物燃烧与温度有关的是( )
A.②④ B.②③ C.①③ D.①④
二、填空题
13.科学中部分概念相互间存在如下 3 种关系。请将下列概念间对应关系序号填在相应横线上。
(1)纯净物与氧化物属于_____;
(2)氧化反应和缓慢氧化属于_____;
(3)氧化反应和化合反应属于_____。
14.实验装置如图所示,甲、乙两个集气瓶用导管连接,玻璃管A的下端紧系一只气球,乙集气瓶中放一块白磷,将此装置放置在阳光下,一段时间后,可能观察到的现象;
(l)白磷 。
(2)气球 。
15.小金同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体示的改进(其他仪器忽略,小丁同学提出应把图红磷换为白磷,理由是____________。拉瓦锡测出的氧气约占空气总体积的1/5,而我们在做图1的实验时,即使红磷足量、操作正确,气体减少的体积往往小于1/5。为什么呢 小高联想到铁丝在空气中不能燃烧,而在氧气中可以燃烧的事实,分析得出原因是______
16.氢气可以用作清洁能源,但它的制取、存储和运输都根困难。科学家开发出一种用糖类制取氢气的新技术,有望解决这几大问题。以这项技术为基础,未来的氢动力汽车将携带易于存储的糖类,如淀粉,其化学式是(C6H10O5)n,科学家使用由多科特殊的路健成的混合物,将淀粉和水转变成和的混合气体,将除去后,进入燃料电池产生电力,驱动汽车前进。根据以上材料,请回答下列问题:
(1)利用该项技术,汽车运动时的机械能最终由___________能量转化而来。
(2)混合物中的酶具有高效性、多样性和___________性。
(3)淀粉等有机物在人体有氧气参与的情况下会进行有氧呼吸,而在暂时缺氧的情况下细胞会进行无氧呼吸,请写出葡萄糖在人体细胞内进行无氧呼吸的文字表达式:___________。
(4)若一辆氢动力汽车正常行驶时,功率是70千瓦,氢气的热值是焦/千克,燃料电池的能量转化效率是50%,在阻力不变和不考虑其它能量损耗时,要使该车能正常行驶。汽车每小时至少消耗氢气___________千克。
17.小强和几位同学在实验室用下列装置制取几种气体。
(1)写出图中标有①②的仪器名称: ;
(2)小强想用高锰酸钾制取较纯净的氧气,他应选择上述装置中的A和 (填字母)进行组装,你认为A装置中还缺少 。写出该反应的文字表达式为 ,加热时试管口要略向下倾斜的原因是 。
(3)小翔选用B和C装置制取氧气,写出反应的文字表达式 。验满氧气的方法是 。
18.如图所示,很多物质分解可以产生氧气。
(1)实验室常用①、②、③三个原理制取氧气。原料中氧元素质量分数最大的是 (选填①、②、③,下同),需要加热条件的是原理 ,反应装置直接输出的气体中会混有水蒸气的是 。
(2)通过途径④获得氧气的反应条件为 ,在生成氧气的同时,还会有 生成,消耗一定体积的水时,氧气与该气体的体积比为 。
三、简答题
19.如图所示是钠在氯气中燃烧的实验,请回答下列问题
(1)钠保存在煤油中,说明钠具有怎样的性质?______________(答出2点即可)
(2)燃烧后生成的白色物质由__________________________(选填“分子”、“原子”或“离子”)构成。
(3)根据这个实验,请你分享你对燃烧产生了什么新的认识________________?
20.2020年3月,四川省木里县再次发生特大森林火灾
(1)消防员开辟防火带主要是为了______(填字母)。
A.隔绝空气 B.隔绝可燃物 C.降低温度 D.便于运水
(2)山林中遭遇火灾,若被大火包围,则要选择杂草稀疏、地势平坦的地段,用衣服藏住头部,快速______(填“顺风”或“逆风”)冲过火线。
四、探究题
21.某校科学兴趣小组就空气中氧气的含量进行实验探究:
(集体讨论):
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择(_______)
A.蜡烛 B.红磷 C.木炭
为了充分消耗容器中的氧气,药品的用量应保证_____。写出红磷燃烧的文字表达式____________。
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是(填编号)_____。为了确保实验的成功,在装药品之前应该___________。
(分组实验):在讨论的基础上,他们分组进行了实验。
(数据分析):实验结束后,整理数据如下:(注:集气瓶容积为100mL)
组 别
1
2
3
4
5
6
进入集气瓶中水的体积(mL)
20
21
19
20
22
18
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的_____。通过实验还可以推断集气瓶中剩余气体的物理性质是___________。
(实验拓展):
(4)已知镁在空气中燃烧可分别与氧气和氮气反应,都生成固体物质,此实验中镁(填“能”或“不能”)_____(填“能”或“不能”)代替红磷,其原因是____________。
试卷第2页,共5页
试卷第1页,共5页
参考答案
1.C
2.C
3.D
4.B
5.A
6.AC
7.A
8.D
9.A
10.C
11.D
12.A
13.A A C
14.
15.白磷的着火点比红磷低 氧气浓度低于一定时燃烧停止,无法耗尽氧气
16.太阳 专一 36
17.
18.(1)②; ①③; ②;
(2)通电; 氢气; 1:2
19.钠比较活泼、密度比煤油大、不能与煤油反应等 离子 燃烧不一定要氧气参与
20.B 逆风
21.B 充足 A 检查装置气密性 难溶于水 不能 镁既能与氧气反应,又能与氮气反应 答案第1页,共2页
答案第1页,共2页
一、选择题
1.遇到着火时,正确处理火情有利于保护生命财产安全,下列处理方式中正确的是( )
A.家用电器着火,应立即用水浇灭
B.厨房天然气泄漏,可打开脱排油烟机排气
C.不慎碰倒燃着的酒精灯而着火,应立刻用湿抹布扑盖
D.炒菜时油锅着火,应立即用大量水冲灭
2.下列实验不能达到目的是( )
A.检查装置气密性 B.比较物质着火点
C.监控O2流速 D.探究微粒运动
3.某校化学兴趣小组设计实验探究燃烧的条件。将三支试管同时放入盛有80oC热水的烧杯中,有关说法不正确的是( )
A.三支试管中只有b试管中有白烟产生
B.气球的作用是防止燃烧产物污染环境
C.对比a和b两试管说明CO2不支持燃烧
D.本实验设计能证明燃烧的三个条件
4.小科用研钵将约20克氢氧化钡[Ba(OH)2]晶体磨成粉末,倒入一小烧杯。在玻璃片上洒上少量水,并将小烧杯放在玻璃片上、再向小烧杯中加入约10克氯化铵[NHCl]晶体,并用玻璃棒迅速搅拌,烧杯中产生刺激性气味的气体,静止片刻,提起小烧杯,观察到如图所示现象。下列对现象的观察分析中正确的是( )
A.用手触摸烧杯外壁,能感觉到发热
B.化学反应中,不同形式的能之间可以相互转化
C.把氢氧化钡晶体磨成粉末可以增加最终产生气体的质量
D.该反应和燃烧一样,反应物总的化学能高于生成物总的化学能
5.某同学用一系列实验探究物质的燃烧,得到下列结论,其中不正确的是( )
A.镁条在氧气和二氧化碳中均能燃烧,说明二氧化碳分子中有氧气
B.玻璃棒不能燃烧而火柴棒可以燃烧,说明燃烧与物质本身性质有关
C.蜡烛在氧气中比在空中燃烧更旺,说明燃烧与氧气的浓度有关
D.燃烧是一种化学反应,需考虑两方面因素:反应物(内因)和反应条件(外因)
6.我们生活中充满了科学的身影,下面一些生活中的现象,科学原理解释错误的是( )
A.生活中铝制品比铁难锈蚀,这是由于铝的化学性质比铁不活泼
B.房屋失火用水扑灭主要是为了将燃烧物的温度降低到着火点以下,而达到灭火的效果
C.棒冰从冰箱拿出来后,棒冰周围有“白气”,是因为棒冰中的冰升华成的水蒸气
D.骑自行车时,脚蹬得越使劲,车就行驶的越快,因为物体的运动需要力
7.用图示装置实验,注射器中吸入足量5%的溶液,广口瓶中放入适量,烧杯中倒入足量80℃的热水,燃烧匙和烧杯中金属盖内分别放置一小块白磷(白磷的着火点为40℃),塞紧瓶塞,打开止水夹,注入适量5%的溶液。通过此实验可验证( )
A.白磷燃烧需要助燃气体
B.白磷的着火点为40℃
C.白磷燃烧的产物为
D.是分解的催化剂
8.在平时做实验的过程中,若发现酒精灯的火焰太小时,我们可以将灯芯拨得松散一些,这样就可使酒精灯的火焰变得更旺。其中涉及的原理是( )
A.降低可燃物的着火点 B.提高可燃物的着火点
C.增加空气中氧气含量 D.增大可燃物与空气的接触面积
9.有一种自动干粉灭火球简称“AFO”,它体积不大,质量也只有1.3千克左右,当发生火灾的时候,只要AFO的引线接触到火焰,内部的高压超细纳米干粉就会热膨胀破裂,起到灭火的效果,AFO的主要灭火原理是( )
A.将可燃物隔绝空气 B.降低可燃物的着火点
C.降低可燃物的温度 D.干粉的催化作用减缓了燃烧的剧烈反应
10.如图所示,某同学在一个保温瓶中放入葡萄糖和酵母菌溶液,用带有双孔的塞子封口,随着反应的进行,可以观察到锥形瓶中指示剂的颜色发生变化。下列有关实验的叙述中,正确的是( )
A.锥形瓶中指示剂的颜色变成蓝色
B.保温瓶中的所有酵母菌是一个群落
C.影响酵母菌呼吸类型的重要因素是保温瓶中O2的含量
D.本实验可以用来精确测定酵母菌呼吸释放的CO2量
11.下列不属于氧化反应的是( )
A.苹果切面变色
B.细胞呼吸作用
C.森林火灾
D.倒碳酸饮料冒气泡
12.通常情况下,燃烧需要三个条件,如图甲所示。图乙所示的实验中,能证明可燃物燃烧与温度有关的是( )
A.②④ B.②③ C.①③ D.①④
二、填空题
13.科学中部分概念相互间存在如下 3 种关系。请将下列概念间对应关系序号填在相应横线上。
(1)纯净物与氧化物属于_____;
(2)氧化反应和缓慢氧化属于_____;
(3)氧化反应和化合反应属于_____。
14.实验装置如图所示,甲、乙两个集气瓶用导管连接,玻璃管A的下端紧系一只气球,乙集气瓶中放一块白磷,将此装置放置在阳光下,一段时间后,可能观察到的现象;
(l)白磷 。
(2)气球 。
15.小金同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图1所示),但测出的氧气的体示的改进(其他仪器忽略,小丁同学提出应把图红磷换为白磷,理由是____________。拉瓦锡测出的氧气约占空气总体积的1/5,而我们在做图1的实验时,即使红磷足量、操作正确,气体减少的体积往往小于1/5。为什么呢 小高联想到铁丝在空气中不能燃烧,而在氧气中可以燃烧的事实,分析得出原因是______
16.氢气可以用作清洁能源,但它的制取、存储和运输都根困难。科学家开发出一种用糖类制取氢气的新技术,有望解决这几大问题。以这项技术为基础,未来的氢动力汽车将携带易于存储的糖类,如淀粉,其化学式是(C6H10O5)n,科学家使用由多科特殊的路健成的混合物,将淀粉和水转变成和的混合气体,将除去后,进入燃料电池产生电力,驱动汽车前进。根据以上材料,请回答下列问题:
(1)利用该项技术,汽车运动时的机械能最终由___________能量转化而来。
(2)混合物中的酶具有高效性、多样性和___________性。
(3)淀粉等有机物在人体有氧气参与的情况下会进行有氧呼吸,而在暂时缺氧的情况下细胞会进行无氧呼吸,请写出葡萄糖在人体细胞内进行无氧呼吸的文字表达式:___________。
(4)若一辆氢动力汽车正常行驶时,功率是70千瓦,氢气的热值是焦/千克,燃料电池的能量转化效率是50%,在阻力不变和不考虑其它能量损耗时,要使该车能正常行驶。汽车每小时至少消耗氢气___________千克。
17.小强和几位同学在实验室用下列装置制取几种气体。
(1)写出图中标有①②的仪器名称: ;
(2)小强想用高锰酸钾制取较纯净的氧气,他应选择上述装置中的A和 (填字母)进行组装,你认为A装置中还缺少 。写出该反应的文字表达式为 ,加热时试管口要略向下倾斜的原因是 。
(3)小翔选用B和C装置制取氧气,写出反应的文字表达式 。验满氧气的方法是 。
18.如图所示,很多物质分解可以产生氧气。
(1)实验室常用①、②、③三个原理制取氧气。原料中氧元素质量分数最大的是 (选填①、②、③,下同),需要加热条件的是原理 ,反应装置直接输出的气体中会混有水蒸气的是 。
(2)通过途径④获得氧气的反应条件为 ,在生成氧气的同时,还会有 生成,消耗一定体积的水时,氧气与该气体的体积比为 。
三、简答题
19.如图所示是钠在氯气中燃烧的实验,请回答下列问题
(1)钠保存在煤油中,说明钠具有怎样的性质?______________(答出2点即可)
(2)燃烧后生成的白色物质由__________________________(选填“分子”、“原子”或“离子”)构成。
(3)根据这个实验,请你分享你对燃烧产生了什么新的认识________________?
20.2020年3月,四川省木里县再次发生特大森林火灾
(1)消防员开辟防火带主要是为了______(填字母)。
A.隔绝空气 B.隔绝可燃物 C.降低温度 D.便于运水
(2)山林中遭遇火灾,若被大火包围,则要选择杂草稀疏、地势平坦的地段,用衣服藏住头部,快速______(填“顺风”或“逆风”)冲过火线。
四、探究题
21.某校科学兴趣小组就空气中氧气的含量进行实验探究:
(集体讨论):
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择(_______)
A.蜡烛 B.红磷 C.木炭
为了充分消耗容器中的氧气,药品的用量应保证_____。写出红磷燃烧的文字表达式____________。
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是(填编号)_____。为了确保实验的成功,在装药品之前应该___________。
(分组实验):在讨论的基础上,他们分组进行了实验。
(数据分析):实验结束后,整理数据如下:(注:集气瓶容积为100mL)
组 别
1
2
3
4
5
6
进入集气瓶中水的体积(mL)
20
21
19
20
22
18
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的_____。通过实验还可以推断集气瓶中剩余气体的物理性质是___________。
(实验拓展):
(4)已知镁在空气中燃烧可分别与氧气和氮气反应,都生成固体物质,此实验中镁(填“能”或“不能”)_____(填“能”或“不能”)代替红磷,其原因是____________。
试卷第2页,共5页
试卷第1页,共5页
参考答案
1.C
2.C
3.D
4.B
5.A
6.AC
7.A
8.D
9.A
10.C
11.D
12.A
13.A A C
14.
15.白磷的着火点比红磷低 氧气浓度低于一定时燃烧停止,无法耗尽氧气
16.太阳 专一 36
17.
18.(1)②; ①③; ②;
(2)通电; 氢气; 1:2
19.钠比较活泼、密度比煤油大、不能与煤油反应等 离子 燃烧不一定要氧气参与
20.B 逆风
21.B 充足 A 检查装置气密性 难溶于水 不能 镁既能与氧气反应,又能与氮气反应 答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
