沪教版九年级化学下册:6.3物质的溶解性(第3课时)(课件19页)
文档属性
| 名称 | 沪教版九年级化学下册:6.3物质的溶解性(第3课时)(课件19页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-02-18 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
物质的溶解性
第3课时 结晶
小红军是如何将食盐成功送给游击队的呢?
溶盐
煮盐
结晶
创设情境
结晶
几种晶体
结晶:一定条件下,从溶液中析出晶体的过程。
结晶的方法有哪些?
[实验1]用酒精灯加热10mL浓的氯化钠溶液,用玻璃棒搅拌至出现较多晶体时停止加热。
[实验2]配制硝酸钾饱和溶液,将烧杯放在冷水中降温,观察实验现象。
结论:
a、析出晶体前溶液必须达到饱和状态.
b、改变条件(蒸发溶剂、降低温度),溶剂溶解溶质的量下降,使饱和溶液析出晶体
活动与探究
操作要点
(1)蒸发皿中的液体量不能超过蒸发皿容积的2/3。
(2)加热时,用玻璃棒不断搅拌,防止局部温度过高造成液滴飞溅。
(3)当蒸发皿中出现较多量固体时,停止加热,并用玻璃棒不断搅拌,利用余热将剩余水分蒸干。
(4)热的蒸发皿用坩埚钳夹持放在石棉网上,以免烫坏实验桌。
蒸发操作
蒸发仪器
蒸发皿、酒精灯、玻璃棒
为什么食盐溶液结晶用蒸发溶剂的方法,而硝酸钾溶液结晶则用冷却热饱和溶液(即降温结晶)的方法?你能根据二者的溶解度随温度改变的规律来做出解释吗?
请你思考
冷却溶液析出晶体
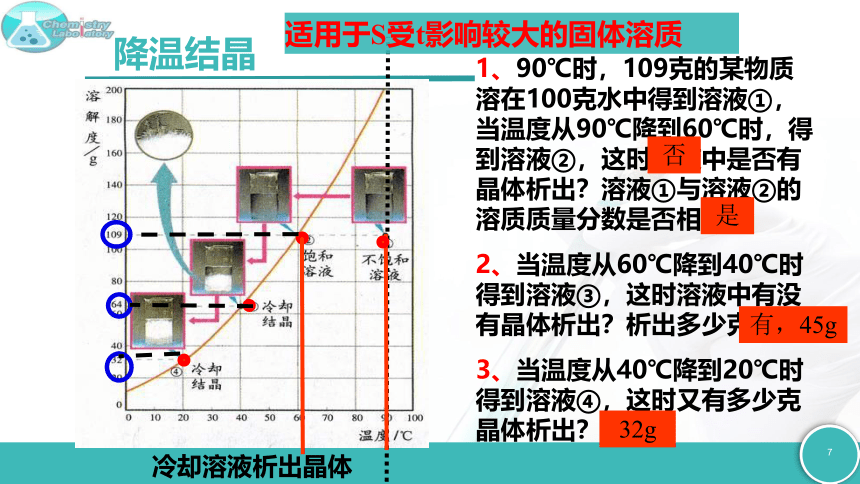
1、90℃时,109克的某物质溶在100克水中得到溶液①,当温度从90℃降到60℃时,得到溶液②,这时溶液中是否有晶体析出?溶液①与溶液②的溶质质量分数是否相同?
2、当温度从60℃降到40℃时得到溶液③,这时溶液中有没有晶体析出?析出多少克?
3、当温度从40℃降到20℃时得到溶液④,这时又有多少克晶体析出?
否
是
有,45g
32g
降温结晶
适用于S受t影响较大的固体溶质
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
①
②
③
④
根据硝酸钾溶解度曲线,分析上述过程中溶液中成分的变化,用“变大”“变小”“不变”填表。
变化 过程 溶质质量 溶剂质量 溶液质量 溶质质量分数 溶解度
①→②
②→③
③→④
不变
不变
不变
不变
变小
变小
不变
变小
变小
变小
变小
不变
变小
变小
变小
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
硝酸钾
氯化钠
39
36
饱和氯化钠溶液降温能否析出大量晶体?
用什么方法可以使氯化钠晶体析出?
(不能)
(蒸发结晶)
适用于各种可溶性固体溶质的结晶
尤其适用于S受t影响较小的固体物质
蒸发结晶
海
水
晒
盐
原理:借助日光和风力使水分蒸发,得到食盐
你能解释海水晒盐的原理了吗?
降温结晶:冷却热饱和溶液;适用于溶解度受温度影响大的可溶物(如:KNO3)。
蒸发结晶:蒸发溶剂;适用于溶解度受温度影响小的可溶物(如:NaCl)。
小结:结晶的方法
我国有许多盐碱地,湖水中溶有大量的氯化钠和纯碱,那里的农民冬天捞碱、夏天晒盐,试用你学过的知识说明其中的道理。
活学活用
海水晒盐制得的食盐中常有少量泥沙,如何除去泥沙获得较纯净的食盐?
请你思考
易溶于水
不溶于水
1.将可溶物与不溶物分离
例1:氯化钠(泥沙)
溶解、过滤、蒸发结晶
例2:从KMnO4分解的物质中回收MnO2?( MnO2 难溶于水,其他易溶)
溶解、过滤
思考:什么情况需要蒸发结晶的步骤?
混合物的分离与提纯
硝酸钾(氯化钠) 硝酸钾
提纯
①配制热的饱和溶液
(溶解 加热浓缩/蒸发浓缩)
溶解度受温度影响大
溶解度受温度影响小
②降温结晶
③过滤
两种可溶物的分离
氯化钠(硝酸钾) 氯化钠
提纯
①溶解
溶解度受温度影响小
溶解度受温度影响大
②蒸发结晶(大部分固体析出)
③趁热过滤
过滤 结晶
适用范围 除去液体中不溶于水固体杂质,或使纯净结晶与母液分离 分离几种可溶性固体的混合物
依据原理 固体颗粒大,不能通过滤纸或过滤层,而滤液可以通过滤纸或过滤层 利用固体物质溶解性不同,以及溶解度受温度变化影响不同,使一种物质先结晶而达到分离目的
主要操作 制过滤器、过滤 蒸发结晶、降温结晶
比较过滤和结晶两种方法
1. 夏天,实验员在实验室里配制了一瓶饱和的硝酸钾溶液并密封放置,到了冬天发现瓶底有大量的晶体析出。这是因为( )
A.溶液变成了不饱和溶液
B.溶液中溶剂质量减小
C.温度下降,硝酸钾溶解度减小
D.溶液中溶质质量增加
课堂训练
C
2. 苯甲酸是一种食品防腐剂,它是一种
片状晶体,在水中的溶解度如下表:
某同学为了提纯某一苯甲酸样品
(其中含泥沙等难溶于水的杂质),进行了如下实验:
常温时,苯甲酸溶解度很小
减少过滤时苯甲酸的损失
(1)常温时,取样品约1g放入烧杯中,加入50mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是 。
(2)将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤。趁热过滤的目的是 。
(3)将所得滤液 ,使苯甲酸以______形式析出,然后过滤得到较纯净的苯甲酸晶体。
冷却至室温
晶体
课堂训练
如何制作硫酸铜晶体?
药品:
步骤:
硫酸铜固体
1. 热水溶解,制成热饱和溶液
2. 降温结晶
拓展延伸
物质的溶解性
第3课时 结晶
小红军是如何将食盐成功送给游击队的呢?
溶盐
煮盐
结晶
创设情境
结晶
几种晶体
结晶:一定条件下,从溶液中析出晶体的过程。
结晶的方法有哪些?
[实验1]用酒精灯加热10mL浓的氯化钠溶液,用玻璃棒搅拌至出现较多晶体时停止加热。
[实验2]配制硝酸钾饱和溶液,将烧杯放在冷水中降温,观察实验现象。
结论:
a、析出晶体前溶液必须达到饱和状态.
b、改变条件(蒸发溶剂、降低温度),溶剂溶解溶质的量下降,使饱和溶液析出晶体
活动与探究
操作要点
(1)蒸发皿中的液体量不能超过蒸发皿容积的2/3。
(2)加热时,用玻璃棒不断搅拌,防止局部温度过高造成液滴飞溅。
(3)当蒸发皿中出现较多量固体时,停止加热,并用玻璃棒不断搅拌,利用余热将剩余水分蒸干。
(4)热的蒸发皿用坩埚钳夹持放在石棉网上,以免烫坏实验桌。
蒸发操作
蒸发仪器
蒸发皿、酒精灯、玻璃棒
为什么食盐溶液结晶用蒸发溶剂的方法,而硝酸钾溶液结晶则用冷却热饱和溶液(即降温结晶)的方法?你能根据二者的溶解度随温度改变的规律来做出解释吗?
请你思考
冷却溶液析出晶体
1、90℃时,109克的某物质溶在100克水中得到溶液①,当温度从90℃降到60℃时,得到溶液②,这时溶液中是否有晶体析出?溶液①与溶液②的溶质质量分数是否相同?
2、当温度从60℃降到40℃时得到溶液③,这时溶液中有没有晶体析出?析出多少克?
3、当温度从40℃降到20℃时得到溶液④,这时又有多少克晶体析出?
否
是
有,45g
32g
降温结晶
适用于S受t影响较大的固体溶质
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
①
②
③
④
根据硝酸钾溶解度曲线,分析上述过程中溶液中成分的变化,用“变大”“变小”“不变”填表。
变化 过程 溶质质量 溶剂质量 溶液质量 溶质质量分数 溶解度
①→②
②→③
③→④
不变
不变
不变
不变
变小
变小
不变
变小
变小
变小
变小
不变
变小
变小
变小
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
硝酸钾
氯化钠
39
36
饱和氯化钠溶液降温能否析出大量晶体?
用什么方法可以使氯化钠晶体析出?
(不能)
(蒸发结晶)
适用于各种可溶性固体溶质的结晶
尤其适用于S受t影响较小的固体物质
蒸发结晶
海
水
晒
盐
原理:借助日光和风力使水分蒸发,得到食盐
你能解释海水晒盐的原理了吗?
降温结晶:冷却热饱和溶液;适用于溶解度受温度影响大的可溶物(如:KNO3)。
蒸发结晶:蒸发溶剂;适用于溶解度受温度影响小的可溶物(如:NaCl)。
小结:结晶的方法
我国有许多盐碱地,湖水中溶有大量的氯化钠和纯碱,那里的农民冬天捞碱、夏天晒盐,试用你学过的知识说明其中的道理。
活学活用
海水晒盐制得的食盐中常有少量泥沙,如何除去泥沙获得较纯净的食盐?
请你思考
易溶于水
不溶于水
1.将可溶物与不溶物分离
例1:氯化钠(泥沙)
溶解、过滤、蒸发结晶
例2:从KMnO4分解的物质中回收MnO2?( MnO2 难溶于水,其他易溶)
溶解、过滤
思考:什么情况需要蒸发结晶的步骤?
混合物的分离与提纯
硝酸钾(氯化钠) 硝酸钾
提纯
①配制热的饱和溶液
(溶解 加热浓缩/蒸发浓缩)
溶解度受温度影响大
溶解度受温度影响小
②降温结晶
③过滤
两种可溶物的分离
氯化钠(硝酸钾) 氯化钠
提纯
①溶解
溶解度受温度影响小
溶解度受温度影响大
②蒸发结晶(大部分固体析出)
③趁热过滤
过滤 结晶
适用范围 除去液体中不溶于水固体杂质,或使纯净结晶与母液分离 分离几种可溶性固体的混合物
依据原理 固体颗粒大,不能通过滤纸或过滤层,而滤液可以通过滤纸或过滤层 利用固体物质溶解性不同,以及溶解度受温度变化影响不同,使一种物质先结晶而达到分离目的
主要操作 制过滤器、过滤 蒸发结晶、降温结晶
比较过滤和结晶两种方法
1. 夏天,实验员在实验室里配制了一瓶饱和的硝酸钾溶液并密封放置,到了冬天发现瓶底有大量的晶体析出。这是因为( )
A.溶液变成了不饱和溶液
B.溶液中溶剂质量减小
C.温度下降,硝酸钾溶解度减小
D.溶液中溶质质量增加
课堂训练
C
2. 苯甲酸是一种食品防腐剂,它是一种
片状晶体,在水中的溶解度如下表:
某同学为了提纯某一苯甲酸样品
(其中含泥沙等难溶于水的杂质),进行了如下实验:
常温时,苯甲酸溶解度很小
减少过滤时苯甲酸的损失
(1)常温时,取样品约1g放入烧杯中,加入50mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是 。
(2)将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤。趁热过滤的目的是 。
(3)将所得滤液 ,使苯甲酸以______形式析出,然后过滤得到较纯净的苯甲酸晶体。
冷却至室温
晶体
课堂训练
如何制作硫酸铜晶体?
药品:
步骤:
硫酸铜固体
1. 热水溶解,制成热饱和溶液
2. 降温结晶
拓展延伸
