第2章 微粒的模型与符号 综合练习(含答案)
文档属性
| 名称 | 第2章 微粒的模型与符号 综合练习(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 175.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-02-21 00:00:00 | ||
图片预览



文档简介
微粒的模型与符号
一、选择题
1.摄入适当剂量的柠檬酸(C6H8O7)对人体无害,可促进体内的正常代谢。在食晶中加入柠檬酸后口感好,并可促进食欲。下列有关柠檬酸的说法正确的是( )
A.柠橡酸是由C、H、O三种原子构成的
B.一个柠檬酸分子由6个碳元素、8个氢元素和7个氧元素组成
C.柠檬酸相对分子质量为192克
D.柠橡酸中氢元素的质量分数最小
2.如图是密闭容器中某反应的微观示意图,“”和“”分别表示不同原子, 则表示反应后生成物微粒的是( )
A. B. C. D.和
3.芯片是所有电脑、“智能家电”的核心部件,它是以高纯度单晶硅(Si)为材料制成的。制取高晶硅的反应原理:①②③。则下列说法中不正确的是( )
A.上述只有一个反应属于化合反成 B.上述三个反应,都有元素化合价发生变化
C.硅是地壳中含量最多的非金属元素 D.单晶硅(Si)属于单质,而属于氧化物
4.某种电池的正极材料由锂(Li)、钻(Co)和氧三种元素组成,其化合价依次是+1、+3、-2价,由此可推知该正极材料的化学式为( )
A.LiCoO B.LiCoO2 C.LiCoO3 D.LiCoO4
5.据日本媒体报道,日本政府计划将充分稀释后排入大海的方法,处理核废水中技术上无法去除的放射性物质“氚”,可以进入生物体内,还可以在体内停留,并引起基因突变。它的原子核由一个质子和二个中子组成。关于氚下列正确的是( )
A.是Li的同位素
B.这种氚原子和氧原子构成的水分子,其相对分子质量为20
C.这种原子的核外电子数为2
D.相对原子质量为3
6.2019年屠呦呦被授予“共和国勋章”,以表彰她在有效提取青蒿素方面作出的杰出贡献。青蒿素是从青蒿中提取出来的一种化学物质,化学式为,下列关于,说法正确的是( )
A.每个分子的质量是282克
B.中碳元素、氢元素和氧元素的质量比为12:1:16
C.中碳、氢和氧元素属于金属元素
D.中碳、氢和氧原子个数比为15:22:5
7.化学中元素符号能表示一定的意义,不同的元素符号表示的意义不同。下列对元素符号表示的意义解释正确的是( )
序号 元素符号 元素符号所表示的意义
A H 只表示氢元素
B Fe 表示铁元素,表示一个铁原子,表示铁这种物质
C N 只表示一个氮原子
D O 表示氧元素,表示一个氧原子,表示氧气这种物质
A.A B.B C.C D.D
8.下列推理或归纳合理的是( )
A.氮离子和氩原子最外层电子数相同
B.离子是带电粒子,所以带电的粒子一定是离子
C.在化合物中金属元素一定显正价,非金属元素可能显负价
D.氢原子和氦原子的化学性质相似
9.卢瑟福的粒子轰击金属箔实验推翻了汤姆森在1903年提出的原子结构模型,为建立现代原子理论打下了基础。该实验能证明的是( )
A.粒子带正电,原子不是实心球体,大部分空间是空的
B.原子始终在做无规则运动
C.原子核是由质子和中子组成的
D.原子核带正电荷
10.科学模型不仅可以表示静止的物体,还可以表示物质变化的过程。水的电解过程可用模型表示如图所示。下列说法中,正确的是( )
A.物质都是由分子构成的
B.分子与原子的本质区别是分子能再分,而原子不能再分
C.在水电解反应前后,原子的种类和数目都没有发生变化
D.在光学显微镜下能看见水分子被破坏,原子重新组合成新分子的过程
11.作为相对原子质量标准的碳—12可以写成,1个原子的质量为a千克,1个分子的质量为b千克,若以,分子中的1个氧原子质量的作为相对原子质量的标准,则的相对分子质量是( )
A. B. C. D.
12.市场上销售的一种食用盐——竹盐,其中富含钙、镁、锌、硒、铁等。这里的钙、镁、锌、硒、铁是指( )
A.分子 B.原子 C.元素 D.单质
二、填空题
13.(1)一种有趣的钟表式周期表如图所示,请根据时针所对应的元素填空:
①6:00对应的元素是___________(填“金属”或“非金属”)元素。
②10:00对应的元素___________(填“易”或“难”)形成化合物。
③12:00时,时针对应元素的离子符号是___________。
(2)从钟表上的元素中选择适当元素组成符合要求的物质,相对分子质量最小的氧化物是___________。
14.(1)A是地壳中含量最高的金属元素,B元素的一种气体单质支持人类呼吸,A和B组成化合物的化学式______。
(2)标出中氮元素的化合价______;
(3)保持水的化学性质的最小粒子______;
(4)高锰酸钾中含有的阴离子______;
(5)氧离子的最外层电子数是______;
(6)写出中“2”的意义______。
15.连花清瘟胶囊源自传统中医名方,被国家药品监督管理局批准用于“新型冠状病毒肺炎轻型、普通型”的治疗,在新冠肺炎患者救治中发挥了重要作用,成为抗疫热点中成药。经科学家检测,其有效成分之一是没食子酸。没食子酸的化学式为:,已知其相对分子质量为170,求:
(1)没食子酸中碳、氢原子的原子个数比为______。
(2)没食子酸中碳、氢元素的质量比为______。
(3)没食子酸的化学式中,x=______。
(4)______g没食子酸中含有42g碳元素。
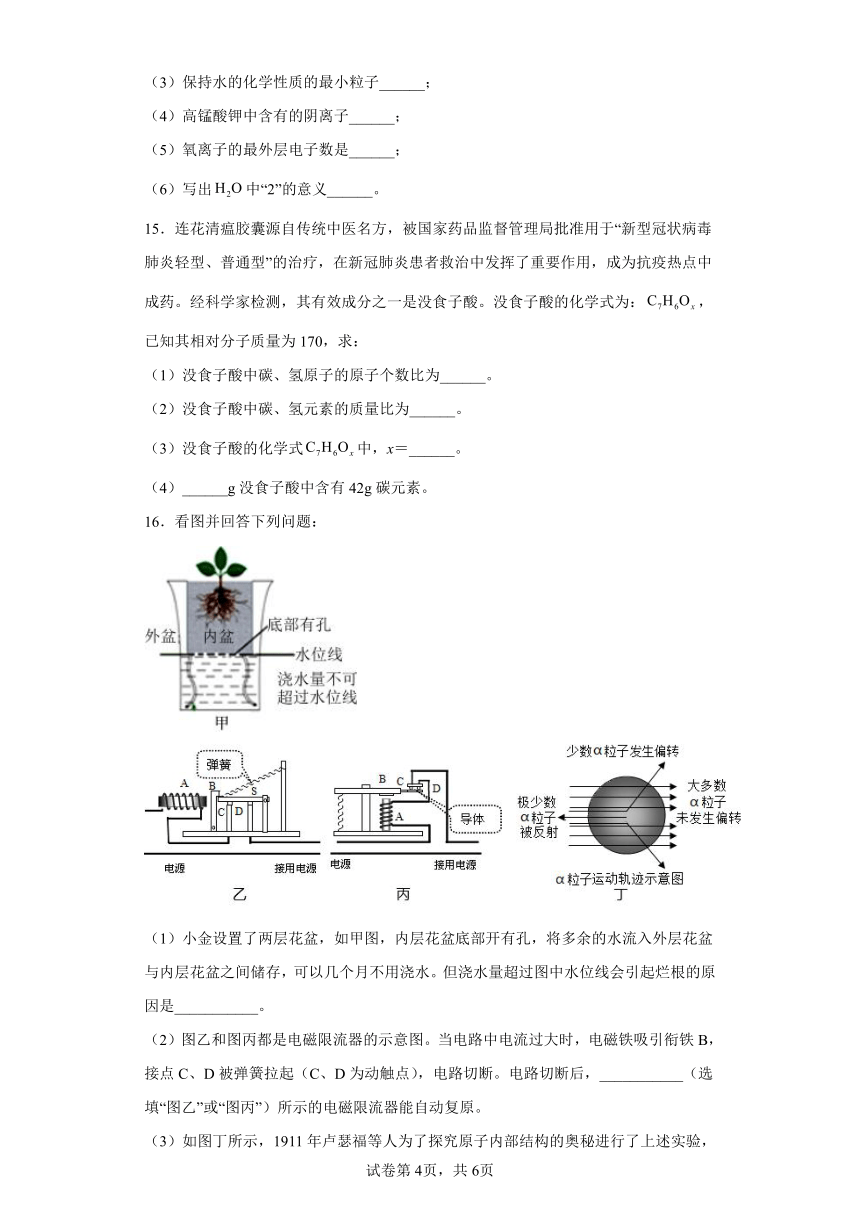
16.看图并回答下列问题:
(1)小金设置了两层花盆,如甲图,内层花盆底部开有孔,将多余的水流入外层花盆与内层花盆之间储存,可以几个月不用浇水。但浇水量超过图中水位线会引起烂根的原因是___________。
(2)图乙和图丙都是电磁限流器的示意图。当电路中电流过大时,电磁铁吸引衔铁B,接点C、D被弹簧拉起(C、D为动触点),电路切断。电路切断后,___________(选填“图乙”或“图丙”)所示的电磁限流器能自动复原。
(3)如图丁所示,1911年卢瑟福等人为了探究原子内部结构的奥秘进行了上述实验,他们用一束带正电、质量比电子大得多的高速运动的ɑ粒子轰击金箱,发现:①大多数ɑ粒子能穿过金箔而不改变原来的运动方向;②一小部分ɑ粒子改变了原来的运动方向;③有极少数ɑ粒子被弹了回来。请你根据原子结构的认识,分析上述现象的原因:现象①的原因是原子核很小,原子内部有很大空间。现象②的原因是原子核带___________(选填“正"或“负”)电,ɑ粒子轰击金原子核时,受到斥力而改变了运动方向。现象③的原因是___________。
17.请用化学用语表示
(1)镁离子的符号___________;
(2)正二价的铜元素___________;
(3)保持氯化钠化学性质的微粒符号___________;
(4)符号“2Fe”中数字2的含义___________。
18.现有下列物质:①水银②氧化镁③液氧④自来水⑤冰水混合物⑥食盐溶液其中属于单质的是______;属于化合物的是______;属于混合物的是______
三、简答题
19.新装修房间中往往会含有较多的甲醛,人体长期摄入超标的甲醛会对健康造成影响。甲醛的化学式为,请回答下列问题:
(1)甲醛由___________种元素组成。
(2)甲醛中碳、氢,氧元素的质量比为___________。(写最简整数比)
(3)计算甲醛中氢元素的质量分数。(保留两位小数)___________
20.人体中钙元素主要以羟基磷酸钙晶体形式存在于骨略和牙齿中,而牛奶是含钙丰富又易吸收的理想食品,下图为某乳业公可纯奶包装标签:
配料:鲜牛奶 净含量:/盒 营养成分(每) 蛋白质 钙 保质期:8个月
(1)羟基磷酸钙由___________种元素组成;
(2)羟基磷酸钙中钙、氧元素的质量比为多少___________(写出计算过程)
(3)若人体每天至少需要钙,每天已从食物中摄入所需钙的一半,则每天至少要喝这种牛奶___________盒。
(4)除了喝牛奶以外,青少年还可以通过服用含碳酸钙的钙片来补钙。求碳酸钙和多少质量的氢氧化钙所含的钙元素质量相等___________?(写出计算过程)
四、探究题
21.某化学兴趣小组利用下图所示装置测定样品中(样品中杂质高温下不分解,也不参加反应)的质量分数,请据图分析完成下列问题。
⑴实验开始时,应先挤压鼓气球持续一段时间,其目的是_____________________;白色粉末逐渐变蓝
⑵反应前准确称量样品的质量为5g,完全反应后C装置增加了1.62g,则样品中的质量分数为__________;
⑶若省去D装置,则实验所测定的样品中的质量分数比实际的质量分数会__________(填“偏大”、“偏小”或“不变”)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.B
5.D
6.D
7.B
8.AC
9.AD
10.C
11.A
12.C
13. 非金属 难 Mg2+ H2O
14. Al2O3 H2O 8 1个水分子中含有2个氧原子
15. 7:6 14:1 5 85
16. 水分过多,根无法进行有氧呼吸 丙 正 金原子核质量比α粒子大很多,且体积很小
17. Mg2+ Na+、Cl- 铁原子的个数为2个
18. ①③ ②⑤ ④⑥
19. 3 6:1:8 6.67%
20. 四 羟基磷酸钙晶体中各组成元素质量比Ca:O=(40×10):(16×26)=25:26 每100mL中含钙至少为0.12g,每盒250mL,则每盒至少含钙元素的质量为,人体每天至少需要来自牛奶的钙为0.6g×50%=0.3g,0.3g÷0.3g/盒=1盒 碳酸钙含钙元素质量为:,
所需氢氧化钙的质量为:
21. 除去装置中的空气,防止加热时发生爆炸 96% 偏大
答案第1页,共2页
答案第1页,共2页
一、选择题
1.摄入适当剂量的柠檬酸(C6H8O7)对人体无害,可促进体内的正常代谢。在食晶中加入柠檬酸后口感好,并可促进食欲。下列有关柠檬酸的说法正确的是( )
A.柠橡酸是由C、H、O三种原子构成的
B.一个柠檬酸分子由6个碳元素、8个氢元素和7个氧元素组成
C.柠檬酸相对分子质量为192克
D.柠橡酸中氢元素的质量分数最小
2.如图是密闭容器中某反应的微观示意图,“”和“”分别表示不同原子, 则表示反应后生成物微粒的是( )
A. B. C. D.和
3.芯片是所有电脑、“智能家电”的核心部件,它是以高纯度单晶硅(Si)为材料制成的。制取高晶硅的反应原理:①②③。则下列说法中不正确的是( )
A.上述只有一个反应属于化合反成 B.上述三个反应,都有元素化合价发生变化
C.硅是地壳中含量最多的非金属元素 D.单晶硅(Si)属于单质,而属于氧化物
4.某种电池的正极材料由锂(Li)、钻(Co)和氧三种元素组成,其化合价依次是+1、+3、-2价,由此可推知该正极材料的化学式为( )
A.LiCoO B.LiCoO2 C.LiCoO3 D.LiCoO4
5.据日本媒体报道,日本政府计划将充分稀释后排入大海的方法,处理核废水中技术上无法去除的放射性物质“氚”,可以进入生物体内,还可以在体内停留,并引起基因突变。它的原子核由一个质子和二个中子组成。关于氚下列正确的是( )
A.是Li的同位素
B.这种氚原子和氧原子构成的水分子,其相对分子质量为20
C.这种原子的核外电子数为2
D.相对原子质量为3
6.2019年屠呦呦被授予“共和国勋章”,以表彰她在有效提取青蒿素方面作出的杰出贡献。青蒿素是从青蒿中提取出来的一种化学物质,化学式为,下列关于,说法正确的是( )
A.每个分子的质量是282克
B.中碳元素、氢元素和氧元素的质量比为12:1:16
C.中碳、氢和氧元素属于金属元素
D.中碳、氢和氧原子个数比为15:22:5
7.化学中元素符号能表示一定的意义,不同的元素符号表示的意义不同。下列对元素符号表示的意义解释正确的是( )
序号 元素符号 元素符号所表示的意义
A H 只表示氢元素
B Fe 表示铁元素,表示一个铁原子,表示铁这种物质
C N 只表示一个氮原子
D O 表示氧元素,表示一个氧原子,表示氧气这种物质
A.A B.B C.C D.D
8.下列推理或归纳合理的是( )
A.氮离子和氩原子最外层电子数相同
B.离子是带电粒子,所以带电的粒子一定是离子
C.在化合物中金属元素一定显正价,非金属元素可能显负价
D.氢原子和氦原子的化学性质相似
9.卢瑟福的粒子轰击金属箔实验推翻了汤姆森在1903年提出的原子结构模型,为建立现代原子理论打下了基础。该实验能证明的是( )
A.粒子带正电,原子不是实心球体,大部分空间是空的
B.原子始终在做无规则运动
C.原子核是由质子和中子组成的
D.原子核带正电荷
10.科学模型不仅可以表示静止的物体,还可以表示物质变化的过程。水的电解过程可用模型表示如图所示。下列说法中,正确的是( )
A.物质都是由分子构成的
B.分子与原子的本质区别是分子能再分,而原子不能再分
C.在水电解反应前后,原子的种类和数目都没有发生变化
D.在光学显微镜下能看见水分子被破坏,原子重新组合成新分子的过程
11.作为相对原子质量标准的碳—12可以写成,1个原子的质量为a千克,1个分子的质量为b千克,若以,分子中的1个氧原子质量的作为相对原子质量的标准,则的相对分子质量是( )
A. B. C. D.
12.市场上销售的一种食用盐——竹盐,其中富含钙、镁、锌、硒、铁等。这里的钙、镁、锌、硒、铁是指( )
A.分子 B.原子 C.元素 D.单质
二、填空题
13.(1)一种有趣的钟表式周期表如图所示,请根据时针所对应的元素填空:
①6:00对应的元素是___________(填“金属”或“非金属”)元素。
②10:00对应的元素___________(填“易”或“难”)形成化合物。
③12:00时,时针对应元素的离子符号是___________。
(2)从钟表上的元素中选择适当元素组成符合要求的物质,相对分子质量最小的氧化物是___________。
14.(1)A是地壳中含量最高的金属元素,B元素的一种气体单质支持人类呼吸,A和B组成化合物的化学式______。
(2)标出中氮元素的化合价______;
(3)保持水的化学性质的最小粒子______;
(4)高锰酸钾中含有的阴离子______;
(5)氧离子的最外层电子数是______;
(6)写出中“2”的意义______。
15.连花清瘟胶囊源自传统中医名方,被国家药品监督管理局批准用于“新型冠状病毒肺炎轻型、普通型”的治疗,在新冠肺炎患者救治中发挥了重要作用,成为抗疫热点中成药。经科学家检测,其有效成分之一是没食子酸。没食子酸的化学式为:,已知其相对分子质量为170,求:
(1)没食子酸中碳、氢原子的原子个数比为______。
(2)没食子酸中碳、氢元素的质量比为______。
(3)没食子酸的化学式中,x=______。
(4)______g没食子酸中含有42g碳元素。
16.看图并回答下列问题:
(1)小金设置了两层花盆,如甲图,内层花盆底部开有孔,将多余的水流入外层花盆与内层花盆之间储存,可以几个月不用浇水。但浇水量超过图中水位线会引起烂根的原因是___________。
(2)图乙和图丙都是电磁限流器的示意图。当电路中电流过大时,电磁铁吸引衔铁B,接点C、D被弹簧拉起(C、D为动触点),电路切断。电路切断后,___________(选填“图乙”或“图丙”)所示的电磁限流器能自动复原。
(3)如图丁所示,1911年卢瑟福等人为了探究原子内部结构的奥秘进行了上述实验,他们用一束带正电、质量比电子大得多的高速运动的ɑ粒子轰击金箱,发现:①大多数ɑ粒子能穿过金箔而不改变原来的运动方向;②一小部分ɑ粒子改变了原来的运动方向;③有极少数ɑ粒子被弹了回来。请你根据原子结构的认识,分析上述现象的原因:现象①的原因是原子核很小,原子内部有很大空间。现象②的原因是原子核带___________(选填“正"或“负”)电,ɑ粒子轰击金原子核时,受到斥力而改变了运动方向。现象③的原因是___________。
17.请用化学用语表示
(1)镁离子的符号___________;
(2)正二价的铜元素___________;
(3)保持氯化钠化学性质的微粒符号___________;
(4)符号“2Fe”中数字2的含义___________。
18.现有下列物质:①水银②氧化镁③液氧④自来水⑤冰水混合物⑥食盐溶液其中属于单质的是______;属于化合物的是______;属于混合物的是______
三、简答题
19.新装修房间中往往会含有较多的甲醛,人体长期摄入超标的甲醛会对健康造成影响。甲醛的化学式为,请回答下列问题:
(1)甲醛由___________种元素组成。
(2)甲醛中碳、氢,氧元素的质量比为___________。(写最简整数比)
(3)计算甲醛中氢元素的质量分数。(保留两位小数)___________
20.人体中钙元素主要以羟基磷酸钙晶体形式存在于骨略和牙齿中,而牛奶是含钙丰富又易吸收的理想食品,下图为某乳业公可纯奶包装标签:
配料:鲜牛奶 净含量:/盒 营养成分(每) 蛋白质 钙 保质期:8个月
(1)羟基磷酸钙由___________种元素组成;
(2)羟基磷酸钙中钙、氧元素的质量比为多少___________(写出计算过程)
(3)若人体每天至少需要钙,每天已从食物中摄入所需钙的一半,则每天至少要喝这种牛奶___________盒。
(4)除了喝牛奶以外,青少年还可以通过服用含碳酸钙的钙片来补钙。求碳酸钙和多少质量的氢氧化钙所含的钙元素质量相等___________?(写出计算过程)
四、探究题
21.某化学兴趣小组利用下图所示装置测定样品中(样品中杂质高温下不分解,也不参加反应)的质量分数,请据图分析完成下列问题。
⑴实验开始时,应先挤压鼓气球持续一段时间,其目的是_____________________;白色粉末逐渐变蓝
⑵反应前准确称量样品的质量为5g,完全反应后C装置增加了1.62g,则样品中的质量分数为__________;
⑶若省去D装置,则实验所测定的样品中的质量分数比实际的质量分数会__________(填“偏大”、“偏小”或“不变”)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.B
5.D
6.D
7.B
8.AC
9.AD
10.C
11.A
12.C
13. 非金属 难 Mg2+ H2O
14. Al2O3 H2O 8 1个水分子中含有2个氧原子
15. 7:6 14:1 5 85
16. 水分过多,根无法进行有氧呼吸 丙 正 金原子核质量比α粒子大很多,且体积很小
17. Mg2+ Na+、Cl- 铁原子的个数为2个
18. ①③ ②⑤ ④⑥
19. 3 6:1:8 6.67%
20. 四 羟基磷酸钙晶体中各组成元素质量比Ca:O=(40×10):(16×26)=25:26 每100mL中含钙至少为0.12g,每盒250mL,则每盒至少含钙元素的质量为,人体每天至少需要来自牛奶的钙为0.6g×50%=0.3g,0.3g÷0.3g/盒=1盒 碳酸钙含钙元素质量为:,
所需氢氧化钙的质量为:
21. 除去装置中的空气,防止加热时发生爆炸 96% 偏大
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
