7.2常见的酸和碱课时作业---2021_2022学年九年级化学沪教版(全国)下册(word版 含答案)
文档属性
| 名称 | 7.2常见的酸和碱课时作业---2021_2022学年九年级化学沪教版(全国)下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 115.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-02 00:00:00 | ||
图片预览

文档简介
7.2常见的酸和碱课时作业
一、选择题:
1、下列关于氢氧化钙的描述不正确的是( )
A.是熟石灰的主要成分 B.对皮肤、衣服等有腐蚀作用
C.水溶液俗称石灰水 D.白色粉末状固体,易潮解
2、氢氧化钙可用于改良酸性土壤,其俗称是( )
A.火碱 B.熟石灰 C.烧碱 D.纯碱
3、下列关于盐酸、硫酸的描述,错误的是( )
A.浓硫酸是黏稠、油状的无色液体
B.浓盐酸和浓硫酸都可以在空气中敞口放置
C.浓盐酸有较强的挥发性
D.浓硫酸有吸水性,可作某些气体的干燥剂
4、我们学习了一些物质,并能进行简单地分类。下列各组内物质表示同一种物质的是( )
A.氢氧化钠、烧碱 B.氢氧化钙、生石灰
C.紫铜、黄铜 D.干冰、水
5、下列物质能除去铁锈的是( )
A.盐酸 B.汽油 C.NaOH溶液 D.酒精
6、草酸是自然界中普遍存在的一种酸,推测它不可能具有的化学性质或用途是( )
A.能用于除铁锈
B.能与二氧化碳反应
C.能与酸碱指示剂作用
D.能用于除水壶内的水垢(CaCO3)
7、室温下,向滴有酚酞试液的盐酸中加入一定量的蒸馏水后溶液的颜色为( )
A.无色 B.红色 C.蓝色 D.紫色
8、下列反应中不属于复分解反应的是( )
A.Na2CO3+2HCl═2NaCl+H2O+CO2↑
B.2NaOH+H2SO4═Na2SO4+2H2O
C.CO2+2NaOH═Na2CO3+H2O
D.Fe2O3+6HCl═2FeCl3+3H2O
9、建立模型是学习化学的重要方法。下列有关模型正确的是( )
A.灭火方法模型 B.原子结构模型
C.氧化反应与复分解反应的关系模型 D.空气组成模型
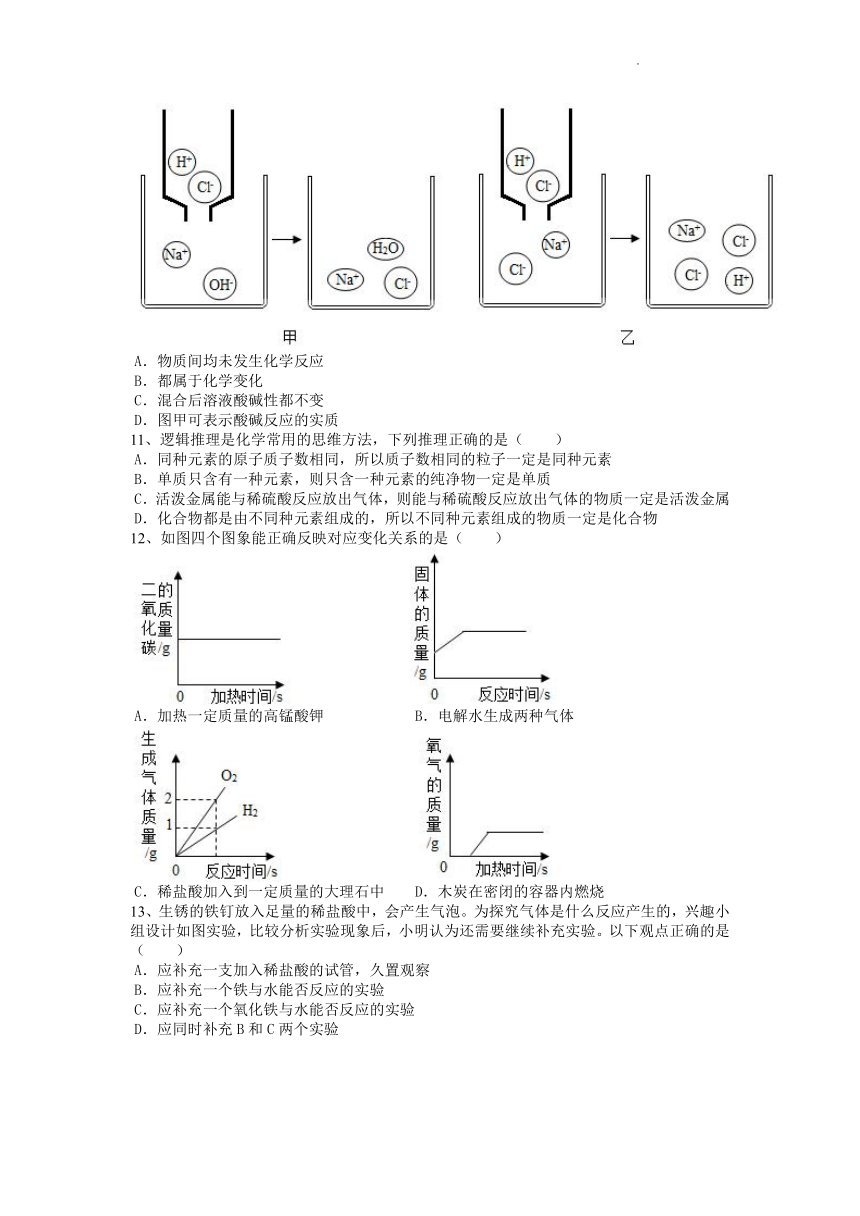
10、将稀HCl分别滴入NaOH溶液和NaCl溶液中,充分混合后均无明显现象。混合后相关变化的微观示意图如图,下列说法正确的是( )
A.物质间均未发生化学反应
B.都属于化学变化
C.混合后溶液酸碱性都不变
D.图甲可表示酸碱反应的实质
11、逻辑推理是化学常用的思维方法,下列推理正确的是( )
A.同种元素的原子质子数相同,所以质子数相同的粒子一定是同种元素
B.单质只含有一种元素,则只含一种元素的纯净物一定是单质
C.活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属
D.化合物都是由不同种元素组成的,所以不同种元素组成的物质一定是化合物
12、如图四个图象能正确反映对应变化关系的是( )
A.加热一定质量的高锰酸钾 B.电解水生成两种气体
C.稀盐酸加入到一定质量的大理石中 D.木炭在密闭的容器内燃烧
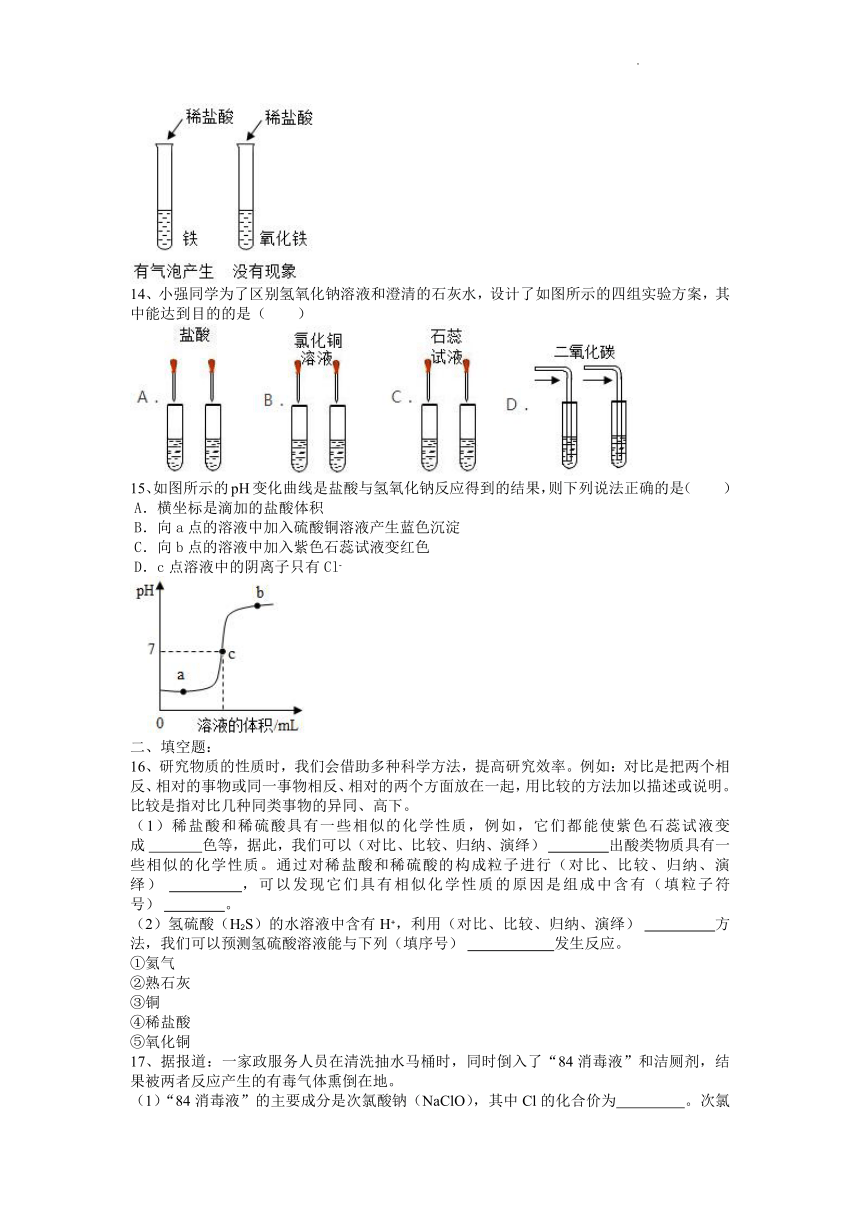
13、生锈的铁钉放入足量的稀盐酸中,会产生气泡。为探究气体是什么反应产生的,兴趣小组设计如图实验,比较分析实验现象后,小明认为还需要继续补充实验。以下观点正确的是( )
A.应补充一支加入稀盐酸的试管,久置观察
B.应补充一个铁与水能否反应的实验
C.应补充一个氧化铁与水能否反应的实验
D.应同时补充B和C两个实验
14、小强同学为了区别氢氧化钠溶液和澄清的石灰水,设计了如图所示的四组实验方案,其中能达到目的的是( )
15、如图所示的pH变化曲线是盐酸与氢氧化钠反应得到的结果,则下列说法正确的是( )
A.横坐标是滴加的盐酸体积
B.向a点的溶液中加入硫酸铜溶液产生蓝色沉淀
C.向b点的溶液中加入紫色石蕊试液变红色
D.c点溶液中的阴离子只有Cl-
二、填空题:
16、研究物质的性质时,我们会借助多种科学方法,提高研究效率。例如:对比是把两个相反、相对的事物或同一事物相反、相对的两个方面放在一起,用比较的方法加以描述或说明。比较是指对比几种同类事物的异同、高下。
(1)稀盐酸和稀硫酸具有一些相似的化学性质,例如,它们都能使紫色石蕊试液变成 色等,据此,我们可以(对比、比较、归纳、演绎) 出酸类物质具有一些相似的化学性质。通过对稀盐酸和稀硫酸的构成粒子进行(对比、比较、归纳、演绎) ,可以发现它们具有相似化学性质的原因是组成中含有(填粒子符号) 。
(2)氢硫酸(H2S)的水溶液中含有H+,利用(对比、比较、归纳、演绎) 方法,我们可以预测氢硫酸溶液能与下列(填序号) 发生反应。
①氦气
②熟石灰
③铜
④稀盐酸
⑤氧化铜
17、据报道:一家政服务人员在清洗抽水马桶时,同时倒入了“84消毒液”和洁厕剂,结果被两者反应产生的有毒气体熏倒在地。
(1)“84消毒液”的主要成分是次氯酸钠(NaClO),其中Cl的化合价为 。次氯酸钠(NaClO) 与盐酸混合后,会生成氯化钠、水及有毒的氯气。请你写出此反应的化学方程式: 。
(2)目前市场上的洁厕剂大多为酸性,含有一定量的稀酸(如稀盐酸、稀磷酸等),具有腐蚀性。下列物体中,表面可用这类洁厕剂清洗的是 。
A.大理石台面(主要成分是CaCO3)
B.釉面砖(釉面的主要成分是SiO2)
C.不锈钢管
(3)洁厕剂中的稀盐酸可用来除锈,写出反应的化学方程式 ,白醋、柠檬酸溶液也能发生类似的反应,因为白醋、柠檬酸溶液、盐酸中都含有 (填离子符号)离子。
18、在圆底烧瓶中充满CO2气体,通过注射器向瓶中注入液体(图1)。图2是向烧瓶中分别注入同体积水和氢氧化钠溶液后通过传感器得到的瓶内气压变化图象。
回答下列问题:
(1)开始向烧瓶内加入水或氢氧化钠溶液,短暂时间内瓶内气体压强增大,原因是什么?
(2)通过曲线①,并不能得出“二氧化碳与水发生了化学反应”的结论,为什么?
(3)对比曲线①和②,能否说明氢氧化钠与CO2发生了化学反应?说明理由。
19、氢氧化钠溶液与稀盐酸反应时无明显现象,为了确定该反应是否发生,某同学设计了如图1所示的实验探究方案,回答下列问题:
(1)玻璃棒在该实验中的作用 ;
(2)仿照填写变化后的粒子符号(如图2):C: 、D: ;
(3)下列关于该实验方案中,能证明氢氧化钠溶液与盐酸发生反应的是 (填序号)。
A.用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀盐酸,测定溶液的pH逐渐减小,最终小于7
B.用温度计测量氢氧化钠溶液在滴加稀盐酸前后的温度,发现其明显上升
C.蒸发反应后所得的无色溶液得到白色的固体
D.向氢氧化钠溶液中滴加稀盐酸,再滴加硫酸铜溶液,有蓝色沉淀生成
三、实验题:
20、小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈 性,还可能呈 性。
【实验验证】
实验操作 实验现象 结论
用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 无色酚酞试液变 溶液呈碱性
无色酚酞试液不变色 溶液呈
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是 (填写微粒符号)。
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:方案:取样,加入碳酸钠溶液,若观察到 ,则所取溶液呈酸性;若无明显现象,则呈中性。
(3)从微观粒子的角度分析,该反应的实质是 。
参考答案
一、选择题:
1、D 2、B 3、B 4、A 5、A 6、B 7、A 8、B 9、D 10、D
11、B 12、A 13、B 14、D 15、D
二、填空题:
16、答案:(1)红;归纳;比较;H+;
(2)演绎;②⑤。
17、答案:(1)+1;NaClO+2HCl=NaCl+H2O+Cl2↑;
(2)B;
(3)Fe2O3+6HCl=2FeCl3+3H2O;H+。
18、答案:(1)瓶内空间减小,气体被压缩(气体体积减小)而使压强增大;
(2)二氧化碳能溶解于水,也会使气压发生改变;
(3)能;加氢氧化钠溶液时,最终气压接近于0,说明气体几乎不存在了。
19、答案:(1)搅拌使反应更充分;
(2)Na+、Cl-;H2O;
(3)AB。
三、实验题:
20、答案:【提出猜想】中;酸;
【实验验证】红色;中性或酸性;
【分析与思考】(1)OH-;(2)有气泡产生;(3)氢离子和氢氧根离子结合生成水分子。
一、选择题:
1、下列关于氢氧化钙的描述不正确的是( )
A.是熟石灰的主要成分 B.对皮肤、衣服等有腐蚀作用
C.水溶液俗称石灰水 D.白色粉末状固体,易潮解
2、氢氧化钙可用于改良酸性土壤,其俗称是( )
A.火碱 B.熟石灰 C.烧碱 D.纯碱
3、下列关于盐酸、硫酸的描述,错误的是( )
A.浓硫酸是黏稠、油状的无色液体
B.浓盐酸和浓硫酸都可以在空气中敞口放置
C.浓盐酸有较强的挥发性
D.浓硫酸有吸水性,可作某些气体的干燥剂
4、我们学习了一些物质,并能进行简单地分类。下列各组内物质表示同一种物质的是( )
A.氢氧化钠、烧碱 B.氢氧化钙、生石灰
C.紫铜、黄铜 D.干冰、水
5、下列物质能除去铁锈的是( )
A.盐酸 B.汽油 C.NaOH溶液 D.酒精
6、草酸是自然界中普遍存在的一种酸,推测它不可能具有的化学性质或用途是( )
A.能用于除铁锈
B.能与二氧化碳反应
C.能与酸碱指示剂作用
D.能用于除水壶内的水垢(CaCO3)
7、室温下,向滴有酚酞试液的盐酸中加入一定量的蒸馏水后溶液的颜色为( )
A.无色 B.红色 C.蓝色 D.紫色
8、下列反应中不属于复分解反应的是( )
A.Na2CO3+2HCl═2NaCl+H2O+CO2↑
B.2NaOH+H2SO4═Na2SO4+2H2O
C.CO2+2NaOH═Na2CO3+H2O
D.Fe2O3+6HCl═2FeCl3+3H2O
9、建立模型是学习化学的重要方法。下列有关模型正确的是( )
A.灭火方法模型 B.原子结构模型
C.氧化反应与复分解反应的关系模型 D.空气组成模型
10、将稀HCl分别滴入NaOH溶液和NaCl溶液中,充分混合后均无明显现象。混合后相关变化的微观示意图如图,下列说法正确的是( )
A.物质间均未发生化学反应
B.都属于化学变化
C.混合后溶液酸碱性都不变
D.图甲可表示酸碱反应的实质
11、逻辑推理是化学常用的思维方法,下列推理正确的是( )
A.同种元素的原子质子数相同,所以质子数相同的粒子一定是同种元素
B.单质只含有一种元素,则只含一种元素的纯净物一定是单质
C.活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属
D.化合物都是由不同种元素组成的,所以不同种元素组成的物质一定是化合物
12、如图四个图象能正确反映对应变化关系的是( )
A.加热一定质量的高锰酸钾 B.电解水生成两种气体
C.稀盐酸加入到一定质量的大理石中 D.木炭在密闭的容器内燃烧
13、生锈的铁钉放入足量的稀盐酸中,会产生气泡。为探究气体是什么反应产生的,兴趣小组设计如图实验,比较分析实验现象后,小明认为还需要继续补充实验。以下观点正确的是( )
A.应补充一支加入稀盐酸的试管,久置观察
B.应补充一个铁与水能否反应的实验
C.应补充一个氧化铁与水能否反应的实验
D.应同时补充B和C两个实验
14、小强同学为了区别氢氧化钠溶液和澄清的石灰水,设计了如图所示的四组实验方案,其中能达到目的的是( )
15、如图所示的pH变化曲线是盐酸与氢氧化钠反应得到的结果,则下列说法正确的是( )
A.横坐标是滴加的盐酸体积
B.向a点的溶液中加入硫酸铜溶液产生蓝色沉淀
C.向b点的溶液中加入紫色石蕊试液变红色
D.c点溶液中的阴离子只有Cl-
二、填空题:
16、研究物质的性质时,我们会借助多种科学方法,提高研究效率。例如:对比是把两个相反、相对的事物或同一事物相反、相对的两个方面放在一起,用比较的方法加以描述或说明。比较是指对比几种同类事物的异同、高下。
(1)稀盐酸和稀硫酸具有一些相似的化学性质,例如,它们都能使紫色石蕊试液变成 色等,据此,我们可以(对比、比较、归纳、演绎) 出酸类物质具有一些相似的化学性质。通过对稀盐酸和稀硫酸的构成粒子进行(对比、比较、归纳、演绎) ,可以发现它们具有相似化学性质的原因是组成中含有(填粒子符号) 。
(2)氢硫酸(H2S)的水溶液中含有H+,利用(对比、比较、归纳、演绎) 方法,我们可以预测氢硫酸溶液能与下列(填序号) 发生反应。
①氦气
②熟石灰
③铜
④稀盐酸
⑤氧化铜
17、据报道:一家政服务人员在清洗抽水马桶时,同时倒入了“84消毒液”和洁厕剂,结果被两者反应产生的有毒气体熏倒在地。
(1)“84消毒液”的主要成分是次氯酸钠(NaClO),其中Cl的化合价为 。次氯酸钠(NaClO) 与盐酸混合后,会生成氯化钠、水及有毒的氯气。请你写出此反应的化学方程式: 。
(2)目前市场上的洁厕剂大多为酸性,含有一定量的稀酸(如稀盐酸、稀磷酸等),具有腐蚀性。下列物体中,表面可用这类洁厕剂清洗的是 。
A.大理石台面(主要成分是CaCO3)
B.釉面砖(釉面的主要成分是SiO2)
C.不锈钢管
(3)洁厕剂中的稀盐酸可用来除锈,写出反应的化学方程式 ,白醋、柠檬酸溶液也能发生类似的反应,因为白醋、柠檬酸溶液、盐酸中都含有 (填离子符号)离子。
18、在圆底烧瓶中充满CO2气体,通过注射器向瓶中注入液体(图1)。图2是向烧瓶中分别注入同体积水和氢氧化钠溶液后通过传感器得到的瓶内气压变化图象。
回答下列问题:
(1)开始向烧瓶内加入水或氢氧化钠溶液,短暂时间内瓶内气体压强增大,原因是什么?
(2)通过曲线①,并不能得出“二氧化碳与水发生了化学反应”的结论,为什么?
(3)对比曲线①和②,能否说明氢氧化钠与CO2发生了化学反应?说明理由。
19、氢氧化钠溶液与稀盐酸反应时无明显现象,为了确定该反应是否发生,某同学设计了如图1所示的实验探究方案,回答下列问题:
(1)玻璃棒在该实验中的作用 ;
(2)仿照填写变化后的粒子符号(如图2):C: 、D: ;
(3)下列关于该实验方案中,能证明氢氧化钠溶液与盐酸发生反应的是 (填序号)。
A.用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀盐酸,测定溶液的pH逐渐减小,最终小于7
B.用温度计测量氢氧化钠溶液在滴加稀盐酸前后的温度,发现其明显上升
C.蒸发反应后所得的无色溶液得到白色的固体
D.向氢氧化钠溶液中滴加稀盐酸,再滴加硫酸铜溶液,有蓝色沉淀生成
三、实验题:
20、小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈 性,还可能呈 性。
【实验验证】
实验操作 实验现象 结论
用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 无色酚酞试液变 溶液呈碱性
无色酚酞试液不变色 溶液呈
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是 (填写微粒符号)。
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:方案:取样,加入碳酸钠溶液,若观察到 ,则所取溶液呈酸性;若无明显现象,则呈中性。
(3)从微观粒子的角度分析,该反应的实质是 。
参考答案
一、选择题:
1、D 2、B 3、B 4、A 5、A 6、B 7、A 8、B 9、D 10、D
11、B 12、A 13、B 14、D 15、D
二、填空题:
16、答案:(1)红;归纳;比较;H+;
(2)演绎;②⑤。
17、答案:(1)+1;NaClO+2HCl=NaCl+H2O+Cl2↑;
(2)B;
(3)Fe2O3+6HCl=2FeCl3+3H2O;H+。
18、答案:(1)瓶内空间减小,气体被压缩(气体体积减小)而使压强增大;
(2)二氧化碳能溶解于水,也会使气压发生改变;
(3)能;加氢氧化钠溶液时,最终气压接近于0,说明气体几乎不存在了。
19、答案:(1)搅拌使反应更充分;
(2)Na+、Cl-;H2O;
(3)AB。
三、实验题:
20、答案:【提出猜想】中;酸;
【实验验证】红色;中性或酸性;
【分析与思考】(1)OH-;(2)有气泡产生;(3)氢离子和氢氧根离子结合生成水分子。
