第2章 微粒的模型与符号 单元培优测试(含答案)
文档属性
| 名称 | 第2章 微粒的模型与符号 单元培优测试(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 528.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-03-13 00:00:00 | ||
图片预览


文档简介
浙教版八年级下册科学第二章 微粒的模型与符号 单元培优测试
一、选择题(共20题,40分)
1.下列图示不属于模型的是( )
A. B. C. D.
2.关于原子及原子结构发现史的说法不正确的是( )
A. 汤姆森、卢瑟福两位科学家都是在实验的基础上,通过推理和想象建构原子模型
B. 汤姆森发现了电子,证实原子是可分的
C. 原子的最外层电子数发生变化时,元素的种类也发生了变化
D. 原子在化学变化中的表现主要取决于原子的最外层电子
3.人类用于制造触屏材料的铟,相关信息如图,下列说法中正确的是( )
A. 铟是一种非金属元素 B. 原子的核电荷数为 49
C. 与其他元素根本区别是中子数不同 D. 相对原子质量是 114.8 克
4.如下图为某原子结构模型的示意图,其中a、b、c是构成该原子的三种不同粒子,下列说法正确的是( )
A. 原子中 a 与 c 的数目一定相同 B. 原子中 b 与 c 的数目一定相同
C. 决定该原子种类的是 b 粒子的数目 D. 原子的质量集中在a 和 c 上
5.下列关于元素符号“H”的说法中,正确的是( )
①表示氢元素 ②表示氢气 ③表示1个氢原子 ④表示1个氢分子
A. ①② B. ②③ C. ①③ D. ②④
6.关于科学符号中数字“2”的含义,下列解释错误的是( )
A. N2:表示氮气分子的个数为2 B. :表示氧化镁中镁元素的化合价为+2价
C. 2Al:表示铝原子的个数为2 D. S2-:表示一个硫离子带2个单位负电荷
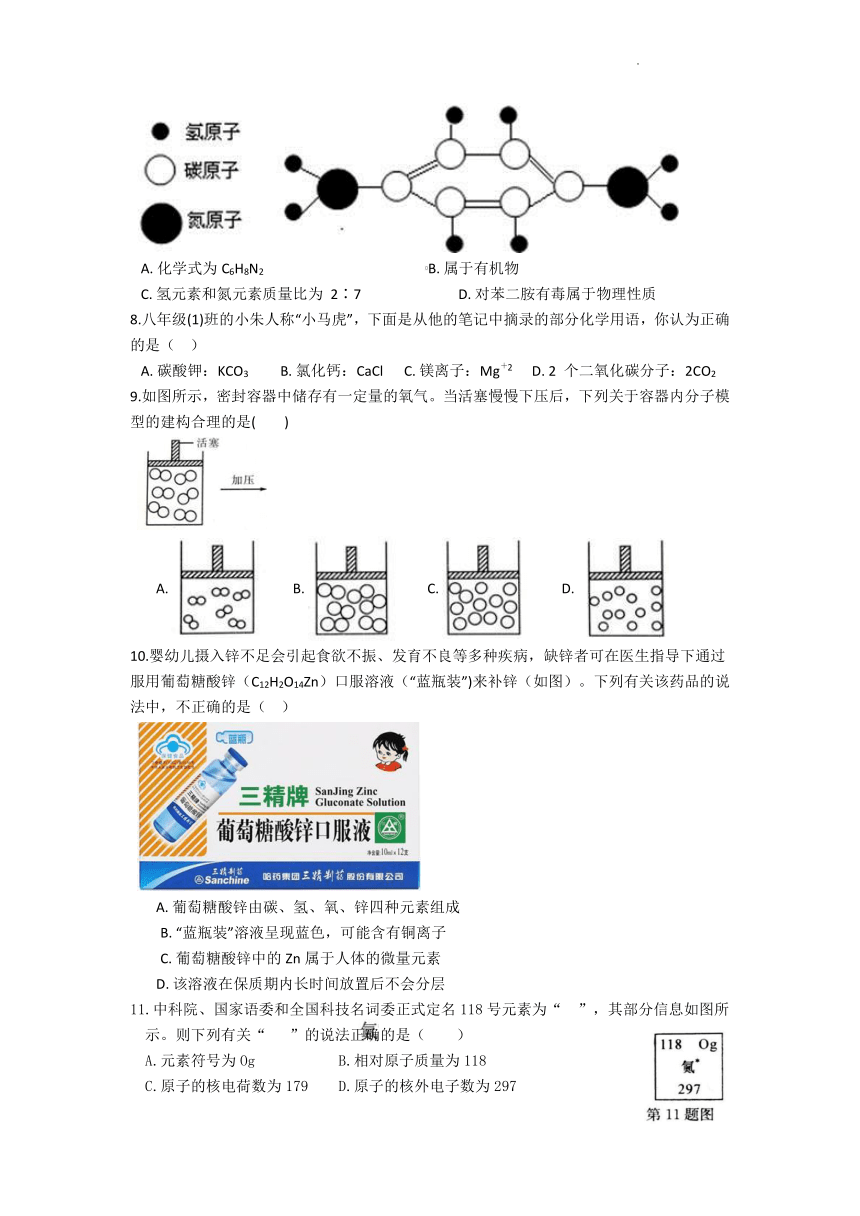
7.染发时一般要用到一种着色剂“对苯二胺”,它是一种有毒的化学药品,有致癌性,会 对染发者的身体带来伤害,其分子结构如图所示。下列有关对苯二胺的说法错误的是( )
A. 化学式为C6H8N2 B. 属于有机物
C. 氢元素和氮元素质量比为 2∶7 D. 对苯二胺有毒属于物理性质
8.八年级(1)班的小朱人称“小马虎”,下面是从他的笔记中摘录的部分化学用语,你认为正确的是( )
A. 碳酸钾:KCO3 B. 氯化钙:CaCl C. 镁离子:Mg+2 D. 2 个二氧化碳分子:2CO2
9.如图所示,密封容器中储存有一定量的氧气。当活塞慢慢下压后,下列关于容器内分子模型的建构合理的是( )
A. B. C. D.
10.婴幼儿摄入锌不足会引起食欲不振、发育不良等多种疾病,缺锌者可在医生指导下通过服用葡萄糖酸锌(C12H2O14Zn)口服溶液(“蓝瓶装”)来补锌(如图)。下列有关该药品的说法中,不正确的是( )
A. 葡萄糖酸锌由碳、氢、氧、锌四种元素组成
B. “蓝瓶装”溶液呈现蓝色,可能含有铜离子
C. 葡萄糖酸锌中的Zn属于人体的微量元素
D. 该溶液在保质期内长时间放置后不会分层
11.中科院、国家语委和全国科技名词委正式定名118号元素为“ ”,其部分信息如图所示。则下列有关“ ”的说法正确的是( )
A.元素符号为Og B.相对原子质量为118
C.原子的核电荷数为179 D.原子的核外电子数为297
12.我国探月工程的一项重要计划,是对月球氦-3含量和分布进行一次由空间到实地的详细勘察,为人类未来利用月球核能奠定坚实的基础。如图是氦-3原子结构示意图,根据该图,我们还不能获得的信息是( )
A.氦-3原子的核外电子数 B.氦-3原子的相对原子质量
C.氦-3原子的核电荷数 D.氦-3原子核的运动规律
13.用 和 代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如图所示,下列说法正确的是( )
A.该反应前后原子种类和数目没有改变,所以属于化学变化
B.该反应的生成物是一种氧化物
C.参加反应的物质在反应前后元素的化合价都发生了改变
D.参加反应的 和 分子的个数比是2:1
14.如图形象地表示了氯化钠的形成过程。下列相关叙述不正确的是( )
A.钠原子在化学反应中容易失去电子 B.钠原子与钠离子都不显电性
C.氯原子得1个电子形成氯离子 D.氯化钠由钠离子和氯离子构成
15.核外电子数相同,核内质子数不同的两种粒子,它们可能是( )
①一种元素的原子和另一种元素的离子 ②同种元素的原子和离子
③两种不同元素的原子 ④两种不同元素的离子
A.①③ B.①④ C.②③ D.③④
16.在“测土配方施肥”技术中,农技员对某土地检测后准备施加CO(NH2)2和KH2PO4的固体混合物,要求固体混合物中氮元素和氧元素的质量比为7:12,则固体混合物中CO(NH2)2和KH2PO4的质量比为( )
A.10:17 B.15:17 C.5:17 D.15:34
17.豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其中含量最多的是亮氨酸(C6H13NO2),关于亮氨酸的说法正确的是( )
A.亮氨酸是由碳原子、氢原子、氮原子、氧原子构成
B.亮氨酸中碳元素的质量分数为27.3%
C.一个亮氨酸分子由22个原子构成
D.亮氨酸中碳、氢、氮、氧四种元素的质量比为6:13:l:2
18.由X、Y两种元素组成的化合物XY3中X的质量分数为40%.由X与Y组成的另一种化合物中含X50%,则后一种化合物的化学式为( )
A.XY B.X2Y C.XY2 D.X2Y3
19.某同学测得海水中含有Cl﹣的质量分数为2.19%,如果其中的Cl﹣全部以NaCl计算,则海水中所含NaCl的质量分数是( )
A.2.18% B.5.85% C.3.61% D.4.19%
20.已知NaHS、MgSO4、NaHSO3组成的混合物中,硫元素的质量为a%,则混合物中氧元素的质量分数是( )
A.a% B.2a%
C.(100﹣1.75a)% D.(1﹣0.75a)%
二、填空题(共5题,20分)
21.化学符号及其意义
(1)用化学符号表示:①氯气________;②n个镁离子________。
(2)写出“ ”中数字的含义:“4”________;“6”________。
22.卢瑟福核式结构模型是利用 α 粒子轰击金箔实验的基础上提出的。
(1)下列能正确反映他的实验结果的示意图是________(选填序号)。
(2)从原子结构模型建立的过程中,我们发现( )(选填序号)
A. 科学模型的建立是一个不断完善、不断修正的过程
B. 模型在科学研究中起着很重要的作用
C. 波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界
D. 人类借助模型的建立,对原子的认识逐渐接近本质
23.“水循环”和“碳循环”是自然界存在的两大重要循环,结合你所学到的科学知识回答下面有关问题。
(1)从微观的角度看,水分子是由________构成的。
(2)从宏观的角度看,二氧化碳是由________组成的。
(3)从分子、原子及元素的角度看,地球表面的“水循环”主要是由________的运动引起的,自然界“碳循环”中的“碳”是指________。
24.下表微粒中,是阳离子的是________,互为同位素的是________(选填字母)。
组别 质子 中子 电子
A 14 14 14
B 26 30 24
C 26 30 26
D 14 16 14
25.已知C2H4、C3H6、C4H8属于同一类型的有机物,称作烯烃,它们的化学式的通式为CnH2n(n代表分子中碳原子个数)。CH4、C2H6、C3H8属于另一类型的有机物,称作烷烃,则碳原子数为9的烷烃的化学式为________,烷烃的化学式的通式为________(用n代表分子中碳原子个数)。
三、实验探究题(10分)
26.电子带负电,原子不带电,说明原子内存在着带正电荷的部分,它们是均匀分布还是集中分布的呢?1910 年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验做法如图:
绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到 180°,像是被金箔弹了回来。
【猜想与假设】α 粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)大多数 α 粒子不改变原来的运动方向,原因是________。
(2)若原子质量、正电荷在原子内均匀分布,则极少数 α 粒子就________(填“会”或“不 会”)发生大角度散射。卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结 构上”中的“很小的结构”指的是________。
(3)科学家对原子结构的探究经历了三个过程,通过 α 粒子散射实验,你认为原子结构为 以下的________。
计算题(共5题,30分)
27.已知一个CO分子的质量为n千克,一个CO2分子的质量为m千克(假设两种分子中碳、氧原子分别具有相同的中子数),若以碳原子质量的为标准,则CO2的相对分子质量是 (用m,n表示).相同分子数的CO和CO2,氧元素的质量比为 ;相同质量的CO和CO2,氧元素的质量比为 .
28.清凉甘甜的汽水中常含柠檬酸,已知柠檬酸的化学式为C6H8Ox,请回答:
(1)已知柠檬酸的相对分子质量为192,则x为
(2)38.4g柠檬酸含氢元素 g.
29.苹果中富含苹果酸,具有增强消化,降低有害胆固醇等作用,苹果酸的分子式为 C4H6O5.试回答下列问题:
①苹果酸的一个分子由 个原子构成,苹果酸的相对分子质量是 ;(每空1分)
②苹果酸中氢、氧两种元素的质量比是 (最简整数比);(每空1分)
③13.4g苹果酸中含碳元素质量为 g(计算结果精确至0.1g)。(每空2分)
30.硝酸铵是一种化肥,化学式是NH4NO3.试计算:
(1)硝酸铵中氮元素的质量分数;
(2)60kg硝酸铵中含有多少氮元素;
(3)多少千克尿素[CO(NH2)2]与40kg硝酸铵中所含氮元素的质量相当?
(4)此化肥中硝酸铵的质量分数为40%,则化肥样品中氮元素的质量分数为 (精确到0.1%)?
31.工业上常用赤铁矿(主要成分是Fe2O3)、磁铁矿(主要成分是Fe3O4)炼铁.计算:
①Fe2O3的相对分子质量= ;
②Fe3O4中铁元素和氧元素的质量比= ;
③通过计算说明,Fe3O4和Fe2O3哪种铁的氧化物含铁量更高?
参考答案
1. D 2. C 3. B 4. A 5. C
6.A 7. D 8.D 9. B 10. B
11.A 12.D 13.C 14.B15.B
16.B 17.C 18.C 19.C 20.C
二、填空题
21.(1)Cl2;nMg2+
(2)每个硫酸根离子中含有4个氧原子;硫酸根离子中硫元素的化合价为+6价
22. (1)乙(2)A,B,D
23. (1)氢原子和氧原子(2)碳元素和氧元素
(3)水分子;二氧化碳
24. B;AD
25. C9H20;CnH2n+2
三、实验探究题
26.(1)原子核在原子中所占体积极小,大多数α粒子穿过原子内与原子间的空隙
(2)不会;原子核(3)C
四.解答题
27、;1:2;11:14;
28.、7;1.6;
29、15;134;3:40;4.8;
30、35%;21千克;30千克;14%
31、160;7:3;Fe2O3含铁量更高
一、选择题(共20题,40分)
1.下列图示不属于模型的是( )
A. B. C. D.
2.关于原子及原子结构发现史的说法不正确的是( )
A. 汤姆森、卢瑟福两位科学家都是在实验的基础上,通过推理和想象建构原子模型
B. 汤姆森发现了电子,证实原子是可分的
C. 原子的最外层电子数发生变化时,元素的种类也发生了变化
D. 原子在化学变化中的表现主要取决于原子的最外层电子
3.人类用于制造触屏材料的铟,相关信息如图,下列说法中正确的是( )
A. 铟是一种非金属元素 B. 原子的核电荷数为 49
C. 与其他元素根本区别是中子数不同 D. 相对原子质量是 114.8 克
4.如下图为某原子结构模型的示意图,其中a、b、c是构成该原子的三种不同粒子,下列说法正确的是( )
A. 原子中 a 与 c 的数目一定相同 B. 原子中 b 与 c 的数目一定相同
C. 决定该原子种类的是 b 粒子的数目 D. 原子的质量集中在a 和 c 上
5.下列关于元素符号“H”的说法中,正确的是( )
①表示氢元素 ②表示氢气 ③表示1个氢原子 ④表示1个氢分子
A. ①② B. ②③ C. ①③ D. ②④
6.关于科学符号中数字“2”的含义,下列解释错误的是( )
A. N2:表示氮气分子的个数为2 B. :表示氧化镁中镁元素的化合价为+2价
C. 2Al:表示铝原子的个数为2 D. S2-:表示一个硫离子带2个单位负电荷
7.染发时一般要用到一种着色剂“对苯二胺”,它是一种有毒的化学药品,有致癌性,会 对染发者的身体带来伤害,其分子结构如图所示。下列有关对苯二胺的说法错误的是( )
A. 化学式为C6H8N2 B. 属于有机物
C. 氢元素和氮元素质量比为 2∶7 D. 对苯二胺有毒属于物理性质
8.八年级(1)班的小朱人称“小马虎”,下面是从他的笔记中摘录的部分化学用语,你认为正确的是( )
A. 碳酸钾:KCO3 B. 氯化钙:CaCl C. 镁离子:Mg+2 D. 2 个二氧化碳分子:2CO2
9.如图所示,密封容器中储存有一定量的氧气。当活塞慢慢下压后,下列关于容器内分子模型的建构合理的是( )
A. B. C. D.
10.婴幼儿摄入锌不足会引起食欲不振、发育不良等多种疾病,缺锌者可在医生指导下通过服用葡萄糖酸锌(C12H2O14Zn)口服溶液(“蓝瓶装”)来补锌(如图)。下列有关该药品的说法中,不正确的是( )
A. 葡萄糖酸锌由碳、氢、氧、锌四种元素组成
B. “蓝瓶装”溶液呈现蓝色,可能含有铜离子
C. 葡萄糖酸锌中的Zn属于人体的微量元素
D. 该溶液在保质期内长时间放置后不会分层
11.中科院、国家语委和全国科技名词委正式定名118号元素为“ ”,其部分信息如图所示。则下列有关“ ”的说法正确的是( )
A.元素符号为Og B.相对原子质量为118
C.原子的核电荷数为179 D.原子的核外电子数为297
12.我国探月工程的一项重要计划,是对月球氦-3含量和分布进行一次由空间到实地的详细勘察,为人类未来利用月球核能奠定坚实的基础。如图是氦-3原子结构示意图,根据该图,我们还不能获得的信息是( )
A.氦-3原子的核外电子数 B.氦-3原子的相对原子质量
C.氦-3原子的核电荷数 D.氦-3原子核的运动规律
13.用 和 代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如图所示,下列说法正确的是( )
A.该反应前后原子种类和数目没有改变,所以属于化学变化
B.该反应的生成物是一种氧化物
C.参加反应的物质在反应前后元素的化合价都发生了改变
D.参加反应的 和 分子的个数比是2:1
14.如图形象地表示了氯化钠的形成过程。下列相关叙述不正确的是( )
A.钠原子在化学反应中容易失去电子 B.钠原子与钠离子都不显电性
C.氯原子得1个电子形成氯离子 D.氯化钠由钠离子和氯离子构成
15.核外电子数相同,核内质子数不同的两种粒子,它们可能是( )
①一种元素的原子和另一种元素的离子 ②同种元素的原子和离子
③两种不同元素的原子 ④两种不同元素的离子
A.①③ B.①④ C.②③ D.③④
16.在“测土配方施肥”技术中,农技员对某土地检测后准备施加CO(NH2)2和KH2PO4的固体混合物,要求固体混合物中氮元素和氧元素的质量比为7:12,则固体混合物中CO(NH2)2和KH2PO4的质量比为( )
A.10:17 B.15:17 C.5:17 D.15:34
17.豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其中含量最多的是亮氨酸(C6H13NO2),关于亮氨酸的说法正确的是( )
A.亮氨酸是由碳原子、氢原子、氮原子、氧原子构成
B.亮氨酸中碳元素的质量分数为27.3%
C.一个亮氨酸分子由22个原子构成
D.亮氨酸中碳、氢、氮、氧四种元素的质量比为6:13:l:2
18.由X、Y两种元素组成的化合物XY3中X的质量分数为40%.由X与Y组成的另一种化合物中含X50%,则后一种化合物的化学式为( )
A.XY B.X2Y C.XY2 D.X2Y3
19.某同学测得海水中含有Cl﹣的质量分数为2.19%,如果其中的Cl﹣全部以NaCl计算,则海水中所含NaCl的质量分数是( )
A.2.18% B.5.85% C.3.61% D.4.19%
20.已知NaHS、MgSO4、NaHSO3组成的混合物中,硫元素的质量为a%,则混合物中氧元素的质量分数是( )
A.a% B.2a%
C.(100﹣1.75a)% D.(1﹣0.75a)%
二、填空题(共5题,20分)
21.化学符号及其意义
(1)用化学符号表示:①氯气________;②n个镁离子________。
(2)写出“ ”中数字的含义:“4”________;“6”________。
22.卢瑟福核式结构模型是利用 α 粒子轰击金箔实验的基础上提出的。
(1)下列能正确反映他的实验结果的示意图是________(选填序号)。
(2)从原子结构模型建立的过程中,我们发现( )(选填序号)
A. 科学模型的建立是一个不断完善、不断修正的过程
B. 模型在科学研究中起着很重要的作用
C. 波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界
D. 人类借助模型的建立,对原子的认识逐渐接近本质
23.“水循环”和“碳循环”是自然界存在的两大重要循环,结合你所学到的科学知识回答下面有关问题。
(1)从微观的角度看,水分子是由________构成的。
(2)从宏观的角度看,二氧化碳是由________组成的。
(3)从分子、原子及元素的角度看,地球表面的“水循环”主要是由________的运动引起的,自然界“碳循环”中的“碳”是指________。
24.下表微粒中,是阳离子的是________,互为同位素的是________(选填字母)。
组别 质子 中子 电子
A 14 14 14
B 26 30 24
C 26 30 26
D 14 16 14
25.已知C2H4、C3H6、C4H8属于同一类型的有机物,称作烯烃,它们的化学式的通式为CnH2n(n代表分子中碳原子个数)。CH4、C2H6、C3H8属于另一类型的有机物,称作烷烃,则碳原子数为9的烷烃的化学式为________,烷烃的化学式的通式为________(用n代表分子中碳原子个数)。
三、实验探究题(10分)
26.电子带负电,原子不带电,说明原子内存在着带正电荷的部分,它们是均匀分布还是集中分布的呢?1910 年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验做法如图:
绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到 180°,像是被金箔弹了回来。
【猜想与假设】α 粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)大多数 α 粒子不改变原来的运动方向,原因是________。
(2)若原子质量、正电荷在原子内均匀分布,则极少数 α 粒子就________(填“会”或“不 会”)发生大角度散射。卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结 构上”中的“很小的结构”指的是________。
(3)科学家对原子结构的探究经历了三个过程,通过 α 粒子散射实验,你认为原子结构为 以下的________。
计算题(共5题,30分)
27.已知一个CO分子的质量为n千克,一个CO2分子的质量为m千克(假设两种分子中碳、氧原子分别具有相同的中子数),若以碳原子质量的为标准,则CO2的相对分子质量是 (用m,n表示).相同分子数的CO和CO2,氧元素的质量比为 ;相同质量的CO和CO2,氧元素的质量比为 .
28.清凉甘甜的汽水中常含柠檬酸,已知柠檬酸的化学式为C6H8Ox,请回答:
(1)已知柠檬酸的相对分子质量为192,则x为
(2)38.4g柠檬酸含氢元素 g.
29.苹果中富含苹果酸,具有增强消化,降低有害胆固醇等作用,苹果酸的分子式为 C4H6O5.试回答下列问题:
①苹果酸的一个分子由 个原子构成,苹果酸的相对分子质量是 ;(每空1分)
②苹果酸中氢、氧两种元素的质量比是 (最简整数比);(每空1分)
③13.4g苹果酸中含碳元素质量为 g(计算结果精确至0.1g)。(每空2分)
30.硝酸铵是一种化肥,化学式是NH4NO3.试计算:
(1)硝酸铵中氮元素的质量分数;
(2)60kg硝酸铵中含有多少氮元素;
(3)多少千克尿素[CO(NH2)2]与40kg硝酸铵中所含氮元素的质量相当?
(4)此化肥中硝酸铵的质量分数为40%,则化肥样品中氮元素的质量分数为 (精确到0.1%)?
31.工业上常用赤铁矿(主要成分是Fe2O3)、磁铁矿(主要成分是Fe3O4)炼铁.计算:
①Fe2O3的相对分子质量= ;
②Fe3O4中铁元素和氧元素的质量比= ;
③通过计算说明,Fe3O4和Fe2O3哪种铁的氧化物含铁量更高?
参考答案
1. D 2. C 3. B 4. A 5. C
6.A 7. D 8.D 9. B 10. B
11.A 12.D 13.C 14.B15.B
16.B 17.C 18.C 19.C 20.C
二、填空题
21.(1)Cl2;nMg2+
(2)每个硫酸根离子中含有4个氧原子;硫酸根离子中硫元素的化合价为+6价
22. (1)乙(2)A,B,D
23. (1)氢原子和氧原子(2)碳元素和氧元素
(3)水分子;二氧化碳
24. B;AD
25. C9H20;CnH2n+2
三、实验探究题
26.(1)原子核在原子中所占体积极小,大多数α粒子穿过原子内与原子间的空隙
(2)不会;原子核(3)C
四.解答题
27、;1:2;11:14;
28.、7;1.6;
29、15;134;3:40;4.8;
30、35%;21千克;30千克;14%
31、160;7:3;Fe2O3含铁量更高
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
