7.1溶液的酸碱性同步练习-2021-2022学年九年级化学沪教版(全国)下册(word版 含答案)
文档属性
| 名称 | 7.1溶液的酸碱性同步练习-2021-2022学年九年级化学沪教版(全国)下册(word版 含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 118.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-03-25 10:22:00 | ||
图片预览


文档简介
沪教版(全国) 7.1 溶液的酸碱性 同步练习
一、单选题
1.一些重要作物最适宜生长的土壤的pH范围如下:
作物 水稻 马铃薯 草莓 薄荷
pH 6~7 4.8~5.5 5~7.5 7~8
下列说法中正确的是( )A.水稻和薄荷生长都适宜酸性土壤
B.草莓生长只适宜酸性土壤
C.马铃薯生长不适宜碱性土壤
D.以上作物都不适宜碱性土壤
2.下列有关溶液酸碱性的说法错误的是( )
A.pH=7的溶液呈中性
B.pH>7的溶液一定呈碱性
C.pH<7的雨水一定是酸雨
D.酸溶液的pH越小酸性越强
3.一些食物的近似pH如下:
食物 葡萄汁 苹果汁 牛奶 鸡蛋清
pH 3.5~4.5 2.9~3.3 6.3~6.6 7.6~8.0
下列说法中不正确的是A.鸡蛋清和牛奶显碱性 B.苹果汁和葡萄汁显酸性
C.苹果汁比葡萄汁的酸性强 D.胃酸过多的人应少饮苹果汁和葡萄汁
4.下列溶液中,能使酚酞试液变红的是( )
A.烧碱溶液 B.稀硫酸 C.稀盐酸 D.食盐水
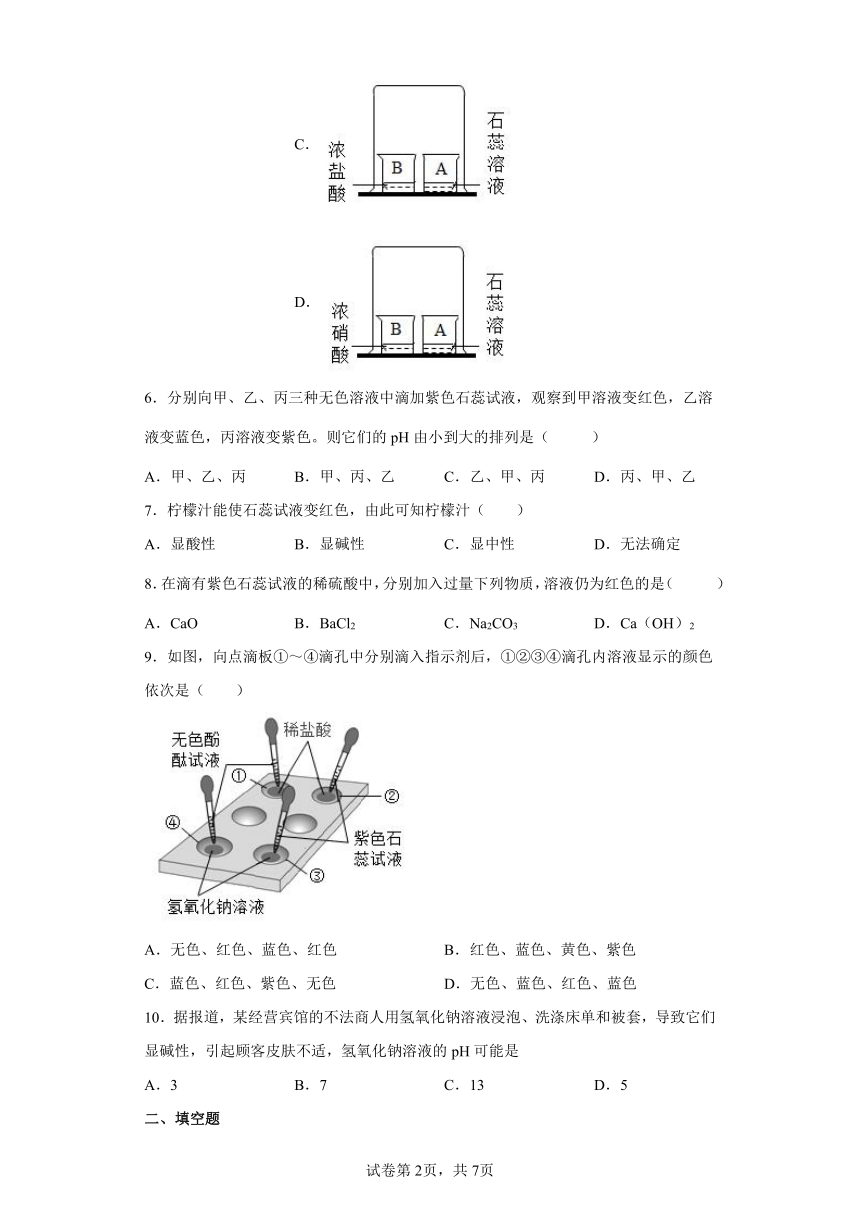
5.小明为验证“分子是运动的”,设计了四个实验。其中不能达到目的的是( )
A. B. C. D.
6.分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液,观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙 B.甲、丙、乙 C.乙、甲、丙 D.丙、甲、乙
7.柠檬汁能使石蕊试液变红色,由此可知柠檬汁( )
A.显酸性 B.显碱性 C.显中性 D.无法确定
8.在滴有紫色石蕊试液的稀硫酸中,分别加入过量下列物质,溶液仍为红色的是( )
A.CaO B.BaCl2 C.Na2CO3 D.Ca(OH)2
9.如图,向点滴板①~④滴孔中分别滴入指示剂后,①②③④滴孔内溶液显示的颜色依次是( )
A.无色、红色、蓝色、红色 B.红色、蓝色、黄色、紫色
C.蓝色、红色、紫色、无色 D.无色、蓝色、红色、蓝色
10.据报道,某经营宾馆的不法商人用氢氧化钠溶液浸泡、洗涤床单和被套,导致它们显碱性,引起顾客皮肤不适,氢氧化钠溶液的pH可能是
A.3 B.7 C.13 D.5
二、填空题
11.在化学晚会上,小华用玻璃棒蘸取一种液体在白纸上画上花,再蘸取另一种液体画上叶,将白纸挂在墙上,又用一种液体向纸上的叶、花喷洒,立即展现出“‘雨’落叶出红花开”的趣味景象。请你想一想,小华先后所用的液体可能是________ ,其化学原理是____________ 。
12.阿斯匹林的主要成分是乙酰水杨酸(化学式为C9H8O4),具有抑制血小板发挥作用的功能,是治疗心血管疾病的重要药物之一。
(1)乙酰水杨酸中氢、氧两种元素的质量比为_______。
(2)乙酰水杨酸具有酸性,若在其无色溶液中滴入紫色石蕊试液,观察到溶液呈____色。
13.现有白纸、溶质质量分数为20%的NaOH溶液(A)、溶质质量分数为10%的H2SO4溶液(B)和10%的紫色石蕊试液(C),设计“雨落叶出红花开”的趣味实验:先在白纸上用玻璃棒蘸取(填序号,下同)_____画上花,在蘸取_____画上叶.将白纸挂起来,用_____向纸上喷洒即可.实验的原理是_____.20%的NaOH溶液呈_____性,因此_____.10%的H2SO4呈_____性,因此_____.
14.化学与生产生活联系紧密,请用所学知识回答问题。
(1)“自热米饭”加热原理是生石灰与水接触放热,该反应的化学方程式为______。
(2)使用硬水会给生活带来许多麻烦,生活中可以用______区分软水和硬水。
(3)铝的化学性质很活泼,但家里用了很久的铝壶很少出现腐蚀,原因是______。
(4)“火立熄”是一种新型的家用灭火用品,“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃气体,使火焰熄灭,“火立熄”的灭火原理是______。
(5)若不小心被蚊虫叮咬(蚊虫能分泌出蚊酸),可用下列物质之一涂抹以减轻疼痛,该物质是______(填字母)。
A食醋(pH<7) B食盐水(pH=7) C肥皂水(pH>7)
15.某学习小组用黑枸杞提取液作了以下实验:
实验一:室温时,将蒸馏水和不同pH的硫酸、氢氧化钠溶液,放入14支试管中,分别向每支试管中滴加3滴黑枸杞提取液。实验结果如下:
pH 1 2 3 4 5 6 7 8 9 10 11 12 13 14
颜色 粉红 粉红 粉红 浅紫 浅紫 紫 紫 蓝 蓝 深蓝 深蓝 灰绿 黄 黄棕
实验二:室温时,向试管中分别加入相同体积的4种物质,各滴加3滴黑枸杞提取液。
实验结果如下:
物质 稀盐酸 牛奶 蒸馏水 炉具清洁剂
颜色 粉红 紫 紫 黄
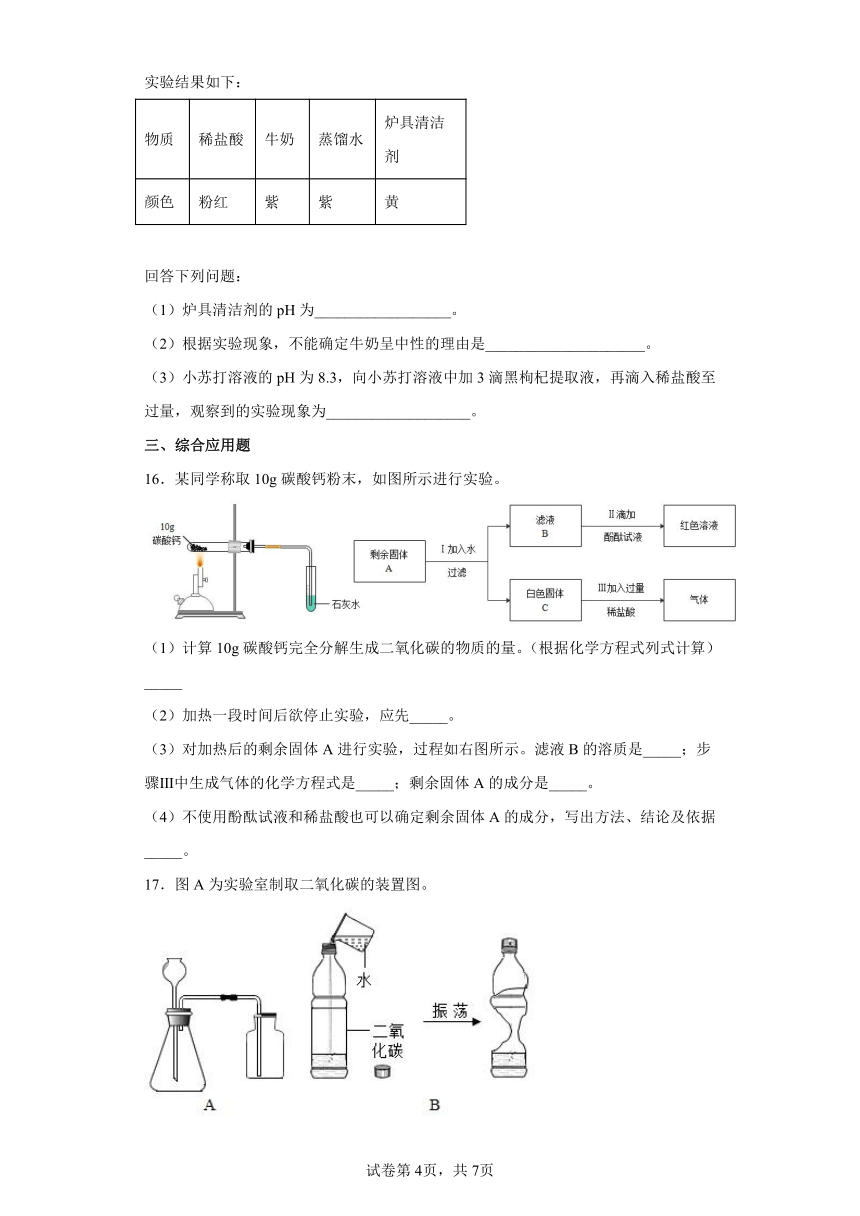
回答下列问题:
(1)炉具清洁剂的pH为__________________。
(2)根据实验现象,不能确定牛奶呈中性的理由是_____________________。
(3)小苏打溶液的pH为8.3,向小苏打溶液中加3滴黑枸杞提取液,再滴入稀盐酸至过量,观察到的实验现象为___________________。
三、综合应用题
16.某同学称取10g碳酸钙粉末,如图所示进行实验。
(1)计算10g碳酸钙完全分解生成二氧化碳的物质的量。(根据化学方程式列式计算)_____
(2)加热一段时间后欲停止实验,应先_____。
(3)对加热后的剩余固体A进行实验,过程如右图所示。滤液B的溶质是_____;步骤Ⅲ中生成气体的化学方程式是_____;剩余固体A的成分是_____。
(4)不使用酚酞试液和稀盐酸也可以确定剩余固体A的成分,写出方法、结论及依据_____。
17.图A为实验室制取二氧化碳的装置图。
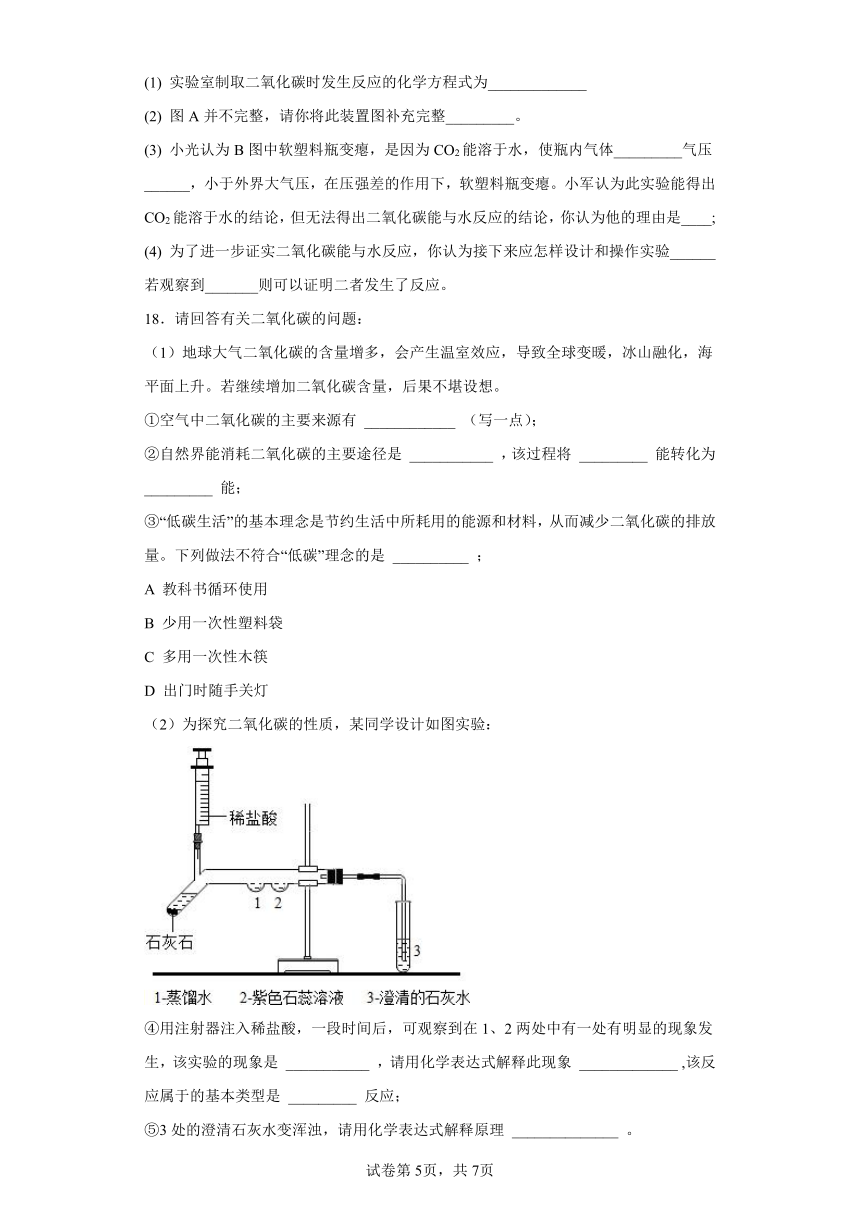
(1) 实验室制取二氧化碳时发生反应的化学方程式为_____________
(2) 图A并不完整,请你将此装置图补充完整_________。
(3) 小光认为B图中软塑料瓶变瘪,是因为CO2能溶于水,使瓶内气体_________气压______,小于外界大气压,在压强差的作用下,软塑料瓶变瘪。小军认为此实验能得出CO2能溶于水的结论,但无法得出二氧化碳能与水反应的结论,你认为他的理由是____;
(4) 为了进一步证实二氧化碳能与水反应,你认为接下来应怎样设计和操作实验______若观察到_______则可以证明二者发生了反应。
18.请回答有关二氧化碳的问题:
(1)地球大气二氧化碳的含量增多,会产生温室效应,导致全球变暖,冰山融化,海平面上升。若继续增加二氧化碳含量,后果不堪设想。
①空气中二氧化碳的主要来源有 ____________ (写一点);
②自然界能消耗二氧化碳的主要途径是 ___________ ,该过程将 _________ 能转化为 _________ 能;
③“低碳生活”的基本理念是节约生活中所耗用的能源和材料,从而减少二氧化碳的排放量。下列做法不符合“低碳”理念的是 __________ ;
A 教科书循环使用
B 少用一次性塑料袋
C 多用一次性木筷
D 出门时随手关灯
(2)为探究二氧化碳的性质,某同学设计如图实验:
④用注射器注入稀盐酸,一段时间后,可观察到在1、2两处中有一处有明显的现象发生,该实验的现象是 ___________ ,请用化学表达式解释此现象 _____________ ,该反应属于的基本类型是 _________ 反应;
⑤3处的澄清石灰水变浑浊,请用化学表达式解释原理 ______________ 。
(3)如图是雪碧汽水标签中的部分內容:
⑥小虎同学取适量雪碧汽水于试管中,稍稍加热后产生大量气泡,发生反应的化学表达式为 ______ ;
⑦已知∶酸性物质能使石蕊变红。将雪碧汽水充分煮沸后滴入石蕊试液,溶液呈红色,使石蕊变红的物质是 ______ 。
19.如图是化肥碳酸氢铵包装袋上的部分说明,可推测碳酸氢铵具有的性质有 _______ (填字母)。
A.易溶于水 B.受热易分解
某同学提出疑问“这种化肥含氮量是否达到16%,化肥中碳酸氢铵的质量分数是多少?”
带着这些问题,该同学进入实验室完成了下列实验。
【查找资料】
①碱石灰能够吸收水和CO2,但是不吸收NH3
②浓硫酸能吸收NH3但是不吸收CO2
③氨气溶于水形成氨水
【性质探究】该同学设计了如下的实验装置:
①用A装置给碳酸氢铵加热,装药品前,必须进行的一步操作是 _____ 。
②取适量碳酸氢铵加入试管,连接A、B装置,加热,观察到B中的现象是 ________ 。
③再取适量碳酸氢铵加入试管,连接A、C、E装置,加热,E中的现象是 __________ 。
④碳酸氢铵在受热时发生反应的化学表达式是 _______ 。
【含量分析】将装置A、C、D依次连接,加入10g化肥样品,加热至A中固体完全消失。称量装置D的质量如表 (各装置对气体吸收是完全的) :
实验前D装置的质量 150.0g
实验后D装置的质量 151.7g
⑤由此分析得知:反应中产生氨气的质量为 __________ g。
⑥通过反应的化学表达式可知:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥中氮元素的质量分数为 __________ (结果保留到0.1%)。
⑦此化肥中碳酸氢铵的质量分数为 __________ (结果保留到0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.A
4.A
5.B
6.B
7.A
8.B
9.A
10.C
11. 稀疏酸、氢氧化钠溶液、紫色石蕊试液 石蕊遇酸显红色,遇碱显蓝色
12. 1:8 红
13. B A C 酸碱指示剂遇到酸、碱溶液呈现不同的颜色; 碱 使紫色石蕊试剂变蓝 酸 使紫色石蕊试剂变红
14. CaO+H2O=Ca(OH)2 肥皂水 铝的表面形成一层致密的氧化物薄膜 使可燃物与氧气隔绝 C
15. 13 黑枸杞提取液在pH=6,pH=7的溶液中均会变紫,故不能确定牛奶呈中性,还可能呈弱酸性 溶液由蓝色变为紫色,又变为粉红色
16. 0.1mol 将导管从石灰水中取出 Ca(OH)2 CaCO3+2HCl=CaCl2+H2O+CO2↑ CaO、CaCO3 称量剩余固体A的质量m,根据质量守恒定律:若m为10g,剩余固体A成分为CaCO3;若5.6g17. CaCO3+2HC====CaCl2+CO2↑+H20 补固体、液体、液面、气泡、玻璃片 减少 变小 由实验现象不能证明有新物质(H2CO3)生成(或CO2溶于水也会观察到相同的实验现象,因此不能证明一定有新物质生成等)(合理即可) 向变瘪的塑料瓶里滴加紫色石蕊溶液 溶液由紫色变红色(合理即可)
18. 化石燃料的燃烧 绿色植物光合作用 太阳 化学 C 2处紫色石蕊变红色 化合反应 柠檬酸
19. AB 检查装置气密性 变浑浊 变红 NH4HCO3 NH3 +H2O+CO2 1.7 14.0% 79.0%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.一些重要作物最适宜生长的土壤的pH范围如下:
作物 水稻 马铃薯 草莓 薄荷
pH 6~7 4.8~5.5 5~7.5 7~8
下列说法中正确的是( )A.水稻和薄荷生长都适宜酸性土壤
B.草莓生长只适宜酸性土壤
C.马铃薯生长不适宜碱性土壤
D.以上作物都不适宜碱性土壤
2.下列有关溶液酸碱性的说法错误的是( )
A.pH=7的溶液呈中性
B.pH>7的溶液一定呈碱性
C.pH<7的雨水一定是酸雨
D.酸溶液的pH越小酸性越强
3.一些食物的近似pH如下:
食物 葡萄汁 苹果汁 牛奶 鸡蛋清
pH 3.5~4.5 2.9~3.3 6.3~6.6 7.6~8.0
下列说法中不正确的是A.鸡蛋清和牛奶显碱性 B.苹果汁和葡萄汁显酸性
C.苹果汁比葡萄汁的酸性强 D.胃酸过多的人应少饮苹果汁和葡萄汁
4.下列溶液中,能使酚酞试液变红的是( )
A.烧碱溶液 B.稀硫酸 C.稀盐酸 D.食盐水
5.小明为验证“分子是运动的”,设计了四个实验。其中不能达到目的的是( )
A. B. C. D.
6.分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液,观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙 B.甲、丙、乙 C.乙、甲、丙 D.丙、甲、乙
7.柠檬汁能使石蕊试液变红色,由此可知柠檬汁( )
A.显酸性 B.显碱性 C.显中性 D.无法确定
8.在滴有紫色石蕊试液的稀硫酸中,分别加入过量下列物质,溶液仍为红色的是( )
A.CaO B.BaCl2 C.Na2CO3 D.Ca(OH)2
9.如图,向点滴板①~④滴孔中分别滴入指示剂后,①②③④滴孔内溶液显示的颜色依次是( )
A.无色、红色、蓝色、红色 B.红色、蓝色、黄色、紫色
C.蓝色、红色、紫色、无色 D.无色、蓝色、红色、蓝色
10.据报道,某经营宾馆的不法商人用氢氧化钠溶液浸泡、洗涤床单和被套,导致它们显碱性,引起顾客皮肤不适,氢氧化钠溶液的pH可能是
A.3 B.7 C.13 D.5
二、填空题
11.在化学晚会上,小华用玻璃棒蘸取一种液体在白纸上画上花,再蘸取另一种液体画上叶,将白纸挂在墙上,又用一种液体向纸上的叶、花喷洒,立即展现出“‘雨’落叶出红花开”的趣味景象。请你想一想,小华先后所用的液体可能是________ ,其化学原理是____________ 。
12.阿斯匹林的主要成分是乙酰水杨酸(化学式为C9H8O4),具有抑制血小板发挥作用的功能,是治疗心血管疾病的重要药物之一。
(1)乙酰水杨酸中氢、氧两种元素的质量比为_______。
(2)乙酰水杨酸具有酸性,若在其无色溶液中滴入紫色石蕊试液,观察到溶液呈____色。
13.现有白纸、溶质质量分数为20%的NaOH溶液(A)、溶质质量分数为10%的H2SO4溶液(B)和10%的紫色石蕊试液(C),设计“雨落叶出红花开”的趣味实验:先在白纸上用玻璃棒蘸取(填序号,下同)_____画上花,在蘸取_____画上叶.将白纸挂起来,用_____向纸上喷洒即可.实验的原理是_____.20%的NaOH溶液呈_____性,因此_____.10%的H2SO4呈_____性,因此_____.
14.化学与生产生活联系紧密,请用所学知识回答问题。
(1)“自热米饭”加热原理是生石灰与水接触放热,该反应的化学方程式为______。
(2)使用硬水会给生活带来许多麻烦,生活中可以用______区分软水和硬水。
(3)铝的化学性质很活泼,但家里用了很久的铝壶很少出现腐蚀,原因是______。
(4)“火立熄”是一种新型的家用灭火用品,“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃气体,使火焰熄灭,“火立熄”的灭火原理是______。
(5)若不小心被蚊虫叮咬(蚊虫能分泌出蚊酸),可用下列物质之一涂抹以减轻疼痛,该物质是______(填字母)。
A食醋(pH<7) B食盐水(pH=7) C肥皂水(pH>7)
15.某学习小组用黑枸杞提取液作了以下实验:
实验一:室温时,将蒸馏水和不同pH的硫酸、氢氧化钠溶液,放入14支试管中,分别向每支试管中滴加3滴黑枸杞提取液。实验结果如下:
pH 1 2 3 4 5 6 7 8 9 10 11 12 13 14
颜色 粉红 粉红 粉红 浅紫 浅紫 紫 紫 蓝 蓝 深蓝 深蓝 灰绿 黄 黄棕
实验二:室温时,向试管中分别加入相同体积的4种物质,各滴加3滴黑枸杞提取液。
实验结果如下:
物质 稀盐酸 牛奶 蒸馏水 炉具清洁剂
颜色 粉红 紫 紫 黄
回答下列问题:
(1)炉具清洁剂的pH为__________________。
(2)根据实验现象,不能确定牛奶呈中性的理由是_____________________。
(3)小苏打溶液的pH为8.3,向小苏打溶液中加3滴黑枸杞提取液,再滴入稀盐酸至过量,观察到的实验现象为___________________。
三、综合应用题
16.某同学称取10g碳酸钙粉末,如图所示进行实验。
(1)计算10g碳酸钙完全分解生成二氧化碳的物质的量。(根据化学方程式列式计算)_____
(2)加热一段时间后欲停止实验,应先_____。
(3)对加热后的剩余固体A进行实验,过程如右图所示。滤液B的溶质是_____;步骤Ⅲ中生成气体的化学方程式是_____;剩余固体A的成分是_____。
(4)不使用酚酞试液和稀盐酸也可以确定剩余固体A的成分,写出方法、结论及依据_____。
17.图A为实验室制取二氧化碳的装置图。
(1) 实验室制取二氧化碳时发生反应的化学方程式为_____________
(2) 图A并不完整,请你将此装置图补充完整_________。
(3) 小光认为B图中软塑料瓶变瘪,是因为CO2能溶于水,使瓶内气体_________气压______,小于外界大气压,在压强差的作用下,软塑料瓶变瘪。小军认为此实验能得出CO2能溶于水的结论,但无法得出二氧化碳能与水反应的结论,你认为他的理由是____;
(4) 为了进一步证实二氧化碳能与水反应,你认为接下来应怎样设计和操作实验______若观察到_______则可以证明二者发生了反应。
18.请回答有关二氧化碳的问题:
(1)地球大气二氧化碳的含量增多,会产生温室效应,导致全球变暖,冰山融化,海平面上升。若继续增加二氧化碳含量,后果不堪设想。
①空气中二氧化碳的主要来源有 ____________ (写一点);
②自然界能消耗二氧化碳的主要途径是 ___________ ,该过程将 _________ 能转化为 _________ 能;
③“低碳生活”的基本理念是节约生活中所耗用的能源和材料,从而减少二氧化碳的排放量。下列做法不符合“低碳”理念的是 __________ ;
A 教科书循环使用
B 少用一次性塑料袋
C 多用一次性木筷
D 出门时随手关灯
(2)为探究二氧化碳的性质,某同学设计如图实验:
④用注射器注入稀盐酸,一段时间后,可观察到在1、2两处中有一处有明显的现象发生,该实验的现象是 ___________ ,请用化学表达式解释此现象 _____________ ,该反应属于的基本类型是 _________ 反应;
⑤3处的澄清石灰水变浑浊,请用化学表达式解释原理 ______________ 。
(3)如图是雪碧汽水标签中的部分內容:
⑥小虎同学取适量雪碧汽水于试管中,稍稍加热后产生大量气泡,发生反应的化学表达式为 ______ ;
⑦已知∶酸性物质能使石蕊变红。将雪碧汽水充分煮沸后滴入石蕊试液,溶液呈红色,使石蕊变红的物质是 ______ 。
19.如图是化肥碳酸氢铵包装袋上的部分说明,可推测碳酸氢铵具有的性质有 _______ (填字母)。
A.易溶于水 B.受热易分解
某同学提出疑问“这种化肥含氮量是否达到16%,化肥中碳酸氢铵的质量分数是多少?”
带着这些问题,该同学进入实验室完成了下列实验。
【查找资料】
①碱石灰能够吸收水和CO2,但是不吸收NH3
②浓硫酸能吸收NH3但是不吸收CO2
③氨气溶于水形成氨水
【性质探究】该同学设计了如下的实验装置:
①用A装置给碳酸氢铵加热,装药品前,必须进行的一步操作是 _____ 。
②取适量碳酸氢铵加入试管,连接A、B装置,加热,观察到B中的现象是 ________ 。
③再取适量碳酸氢铵加入试管,连接A、C、E装置,加热,E中的现象是 __________ 。
④碳酸氢铵在受热时发生反应的化学表达式是 _______ 。
【含量分析】将装置A、C、D依次连接,加入10g化肥样品,加热至A中固体完全消失。称量装置D的质量如表 (各装置对气体吸收是完全的) :
实验前D装置的质量 150.0g
实验后D装置的质量 151.7g
⑤由此分析得知:反应中产生氨气的质量为 __________ g。
⑥通过反应的化学表达式可知:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥中氮元素的质量分数为 __________ (结果保留到0.1%)。
⑦此化肥中碳酸氢铵的质量分数为 __________ (结果保留到0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.A
4.A
5.B
6.B
7.A
8.B
9.A
10.C
11. 稀疏酸、氢氧化钠溶液、紫色石蕊试液 石蕊遇酸显红色,遇碱显蓝色
12. 1:8 红
13. B A C 酸碱指示剂遇到酸、碱溶液呈现不同的颜色; 碱 使紫色石蕊试剂变蓝 酸 使紫色石蕊试剂变红
14. CaO+H2O=Ca(OH)2 肥皂水 铝的表面形成一层致密的氧化物薄膜 使可燃物与氧气隔绝 C
15. 13 黑枸杞提取液在pH=6,pH=7的溶液中均会变紫,故不能确定牛奶呈中性,还可能呈弱酸性 溶液由蓝色变为紫色,又变为粉红色
16. 0.1mol 将导管从石灰水中取出 Ca(OH)2 CaCO3+2HCl=CaCl2+H2O+CO2↑ CaO、CaCO3 称量剩余固体A的质量m,根据质量守恒定律:若m为10g,剩余固体A成分为CaCO3;若5.6g
18. 化石燃料的燃烧 绿色植物光合作用 太阳 化学 C 2处紫色石蕊变红色 化合反应 柠檬酸
19. AB 检查装置气密性 变浑浊 变红 NH4HCO3 NH3 +H2O+CO2 1.7 14.0% 79.0%
答案第1页,共2页
答案第1页,共2页
