8.1什么是有机化合物同步练习-2021-2022学年九年级化学沪教版下册(word版 含答案)
文档属性
| 名称 | 8.1什么是有机化合物同步练习-2021-2022学年九年级化学沪教版下册(word版 含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 167.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-01 09:35:45 | ||
图片预览




文档简介
沪教版(全国) 8.1 什么是有机化合物 同步练习
一、单选题
1.清华大学研究人员成功研发出一种纳米纤维催化剂,可将二氧化碳催化转化成液体燃料甲醇,如图为该反应的微观模拟示意图(图中微粒恰好完全反应)。下列说法正确的是
A.丁的化学式为H2O,该反应为置换反应
B.参加反应的甲、乙质量之比为3:l
C.生成物丙和丁均为氧化物
D.该反应实现了无机物到有机物的转化
2.下列化合物中,属于有机物的是
A.盐酸 B.碳酸 C.醋酸 D.硫酸
3.下列有关甲烷的说法正确的是
A.甲烷的化学式为C2H4 B.甲烷是最简单的有机物
C.甲烷密度比空气的大 D.甲烷与空气的混合物遇火不会发生爆炸
4.抗击新冠肺炎疫情离不开化学知识和技术。下列说法错误的是
A.高温消毒餐具,使病毒在高温下失去活性
B.使用医用酒精消毒要远离火源,因为酒精有可燃性
C.将酒精加工成免洗消毒凝胶,使酒精分子停止运动而不挥发
D.测定新冠病毒的组成和结构,有助于研发治疗新冠肺炎的药物
5.下列物质中均含有碳元素,其中不属于有机物的是
A.酒精 B.醋酸 C.碳酸 D.甲烷
6.下列各组物质中,富含蛋白质的是
A.鸡蛋、牛奶 B.米饭、土豆
C.香蕉、桃子 D.牛油、奶油
7.河南地处中原,物产丰富。下列食材或食品中富含蛋白质的是( )
A.黄河鲤鱼 B.新郑大枣 C.叶县岩盐 D.原阳大米
8.下列做法不能达到目的是( )
A.用洗涤剂去除油污 B.用白酒去除水垢
C.用小苏打发酵面粉 D.用煮沸的方法软化硬水
9.分析推理是化学学习和研究中常用的思维方法,下列分析推理正确的是
A.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
B.有机化合物都含有碳元素,所以含有碳元素的化合物一定是有机化合物
C.燃烧都伴随着发光、放热现象,所以有发光、放热现象的就是燃烧
D.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液呈碱性
10.烈性炸药TNT(化学式为C7H5N3O6)广泛用于开矿、修路、兴修水利等,下列关于TNT的说法错误的是
A.TNT是一种有机物
B.TNT爆炸后会产生二氧化硫
C.TNT由四种元素组成
D.每个TNT分子含有21个原子
二、填空题
11.纳米材料具有特殊的性质和功能,纳米级四氧化三铁具有类似人工模拟酶的催化性能。
(1)四氧化三铁属于______(填“无机物”或“有机物”)。
(2)纳米级四氧化三铁能将过氧化氢催化分解为水和氧气,该反应的化学方程式为______。
12.古代“丝绸之路”把中国的丝绸、茶叶传入西方,将西方的宝石传入中国。茶叶中含有维生素C(化学式为C6H8O6),请回答下列问题:
(1)维生素C属于______(填“有机”或“无机”)化合物。
(2)维生素C是由______种元素组成,其中碳、氢两种元素的质量比为______(填最简整数比)。
(3)将维生素C在一定质量的氧气中充分燃烧,生成CO、CO2和H2O,测得生成物的总质量为30.4克,其中水的质量为7.2克,则参加反应的氧气质量为______克。
13.微粒结构示意图是初中化学常见的示意图。现有下列微粒结构示意图,根据题意回答问题:
(1)写出沼气主要成分的化学式_____________。
(2)写出人体中含量最多金属元素的离子符号____________。
(3)写出雪碧、可乐等饮料中含有的一种酸的化学式____________。
(4)写出一种可用于中和胃酸过多的碱的化学式____________。
(5)写出六大营养素中最简单营养素的化学式____________。
14.2012年伦敦奥运会火炬采用轻薄高品质的航天铝合金材料制造,奥运火炬是奥林匹克圣火的载体。
(1)轻金属铝常以通电分解氧化铝(Al2O3)得到单质铝,同时生成了氧气,则该反应的化学方程式为________,该反应的基本类型为______。
(2)我国华帝股份力争成为伦敦奥运会的火炬制造商。火炬的外壳用铝合金制作有利于火炬手收藏火炬。其原因是铝在空气中易氧化而形成一层___________,保护铝制品不被继续腐蚀。请你还说出利用铝合金材料的其他优点(至少一点)___________________。
(3)5月10日正午12时采集伦敦奥林匹克圣火,唯一方式是在奥林匹克的赫拉神庙前利用凹面镜集中阳光来引燃火种。阳光为火种的燃烧提供了_________。火炬燃烧时,_______能转化为热能和光能。
(4)火炬燃烧系统内装环保型燃料丙烷(C3H8 ),丙烷属于_____(选“无机”或“有机”)化合物。当火炬点燃后,所发生反应的化学方程式为__________,所用燃料符合“绿色奥运”的要求,原因是____________。
15.化学在实际的生产生活中发挥着重要的作用。
(1)五氧化二碘(I2O5)可用于测定空气中一氧化碳的含量。I2O5与CO反应的化学方程式为,化学计量数a=___________,X的化学式为___________。
(2)电解水的实验中,负极产生的气体为___________(填化学式);正、负极产生气体的体积比约为___________。
(3)我国研制的航天员舱外服的面料是用高级合成纤维制造而成的,这种面料主要由___________(填“无机物”或“有机物”)组成。航天服密封的空间中要有通讯系统、动力系统、输送养料系统和废气处理系统,在废气处理中用氢氧化锂(LiOH)作吸收剂除去二氧化碳(氢氧化锂和氢氧化钠都是碱,具有相似的化学性质),写出该反应的化学方程式___________。
三、综合应用题
16.物质之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法。
(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序。
规律 排序
示例:标准状况下,密度由大到小 CO2、C2H4(乙烯)、C2H2(乙炔)、CH4
_________ _________
_________ _________
(2)由CH4、CO、H2中的一种、两种或三种组成的气体,完全燃烧后,生成的CO2和H2O的质量之比是11︰9,下列判断中正确的是_________。
A.原气体可能是H2和CH4 的混合物
B.原气体中一定含有CH4
C.原气体中若含有CO,则一定含有H2
D.气体中若同时含有CH4、CO和H2,则CO与H2的质量之比为7︰1
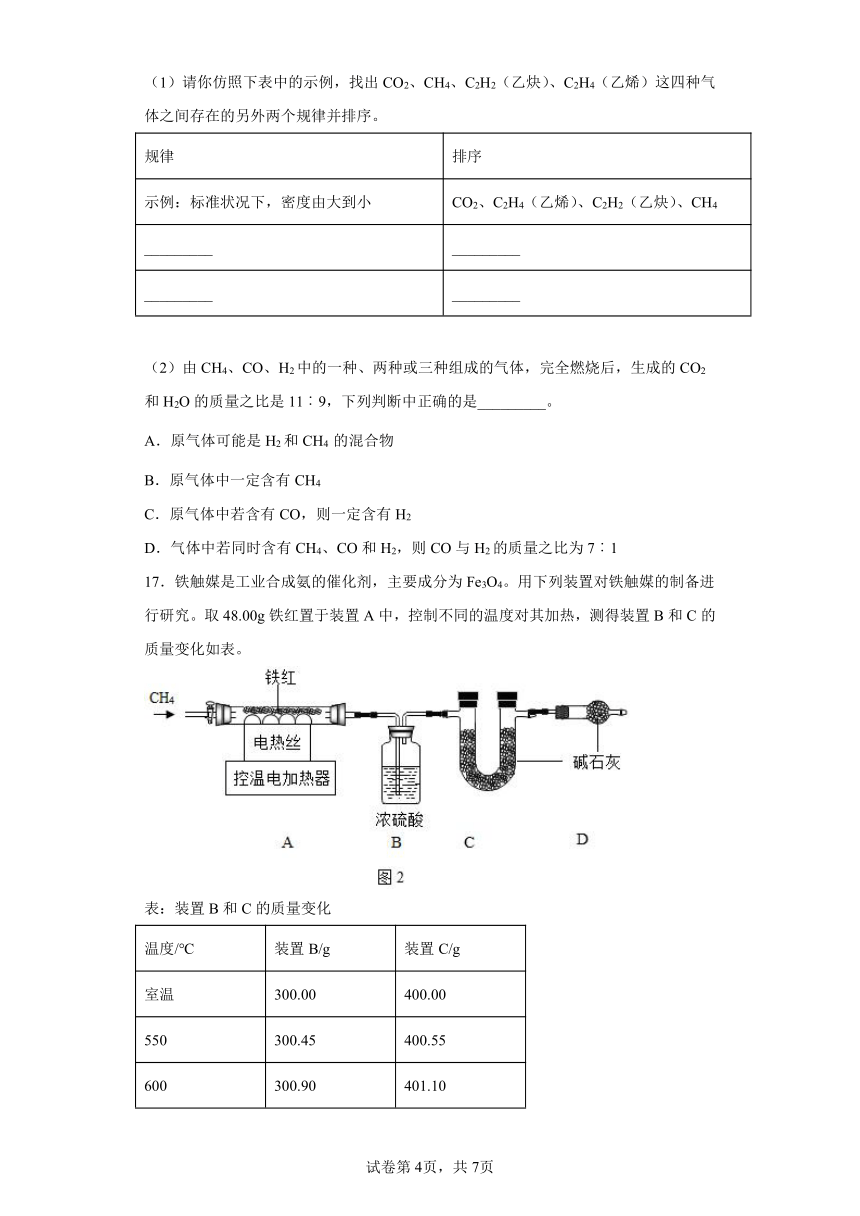
17.铁触媒是工业合成氨的催化剂,主要成分为Fe3O4。用下列装置对铁触媒的制备进行研究。取48.00g铁红置于装置A中,控制不同的温度对其加热,测得装置B和C的质量变化如表。
表:装置B和C的质量变化
温度/℃ 装置B/g 装置C/g
室温 300.00 400.00
550 300.45 400.55
600 300.90 401.10
650 301.80 402.20
资料:加热到500℃以上,Fe2O3和CH4开始反应,生成铁的其他氧化物、CO2和H2O。温度高于700℃,生成Fe。
(1)装配好实验装置后,先要______。
(2)加热前后及过程中均需通入CH4,加热前通CH4的目的是______。
(3)加热到650℃时,装置A中剩余固体为FeO和Fe3O4的混合物,则两物质的质量比m(FeO):m(Fe3O4)=______。
(4)用铁红制取铁触媒,装置A应控制的适宜温度为______℃。
18.新型冠状病毒肺炎威胁着人们的身体健康,预防病毒除了戴口罩、勤洗手,还要做好消毒工作。请按要求填空:
(1)一次性医用口罩成为每个人的生活必需品,它是由专业两层纤维无纺布和中间一层熔喷布,经超声波焊接而成,能像滤纸一样起到___________(填一种实验操作名称)作用。
(2)生活中我们使用75%的医用酒精进行消毒。
在家里使用医用酒精对门把手、桌面等物品消毒的正确方式是___________(填“擦拭”或“喷洒”)。
(3)下图是酒精完全燃烧的微观示意图。
酒精的化学式为C2H6O,是由___________构成的(填“分子”或“原子”或“离子”),酒精中C、H、O元素的质量比为___________,酒精完全燃烧的化学方程式为___________。
(4)过氧乙酸【CH3COOOH】也是常用消毒剂,常用于校园环境消毒。过氧乙酸具有酸性、腐蚀性(尤其是对金属)、可燃性,遇热、遇碱易分解。用浓硫酸作催化剂,制备过氧乙酸的一种模拟流程如下(部分反应条件未标出):
①认识过氧乙酸:它___________氧化物(填“是”或“不是”)。
②制备过氧乙酸:写出反应③的化学方程式___________;浓硫酸在反应前后___________和化学性质不变。
③下列关于过氧乙酸使用的说法不正确的是___________(填字母序号)。
A.应低温、避开火源贮存
B.环境消毒,浓度越大越好
C.谨防溅到眼睛和皮肤上
D.最好不要用金属容器盛放
19.铁及其化合物在生产生活中发挥着重要作用。
(一)铁的冶炼和应用
(1)我国早在春秋战国时期就开始生产和使用铁器。
胆矾为晶体,《梦溪笔谈》记载“熬胆矾铁釜久亦化为铜”,用化学方程式表示其原理:___________。
(2)用焦炭和氧化铁炼铁,反应的化学方程式为___________。生铁炼钢,主要是降低______元素含量,除去生铁中硅、硫和磷等元素。
(二)铁红()的制备
用工业烧渣(含有、和)制备化工原料铁红的实验流程如图:
(3)酸溶前将烧渣粉碎,目的是_____________。
(4)氧化时发生的反应为反应温度不宜太高,原因是______________。
(三)铁触媒的制备
铁触媒是工业合成氨的催化剂,主要成分为。用下列装置对铁触媒的制备进行研究。取铁红置于装置中,控制不同的温度对其加热,测得装置和的质量变化如表。(资料:)
表:装置和的质量变化
温度 装置 装置
室温
资料:①实验室中浓硫酸用于吸收水分,碱石灰用于吸收二氧化碳和水分。
②加热到以上,和CH4开始反应,生成铁的其他氧化物、和。温度高于,生成。
(5)加热前后及过程中均需通入,加热前通的目的是____________。
(6)用铁红制取铁触媒,装置应控制的适宜温度为__________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.B
4.C
5.C
6.A
7.A
8.B
9.D
10.B
11. 无机物
12. 有机 三 9:1 12.8
13. CH4 H2CO3 Al(OH)3 H2O
14. 2Al2O3 4Al+3O2↑ 分解反应 致密的氧化膜 密度小轻便、硬度较大等 足够的热量 化学 有机 C3H8+5O23CO2+4H2O 生成水和二氧化碳则不会污染空气
15. 5 CO2 H2 1:2 有机物
16. 相对分子质量由大到小 CO2、C2H4、C2H2、CH4 一个分子中原子个数由多到少 C2H4、CH4、C2H2、CO2(其他合理的均可) CD
17.(1)检查装置的气密性
(2)排尽装置内的空气,防止加热时发生爆炸(或排尽装置内的空气,防止甲烷和氧气发生反应生成二氧化碳和水,影响测定结果)
(3)27:29
(4)600℃
18.(1)过滤
(2)擦拭
(3) 分子
12:3:8
(4) 不是
质量
B
19.(1)
(2) ↑ 碳##C
(3)增大接触面积,加快反应速率
(4)温度太高,过氧化氢发生分解
(5)赶尽装置内的空气,防止氧气与CH4反应生成H2O 和CO2,影响测定结果
(6)600
答案第1页,共2页
答案第1页,共2页
一、单选题
1.清华大学研究人员成功研发出一种纳米纤维催化剂,可将二氧化碳催化转化成液体燃料甲醇,如图为该反应的微观模拟示意图(图中微粒恰好完全反应)。下列说法正确的是
A.丁的化学式为H2O,该反应为置换反应
B.参加反应的甲、乙质量之比为3:l
C.生成物丙和丁均为氧化物
D.该反应实现了无机物到有机物的转化
2.下列化合物中,属于有机物的是
A.盐酸 B.碳酸 C.醋酸 D.硫酸
3.下列有关甲烷的说法正确的是
A.甲烷的化学式为C2H4 B.甲烷是最简单的有机物
C.甲烷密度比空气的大 D.甲烷与空气的混合物遇火不会发生爆炸
4.抗击新冠肺炎疫情离不开化学知识和技术。下列说法错误的是
A.高温消毒餐具,使病毒在高温下失去活性
B.使用医用酒精消毒要远离火源,因为酒精有可燃性
C.将酒精加工成免洗消毒凝胶,使酒精分子停止运动而不挥发
D.测定新冠病毒的组成和结构,有助于研发治疗新冠肺炎的药物
5.下列物质中均含有碳元素,其中不属于有机物的是
A.酒精 B.醋酸 C.碳酸 D.甲烷
6.下列各组物质中,富含蛋白质的是
A.鸡蛋、牛奶 B.米饭、土豆
C.香蕉、桃子 D.牛油、奶油
7.河南地处中原,物产丰富。下列食材或食品中富含蛋白质的是( )
A.黄河鲤鱼 B.新郑大枣 C.叶县岩盐 D.原阳大米
8.下列做法不能达到目的是( )
A.用洗涤剂去除油污 B.用白酒去除水垢
C.用小苏打发酵面粉 D.用煮沸的方法软化硬水
9.分析推理是化学学习和研究中常用的思维方法,下列分析推理正确的是
A.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
B.有机化合物都含有碳元素,所以含有碳元素的化合物一定是有机化合物
C.燃烧都伴随着发光、放热现象,所以有发光、放热现象的就是燃烧
D.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液呈碱性
10.烈性炸药TNT(化学式为C7H5N3O6)广泛用于开矿、修路、兴修水利等,下列关于TNT的说法错误的是
A.TNT是一种有机物
B.TNT爆炸后会产生二氧化硫
C.TNT由四种元素组成
D.每个TNT分子含有21个原子
二、填空题
11.纳米材料具有特殊的性质和功能,纳米级四氧化三铁具有类似人工模拟酶的催化性能。
(1)四氧化三铁属于______(填“无机物”或“有机物”)。
(2)纳米级四氧化三铁能将过氧化氢催化分解为水和氧气,该反应的化学方程式为______。
12.古代“丝绸之路”把中国的丝绸、茶叶传入西方,将西方的宝石传入中国。茶叶中含有维生素C(化学式为C6H8O6),请回答下列问题:
(1)维生素C属于______(填“有机”或“无机”)化合物。
(2)维生素C是由______种元素组成,其中碳、氢两种元素的质量比为______(填最简整数比)。
(3)将维生素C在一定质量的氧气中充分燃烧,生成CO、CO2和H2O,测得生成物的总质量为30.4克,其中水的质量为7.2克,则参加反应的氧气质量为______克。
13.微粒结构示意图是初中化学常见的示意图。现有下列微粒结构示意图,根据题意回答问题:
(1)写出沼气主要成分的化学式_____________。
(2)写出人体中含量最多金属元素的离子符号____________。
(3)写出雪碧、可乐等饮料中含有的一种酸的化学式____________。
(4)写出一种可用于中和胃酸过多的碱的化学式____________。
(5)写出六大营养素中最简单营养素的化学式____________。
14.2012年伦敦奥运会火炬采用轻薄高品质的航天铝合金材料制造,奥运火炬是奥林匹克圣火的载体。
(1)轻金属铝常以通电分解氧化铝(Al2O3)得到单质铝,同时生成了氧气,则该反应的化学方程式为________,该反应的基本类型为______。
(2)我国华帝股份力争成为伦敦奥运会的火炬制造商。火炬的外壳用铝合金制作有利于火炬手收藏火炬。其原因是铝在空气中易氧化而形成一层___________,保护铝制品不被继续腐蚀。请你还说出利用铝合金材料的其他优点(至少一点)___________________。
(3)5月10日正午12时采集伦敦奥林匹克圣火,唯一方式是在奥林匹克的赫拉神庙前利用凹面镜集中阳光来引燃火种。阳光为火种的燃烧提供了_________。火炬燃烧时,_______能转化为热能和光能。
(4)火炬燃烧系统内装环保型燃料丙烷(C3H8 ),丙烷属于_____(选“无机”或“有机”)化合物。当火炬点燃后,所发生反应的化学方程式为__________,所用燃料符合“绿色奥运”的要求,原因是____________。
15.化学在实际的生产生活中发挥着重要的作用。
(1)五氧化二碘(I2O5)可用于测定空气中一氧化碳的含量。I2O5与CO反应的化学方程式为,化学计量数a=___________,X的化学式为___________。
(2)电解水的实验中,负极产生的气体为___________(填化学式);正、负极产生气体的体积比约为___________。
(3)我国研制的航天员舱外服的面料是用高级合成纤维制造而成的,这种面料主要由___________(填“无机物”或“有机物”)组成。航天服密封的空间中要有通讯系统、动力系统、输送养料系统和废气处理系统,在废气处理中用氢氧化锂(LiOH)作吸收剂除去二氧化碳(氢氧化锂和氢氧化钠都是碱,具有相似的化学性质),写出该反应的化学方程式___________。
三、综合应用题
16.物质之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法。
(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序。
规律 排序
示例:标准状况下,密度由大到小 CO2、C2H4(乙烯)、C2H2(乙炔)、CH4
_________ _________
_________ _________
(2)由CH4、CO、H2中的一种、两种或三种组成的气体,完全燃烧后,生成的CO2和H2O的质量之比是11︰9,下列判断中正确的是_________。
A.原气体可能是H2和CH4 的混合物
B.原气体中一定含有CH4
C.原气体中若含有CO,则一定含有H2
D.气体中若同时含有CH4、CO和H2,则CO与H2的质量之比为7︰1
17.铁触媒是工业合成氨的催化剂,主要成分为Fe3O4。用下列装置对铁触媒的制备进行研究。取48.00g铁红置于装置A中,控制不同的温度对其加热,测得装置B和C的质量变化如表。
表:装置B和C的质量变化
温度/℃ 装置B/g 装置C/g
室温 300.00 400.00
550 300.45 400.55
600 300.90 401.10
650 301.80 402.20
资料:加热到500℃以上,Fe2O3和CH4开始反应,生成铁的其他氧化物、CO2和H2O。温度高于700℃,生成Fe。
(1)装配好实验装置后,先要______。
(2)加热前后及过程中均需通入CH4,加热前通CH4的目的是______。
(3)加热到650℃时,装置A中剩余固体为FeO和Fe3O4的混合物,则两物质的质量比m(FeO):m(Fe3O4)=______。
(4)用铁红制取铁触媒,装置A应控制的适宜温度为______℃。
18.新型冠状病毒肺炎威胁着人们的身体健康,预防病毒除了戴口罩、勤洗手,还要做好消毒工作。请按要求填空:
(1)一次性医用口罩成为每个人的生活必需品,它是由专业两层纤维无纺布和中间一层熔喷布,经超声波焊接而成,能像滤纸一样起到___________(填一种实验操作名称)作用。
(2)生活中我们使用75%的医用酒精进行消毒。
在家里使用医用酒精对门把手、桌面等物品消毒的正确方式是___________(填“擦拭”或“喷洒”)。
(3)下图是酒精完全燃烧的微观示意图。
酒精的化学式为C2H6O,是由___________构成的(填“分子”或“原子”或“离子”),酒精中C、H、O元素的质量比为___________,酒精完全燃烧的化学方程式为___________。
(4)过氧乙酸【CH3COOOH】也是常用消毒剂,常用于校园环境消毒。过氧乙酸具有酸性、腐蚀性(尤其是对金属)、可燃性,遇热、遇碱易分解。用浓硫酸作催化剂,制备过氧乙酸的一种模拟流程如下(部分反应条件未标出):
①认识过氧乙酸:它___________氧化物(填“是”或“不是”)。
②制备过氧乙酸:写出反应③的化学方程式___________;浓硫酸在反应前后___________和化学性质不变。
③下列关于过氧乙酸使用的说法不正确的是___________(填字母序号)。
A.应低温、避开火源贮存
B.环境消毒,浓度越大越好
C.谨防溅到眼睛和皮肤上
D.最好不要用金属容器盛放
19.铁及其化合物在生产生活中发挥着重要作用。
(一)铁的冶炼和应用
(1)我国早在春秋战国时期就开始生产和使用铁器。
胆矾为晶体,《梦溪笔谈》记载“熬胆矾铁釜久亦化为铜”,用化学方程式表示其原理:___________。
(2)用焦炭和氧化铁炼铁,反应的化学方程式为___________。生铁炼钢,主要是降低______元素含量,除去生铁中硅、硫和磷等元素。
(二)铁红()的制备
用工业烧渣(含有、和)制备化工原料铁红的实验流程如图:
(3)酸溶前将烧渣粉碎,目的是_____________。
(4)氧化时发生的反应为反应温度不宜太高,原因是______________。
(三)铁触媒的制备
铁触媒是工业合成氨的催化剂,主要成分为。用下列装置对铁触媒的制备进行研究。取铁红置于装置中,控制不同的温度对其加热,测得装置和的质量变化如表。(资料:)
表:装置和的质量变化
温度 装置 装置
室温
资料:①实验室中浓硫酸用于吸收水分,碱石灰用于吸收二氧化碳和水分。
②加热到以上,和CH4开始反应,生成铁的其他氧化物、和。温度高于,生成。
(5)加热前后及过程中均需通入,加热前通的目的是____________。
(6)用铁红制取铁触媒,装置应控制的适宜温度为__________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.B
4.C
5.C
6.A
7.A
8.B
9.D
10.B
11. 无机物
12. 有机 三 9:1 12.8
13. CH4 H2CO3 Al(OH)3 H2O
14. 2Al2O3 4Al+3O2↑ 分解反应 致密的氧化膜 密度小轻便、硬度较大等 足够的热量 化学 有机 C3H8+5O23CO2+4H2O 生成水和二氧化碳则不会污染空气
15. 5 CO2 H2 1:2 有机物
16. 相对分子质量由大到小 CO2、C2H4、C2H2、CH4 一个分子中原子个数由多到少 C2H4、CH4、C2H2、CO2(其他合理的均可) CD
17.(1)检查装置的气密性
(2)排尽装置内的空气,防止加热时发生爆炸(或排尽装置内的空气,防止甲烷和氧气发生反应生成二氧化碳和水,影响测定结果)
(3)27:29
(4)600℃
18.(1)过滤
(2)擦拭
(3) 分子
12:3:8
(4) 不是
质量
B
19.(1)
(2) ↑ 碳##C
(3)增大接触面积,加快反应速率
(4)温度太高,过氧化氢发生分解
(5)赶尽装置内的空气,防止氧气与CH4反应生成H2O 和CO2,影响测定结果
(6)600
答案第1页,共2页
答案第1页,共2页
