2.3 原子结构的模型 导学案(含答案)
文档属性
| 名称 | 2.3 原子结构的模型 导学案(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 343.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-05-19 00:00:00 | ||
图片预览



文档简介
2.3原子结构的模型
【学习目标】
1.知道原子结构模型发展历程,元素的概念,同位素的结构特点。
2.知道物质也可以由离子构成。
3.认识离子微粒大小的数量级。
【学习重难点】
同位素、离子的特点。
【学习过程】
一、我预学
1.原子结构模型的建立与修正
(1)1803年道尔顿--实心球原子结构(原子是坚实的、不可再分的实心球)——发现原子。
(2)1897年汤姆生--“汤姆生模型”:原子是一个平均分布着正电荷的球体,带负电荷的电子嵌在中间。--发现电子。
(3)1911年卢瑟福--“卢瑟福模型”:电子绕原子核运行。
(4)1913年波尔--“分层模型”:电子在固定的轨道上运动。
(5)“电子云模型”--电子在核周围有的区域出现的次数多,有的区域出现的次数少,就象“云雾”一样笼罩在核的周围。
2.科学家最终发现原子核是由更小的两种粒子—— 和 构成。
3.科学家们又对质子和中子的构成进行研究,发现它们都是由更小的基本粒子——
构成。
4.科学家们测定:一个质子带一个单位 电荷,中子 。
二、我探究
1.通过阅读原子结构模型的建立过程,你能用图画出汤姆生、卢瑟福提出的原子模型吗?
图1: 图2:
2.阅读图片——原子模型
思考:氦原子核外有2个电子,你能建立一个氦原子的模型吗?(用图表示)
图:
小结:原子是由居中间的带 电的 和其外的带 电的 构成的。
3.原子核又是由什么构成的呢?
原子核是由更小的两种粒子 和 构成的。它们的带电情况是 。
4.试阅读书本,请比较原子中电子、质子、中子的质量大小?
5.读课本表格,思考:在原子中哪些数目总是相等的?
(1)
(2)
(3)
6.质子、中子都是由更微小的基本粒子 构成的。
7.完成下列有关原子的结构:
( )
原子
( )
原子核
( )
8.原子中哪些数目是相等的? = =
9.元素:具有相同 (即 )的同一类原子的总称。如质子数为8的氧原子总称为氧元素。二氧化碳分子中、水分子中都有质子数为8的氧原子,这些氧原子统称为 。
10.同种元素的原子 一定相同,不同种元素的 一定不同。元素的种类是由原子的 决定。
11.同位素:原子中原子核内 相同 不相同的同类原子的统称。
12.离子: 的原子(或 原子团 )叫离子。
三、我探究
1.阅读课本图片,回答下列问题:
(1)A原子核中有 个质子, 个中子。
(2)B原子核中有 个质子, 个中子。
(3)C原子核中有 个质子, 个中子。
小结:科学上把具有相同 的一类原子总称为元素。
2.思考:同种元素的不同原子,它们的质子数、中子数、电子数都相同吗?
小结:原子中原子核内 的同类原子统称为同位素。
3.常见的同位素有哪些?分别怎样表达?同位素有什么应用?
4.分析粒子模型回答相应的问题:
粒子 质子数 中子数 电子数
A 11 11 11
B 11 11 10
C 17 18 18
D 17 18 17
四种粒子不显电性的是 ;显电性的是
小结:带电的原子或原子团叫 。
阳离子:带 电;如:
阴离子:带 电;如:
5.铝是由 构成的,二氧化碳是由 构成的,氯化钠晶体是由 构成的。
小结: 和 、 一样也是构成物质的基本粒子。
四、我巩固
1.我区存在大面积富硒土壤,有利于提高水果的品质,富硒土壤中的“硒”指的是( )
A.元素 B.分子 C.原子 D.单质
2.2019年意大利科学家首次测得氙-124的半衰期大约为年,氙-124是一种稀有气体元素,元素符号,原子序数54,相对原子质量为124.下列说法正确的是( )
A.氙-124原子的电子数为54 B.氙-124原子的电子数为70
C.氙-124原子的中子数为54 D.氙-124原子的质子数为70
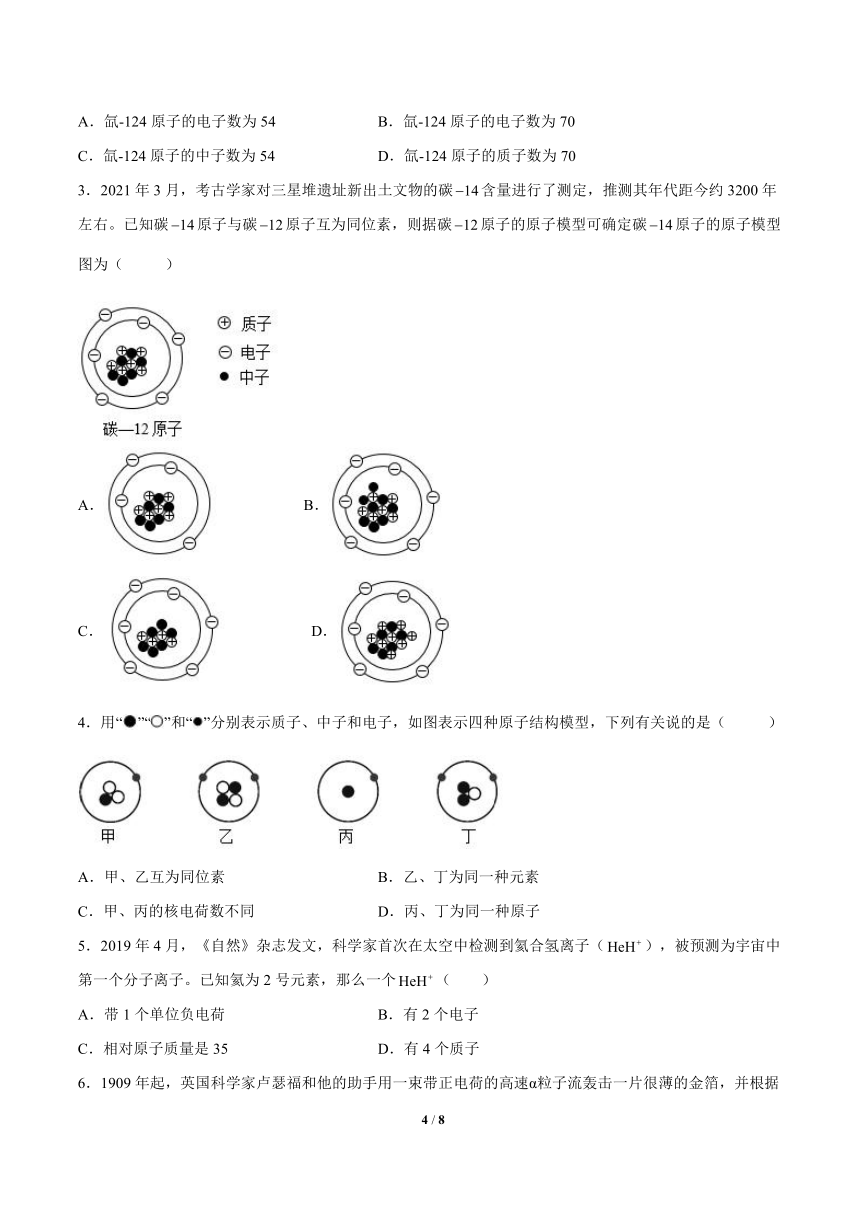
3.2021年3月,考古学家对三星堆遗址新出土文物的碳含量进行了测定,推测其年代距今约3200年左右。已知碳原子与碳原子互为同位素,则据碳原子的原子模型可确定碳原子的原子模型图为( )
B.
C. D.
4.用“”“”和“”分别表示质子、中子和电子,如图表示四种原子结构模型,下列有关说的是( )
A.甲、乙互为同位素 B.乙、丁为同一种元素
C.甲、丙的核电荷数不同 D.丙、丁为同一种原子
5.2019年4月,《自然》杂志发文,科学家首次在太空中检测到氦合氢离子(),被预测为宇宙中第一个分子离子。已知氦为2号元素,那么一个( )
A.带1个单位负电荷 B.有2个电子
C.相对原子质量是35 D.有4个质子
6.1909年起,英国科学家卢瑟福和他的助手用一束带正电荷的高速α粒子流轰击一片很薄的金箔,并根据如图所示的实验现象和已有知识,在1911年提出了原子的有核模型。要解释本实验现象产生的原因,下列知识中不需要用到的是( )
A.同种电荷相互排斥
B.电荷的定向移动形成电流
C.力是改变物体运动状态的原因
D.一个α粒子的质量比一个电子的质量大得多
7.在近代原子学说的发展过程中,有下列观点:①物质都是由原子构成的;②原子都是实心球体;③正电荷均匀分布在整个原子内。
1911年卢瑟福用带正电的a粒子轰击原子,发现多数a粒子穿过后仍保持原来的运动方向,但有绝少数a粒子发生了较大角度的偏转,如图所示,分析实验结果,可以否定上述观点中的( )
A.①② B.③ C.②③ D.①②③
8.原子结构模型是经过一代代科学家不断地发现和提出新的原子结构模型的过程。下列有关图①②③④所示的四种原子结构模型的叙述错误的是( )
①葡萄干面包模型 ②分层结构模型 ③电子云模型 ④行星模型
A.汤姆生认为图①模型中正电荷均匀分布在整个面包内,电子像葡萄干镶嵌其中
B.如图②模型波尔认为电子只能在原子内的一些特定的稳定轨道上绕核运动
C.卢瑟福在实验的基础上提出带负电的电子绕带正电且体积很小的原子核运动的图④模型
D.依据提出时间先后顺序,正确的排列是①②④③
9.知识梳理有助于我们对已学知识进行巩固,如图所示,某同学学习物质结构层次后以氧气为例进行了梳理,下列选项中与、、相对应的是( )
A.原子、原子核、核外电子 B.原子核、原子、核外电子
C.原子、核外电子、原子核 D.核外电子、原子核、原子
10.某补铁剂富马酸亚铁颗粒的化学式为,其中Fe指的是( )
A.单质 B.原子 C.元素 D.离子
11.如图是118号元素在元素周期表中的相关信息。下列有关该元素的说法正确的是( )
A.元素符号为Og
B.该原子的电子数为179
C.该原子的中子数为118
D.相对原子质量为297克
12.1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带两个单位正电荷的氦原子)轰击金箔时,发现大多数α粒子能穿透金箔,而且不改变原来的运动方向,但是也有一小部分α粒子改变了原来的运动路径,甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来(如图)。
(1)有一小部分α粒子稍微改变了原来的运动路径,原因是__________;
(2)大多数α粒子能穿透金箔,不改变原来的运动方向,原因是__________;
(3)只有极少数α粒子被弹了回来,原因是____________。
13.据报道钬元素的原子可有效治疗肝癌,该原子中的中子数与核外电子数之差是___________,现有和两种原子,则X和Y是否是同种元素?___________理由是___________。我们把X和Y原子称之为___________原子。
参考答案:
1.A
2.A
3.B
4.B
5.B
6.B
7.C
8.D
9.A
10.C
11.A
12. 原子核质量很大
13. 32 是 质子数相同 同位素
3 / 3
【学习目标】
1.知道原子结构模型发展历程,元素的概念,同位素的结构特点。
2.知道物质也可以由离子构成。
3.认识离子微粒大小的数量级。
【学习重难点】
同位素、离子的特点。
【学习过程】
一、我预学
1.原子结构模型的建立与修正
(1)1803年道尔顿--实心球原子结构(原子是坚实的、不可再分的实心球)——发现原子。
(2)1897年汤姆生--“汤姆生模型”:原子是一个平均分布着正电荷的球体,带负电荷的电子嵌在中间。--发现电子。
(3)1911年卢瑟福--“卢瑟福模型”:电子绕原子核运行。
(4)1913年波尔--“分层模型”:电子在固定的轨道上运动。
(5)“电子云模型”--电子在核周围有的区域出现的次数多,有的区域出现的次数少,就象“云雾”一样笼罩在核的周围。
2.科学家最终发现原子核是由更小的两种粒子—— 和 构成。
3.科学家们又对质子和中子的构成进行研究,发现它们都是由更小的基本粒子——
构成。
4.科学家们测定:一个质子带一个单位 电荷,中子 。
二、我探究
1.通过阅读原子结构模型的建立过程,你能用图画出汤姆生、卢瑟福提出的原子模型吗?
图1: 图2:
2.阅读图片——原子模型
思考:氦原子核外有2个电子,你能建立一个氦原子的模型吗?(用图表示)
图:
小结:原子是由居中间的带 电的 和其外的带 电的 构成的。
3.原子核又是由什么构成的呢?
原子核是由更小的两种粒子 和 构成的。它们的带电情况是 。
4.试阅读书本,请比较原子中电子、质子、中子的质量大小?
5.读课本表格,思考:在原子中哪些数目总是相等的?
(1)
(2)
(3)
6.质子、中子都是由更微小的基本粒子 构成的。
7.完成下列有关原子的结构:
( )
原子
( )
原子核
( )
8.原子中哪些数目是相等的? = =
9.元素:具有相同 (即 )的同一类原子的总称。如质子数为8的氧原子总称为氧元素。二氧化碳分子中、水分子中都有质子数为8的氧原子,这些氧原子统称为 。
10.同种元素的原子 一定相同,不同种元素的 一定不同。元素的种类是由原子的 决定。
11.同位素:原子中原子核内 相同 不相同的同类原子的统称。
12.离子: 的原子(或 原子团 )叫离子。
三、我探究
1.阅读课本图片,回答下列问题:
(1)A原子核中有 个质子, 个中子。
(2)B原子核中有 个质子, 个中子。
(3)C原子核中有 个质子, 个中子。
小结:科学上把具有相同 的一类原子总称为元素。
2.思考:同种元素的不同原子,它们的质子数、中子数、电子数都相同吗?
小结:原子中原子核内 的同类原子统称为同位素。
3.常见的同位素有哪些?分别怎样表达?同位素有什么应用?
4.分析粒子模型回答相应的问题:
粒子 质子数 中子数 电子数
A 11 11 11
B 11 11 10
C 17 18 18
D 17 18 17
四种粒子不显电性的是 ;显电性的是
小结:带电的原子或原子团叫 。
阳离子:带 电;如:
阴离子:带 电;如:
5.铝是由 构成的,二氧化碳是由 构成的,氯化钠晶体是由 构成的。
小结: 和 、 一样也是构成物质的基本粒子。
四、我巩固
1.我区存在大面积富硒土壤,有利于提高水果的品质,富硒土壤中的“硒”指的是( )
A.元素 B.分子 C.原子 D.单质
2.2019年意大利科学家首次测得氙-124的半衰期大约为年,氙-124是一种稀有气体元素,元素符号,原子序数54,相对原子质量为124.下列说法正确的是( )
A.氙-124原子的电子数为54 B.氙-124原子的电子数为70
C.氙-124原子的中子数为54 D.氙-124原子的质子数为70
3.2021年3月,考古学家对三星堆遗址新出土文物的碳含量进行了测定,推测其年代距今约3200年左右。已知碳原子与碳原子互为同位素,则据碳原子的原子模型可确定碳原子的原子模型图为( )
B.
C. D.
4.用“”“”和“”分别表示质子、中子和电子,如图表示四种原子结构模型,下列有关说的是( )
A.甲、乙互为同位素 B.乙、丁为同一种元素
C.甲、丙的核电荷数不同 D.丙、丁为同一种原子
5.2019年4月,《自然》杂志发文,科学家首次在太空中检测到氦合氢离子(),被预测为宇宙中第一个分子离子。已知氦为2号元素,那么一个( )
A.带1个单位负电荷 B.有2个电子
C.相对原子质量是35 D.有4个质子
6.1909年起,英国科学家卢瑟福和他的助手用一束带正电荷的高速α粒子流轰击一片很薄的金箔,并根据如图所示的实验现象和已有知识,在1911年提出了原子的有核模型。要解释本实验现象产生的原因,下列知识中不需要用到的是( )
A.同种电荷相互排斥
B.电荷的定向移动形成电流
C.力是改变物体运动状态的原因
D.一个α粒子的质量比一个电子的质量大得多
7.在近代原子学说的发展过程中,有下列观点:①物质都是由原子构成的;②原子都是实心球体;③正电荷均匀分布在整个原子内。
1911年卢瑟福用带正电的a粒子轰击原子,发现多数a粒子穿过后仍保持原来的运动方向,但有绝少数a粒子发生了较大角度的偏转,如图所示,分析实验结果,可以否定上述观点中的( )
A.①② B.③ C.②③ D.①②③
8.原子结构模型是经过一代代科学家不断地发现和提出新的原子结构模型的过程。下列有关图①②③④所示的四种原子结构模型的叙述错误的是( )
①葡萄干面包模型 ②分层结构模型 ③电子云模型 ④行星模型
A.汤姆生认为图①模型中正电荷均匀分布在整个面包内,电子像葡萄干镶嵌其中
B.如图②模型波尔认为电子只能在原子内的一些特定的稳定轨道上绕核运动
C.卢瑟福在实验的基础上提出带负电的电子绕带正电且体积很小的原子核运动的图④模型
D.依据提出时间先后顺序,正确的排列是①②④③
9.知识梳理有助于我们对已学知识进行巩固,如图所示,某同学学习物质结构层次后以氧气为例进行了梳理,下列选项中与、、相对应的是( )
A.原子、原子核、核外电子 B.原子核、原子、核外电子
C.原子、核外电子、原子核 D.核外电子、原子核、原子
10.某补铁剂富马酸亚铁颗粒的化学式为,其中Fe指的是( )
A.单质 B.原子 C.元素 D.离子
11.如图是118号元素在元素周期表中的相关信息。下列有关该元素的说法正确的是( )
A.元素符号为Og
B.该原子的电子数为179
C.该原子的中子数为118
D.相对原子质量为297克
12.1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带两个单位正电荷的氦原子)轰击金箔时,发现大多数α粒子能穿透金箔,而且不改变原来的运动方向,但是也有一小部分α粒子改变了原来的运动路径,甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来(如图)。
(1)有一小部分α粒子稍微改变了原来的运动路径,原因是__________;
(2)大多数α粒子能穿透金箔,不改变原来的运动方向,原因是__________;
(3)只有极少数α粒子被弹了回来,原因是____________。
13.据报道钬元素的原子可有效治疗肝癌,该原子中的中子数与核外电子数之差是___________,现有和两种原子,则X和Y是否是同种元素?___________理由是___________。我们把X和Y原子称之为___________原子。
参考答案:
1.A
2.A
3.B
4.B
5.B
6.B
7.C
8.D
9.A
10.C
11.A
12. 原子核质量很大
13. 32 是 质子数相同 同位素
3 / 3
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
