7.2常见的酸和碱课件—2021-2022学年九年级化学沪教版(全国)下册(共26张PPT)
文档属性
| 名称 | 7.2常见的酸和碱课件—2021-2022学年九年级化学沪教版(全国)下册(共26张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-25 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
常见的酸和碱
如何去掉杯子上的茶垢呢? 用加热过的米醋浸泡一昼夜,再用牙刷刷洗就可以轻松清洗干净。
生活小常识
请大家思考:这几种金属被放在什么溶液中?
稀盐酸或稀硫酸
知识链接
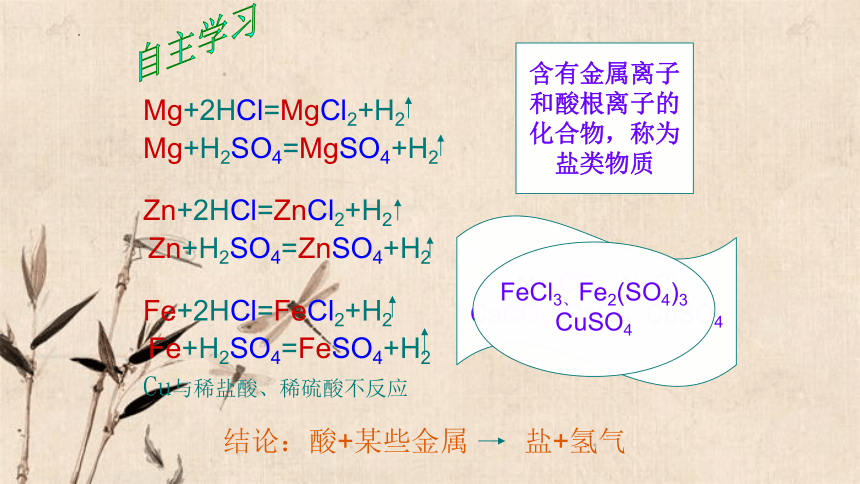
结论:酸+某些金属 盐+氢气
Mg+2HCl=MgCl2+H2
Mg+H2SO4=MgSO4+H2
Zn+2HCl=ZnCl2+H2
Zn+H2SO4=ZnSO4+H2
Fe+2HCl=FeCl2+H2
Fe+H2SO4=FeSO4+H2
Cu与稀盐酸、稀硫酸不反应
含有金属离子
和酸根离子的
化合物,称为
盐类物质
Na2CO3、NaCl
CaCO3、CaCl2、CuSO4
FeCl3、Fe2(SO4)3
CuSO4
自主学习
二、 取少量的黑色氧化铜粉末放在试管中,倒入2毫升的稀硫酸,为了加快反应速率,可用酒精灯加热
合作探究:
一、请大家将生锈的铁钉分别放在两只试管中,分别倒入2毫升的稀盐酸、稀硫酸,观察现象
结论:酸+某些金属氧化物反应 盐+水
OH
Na
H
Cl
你对盐酸与氢氧化钠溶液反应有哪些认识?
一、中和反应
HCl+NaOH==
H2O+
酸 + 碱 → 水 + 盐
水分子在溶液中不易电离。反应后,
溶液中减少的离子是 。
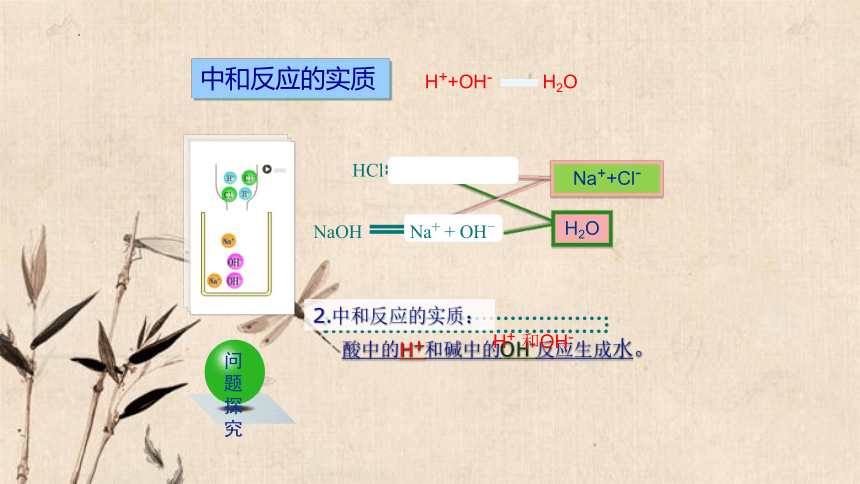
酸中的H+和碱中的OH-反应生成水。
问题探究
HCl H+ + Cl-
H++OH- H2O
H2O
Na++Cl-
H+ 和OH-
2.中和反应的实质:
中和反应的实质
NaOH Na+ + OH-
随学随练,效果好
下列属于复分解反应的是( ),属于中和反应的是( ),属于氧化反应的是( )。
A. Zn + 2HCl == ZnCl2 + H2↑
B. CuO + 2HCl == CuCl2 + H2O
C. Cu(OH)2 + H2SO4== CuSO4 + 2H2O
D. H2CO3 == H2O + CO2↑
E. H2 + O2 == 2H2O
B、C
C
置换反应
分解反应
点燃
化合反应
复分解反应
复分解反应
中和反应属于复分解反应!
中和反应、氧化反应不属于基本反应类型!
E
交流讨论:
1、酚酞在实验中起到什么作用?
2、盐酸与氢氧化钠恰好完全反应的现象是什么?
3、若滴加盐酸至过量,溶液酸碱性及pH变化呢?
答:指示作用,因为NaOH与HCl反应无明显现象发生,根据酚酞溶液的颜色变化来判断反应的发生。
答:酚酞溶液由红色变为无色,说明两者恰好完全反应,此时溶液变成中性。(边滴加边振荡至恰好变无色!)
答:溶液:碱性 中性 酸性
pH值:>7 =7 <7
(石蕊试液颜色变化不明显不利于观察)
展示交流
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
醋酸
发生中和反应
皮蛋和食醋更配哦!
二、中和反应在实际中的应用
1 .农业上:改变土壤的酸碱性
⑴酸性土壤:
如用熟石灰改良酸性土壤
⑵碱性土壤:
如用碳酸饮料浇树
改良土壤的碱性
促进植物的光合作用
2.工业上:处理工厂的废水
硫酸厂的污水中含有硫酸等杂质,可以用熟石灰进行中和处理。
H2SO4+ Ca(OH)2=CaSO4+2H2O
(1)酸性废水:
(2)碱性废水:
如造纸厂的废水
3.用于医药
胃酸(主要HCl)过多的病人,可以服用含氢氧化铝的药来治病。
铝离子对身体有不良作用,所以氢氧化铝的药物逐渐被取代,改用含氢氧化镁的药物。
3HCl+Al(OH)3=AlCl3+3H2O
中和胃酸
2HCl+Mg(OH)2=MgCl2+2H2O
蚊虫能分泌出蚁酸,使皮肤肿痛,怎么办呢
可以涂一些含有碱性物质(如肥皂水、牙膏或NH3·H2O)等药水,就可以减轻痛痒。
你能帮助他吗?
思考: 改良酸性土壤、治疗胃酸过多时,为什么不使用NaOH呢?
NaOH具有强烈的腐蚀性
OH-
Na+
H+
Cl-
HCl+NaOH==
H2O+
2、此时溶液中的溶质是什么?
分析:
反应后溶液的酸碱性如何?
拓展延伸:NaOH溶液和稀盐酸(HCl)反应的微观过程
化学方程式:
NaOH + HCl = NaCl + H2O
反应实质: H+ + OH- → H2O
酸溶液中的H+和碱溶液中的OH-反应生成水分子的过程。
NaOH溶液和稀盐酸(HCl)反应的微观实质:
OH-
H+
Na+
Cl-
NaOH + HCl = NaCl + H2O
碱
酸
水
盐
金属离子
酸根离子
上页
下页
盐是金属离子(NH+)和酸根
离子组成的化合物
归纳:
中和反应
H+ + OHˉ= H2O
1、中和反应是酸与碱作用生成盐和水的
反应。反应过程中放出热量。
2、酸与碱反应的结果是酸和碱各自的特
性都消失···
HCl + NaOH = NaCl + H2O
3、中和反应属于复分解反应
三、中和反应的实际应用
1、调节土壤的酸碱性
如向酸性土壤中加入熟石灰或施加稀氨水可以使土壤的酸性降低;可用碳酸水改良碱性土壤。
例如,某硝酸(HNO3)
厂附近的土地因工业污染,土壤中含有硝酸,不利于作物的生长,周围的农民为此向土壤中撒适量的熟石灰。
你能用化学方程式表达出它的原理么?
胃乐说明书
[药品名称] 胃乐胶囊
[性状] 本品为胶囊剂,内容物为灰黄棕色,气味香,味微苦
[主要成分] 氢氧化铝[Al(OH)3 ]、甘草提取物、白芨、木香等
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
[用法与用量] 口服,一次2~3粒,一日3次,空腹服用
[规格] 0.4g/粒
[贮藏] 密封,置干燥阴凉处
[包装] 20粒/盒
[有效期] 两年
胶
囊
胃 乐
2、用于医药
试用方程式表示出胃乐胶囊治疗胃酸过多的原理:
Al(OH)3+3HCl = AlCl3 + 3H2O
3、处理工厂排放的酸性或碱性废水
或处理实验室里的酸、碱性废液。
H2SO4+2NH3·H2O =(NH4)2SO4+2H2O
污
水
处
理
有些化工厂排放的废水中含有硫酸,如果用氨水(NH3·H2O)中和它,能得到一种氮肥——硫酸铵〔(NH4)2SO4 〕,试写出该反应的化学方程式:
(1)洗发时,先用洗发剂(弱碱性)洗净头发,再用护发素(弱酸性)护理,调节头发的酸碱平衡。
4、日常生活
(2)被蚂蚁、蚊子叮咬后,昆虫分泌的酸性物质进入肌肉,使肌肉酸痛,涂上稀氨水或肥皂水等物质可以止痛消肿,你知道其中的道理吗?
归纳整理
1.农业
2.工业
3.医疗
中和反应在实际中的应用
4.生活
中和
反应
定义
课堂小结
本质
应用
酸 + 碱 → 水 + 盐
H++OH- H2O
改变土壤、工业废水酸碱性
治疗胃酸过多,蚊虫叮咬等等
谢谢
常见的酸和碱
如何去掉杯子上的茶垢呢? 用加热过的米醋浸泡一昼夜,再用牙刷刷洗就可以轻松清洗干净。
生活小常识
请大家思考:这几种金属被放在什么溶液中?
稀盐酸或稀硫酸
知识链接
结论:酸+某些金属 盐+氢气
Mg+2HCl=MgCl2+H2
Mg+H2SO4=MgSO4+H2
Zn+2HCl=ZnCl2+H2
Zn+H2SO4=ZnSO4+H2
Fe+2HCl=FeCl2+H2
Fe+H2SO4=FeSO4+H2
Cu与稀盐酸、稀硫酸不反应
含有金属离子
和酸根离子的
化合物,称为
盐类物质
Na2CO3、NaCl
CaCO3、CaCl2、CuSO4
FeCl3、Fe2(SO4)3
CuSO4
自主学习
二、 取少量的黑色氧化铜粉末放在试管中,倒入2毫升的稀硫酸,为了加快反应速率,可用酒精灯加热
合作探究:
一、请大家将生锈的铁钉分别放在两只试管中,分别倒入2毫升的稀盐酸、稀硫酸,观察现象
结论:酸+某些金属氧化物反应 盐+水
OH
Na
H
Cl
你对盐酸与氢氧化钠溶液反应有哪些认识?
一、中和反应
HCl+NaOH==
H2O+
酸 + 碱 → 水 + 盐
水分子在溶液中不易电离。反应后,
溶液中减少的离子是 。
酸中的H+和碱中的OH-反应生成水。
问题探究
HCl H+ + Cl-
H++OH- H2O
H2O
Na++Cl-
H+ 和OH-
2.中和反应的实质:
中和反应的实质
NaOH Na+ + OH-
随学随练,效果好
下列属于复分解反应的是( ),属于中和反应的是( ),属于氧化反应的是( )。
A. Zn + 2HCl == ZnCl2 + H2↑
B. CuO + 2HCl == CuCl2 + H2O
C. Cu(OH)2 + H2SO4== CuSO4 + 2H2O
D. H2CO3 == H2O + CO2↑
E. H2 + O2 == 2H2O
B、C
C
置换反应
分解反应
点燃
化合反应
复分解反应
复分解反应
中和反应属于复分解反应!
中和反应、氧化反应不属于基本反应类型!
E
交流讨论:
1、酚酞在实验中起到什么作用?
2、盐酸与氢氧化钠恰好完全反应的现象是什么?
3、若滴加盐酸至过量,溶液酸碱性及pH变化呢?
答:指示作用,因为NaOH与HCl反应无明显现象发生,根据酚酞溶液的颜色变化来判断反应的发生。
答:酚酞溶液由红色变为无色,说明两者恰好完全反应,此时溶液变成中性。(边滴加边振荡至恰好变无色!)
答:溶液:碱性 中性 酸性
pH值:>7 =7 <7
(石蕊试液颜色变化不明显不利于观察)
展示交流
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
醋酸
发生中和反应
皮蛋和食醋更配哦!
二、中和反应在实际中的应用
1 .农业上:改变土壤的酸碱性
⑴酸性土壤:
如用熟石灰改良酸性土壤
⑵碱性土壤:
如用碳酸饮料浇树
改良土壤的碱性
促进植物的光合作用
2.工业上:处理工厂的废水
硫酸厂的污水中含有硫酸等杂质,可以用熟石灰进行中和处理。
H2SO4+ Ca(OH)2=CaSO4+2H2O
(1)酸性废水:
(2)碱性废水:
如造纸厂的废水
3.用于医药
胃酸(主要HCl)过多的病人,可以服用含氢氧化铝的药来治病。
铝离子对身体有不良作用,所以氢氧化铝的药物逐渐被取代,改用含氢氧化镁的药物。
3HCl+Al(OH)3=AlCl3+3H2O
中和胃酸
2HCl+Mg(OH)2=MgCl2+2H2O
蚊虫能分泌出蚁酸,使皮肤肿痛,怎么办呢
可以涂一些含有碱性物质(如肥皂水、牙膏或NH3·H2O)等药水,就可以减轻痛痒。
你能帮助他吗?
思考: 改良酸性土壤、治疗胃酸过多时,为什么不使用NaOH呢?
NaOH具有强烈的腐蚀性
OH-
Na+
H+
Cl-
HCl+NaOH==
H2O+
2、此时溶液中的溶质是什么?
分析:
反应后溶液的酸碱性如何?
拓展延伸:NaOH溶液和稀盐酸(HCl)反应的微观过程
化学方程式:
NaOH + HCl = NaCl + H2O
反应实质: H+ + OH- → H2O
酸溶液中的H+和碱溶液中的OH-反应生成水分子的过程。
NaOH溶液和稀盐酸(HCl)反应的微观实质:
OH-
H+
Na+
Cl-
NaOH + HCl = NaCl + H2O
碱
酸
水
盐
金属离子
酸根离子
上页
下页
盐是金属离子(NH+)和酸根
离子组成的化合物
归纳:
中和反应
H+ + OHˉ= H2O
1、中和反应是酸与碱作用生成盐和水的
反应。反应过程中放出热量。
2、酸与碱反应的结果是酸和碱各自的特
性都消失···
HCl + NaOH = NaCl + H2O
3、中和反应属于复分解反应
三、中和反应的实际应用
1、调节土壤的酸碱性
如向酸性土壤中加入熟石灰或施加稀氨水可以使土壤的酸性降低;可用碳酸水改良碱性土壤。
例如,某硝酸(HNO3)
厂附近的土地因工业污染,土壤中含有硝酸,不利于作物的生长,周围的农民为此向土壤中撒适量的熟石灰。
你能用化学方程式表达出它的原理么?
胃乐说明书
[药品名称] 胃乐胶囊
[性状] 本品为胶囊剂,内容物为灰黄棕色,气味香,味微苦
[主要成分] 氢氧化铝[Al(OH)3 ]、甘草提取物、白芨、木香等
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
[用法与用量] 口服,一次2~3粒,一日3次,空腹服用
[规格] 0.4g/粒
[贮藏] 密封,置干燥阴凉处
[包装] 20粒/盒
[有效期] 两年
胶
囊
胃 乐
2、用于医药
试用方程式表示出胃乐胶囊治疗胃酸过多的原理:
Al(OH)3+3HCl = AlCl3 + 3H2O
3、处理工厂排放的酸性或碱性废水
或处理实验室里的酸、碱性废液。
H2SO4+2NH3·H2O =(NH4)2SO4+2H2O
污
水
处
理
有些化工厂排放的废水中含有硫酸,如果用氨水(NH3·H2O)中和它,能得到一种氮肥——硫酸铵〔(NH4)2SO4 〕,试写出该反应的化学方程式:
(1)洗发时,先用洗发剂(弱碱性)洗净头发,再用护发素(弱酸性)护理,调节头发的酸碱平衡。
4、日常生活
(2)被蚂蚁、蚊子叮咬后,昆虫分泌的酸性物质进入肌肉,使肌肉酸痛,涂上稀氨水或肥皂水等物质可以止痛消肿,你知道其中的道理吗?
归纳整理
1.农业
2.工业
3.医疗
中和反应在实际中的应用
4.生活
中和
反应
定义
课堂小结
本质
应用
酸 + 碱 → 水 + 盐
H++OH- H2O
改变土壤、工业废水酸碱性
治疗胃酸过多,蚊虫叮咬等等
谢谢
