试卷讲评(空气与生命单元试卷)
图片预览




文档简介
课件27张PPT。试卷讲评考试内容要求:
1.说出空气的主要成分。
2.认识氧气、二氧化碳等物质的主要性质并列举其用途。初步学习在实验室制取氧气和二氧化碳。
3.能说出化合反应、分解反应的特点。
4.知道在化学反应过程中伴随能量变化。
5.知道催化剂在化学反应中的作用。
6.知道燃烧的条件,知道剧烈氧化和缓慢氧化的过程,具有安全意识,了解火灾自救的一般方法。
7.通过实验认识质量守恒定律,并能用它来解释常见的现象。
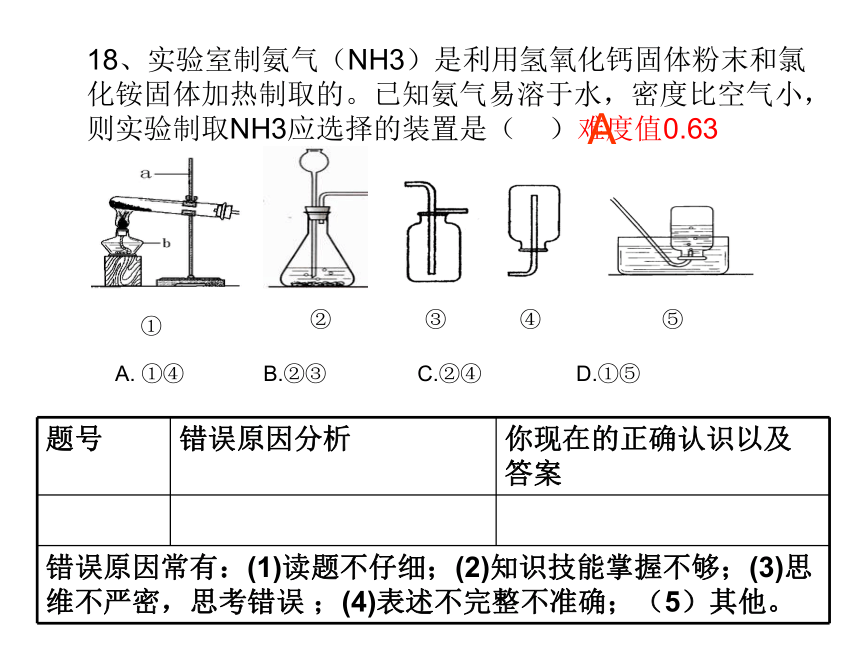
8.知道化学方程式表示的意义,能根据化学方程式进行生成物和反应物之间的计算。18、实验室制氨气(NH3)是利用氢氧化钙固体粉末和氯化铵固体加热制取的。已知氨气易溶于水,密度比空气小,则实验制取NH3应选择的装置是( )难度值0.63
A. ①④ B.②③ C.②④ D.①⑤①②④③⑤A24、(4)说明二氧化碳具有的性质是 、密度比空气的大,
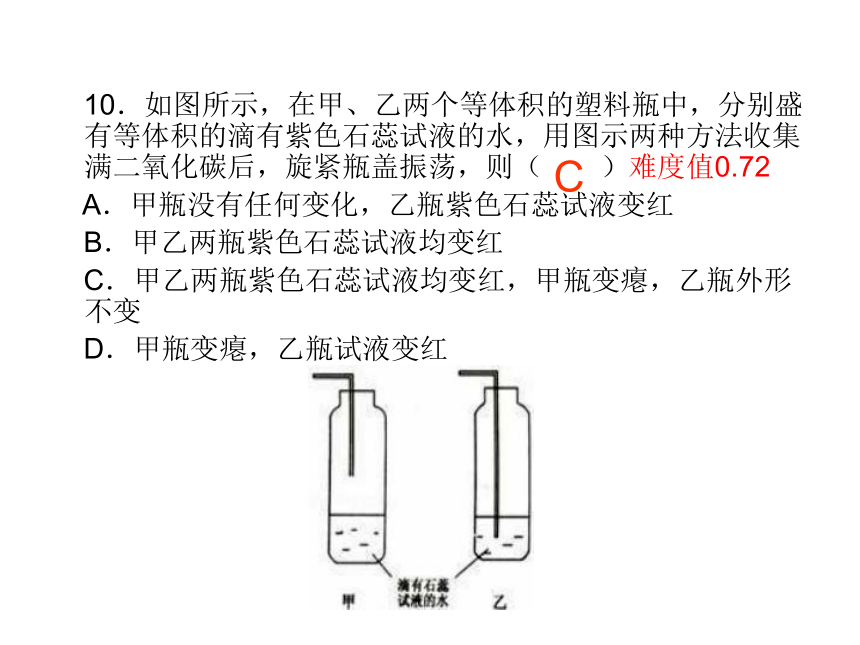
因此,二氧化碳可用于灭火。难度值0.46不能燃烧也不支持燃烧22、(1)根据上述信息,写出金属铬的一种物理性质: 。难度值0.44呈银白色或难溶于水28、(1)根据上述内容推断乙炔(C2H2)具有的化学性质是 。难度值0.28 可燃性 10.如图所示,在甲、乙两个等体积的塑料瓶中,分别盛有等体积的滴有紫色石蕊试液的水,用图示两种方法收集满二氧化碳后,旋紧瓶盖振荡,则( )难度值0.72
A.甲瓶没有任何变化,乙瓶紫色石蕊试液变红
B.甲乙两瓶紫色石蕊试液均变红
C.甲乙两瓶紫色石蕊试液均变红,甲瓶变瘪,乙瓶外形 不变
D.甲瓶变瘪,乙瓶试液变红
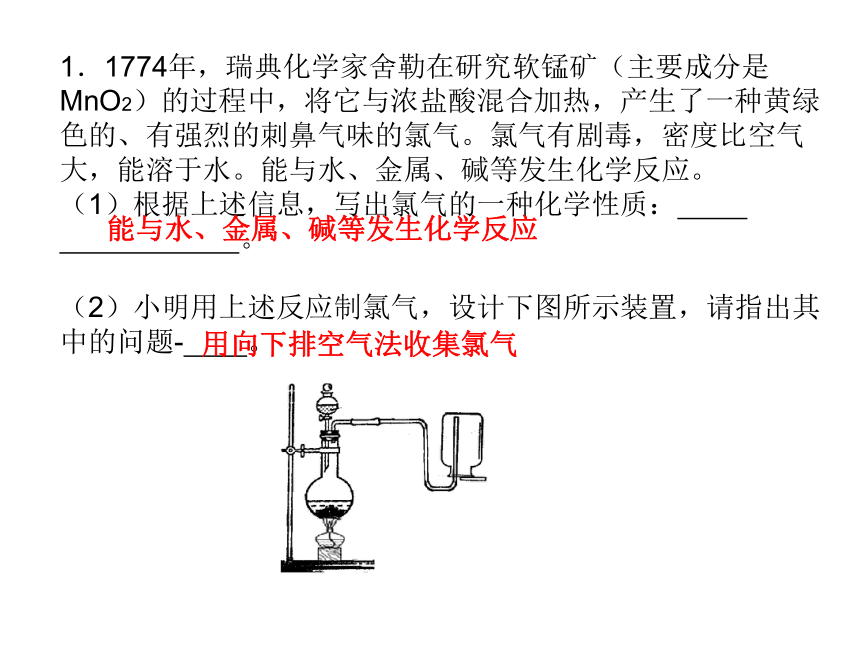
C1.1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色的、有强烈的刺鼻气味的氯气。氯气有剧毒,密度比空气大,能溶于水。能与水、金属、碱等发生化学反应。
(1)根据上述信息,写出氯气的一种化学性质: 。
(2)小明用上述反应制氯气,设计下图所示装置,请指出其中的问题- 。
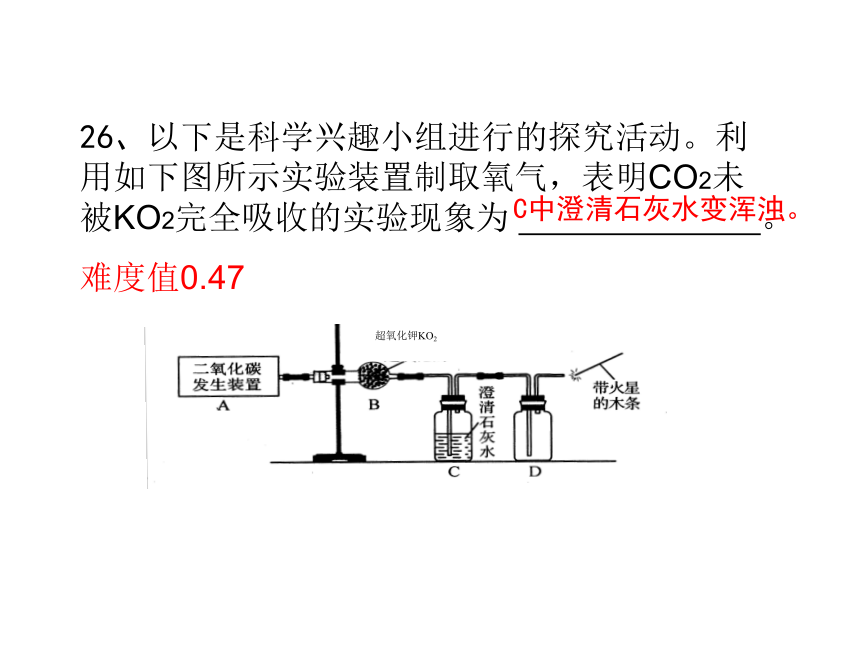
能与水、金属、碱等发生化学反应用向下排空气法收集氯气26、以下是科学兴趣小组进行的探究活动。利用如下图所示实验装置制取氧气,表明CO2未被KO2完全吸收的实验现象为 。
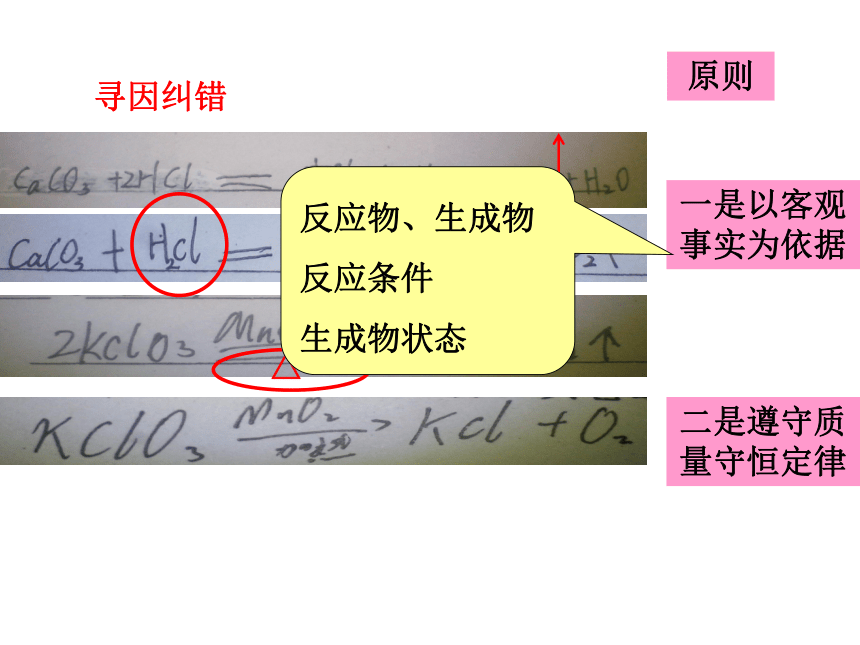
难度值0.47超氧化钾KO2C中澄清石灰水变浑浊。寻因纠错△原则一是以客观事实为依据反应物、生成物
反应条件
生成物状态二是遵守质量守恒定律正确范例:2124(2)24(3)难度值0.53难度值0.75难度值0.452. 哥伦比亚号航天飞机曾用金属铝和高氯酸铵(NH4ClO4)的混合物作为固体燃料。加热铝粉使其被氧气氧化,放出大量的热,促使混合物中的高氯酸铵受热分解,同时生成四种气体:两种气体是空气中的主要成分,一种气体是Cl2,还有一种气体是化合物(常温下是液态),因而产生巨大的推动力。试写出高氯酸铵受热分解的化学方程式:
;2NH4ClO4 ===2O2↑+N2↑+Cl2↑ +4H2O↑△15、下列观点符合质量守恒定律的是( ) 难度值0.11A.煤燃烧后剩余残渣的质量减轻了D.水遇冷凝固成冰块,变化前后质量不变质量守恒定律内容:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。· ·· ·C.一定条件下,SO2和O2生成SO3,反应前后分子总数不变B.12克碳在16克氧气中燃烧一定生成28克二氧化碳A26、 “化学氧自救器”,主要用于煤矿井下应急。它利用人呼出的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)在常温下接触产生氧气,该反应的化学方程式为:
4KO2 +2CO2 ====2X +3O2,则X的化学式是 。K2CO3难度值0.5920、在化学反应A+B===C中,A与B反应的质量关系如图所示, 现将6gA和8gB充分反应,则生成C的质量是 ( )难度值0.33
A.9g B.11g C.12g D.14gC23、化学反应A+B=C+2D,40克A恰好与60克B完全反应,生成80克C,则同时生成D 克。难度值0.28
现已知物质的相对分子质量A为80,B为120,C为160,则D的相对分子质量为 。难度值0.53202031、完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数。
【研究方案】先称取一定质量的氯酸钾和二氧化锰混合物放入大试管中加热至质量不再变化为止。根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量。
【解决问题】实验测得固体混合物质量随加热时间变化的相关数据如图所示。
(1)反应结束后,11.2克固体中含有的物质是___。
难度值0.41(2) 反应中生成的氧气的质量为____________。
(3)计算原混合物中氯酸钾的质量是多少?难度值0.45帮这些同学找找他们的错因:正确范例: 3.某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
⑴ 根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
⑵ 求该石灰石中碳酸钙的质量分数。
25.某课外活动小组为测定空气中氧气的含量,做了如下实验:在由两个注射器组成的密闭系统内共有50mL 空气(如右图)。然后给装有红磷的玻璃管加热,同时交替推动两个注射器使注射器内的氧气充分与红磷反应,至玻璃管内的红磷变成白烟,反应完毕停止加热后,待冷却至室温将气体全部推至一个注射器内。0.47
(1)实验结束后,注射器内的气体体积理论上应该减少 mL。
(2)某同学建议用木碳代替红磷的方案,可马上被否定,否定该方案的依据是 ;
0.1410碳燃烧产生二氧化碳气体,装置内气压变化不大(3)小强测得实验结果如下:
造成该实验出现误差的原因可能是 。
0.67装置气密性不好或红磷过少27、某研究性学习小组在学习了双氧水分解制氧气的实验后,知道催化剂(Mn02)能改变化学反应速率。到底还有哪些因素与化学反应速率有关呢?
【小组讨论】:甲同学观点:化学反应速率与反应物的质量分数有关
乙同学观点:化学反应速率与反应温度有关
【设计实验】:他们设计并进行了以下4次实验(2)由以上实验还能得出:其他条件相同时,反应温度越高或反应物的质量分数越大,则反应速率____ _____。0.53
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总质量 (选填“减小”或“不变”或“增大”)。0.42越快不变相信自己,不断进步!试题知识方法审题→考什么
析题→怎么考
答题→怎么答
谢谢!4.水煤气是重要的气体燃料,某水煤气样品可能含有CO2、CO和H2,某科学兴趣小组的同学对该水煤气样品的成分进行探究. (1)为了证明该水煤气样品中含有CO,小明设计了如图所示装置进行实验,证明该气体样品中含有CO。
请回答:为了能使检验顺利进行,A中的药品是______________.NaOH溶液(2)小张认为小明的实验不够严密,请指出 ____________________________________________________,
如何改进:________________________________________。不能证明原水煤气中二氧化碳是否除尽在A后面再增加一个同样的装置,内乘同样样品(2)小张认为小明的实验不够严密,做了如图的改进:则B中澄清石灰水的作用是_______________________________,当观察到________________________________________的现象时,可以肯定该水煤气样品中一定含有CO.检验CO2是否已除尽B中澄清石灰水不变浑浊;C中变浑浊5.带火星的木条在氧气中可以复燃.那么,是不是只有纯净的氧气才能使带火星的木条复燃呢?为此,同学们开展了相关探究实验.实验主要步骤如下:先制取一定量的氧气备用,再测得集气瓶实际容积为317毫升,然后采用某种方法得到5瓶含氧量不同的空气,最后用带火星的木条来试验,观察是否复燃.相关的数据见下表:
(1)请指出得到5瓶含氧量不同的空气的具体方法 ;
(2)试将上表空白处补充完整(保留1位小数); 。
(3)由该实验可得到的结论是 _______ __ 。
先在集气瓶里预先加一定体积的水,再用排水集气法收集氧气。45.2%当空气中氧气所占体积比达到41.9%以上时,能使带火星的木条复燃。
1.说出空气的主要成分。
2.认识氧气、二氧化碳等物质的主要性质并列举其用途。初步学习在实验室制取氧气和二氧化碳。
3.能说出化合反应、分解反应的特点。
4.知道在化学反应过程中伴随能量变化。
5.知道催化剂在化学反应中的作用。
6.知道燃烧的条件,知道剧烈氧化和缓慢氧化的过程,具有安全意识,了解火灾自救的一般方法。
7.通过实验认识质量守恒定律,并能用它来解释常见的现象。
8.知道化学方程式表示的意义,能根据化学方程式进行生成物和反应物之间的计算。18、实验室制氨气(NH3)是利用氢氧化钙固体粉末和氯化铵固体加热制取的。已知氨气易溶于水,密度比空气小,则实验制取NH3应选择的装置是( )难度值0.63
A. ①④ B.②③ C.②④ D.①⑤①②④③⑤A24、(4)说明二氧化碳具有的性质是 、密度比空气的大,
因此,二氧化碳可用于灭火。难度值0.46不能燃烧也不支持燃烧22、(1)根据上述信息,写出金属铬的一种物理性质: 。难度值0.44呈银白色或难溶于水28、(1)根据上述内容推断乙炔(C2H2)具有的化学性质是 。难度值0.28 可燃性 10.如图所示,在甲、乙两个等体积的塑料瓶中,分别盛有等体积的滴有紫色石蕊试液的水,用图示两种方法收集满二氧化碳后,旋紧瓶盖振荡,则( )难度值0.72
A.甲瓶没有任何变化,乙瓶紫色石蕊试液变红
B.甲乙两瓶紫色石蕊试液均变红
C.甲乙两瓶紫色石蕊试液均变红,甲瓶变瘪,乙瓶外形 不变
D.甲瓶变瘪,乙瓶试液变红
C1.1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色的、有强烈的刺鼻气味的氯气。氯气有剧毒,密度比空气大,能溶于水。能与水、金属、碱等发生化学反应。
(1)根据上述信息,写出氯气的一种化学性质: 。
(2)小明用上述反应制氯气,设计下图所示装置,请指出其中的问题- 。
能与水、金属、碱等发生化学反应用向下排空气法收集氯气26、以下是科学兴趣小组进行的探究活动。利用如下图所示实验装置制取氧气,表明CO2未被KO2完全吸收的实验现象为 。
难度值0.47超氧化钾KO2C中澄清石灰水变浑浊。寻因纠错△原则一是以客观事实为依据反应物、生成物
反应条件
生成物状态二是遵守质量守恒定律正确范例:2124(2)24(3)难度值0.53难度值0.75难度值0.452. 哥伦比亚号航天飞机曾用金属铝和高氯酸铵(NH4ClO4)的混合物作为固体燃料。加热铝粉使其被氧气氧化,放出大量的热,促使混合物中的高氯酸铵受热分解,同时生成四种气体:两种气体是空气中的主要成分,一种气体是Cl2,还有一种气体是化合物(常温下是液态),因而产生巨大的推动力。试写出高氯酸铵受热分解的化学方程式:
;2NH4ClO4 ===2O2↑+N2↑+Cl2↑ +4H2O↑△15、下列观点符合质量守恒定律的是( ) 难度值0.11A.煤燃烧后剩余残渣的质量减轻了D.水遇冷凝固成冰块,变化前后质量不变质量守恒定律内容:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。· ·· ·C.一定条件下,SO2和O2生成SO3,反应前后分子总数不变B.12克碳在16克氧气中燃烧一定生成28克二氧化碳A26、 “化学氧自救器”,主要用于煤矿井下应急。它利用人呼出的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)在常温下接触产生氧气,该反应的化学方程式为:
4KO2 +2CO2 ====2X +3O2,则X的化学式是 。K2CO3难度值0.5920、在化学反应A+B===C中,A与B反应的质量关系如图所示, 现将6gA和8gB充分反应,则生成C的质量是 ( )难度值0.33
A.9g B.11g C.12g D.14gC23、化学反应A+B=C+2D,40克A恰好与60克B完全反应,生成80克C,则同时生成D 克。难度值0.28
现已知物质的相对分子质量A为80,B为120,C为160,则D的相对分子质量为 。难度值0.53202031、完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数。
【研究方案】先称取一定质量的氯酸钾和二氧化锰混合物放入大试管中加热至质量不再变化为止。根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量。
【解决问题】实验测得固体混合物质量随加热时间变化的相关数据如图所示。
(1)反应结束后,11.2克固体中含有的物质是___。
难度值0.41(2) 反应中生成的氧气的质量为____________。
(3)计算原混合物中氯酸钾的质量是多少?难度值0.45帮这些同学找找他们的错因:正确范例: 3.某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
⑴ 根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
⑵ 求该石灰石中碳酸钙的质量分数。
25.某课外活动小组为测定空气中氧气的含量,做了如下实验:在由两个注射器组成的密闭系统内共有50mL 空气(如右图)。然后给装有红磷的玻璃管加热,同时交替推动两个注射器使注射器内的氧气充分与红磷反应,至玻璃管内的红磷变成白烟,反应完毕停止加热后,待冷却至室温将气体全部推至一个注射器内。0.47
(1)实验结束后,注射器内的气体体积理论上应该减少 mL。
(2)某同学建议用木碳代替红磷的方案,可马上被否定,否定该方案的依据是 ;
0.1410碳燃烧产生二氧化碳气体,装置内气压变化不大(3)小强测得实验结果如下:
造成该实验出现误差的原因可能是 。
0.67装置气密性不好或红磷过少27、某研究性学习小组在学习了双氧水分解制氧气的实验后,知道催化剂(Mn02)能改变化学反应速率。到底还有哪些因素与化学反应速率有关呢?
【小组讨论】:甲同学观点:化学反应速率与反应物的质量分数有关
乙同学观点:化学反应速率与反应温度有关
【设计实验】:他们设计并进行了以下4次实验(2)由以上实验还能得出:其他条件相同时,反应温度越高或反应物的质量分数越大,则反应速率____ _____。0.53
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总质量 (选填“减小”或“不变”或“增大”)。0.42越快不变相信自己,不断进步!试题知识方法审题→考什么
析题→怎么考
答题→怎么答
谢谢!4.水煤气是重要的气体燃料,某水煤气样品可能含有CO2、CO和H2,某科学兴趣小组的同学对该水煤气样品的成分进行探究. (1)为了证明该水煤气样品中含有CO,小明设计了如图所示装置进行实验,证明该气体样品中含有CO。
请回答:为了能使检验顺利进行,A中的药品是______________.NaOH溶液(2)小张认为小明的实验不够严密,请指出 ____________________________________________________,
如何改进:________________________________________。不能证明原水煤气中二氧化碳是否除尽在A后面再增加一个同样的装置,内乘同样样品(2)小张认为小明的实验不够严密,做了如图的改进:则B中澄清石灰水的作用是_______________________________,当观察到________________________________________的现象时,可以肯定该水煤气样品中一定含有CO.检验CO2是否已除尽B中澄清石灰水不变浑浊;C中变浑浊5.带火星的木条在氧气中可以复燃.那么,是不是只有纯净的氧气才能使带火星的木条复燃呢?为此,同学们开展了相关探究实验.实验主要步骤如下:先制取一定量的氧气备用,再测得集气瓶实际容积为317毫升,然后采用某种方法得到5瓶含氧量不同的空气,最后用带火星的木条来试验,观察是否复燃.相关的数据见下表:
(1)请指出得到5瓶含氧量不同的空气的具体方法 ;
(2)试将上表空白处补充完整(保留1位小数); 。
(3)由该实验可得到的结论是 _______ __ 。
先在集气瓶里预先加一定体积的水,再用排水集气法收集氧气。45.2%当空气中氧气所占体积比达到41.9%以上时,能使带火星的木条复燃。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
