八年级下科学第二章1-5节检测讲评
图片预览





文档简介
课件35张PPT。八年级(下)科学
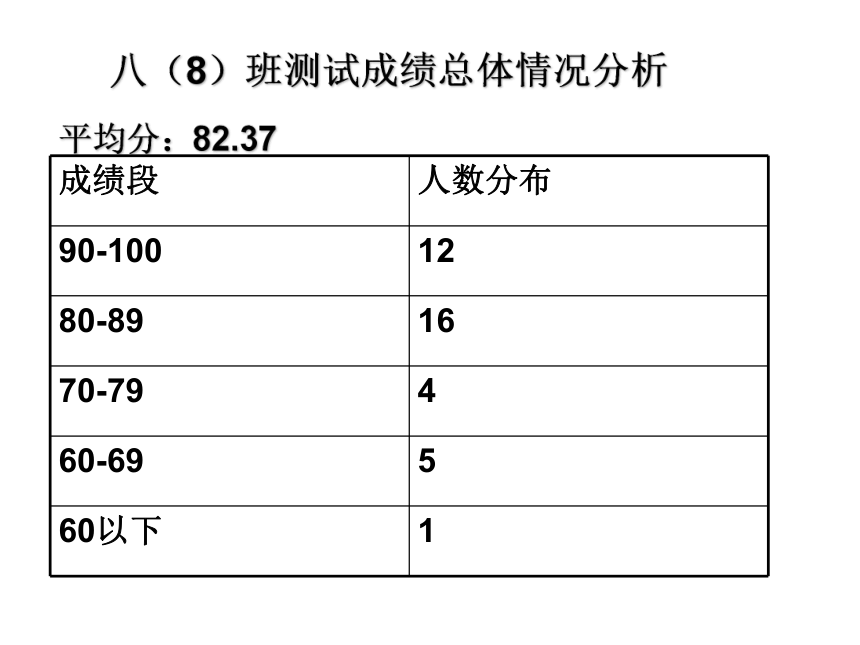
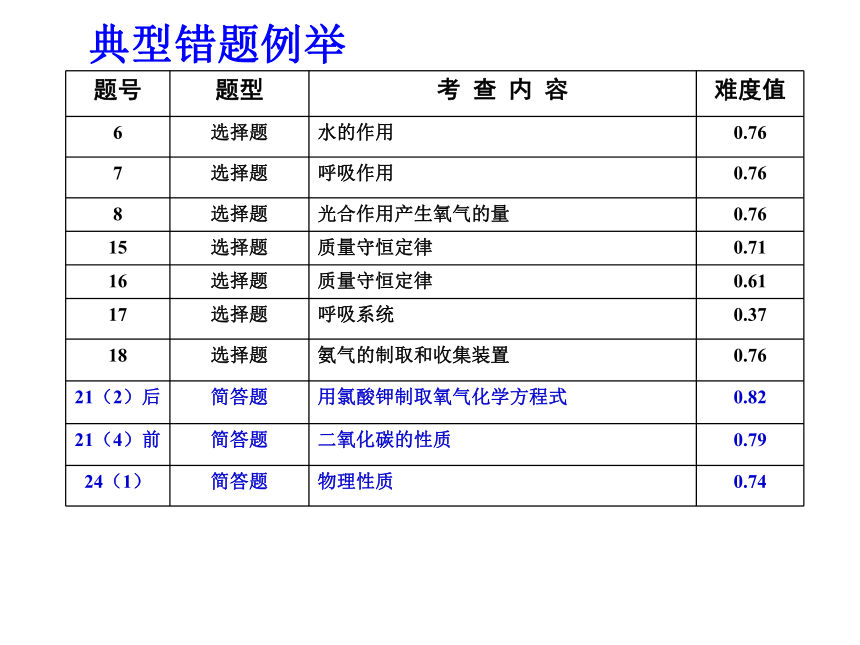
第二章1-5节试卷讲评八(8)班测试成绩总体情况分析平均分:82.37典型错题例举典型错题例举考什么?错误点1、物质的制取、收集和性质及检验。
4、18、21(4)、24(1)、25(1)、27后、
30(1)、31(1)
2、化学方程式的书写。21(2)后、25(2)后
3、质量守恒定律。15、16、27前
4、生物的生命活动(呼吸、呼吸作用和光合作用)。
7、8、17、26(3)
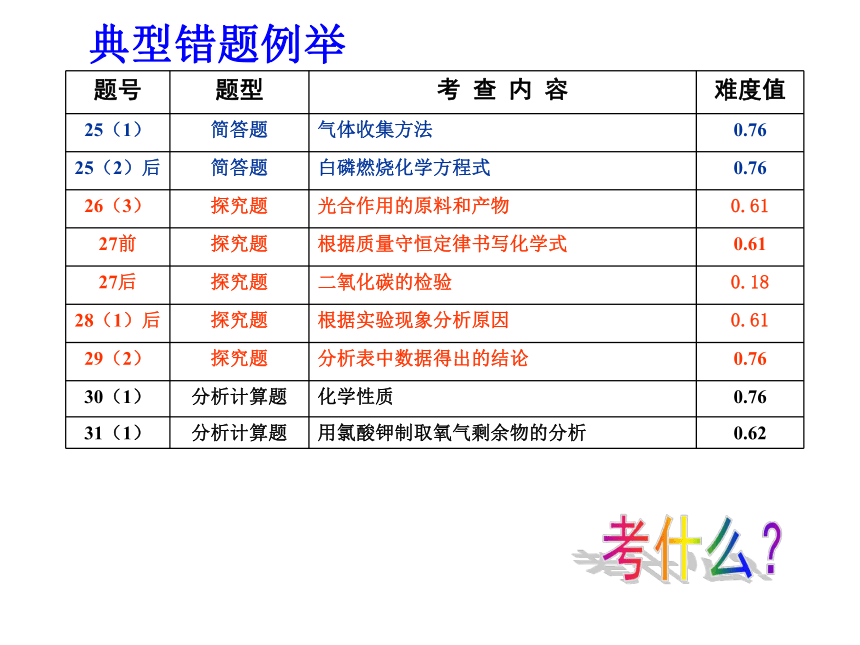
5、实验结果的分析。28(1)后、29(2) 、
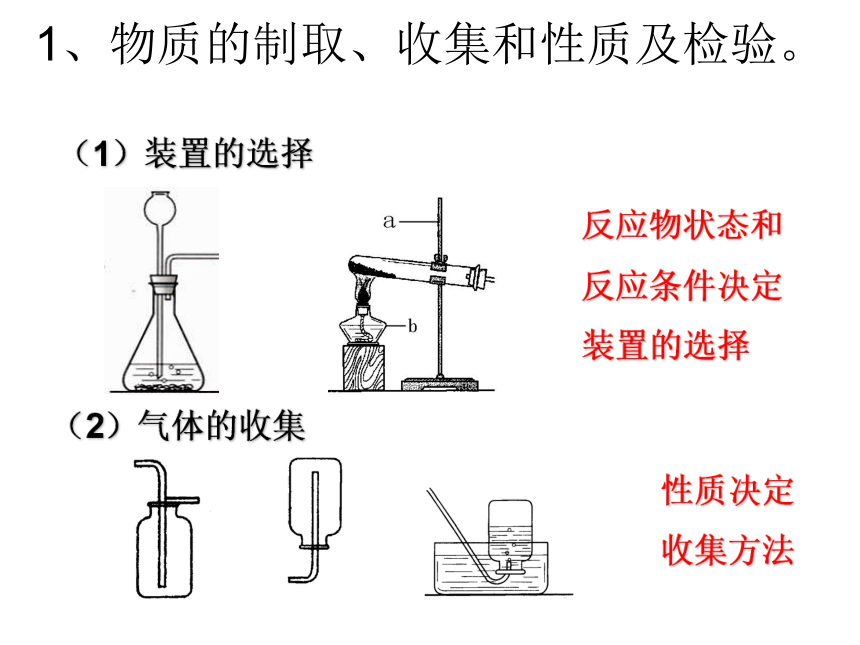
31(1)考什么?1、物质的制取、收集和性质及检验。(1)装置的选择(2)气体的收集性质决定
收集方法反应物状态和
反应条件决定
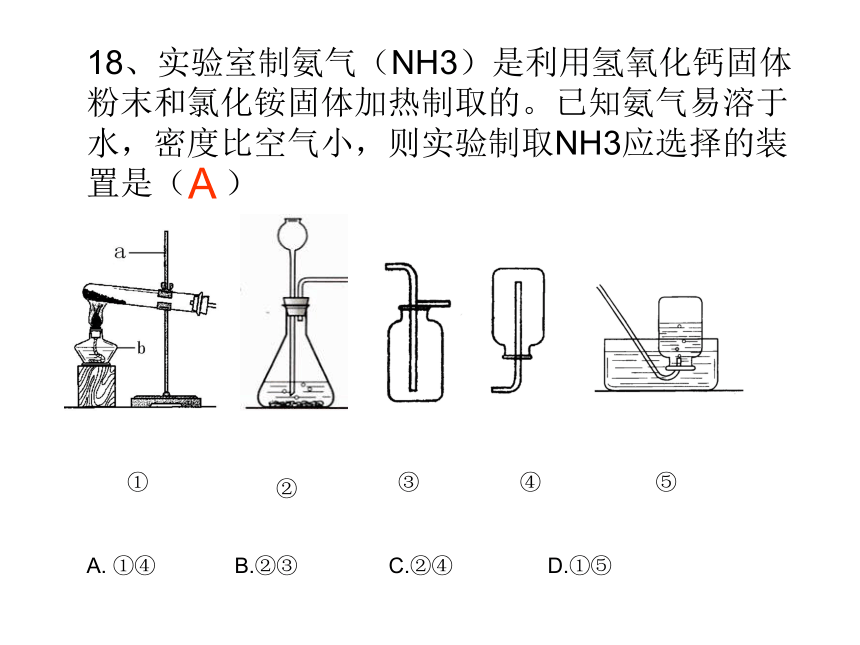
装置的选择18、实验室制氨气(NH3)是利用氢氧化钙固体粉末和氯化铵固体加热制取的。已知氨气易溶于水,密度比空气小,则实验制取NH3应选择的装置是( )
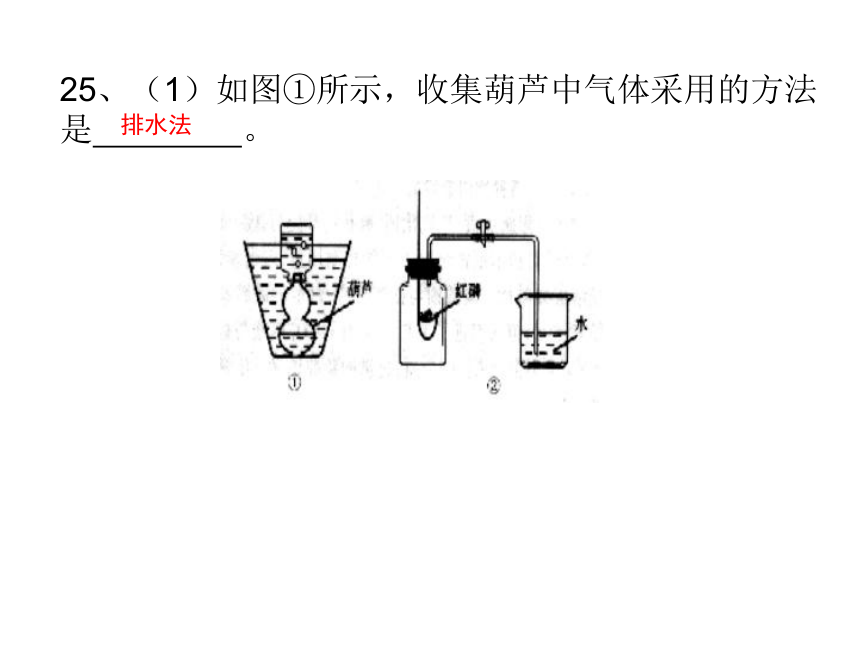
A. ①④ B.②③ C.②④ D.①⑤①②④③⑤A25、(1)如图①所示,收集葫芦中气体采用的方法是 。排水法(3)物质的性质性质物理性质:化学性质:颜色、状态、气味、味道、密度溶解性、熔点、沸点、硬度、导电性、导热性、延展性等 可燃性、氧化性、助燃性、还原性、酸碱性等24、(1)根据上述信息,写出金属铬的一种物理性质: 。呈银白色或难溶于水30、(1)根据上述内容推断乙炔(C2H2)具有的化学性质是 。 可燃性21、(4)说明二氧化碳具有的性质是 、密度比空气的大,
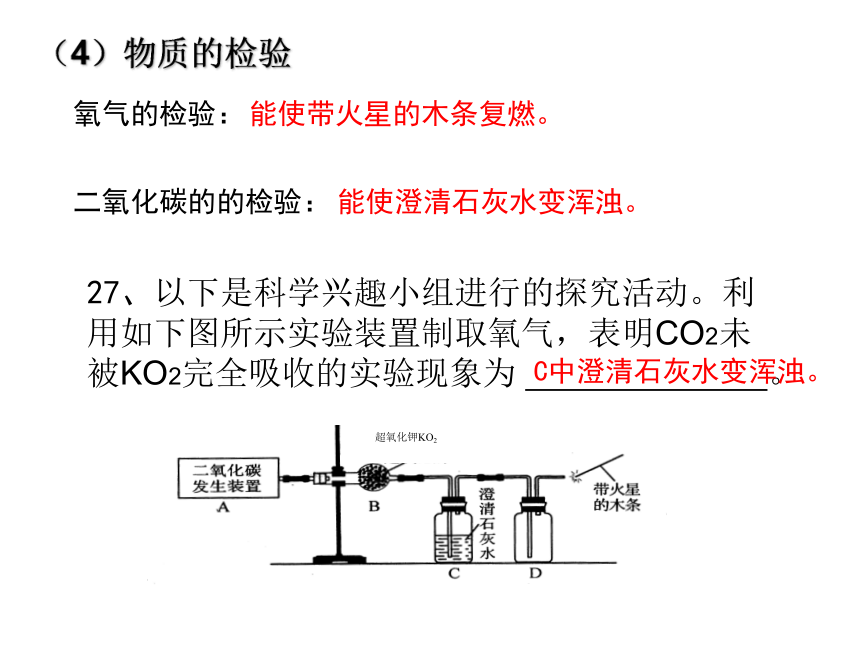
因此,二氧化碳可用于 。不能燃烧也不支持燃烧灭火(4)物质的检验氧气的检验:能使带火星的木条复燃。二氧化碳的的检验:能使澄清石灰水变浑浊。27、以下是科学兴趣小组进行的探究活动。利用如下图所示实验装置制取氧气,表明CO2未被KO2完全吸收的实验现象为 。超氧化钾KO2C中澄清石灰水变浑浊。15、下列观点符合质量守恒定律的是( ) A.铁生锈后铁锈质量比铁大 D.水遇冷凝固成冰块,变化前后质量不变质量守恒定律内容:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。· ·· ·2、质量守恒定律C.8 g CH4完全燃烧生成8 g CO2B.一定条件下,SO2和O2生成SO3,反应前后分子总数不变A16、某密闭容器内有四种物质,在一定条件下充分反应。测得反应前后各物质质量如下表,下列有关说法中不正确的是 ( )
A.a的值等于20
B.参加化学反应的X为222g
C.该反应属于化合反应
D.X一定是化合物质量守恒定律内容:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。· ·· ·C原子数目原子质量原子种类物质的总质量元素质量元素种类物质的种类分子的种类27、 “化学氧自救器”,主要用于煤矿井下应急。它利用人呼出的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)在常温下接触产生氧气,该反应的化学方程式为:
4KO2 +2CO2 ====2X +3O2,则X的化学式是 。K2CO3例.1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色的、有强烈的刺鼻气味的氯气。氯气有剧毒,密度比空气大,能溶于水。能与水、金属、碱等发生化学反应。
(1)根据上述信息,写出氯气的一种化学性质: 。
(2)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请补充完善其反应的化学方程式:
△
MnO2 +4HCl(浓)=== 2H2O + + Cl2↑。
(3)小明用上述反应制氯气,设计下图所示装置,请指出其中的问题- 。
能与水、金属、碱等发生化学反应MnCl2用向下排空气法收集氯气3、化学方程式寻因纠错点燃△MnO2原则一是以客观事实为依据反应物、生成物
反应条件
生成物状态二是遵守质量守恒定律正确范例:朱载歌陈慧慧4、生物的生命活动(呼吸运动、呼吸作用、光合作用)7、除了下列哪一项以外,其余现象都表明植物进行了呼吸作用( )
A.大量潮湿种子周围的空气可使澄清的石灰水变浑浊
B.贮存大量蔬菜的地窖比空地窖要暖和许多
C.地窖内的蔬菜腐烂散发出霉味
D.进入贮存大量水果的地方,点燃蜡烛发现火焰不大,燃烧不旺17、气体从外界进入人体血液中的路线可以表示为 ①鼻腔 ②咽 ③喉 ④支气管 ⑤气管 ⑥肺泡外毛细血管 ⑦肺泡( )
A.①→②→③→④→⑤→⑥→⑦ B.①→②→③→⑤→④→⑦→⑥
C.①→②→③→⑤→④→⑥→⑦ D.①→②→③→④→⑤→⑦→⑥CB呼吸系统呼吸道肺:鼻腔咽喉气管、支气管基本结构为肺泡,它仅由一层上皮细胞构成,外缠毛细血管和弹性纤维呼吸作用:8、温室中的绿色植物受阳光的照射生长,昼夜测定温室内氧气的含量如下图所示,其中正确的( )C光合作用:26、选取生长正常的爬山虎进行如下图所示的光合作用实验:
①实验前应将此装置放在黑暗处一昼夜后,移至光下几小时,再将甲、乙、丙三片叶取下,分别放入盛有酒精的小烧杯中,隔水加热,使叶绿素溶解到酒精中。
②将叶片用清水漂洗后放入培养皿中,分别向这三片叶上滴
加碘液,观察三片叶是否变蓝。
(3)将叶片用清水漂洗后放入培养皿中,分别向这三片叶上滴加碘液,其中叶片乙 蓝色。不 变例、某同学用玉米幼苗作实验材料,利用右图实验装置进行
探究活动。装置中隔板与无色透明钟罩之间以及隔板中
央小孔与玉米茎之间都用凡士林密 封,钟罩内放一盛有
某种液体的小烧杯。
⑴若小烧杯中的液体是澄清的石灰水,将装置放在暗处
一段时间后,小烧杯中的石灰水变浑浊,由此可证
明 。
⑵若小烧杯中是氢氧化钠溶液(氢氧化钠溶液能吸收二氧化碳),
则要探究的问题是 ,要验证这一问题,需要设置一组对照实验。二氧化碳是光合作用的原料 玉米幼苗呼吸作用产生了二氧化碳 5、实验结果的分析28、某同学用右图的实验装置测量动物呼吸作用,小试管中的碱石灰能够充分吸收二氧化碳气体,(实验装置足以维持实验期间老鼠的生命活动,瓶口密封)请据图回答问题:
(1)15分钟后,红墨水柱移动情况如何_____,原因是 。甲瓶中的动物呼吸作用消耗了氧气,产生的二氧化碳被碱石灰吸收,导致甲瓶内气压下降 向左移动29、某研究性学习小组在学习了双氧水分解制氧气的实验后,知道催化剂(Mn02)能改变化学反应速率。到底还有哪些因素与化学反应速率有关呢?
【小组讨论】:甲同学观点:化学反应速率与反应物的质量分数有关
乙同学观点:化学反应速率与反应温度有关
【设计实验】:他们设计并进行了以下4次实验(2)由以上实验还能得出:其他条件相同时,反应温度越高或反应物的质量分数越大,则反应速率____ _____。越快31、完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数。
【研究方案】先称取一定质量的氯酸钾和二氧化锰混合物放入大试管中加热至质量不再变化为止。根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量。
【解决问题】实验测得固体混合物质量随加热时间变化的相关数据如图所示。
(1)反应结束后,11.2克固体中含有的物质是___。氯化钾和二氧化锰 例、土豆中含有的过氧化氢酶对过氧化氢分解具有催化作用。楚楚同学设计实验证明新鲜的土豆片也能加快过氧化氢的分解,并与二氧化锰的催化效果进行比较。用如图装置进行实验,图Ⅰ为过氧化氢分解的反应装置,图Ⅱ用于测量产生O2的体积。实验时均以生成25 mL气体为准,其他可能影响实验的因素均忽略不计,相关数据见下表:回答下列问题:
(1)图Ⅱ装置中油层的作用是 。
(2)上述实验中的“待测数据”指 ;欲探究鲜土豆片与二氧化锰的催化效果,应比较b和 (选填“a”、“b”或“c”)的大小。形成油封,气体将Ⅱ中液体压入量气管,从而测得产生氧气的体积 。反应时间 c 分析错题的方法
首要任务
——寻找错误的原因学习建议相信自己,不断进步!审题细心
关键词
题意指向
……知识方法扎实
细节
能力
(实验)
……答题技巧
答题规范
答题完整
书写工整
……谢谢!例、在班会上,小明的同桌表演了“水能生火”魔术:他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小明很感兴趣,于是,他进行探究。 【提出问题】过氧化钠与水反应生成什么物质?为什么脱脂棉会燃烧? 【猜想与假设】①可能生成了Na2CO3和氢气;也有可能生成了Na2CO3和氧气。
②脱脂棉燃烧可能是因为Na2O2与水反应放出热量。 【设计装置】如图所示。
【实验与分析】
(1)小军对小明的猜想进行了理论的分析,他认为不可能有
Na2CO3生成。小军的依据是 。
(2)为了检验产生的气体是否为氧气,小明在实验中应进行
怎样的操作?
(3)如果小明在实验过程中观察到伸入烧杯中的导管口出现
了 的现象,则说明小明的猜想②是正确的。根据质量守恒定律,反应前后元素种类不变 将带火星的木条靠近导管口P处,若木条复燃,说明是氧气 冒气泡 例、研究人员曾经对绿色植物的光合作用与呼吸作用作过以下研究。
实验一:将某绿色植物放在黑暗装置中,分别测定在不同温度下植物对氧气的吸收量,如图1所示.a、b分别表示10℃和20℃时植物吸收氧气量随时间变化的情况。
实验二:按图2所示装置进行黄豆种子呼吸作用和番茄植株光合作用实验。
请分析回答:
(1)分析实验一可知,温度越高植物吸收氧气越 。
(2)由实验一结果可推知:在实验二中,当广口瓶内黄豆种子温度适当 时.就会促进玻璃罩内番茄植株的光合作用。
(3)联系本实验,试分析吐鲁番瓜果特别甜的原因。 快 升高 晚上温度低,呼吸作用弱,有机物分解少。 例.将等容积、等质量(含瓶塞、导管、燃烧匙及瓶内少量的细砂)的两个集气瓶置于天平的左右两盘,并调至平衡。然后同时迅速放入点燃的等质量的白磷和木炭(如右图所示),使两者充分燃烧后冷却至室温,打开止水夹后,此时的天平( )
A.指针偏向右
B.指针偏向左
C.仍处于平衡状态
D.指针先向左后向右偏B例题.带火星的木条在氧气中可以复燃.那么,是不是只有纯净的氧气才能使带火星的木条复燃呢?为此,同学们开展了相关探究实验.实验主要步骤如下:先制取一定量的氧气备用,再测得集气瓶实际容积为317毫升,然后采用某种方法得到5瓶含氧量不同的空气,最后用带火星的木条来试验,观察是否复燃.相关的数据见下表:
(1)请指出得到5瓶含氧量不同的空气的具体方法 ;
(2)试将上表空白处补充完整(保留1位小数); 。
(3)由该实验可得到的结论是 _______ __ 。
先在集气瓶里预先加一定体积的水,再用排水集气法收集氧气。45.2%当空气中氧气所占体积比达到41.9%以上时,能使带火星的木条复燃。
第二章1-5节试卷讲评八(8)班测试成绩总体情况分析平均分:82.37典型错题例举典型错题例举考什么?错误点1、物质的制取、收集和性质及检验。
4、18、21(4)、24(1)、25(1)、27后、
30(1)、31(1)
2、化学方程式的书写。21(2)后、25(2)后
3、质量守恒定律。15、16、27前
4、生物的生命活动(呼吸、呼吸作用和光合作用)。
7、8、17、26(3)
5、实验结果的分析。28(1)后、29(2) 、
31(1)考什么?1、物质的制取、收集和性质及检验。(1)装置的选择(2)气体的收集性质决定
收集方法反应物状态和
反应条件决定
装置的选择18、实验室制氨气(NH3)是利用氢氧化钙固体粉末和氯化铵固体加热制取的。已知氨气易溶于水,密度比空气小,则实验制取NH3应选择的装置是( )
A. ①④ B.②③ C.②④ D.①⑤①②④③⑤A25、(1)如图①所示,收集葫芦中气体采用的方法是 。排水法(3)物质的性质性质物理性质:化学性质:颜色、状态、气味、味道、密度溶解性、熔点、沸点、硬度、导电性、导热性、延展性等 可燃性、氧化性、助燃性、还原性、酸碱性等24、(1)根据上述信息,写出金属铬的一种物理性质: 。呈银白色或难溶于水30、(1)根据上述内容推断乙炔(C2H2)具有的化学性质是 。 可燃性21、(4)说明二氧化碳具有的性质是 、密度比空气的大,
因此,二氧化碳可用于 。不能燃烧也不支持燃烧灭火(4)物质的检验氧气的检验:能使带火星的木条复燃。二氧化碳的的检验:能使澄清石灰水变浑浊。27、以下是科学兴趣小组进行的探究活动。利用如下图所示实验装置制取氧气,表明CO2未被KO2完全吸收的实验现象为 。超氧化钾KO2C中澄清石灰水变浑浊。15、下列观点符合质量守恒定律的是( ) A.铁生锈后铁锈质量比铁大 D.水遇冷凝固成冰块,变化前后质量不变质量守恒定律内容:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。· ·· ·2、质量守恒定律C.8 g CH4完全燃烧生成8 g CO2B.一定条件下,SO2和O2生成SO3,反应前后分子总数不变A16、某密闭容器内有四种物质,在一定条件下充分反应。测得反应前后各物质质量如下表,下列有关说法中不正确的是 ( )
A.a的值等于20
B.参加化学反应的X为222g
C.该反应属于化合反应
D.X一定是化合物质量守恒定律内容:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。· ·· ·C原子数目原子质量原子种类物质的总质量元素质量元素种类物质的种类分子的种类27、 “化学氧自救器”,主要用于煤矿井下应急。它利用人呼出的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)在常温下接触产生氧气,该反应的化学方程式为:
4KO2 +2CO2 ====2X +3O2,则X的化学式是 。K2CO3例.1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色的、有强烈的刺鼻气味的氯气。氯气有剧毒,密度比空气大,能溶于水。能与水、金属、碱等发生化学反应。
(1)根据上述信息,写出氯气的一种化学性质: 。
(2)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请补充完善其反应的化学方程式:
△
MnO2 +4HCl(浓)=== 2H2O + + Cl2↑。
(3)小明用上述反应制氯气,设计下图所示装置,请指出其中的问题- 。
能与水、金属、碱等发生化学反应MnCl2用向下排空气法收集氯气3、化学方程式寻因纠错点燃△MnO2原则一是以客观事实为依据反应物、生成物
反应条件
生成物状态二是遵守质量守恒定律正确范例:朱载歌陈慧慧4、生物的生命活动(呼吸运动、呼吸作用、光合作用)7、除了下列哪一项以外,其余现象都表明植物进行了呼吸作用( )
A.大量潮湿种子周围的空气可使澄清的石灰水变浑浊
B.贮存大量蔬菜的地窖比空地窖要暖和许多
C.地窖内的蔬菜腐烂散发出霉味
D.进入贮存大量水果的地方,点燃蜡烛发现火焰不大,燃烧不旺17、气体从外界进入人体血液中的路线可以表示为 ①鼻腔 ②咽 ③喉 ④支气管 ⑤气管 ⑥肺泡外毛细血管 ⑦肺泡( )
A.①→②→③→④→⑤→⑥→⑦ B.①→②→③→⑤→④→⑦→⑥
C.①→②→③→⑤→④→⑥→⑦ D.①→②→③→④→⑤→⑦→⑥CB呼吸系统呼吸道肺:鼻腔咽喉气管、支气管基本结构为肺泡,它仅由一层上皮细胞构成,外缠毛细血管和弹性纤维呼吸作用:8、温室中的绿色植物受阳光的照射生长,昼夜测定温室内氧气的含量如下图所示,其中正确的( )C光合作用:26、选取生长正常的爬山虎进行如下图所示的光合作用实验:
①实验前应将此装置放在黑暗处一昼夜后,移至光下几小时,再将甲、乙、丙三片叶取下,分别放入盛有酒精的小烧杯中,隔水加热,使叶绿素溶解到酒精中。
②将叶片用清水漂洗后放入培养皿中,分别向这三片叶上滴
加碘液,观察三片叶是否变蓝。
(3)将叶片用清水漂洗后放入培养皿中,分别向这三片叶上滴加碘液,其中叶片乙 蓝色。不 变例、某同学用玉米幼苗作实验材料,利用右图实验装置进行
探究活动。装置中隔板与无色透明钟罩之间以及隔板中
央小孔与玉米茎之间都用凡士林密 封,钟罩内放一盛有
某种液体的小烧杯。
⑴若小烧杯中的液体是澄清的石灰水,将装置放在暗处
一段时间后,小烧杯中的石灰水变浑浊,由此可证
明 。
⑵若小烧杯中是氢氧化钠溶液(氢氧化钠溶液能吸收二氧化碳),
则要探究的问题是 ,要验证这一问题,需要设置一组对照实验。二氧化碳是光合作用的原料 玉米幼苗呼吸作用产生了二氧化碳 5、实验结果的分析28、某同学用右图的实验装置测量动物呼吸作用,小试管中的碱石灰能够充分吸收二氧化碳气体,(实验装置足以维持实验期间老鼠的生命活动,瓶口密封)请据图回答问题:
(1)15分钟后,红墨水柱移动情况如何_____,原因是 。甲瓶中的动物呼吸作用消耗了氧气,产生的二氧化碳被碱石灰吸收,导致甲瓶内气压下降 向左移动29、某研究性学习小组在学习了双氧水分解制氧气的实验后,知道催化剂(Mn02)能改变化学反应速率。到底还有哪些因素与化学反应速率有关呢?
【小组讨论】:甲同学观点:化学反应速率与反应物的质量分数有关
乙同学观点:化学反应速率与反应温度有关
【设计实验】:他们设计并进行了以下4次实验(2)由以上实验还能得出:其他条件相同时,反应温度越高或反应物的质量分数越大,则反应速率____ _____。越快31、完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数。
【研究方案】先称取一定质量的氯酸钾和二氧化锰混合物放入大试管中加热至质量不再变化为止。根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量。
【解决问题】实验测得固体混合物质量随加热时间变化的相关数据如图所示。
(1)反应结束后,11.2克固体中含有的物质是___。氯化钾和二氧化锰 例、土豆中含有的过氧化氢酶对过氧化氢分解具有催化作用。楚楚同学设计实验证明新鲜的土豆片也能加快过氧化氢的分解,并与二氧化锰的催化效果进行比较。用如图装置进行实验,图Ⅰ为过氧化氢分解的反应装置,图Ⅱ用于测量产生O2的体积。实验时均以生成25 mL气体为准,其他可能影响实验的因素均忽略不计,相关数据见下表:回答下列问题:
(1)图Ⅱ装置中油层的作用是 。
(2)上述实验中的“待测数据”指 ;欲探究鲜土豆片与二氧化锰的催化效果,应比较b和 (选填“a”、“b”或“c”)的大小。形成油封,气体将Ⅱ中液体压入量气管,从而测得产生氧气的体积 。反应时间 c 分析错题的方法
首要任务
——寻找错误的原因学习建议相信自己,不断进步!审题细心
关键词
题意指向
……知识方法扎实
细节
能力
(实验)
……答题技巧
答题规范
答题完整
书写工整
……谢谢!例、在班会上,小明的同桌表演了“水能生火”魔术:他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小明很感兴趣,于是,他进行探究。 【提出问题】过氧化钠与水反应生成什么物质?为什么脱脂棉会燃烧? 【猜想与假设】①可能生成了Na2CO3和氢气;也有可能生成了Na2CO3和氧气。
②脱脂棉燃烧可能是因为Na2O2与水反应放出热量。 【设计装置】如图所示。
【实验与分析】
(1)小军对小明的猜想进行了理论的分析,他认为不可能有
Na2CO3生成。小军的依据是 。
(2)为了检验产生的气体是否为氧气,小明在实验中应进行
怎样的操作?
(3)如果小明在实验过程中观察到伸入烧杯中的导管口出现
了 的现象,则说明小明的猜想②是正确的。根据质量守恒定律,反应前后元素种类不变 将带火星的木条靠近导管口P处,若木条复燃,说明是氧气 冒气泡 例、研究人员曾经对绿色植物的光合作用与呼吸作用作过以下研究。
实验一:将某绿色植物放在黑暗装置中,分别测定在不同温度下植物对氧气的吸收量,如图1所示.a、b分别表示10℃和20℃时植物吸收氧气量随时间变化的情况。
实验二:按图2所示装置进行黄豆种子呼吸作用和番茄植株光合作用实验。
请分析回答:
(1)分析实验一可知,温度越高植物吸收氧气越 。
(2)由实验一结果可推知:在实验二中,当广口瓶内黄豆种子温度适当 时.就会促进玻璃罩内番茄植株的光合作用。
(3)联系本实验,试分析吐鲁番瓜果特别甜的原因。 快 升高 晚上温度低,呼吸作用弱,有机物分解少。 例.将等容积、等质量(含瓶塞、导管、燃烧匙及瓶内少量的细砂)的两个集气瓶置于天平的左右两盘,并调至平衡。然后同时迅速放入点燃的等质量的白磷和木炭(如右图所示),使两者充分燃烧后冷却至室温,打开止水夹后,此时的天平( )
A.指针偏向右
B.指针偏向左
C.仍处于平衡状态
D.指针先向左后向右偏B例题.带火星的木条在氧气中可以复燃.那么,是不是只有纯净的氧气才能使带火星的木条复燃呢?为此,同学们开展了相关探究实验.实验主要步骤如下:先制取一定量的氧气备用,再测得集气瓶实际容积为317毫升,然后采用某种方法得到5瓶含氧量不同的空气,最后用带火星的木条来试验,观察是否复燃.相关的数据见下表:
(1)请指出得到5瓶含氧量不同的空气的具体方法 ;
(2)试将上表空白处补充完整(保留1位小数); 。
(3)由该实验可得到的结论是 _______ __ 。
先在集气瓶里预先加一定体积的水,再用排水集气法收集氧气。45.2%当空气中氧气所占体积比达到41.9%以上时,能使带火星的木条复燃。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
