1.7元素符号表示的量(第2课时)
图片预览








文档简介
课件21张PPT。1已知:C—12 O—16 H—1 N—14 Ca—40 S—32 Mg—24
求出下列相对分子质量:
CH4_____ Ca(OH)2_____
(NH4)2SO4______3H2O_____ 4CO2_____ 5Mg(OH)2_____167413254176290(1)表示该种物质(二氧化碳气体)
(2)表示该物质的一个分子的构成(CO2分子由碳原子和氧原子构成)
(3)表示这种物质的组成(二氧化碳由碳元素和氧元素组成)
(4)表示该物质的一个分子(一个二氧化碳分子)
(5)表示该物质的相对分子质量化学式的含义:例题1:求水中氢元素和氧元素的质量比解:水的化学式:H2O
H-1 O-16
H:O =(1×2):16 = 1:82 求H2SO4中各元素的质量比?解:H-1 S-32 O-16
H:S:O=(1×2):(32×1):(16×4)=1:16:32答 :H2SO4中各元素的质量比是1:16:32。
(1)计算二氧化碳中各元素的质量比。
(C-12 O-16)
(2)计算硫酸铵[(NH4)2SO4)]中各元素的质量比。(N-14 H-1 S-32 O-16)
(3)计算碳酸氢铵(NH4HCO3)中各元素的质量比。( N-14 H-1 C-12 O-16)
练一练:(C:O=3:8)(N:H:S:O=7:8:16:32)(N:H:C:O=14:5:12:48)
2、元素的质量分数某元素的质量分数=
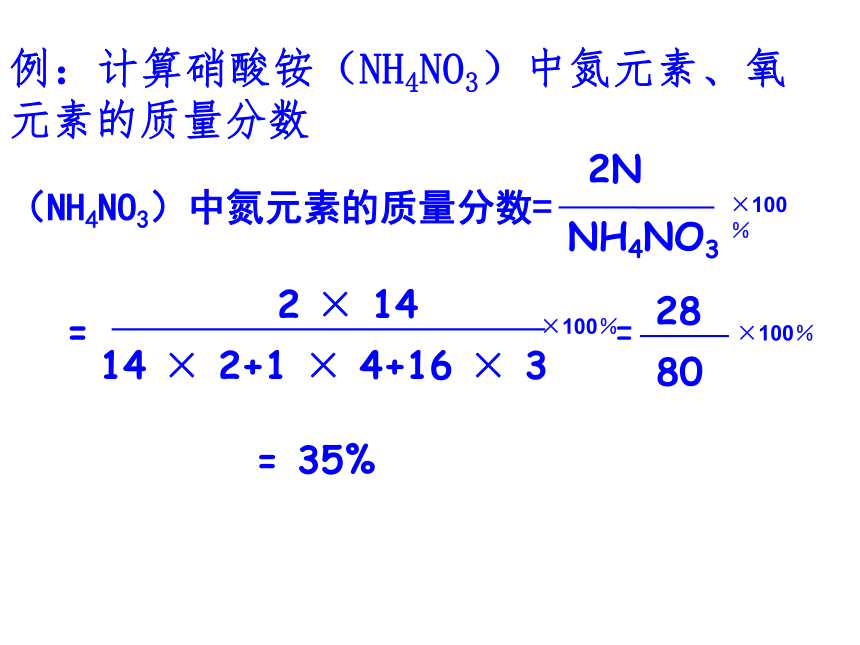
×100%例:计算硝酸铵(NH4NO3)中氮元素、氧元素的质量分数(NH4NO3)中氮元素的质量分数=
2NNH4NO3=2 × 1414 × 2+1 × 4+16 × 3=2880=35%×100%
×100%
×100%
氮肥是含有氮元素的物质,请比较碳酸氢铵(NH4HCO3)、尿素[ CO(NH2)2 ]、硫酸铵[ (NH4)2SO4 ]、硝酸铵(NH4NO3)中氮元素质量分数大小,并与同学交流你的计算方法。讨论:例题:18克水中氢元素的质量是多少?解: 2H
mH =18克× ——×100%
H2O
2
=18克× ——×100%
18
=2克
答:18克水中氢元素的质量是2克.化合物里含某元素的质量=化合物的质量×化合物里某元素的质量分数m元素 =m纯净物 ×该元素的质量分数3 化合物里含某元素的质量 某市场中硫酸铵和尿素两种化肥,每千克的售价分别为1.3元和1.8元,根据它们所含氮的比例分析,买哪种化肥更经济?讨论:解:每千克硫酸铵中含氮元素的质量=1千克2N(NH4 )2SO4×=1千克×28132=0.212千克每千克尿素中含氮元素的质量=1千克×2NCO(NH2)2=1千克×2860 =0.46千克×100%
×100%
×100%
练习
1、现有5吨含杂质10%的氧化铁(Fe2O3),其中含铁多少吨?含氧多少吨?若想提炼7吨铁,则需多少纯的氧化铁?解:5吨物质中含氧化铁(Fe2O3)的质量为5×(1-10%)=4.5吨氧化铁(Fe2O3)中铁元素的
质量分数为4.5吨氧化铁中含铁=4.5×70%=3.15吨
含氧=4.5-3.15=1.35吨若炼7吨铁则需要氧化铁=7÷70%=10吨2.已知硫酸铵的化学式为(NH4)2SO4,
求(1)硫酸铵的相对分子质量。
(2)硫酸铵中各元素的质量比。
(3)66克硫酸铵中含氮元素的质量。
(4)多少克硫酸铵中含氮元素质量为28克。(5)132克硫酸铵的含氮量和多少克硝酸铵(NH4NO3)的含氮量相当?4、小结1)计算相对分子质量2)计算组成化合物的各元素质量比3)计算组成化合物中各元素的质量分数某元素的
质量分数= ×100%4)m元素 =m纯净物 ×该元素的质量分数练习1:已知尿素的化学式为CO(NH2)2 ,求:
(1)它的相对分子质量;
(2)该化合物中各元素的质量比;
(3)氮元素的质量分数;
(4)若有一袋纯度为90%的尿素质量为60千克,,则其中含氮多少克?
(5)120千克纯尿素的含氮量和多少千克碳酸氢铵
(NH4HCO3)的含氮量相当?练习2. “9.11事件发生不久,在美国又出现了炭疽病。这种病是一种有炭疽热杆菌引发的急性传染病,致死率高达25%至60%。其化学式C17H18N3O3 。它由___ 种元素组成,每个分子中含有___ 个原子,其相对分子质量是__ ,其中氧元素的质量分数是____,元素间的质量比是_____.3、已知一种碳原子(碳12)的质量是xkg,另
一种原子的质量是ykg,则此原子的相对
原子质量是( )A.12Y/X B.12X/Y C.Y/12X D.X/12YA4、已知某元素的原子与碳-12原子的质量比为9,则该元素的相对原子质量为( )
A 108 B 1.33
C 108克 D 1.33克 6、 在一种碳和氢组成的化合物A中,碳和氢的原子个数比为1∶2,相对分子质量为28,则A的化学式为( )
A CH2 B C2H4
C C3H6 D C4H8B 7、元素A和氧元素所组成化合物的化学式为AO2,其中A元素的质量分数是50%,则A元素的相对原子质量为( )
A 16克 B 16
C 32克 D 32 D该化合物的相对分子质量为多少? 8、金属元素R为+2价元素,它和氧元素所组成的化合物中,R与氧元素的质量比为3∶2,则R元素的相对原子质量为( )
A、 6 B、 6克
C、 24 D、 24克 C9、 X、Y两元素的相对原子质量分别为M和N,化合价分别为+a和-b,则由此两元素组成的化合物中X元素和Y元素的质量比为( )
A aM∶bN B aN∶Bm
C bM∶aN D M∶NC
求出下列相对分子质量:
CH4_____ Ca(OH)2_____
(NH4)2SO4______3H2O_____ 4CO2_____ 5Mg(OH)2_____167413254176290(1)表示该种物质(二氧化碳气体)
(2)表示该物质的一个分子的构成(CO2分子由碳原子和氧原子构成)
(3)表示这种物质的组成(二氧化碳由碳元素和氧元素组成)
(4)表示该物质的一个分子(一个二氧化碳分子)
(5)表示该物质的相对分子质量化学式的含义:例题1:求水中氢元素和氧元素的质量比解:水的化学式:H2O
H-1 O-16
H:O =(1×2):16 = 1:82 求H2SO4中各元素的质量比?解:H-1 S-32 O-16
H:S:O=(1×2):(32×1):(16×4)=1:16:32答 :H2SO4中各元素的质量比是1:16:32。
(1)计算二氧化碳中各元素的质量比。
(C-12 O-16)
(2)计算硫酸铵[(NH4)2SO4)]中各元素的质量比。(N-14 H-1 S-32 O-16)
(3)计算碳酸氢铵(NH4HCO3)中各元素的质量比。( N-14 H-1 C-12 O-16)
练一练:(C:O=3:8)(N:H:S:O=7:8:16:32)(N:H:C:O=14:5:12:48)
2、元素的质量分数某元素的质量分数=
×100%例:计算硝酸铵(NH4NO3)中氮元素、氧元素的质量分数(NH4NO3)中氮元素的质量分数=
2NNH4NO3=2 × 1414 × 2+1 × 4+16 × 3=2880=35%×100%
×100%
×100%
氮肥是含有氮元素的物质,请比较碳酸氢铵(NH4HCO3)、尿素[ CO(NH2)2 ]、硫酸铵[ (NH4)2SO4 ]、硝酸铵(NH4NO3)中氮元素质量分数大小,并与同学交流你的计算方法。讨论:例题:18克水中氢元素的质量是多少?解: 2H
mH =18克× ——×100%
H2O
2
=18克× ——×100%
18
=2克
答:18克水中氢元素的质量是2克.化合物里含某元素的质量=化合物的质量×化合物里某元素的质量分数m元素 =m纯净物 ×该元素的质量分数3 化合物里含某元素的质量 某市场中硫酸铵和尿素两种化肥,每千克的售价分别为1.3元和1.8元,根据它们所含氮的比例分析,买哪种化肥更经济?讨论:解:每千克硫酸铵中含氮元素的质量=1千克2N(NH4 )2SO4×=1千克×28132=0.212千克每千克尿素中含氮元素的质量=1千克×2NCO(NH2)2=1千克×2860 =0.46千克×100%
×100%
×100%
练习
1、现有5吨含杂质10%的氧化铁(Fe2O3),其中含铁多少吨?含氧多少吨?若想提炼7吨铁,则需多少纯的氧化铁?解:5吨物质中含氧化铁(Fe2O3)的质量为5×(1-10%)=4.5吨氧化铁(Fe2O3)中铁元素的
质量分数为4.5吨氧化铁中含铁=4.5×70%=3.15吨
含氧=4.5-3.15=1.35吨若炼7吨铁则需要氧化铁=7÷70%=10吨2.已知硫酸铵的化学式为(NH4)2SO4,
求(1)硫酸铵的相对分子质量。
(2)硫酸铵中各元素的质量比。
(3)66克硫酸铵中含氮元素的质量。
(4)多少克硫酸铵中含氮元素质量为28克。(5)132克硫酸铵的含氮量和多少克硝酸铵(NH4NO3)的含氮量相当?4、小结1)计算相对分子质量2)计算组成化合物的各元素质量比3)计算组成化合物中各元素的质量分数某元素的
质量分数= ×100%4)m元素 =m纯净物 ×该元素的质量分数练习1:已知尿素的化学式为CO(NH2)2 ,求:
(1)它的相对分子质量;
(2)该化合物中各元素的质量比;
(3)氮元素的质量分数;
(4)若有一袋纯度为90%的尿素质量为60千克,,则其中含氮多少克?
(5)120千克纯尿素的含氮量和多少千克碳酸氢铵
(NH4HCO3)的含氮量相当?练习2. “9.11事件发生不久,在美国又出现了炭疽病。这种病是一种有炭疽热杆菌引发的急性传染病,致死率高达25%至60%。其化学式C17H18N3O3 。它由___ 种元素组成,每个分子中含有___ 个原子,其相对分子质量是__ ,其中氧元素的质量分数是____,元素间的质量比是_____.3、已知一种碳原子(碳12)的质量是xkg,另
一种原子的质量是ykg,则此原子的相对
原子质量是( )A.12Y/X B.12X/Y C.Y/12X D.X/12YA4、已知某元素的原子与碳-12原子的质量比为9,则该元素的相对原子质量为( )
A 108 B 1.33
C 108克 D 1.33克 6、 在一种碳和氢组成的化合物A中,碳和氢的原子个数比为1∶2,相对分子质量为28,则A的化学式为( )
A CH2 B C2H4
C C3H6 D C4H8B 7、元素A和氧元素所组成化合物的化学式为AO2,其中A元素的质量分数是50%,则A元素的相对原子质量为( )
A 16克 B 16
C 32克 D 32 D该化合物的相对分子质量为多少? 8、金属元素R为+2价元素,它和氧元素所组成的化合物中,R与氧元素的质量比为3∶2,则R元素的相对原子质量为( )
A、 6 B、 6克
C、 24 D、 24克 C9、 X、Y两元素的相对原子质量分别为M和N,化合价分别为+a和-b,则由此两元素组成的化合物中X元素和Y元素的质量比为( )
A aM∶bN B aN∶Bm
C bM∶aN D M∶NC
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
