沪教版化学九年级下册第7章应用广泛的酸·碱·盐第3节几种重要的盐 课件(共31张PPT)
文档属性
| 名称 | 沪教版化学九年级下册第7章应用广泛的酸·碱·盐第3节几种重要的盐 课件(共31张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-07-18 00:00:00 | ||
图片预览











文档简介
(共31张PPT)
第3节 几种重要的盐
1、学生掌握盐的化学性质、熟练运用复分解反应条件书写化学方程式;
2、通过对性质的学习,联系生活实际,解决问题;
3、学生创新思维能力得到提升,增强学习兴趣;
学习目标
一次,葛洪徒弟用铁勺盛曾青(硫酸铜溶液),几天后,葛洪拿那铁勺使用,奇妙的现象出现了:铁勺变成“铜勺”了,红光闪闪的。葛洪的徒弟高兴得跳起来。
“点铁成金啦!”
Fe + CuSO4 == FeSO4 + Cu
盐的化学性质一:金属+盐→新盐+新金属(置换反应)
位于前面
位于后面
盐溶液
无
可溶性
不要用K、Ca、Na置换盐溶液中的金属
铁参加的置换反应生成的都是亚铁盐
在金属活动性顺序表中,只有_________ 的金属才能把________的金属从它的___ 中置换出来,与氢的位置 __关;盐必须
是______盐。
Fe + CuSO4 = FeSO4 + Cu
[ 复习之旅第一站:历史中的化学 ]
小雨在家炒菜时他发现炒的菜不咸反而有一种涩味.你猜他错用了哪种物质
你能帮助他利用
生活中的物质鉴别
食盐和纯碱这两
种物质吗
取食盐和纯碱两种固体少量,分别向其中加入食醋(醋酸),能产生气泡的为纯碱( Na2CO3 ),无现象的为食盐(主要成分为NaCl)。
[ 复习之旅第二站:生活中的化学 ]
盐的化学性质二:盐+酸---新盐+新酸
CaCO3 (难溶) +HNO3 —
(2) AgCl (难溶) +HNO3 —
(3) BaSO4 (难溶) +HNO3—
(4) BaCl2 +H2SO4 —
(5) NaNO3 +H2SO4 —
例1、判断下列反应能否在水中发生:
(1)CaCO3+2HNO3=Ca(NO3)2+H2O+CO2↑
(2)不反应
(3)不反应
(4) BaCl2+H2SO4=BaSO4↓+2HCl
(5)不反应
Na2CO3+2HCl=2NaCl+H2O+CO2↑
农业中,如何配置农药波尔多液?
Ca(OH)2+ CuSO4=Cu(OH)2 ↓ + CaSO4
[ 复习之旅第三站:农业中的化学 ]
盐的化学性质三:盐+碱---新盐+新碱
(1)KNO3 +NaOH –
(2)BaCO3 +NaOH –
(3)FeCl3 +Ca(OH)2 –
(4)Na2CO3 +Ca(OH)2 –
例2、判断下列反应能否在水中发生:
(3)2FeCl3+3Ca(OH)2=2Fe(OH)3 ↓+3CaCl 2
(1)不反应
(4) Na2CO3+Ca(OH)2=2NaOH +CaCO3 ↓
(2)不反应
·
[ 复习之旅第四站:工业生产中的化学 ]
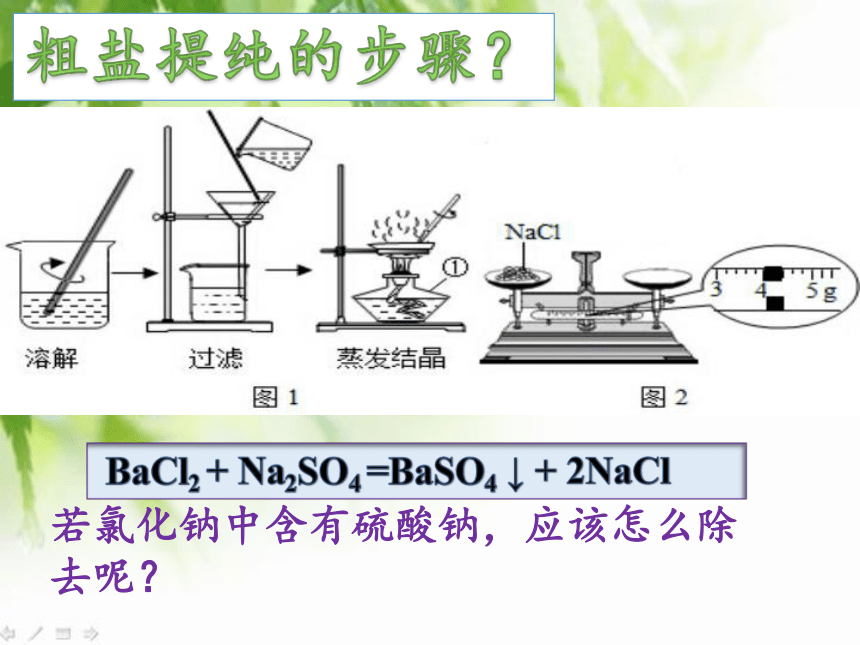
粗盐提纯的步骤?
这样能得到得到纯净的氯化钠吗?若氯化钠中含有硫酸钠,应该怎么除去呢?
BaCl2 + Na2SO4 =BaSO4 ↓ + 2NaCl
盐的化学性质四:盐+盐---新盐+新盐
(1)AgNO3 + NaCl —
(2)BaSO4(难溶) +Na2CO3—
(3)BaCl2 + Na2CO3—
(4)KNO3 + NaCl —
例3、判断下列反应能否在水中发生:
(1)AgNO3+NaCl = AgCl↓+NaNO3
(4)不反应
(3)BaCl2+Na2CO3=BaCO3↓+2NaCl
(2)不反应
盐的主要化学性质:
(可溶)
(可溶)
(可溶)
(可溶)
(可溶)
(至少有一种沉淀)
(至少有一种沉淀)
1.盐 + 金属 - 新盐 + 新金属
2.盐 + 酸 - 新盐 + 新酸
3.盐 + 碱 - 新盐 + 新碱
4.盐 + 盐 - 新盐 + 新盐
归纳小结
(有沉淀或气体或沉淀生成)
(活动性:金属>新金属)
金属+
盐
+
盐
+碱
+
酸
复分解反应
表达式:
AB + CD ==
条件:
反应物之间要能互溶,生成物中有沉淀或有气体或有水。
特点:
交换成分,价不变
盐的化学性质:
AD +CB
1.初中化学常见的8个沉淀:AgCl、BaSO4、BaCO3
CaCO3、Cu(OH)2、Fe(OH)3、Mg(OH)2、Al(OH)3
总 结:
2.生成水的几种类型:
H+ + OH- = H2O 2H+ + CO32- = CO2↑ + H2O
H+ + HCO3- = CO2↑ + H2O
NH4+ + OH- = NH3 + H2O
3. 生成气体的几种类型:
2H+ + CO32- = CO2↑ + H2O
H+ + HCO3- = CO2↑ + H2O
NH4+ + OH- = NH3 + H2O
《山中探险》
“探险队员”—硫酸铜,不小心走进了有许多“吃人的野兽”(即能与硫酸铜发生化学反应的物质)的小山,请你帮助它走出小山(请用图中物质前的序号连接起来表示所走的路线):
入口→ → → → →出口。
CuSO4溶液
CuSO4溶液
《山中探险》
CuSO4溶液
《山中探险》
利用盐的化学性质,
让我们一起直击中考题型
学以致用
2.一次性区别氯化钠、氯化钡、碳酸钾三种物质的溶液,
应选用( )
A.硝酸银溶液 B.稀硫酸 C.稀盐酸 D.石灰水
B
盐化学性质应用一:物质鉴别
1.将珍珠放入稀盐酸中,有气泡产生,生成的气体能使澄
清的石灰水变浑浊,则珍珠中含有下列离子中的( )
A、氯离子 B、硫酸根离子
C、碳酸根离子 D、氢氧根离子
C
1. 用Mg、MgO、Mg(OH)2、H2SO4溶液、CuSO4溶液五种
物质两两进行反应,能得到MgSO4的方法有 ( )
A.3种 B.4种 C.5种 D.无法确定
B
盐
酸+碱
金属+酸
金属+盐
酸+盐
盐+碱
盐+盐
金属氧化物+酸
非金属氧化物+碱
√
√
√
√
盐化学性质应用二:物质制备
1、下列物质的转变,不能通过一步反应实现的是( )
A.K2SO4→KOH B.CO2→CaCO3
C.Cu(NO3)2→CuCl2 D.FeCl3→Fe(OH)3
C
2、下列各组物质能同时存在于同一溶液中的是 ( )
A.AgNO3、NaCl、KNO3
B.CuSO4、KNO3、Na2CO3
C.NaOH、KCl、Fe(NO3)3
D.KCl、NaOH、Na2CO3
D
盐化学性质应用三:物质转化与共存
3、下列各组离子能共存的是( )
A、 Ba2+、K+、NO3-、CO32-、H+
B、K+、Cl-、Mg2+、NO3-、H+
C、Fe3+、SO42-、OH-、Na+、Cu2+
D、Ag+、Ba2+、Cl-、NO3-、K+
B
1、从Ba(OH)2、Na2SO4、稀盐酸、BaCl2四种溶液中,选择适当的物质填入下图方框中。
Na2SO4
BaCl2
Ba(OH)2
HCl
盐化学性质应用四:物质推断
1、除去下列物质中的杂质(括号中为杂质),应选什么试剂?
①NaCl[Na2CO3]
②KNO3[KCl]
③CaCl2[NH4Cl]
④NaCl[MgSO4]
HCl
AgNO3
Ca(OH)2
Ba(OH)2
KCl+AgNO3=AgCl↓+KNO3
2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O
MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓
2HCl+Na2CO3=2NaCl+CO2↑+H2O
盐化学性质应用五:除杂质
1、鱼胆弄破后会使鱼肉粘上难溶解于水的胆汁(一种酸)而变苦,要减少这种苦味,用来洗涤的最佳物质是( )。
A、水 B、食盐
C、纯碱 D、食醋
C
生活与化学
2、某医院来了一急救病人。
病因:昨天晚上该病人感觉胃部不适、反酸,于是他
服用了一种主要成分为NaHCO3胃药。
病症:胃出血
既往病史:患有胃溃疡。
如果你是该病人的主治医师,请你分析出该病人胃出血的原因:
写出化学方程式:________________________
NaHCO3与胃酸反应生成CO2,在溃疡处造成胃穿孔而出血
NaHCO3+HCl=NaCl+H2O+CO2↑
[环保与化学]
蓝色多“恼”河
丹阳市蓝色多“恼”河
新闻链接:
2012年10月19日上午,江苏丹阳城区许多市民发现,一向土黄色的京杭大运河丹阳城区段一夜之间变成了“蓝色大运河”。环境监察大队及环境监测站人员分组赶赴现场展开调查。当日下午,环保部门已查明,大运河河水发蓝是某化工公司非正常排污所致。
1. 你猜测变蓝的河水中可能有什么离子?
2. 你认为含有该离子的水对人体有危害吗?
3. 你打算如何处理该河段污染?
这节课你学到了什么?
谁来总结一下!!!!
本
课
小
结
初级目标:理解盐的化学性质,并能准确书写化学方程式;
中级目标:能解析有关盐的化学性质的相关中考题型;
高级目标:通过练习能提升自己逻辑思维能力,学会举一反三;
超级目标:学会知识总结归纳,能将酸碱盐性质形成知识网络,能将化学知识联系生活实际问题;
谢 谢
第3节 几种重要的盐
1、学生掌握盐的化学性质、熟练运用复分解反应条件书写化学方程式;
2、通过对性质的学习,联系生活实际,解决问题;
3、学生创新思维能力得到提升,增强学习兴趣;
学习目标
一次,葛洪徒弟用铁勺盛曾青(硫酸铜溶液),几天后,葛洪拿那铁勺使用,奇妙的现象出现了:铁勺变成“铜勺”了,红光闪闪的。葛洪的徒弟高兴得跳起来。
“点铁成金啦!”
Fe + CuSO4 == FeSO4 + Cu
盐的化学性质一:金属+盐→新盐+新金属(置换反应)
位于前面
位于后面
盐溶液
无
可溶性
不要用K、Ca、Na置换盐溶液中的金属
铁参加的置换反应生成的都是亚铁盐
在金属活动性顺序表中,只有_________ 的金属才能把________的金属从它的___ 中置换出来,与氢的位置 __关;盐必须
是______盐。
Fe + CuSO4 = FeSO4 + Cu
[ 复习之旅第一站:历史中的化学 ]
小雨在家炒菜时他发现炒的菜不咸反而有一种涩味.你猜他错用了哪种物质
你能帮助他利用
生活中的物质鉴别
食盐和纯碱这两
种物质吗
取食盐和纯碱两种固体少量,分别向其中加入食醋(醋酸),能产生气泡的为纯碱( Na2CO3 ),无现象的为食盐(主要成分为NaCl)。
[ 复习之旅第二站:生活中的化学 ]
盐的化学性质二:盐+酸---新盐+新酸
CaCO3 (难溶) +HNO3 —
(2) AgCl (难溶) +HNO3 —
(3) BaSO4 (难溶) +HNO3—
(4) BaCl2 +H2SO4 —
(5) NaNO3 +H2SO4 —
例1、判断下列反应能否在水中发生:
(1)CaCO3+2HNO3=Ca(NO3)2+H2O+CO2↑
(2)不反应
(3)不反应
(4) BaCl2+H2SO4=BaSO4↓+2HCl
(5)不反应
Na2CO3+2HCl=2NaCl+H2O+CO2↑
农业中,如何配置农药波尔多液?
Ca(OH)2+ CuSO4=Cu(OH)2 ↓ + CaSO4
[ 复习之旅第三站:农业中的化学 ]
盐的化学性质三:盐+碱---新盐+新碱
(1)KNO3 +NaOH –
(2)BaCO3 +NaOH –
(3)FeCl3 +Ca(OH)2 –
(4)Na2CO3 +Ca(OH)2 –
例2、判断下列反应能否在水中发生:
(3)2FeCl3+3Ca(OH)2=2Fe(OH)3 ↓+3CaCl 2
(1)不反应
(4) Na2CO3+Ca(OH)2=2NaOH +CaCO3 ↓
(2)不反应
·
[ 复习之旅第四站:工业生产中的化学 ]
粗盐提纯的步骤?
这样能得到得到纯净的氯化钠吗?若氯化钠中含有硫酸钠,应该怎么除去呢?
BaCl2 + Na2SO4 =BaSO4 ↓ + 2NaCl
盐的化学性质四:盐+盐---新盐+新盐
(1)AgNO3 + NaCl —
(2)BaSO4(难溶) +Na2CO3—
(3)BaCl2 + Na2CO3—
(4)KNO3 + NaCl —
例3、判断下列反应能否在水中发生:
(1)AgNO3+NaCl = AgCl↓+NaNO3
(4)不反应
(3)BaCl2+Na2CO3=BaCO3↓+2NaCl
(2)不反应
盐的主要化学性质:
(可溶)
(可溶)
(可溶)
(可溶)
(可溶)
(至少有一种沉淀)
(至少有一种沉淀)
1.盐 + 金属 - 新盐 + 新金属
2.盐 + 酸 - 新盐 + 新酸
3.盐 + 碱 - 新盐 + 新碱
4.盐 + 盐 - 新盐 + 新盐
归纳小结
(有沉淀或气体或沉淀生成)
(活动性:金属>新金属)
金属+
盐
+
盐
+碱
+
酸
复分解反应
表达式:
AB + CD ==
条件:
反应物之间要能互溶,生成物中有沉淀或有气体或有水。
特点:
交换成分,价不变
盐的化学性质:
AD +CB
1.初中化学常见的8个沉淀:AgCl、BaSO4、BaCO3
CaCO3、Cu(OH)2、Fe(OH)3、Mg(OH)2、Al(OH)3
总 结:
2.生成水的几种类型:
H+ + OH- = H2O 2H+ + CO32- = CO2↑ + H2O
H+ + HCO3- = CO2↑ + H2O
NH4+ + OH- = NH3 + H2O
3. 生成气体的几种类型:
2H+ + CO32- = CO2↑ + H2O
H+ + HCO3- = CO2↑ + H2O
NH4+ + OH- = NH3 + H2O
《山中探险》
“探险队员”—硫酸铜,不小心走进了有许多“吃人的野兽”(即能与硫酸铜发生化学反应的物质)的小山,请你帮助它走出小山(请用图中物质前的序号连接起来表示所走的路线):
入口→ → → → →出口。
CuSO4溶液
CuSO4溶液
《山中探险》
CuSO4溶液
《山中探险》
利用盐的化学性质,
让我们一起直击中考题型
学以致用
2.一次性区别氯化钠、氯化钡、碳酸钾三种物质的溶液,
应选用( )
A.硝酸银溶液 B.稀硫酸 C.稀盐酸 D.石灰水
B
盐化学性质应用一:物质鉴别
1.将珍珠放入稀盐酸中,有气泡产生,生成的气体能使澄
清的石灰水变浑浊,则珍珠中含有下列离子中的( )
A、氯离子 B、硫酸根离子
C、碳酸根离子 D、氢氧根离子
C
1. 用Mg、MgO、Mg(OH)2、H2SO4溶液、CuSO4溶液五种
物质两两进行反应,能得到MgSO4的方法有 ( )
A.3种 B.4种 C.5种 D.无法确定
B
盐
酸+碱
金属+酸
金属+盐
酸+盐
盐+碱
盐+盐
金属氧化物+酸
非金属氧化物+碱
√
√
√
√
盐化学性质应用二:物质制备
1、下列物质的转变,不能通过一步反应实现的是( )
A.K2SO4→KOH B.CO2→CaCO3
C.Cu(NO3)2→CuCl2 D.FeCl3→Fe(OH)3
C
2、下列各组物质能同时存在于同一溶液中的是 ( )
A.AgNO3、NaCl、KNO3
B.CuSO4、KNO3、Na2CO3
C.NaOH、KCl、Fe(NO3)3
D.KCl、NaOH、Na2CO3
D
盐化学性质应用三:物质转化与共存
3、下列各组离子能共存的是( )
A、 Ba2+、K+、NO3-、CO32-、H+
B、K+、Cl-、Mg2+、NO3-、H+
C、Fe3+、SO42-、OH-、Na+、Cu2+
D、Ag+、Ba2+、Cl-、NO3-、K+
B
1、从Ba(OH)2、Na2SO4、稀盐酸、BaCl2四种溶液中,选择适当的物质填入下图方框中。
Na2SO4
BaCl2
Ba(OH)2
HCl
盐化学性质应用四:物质推断
1、除去下列物质中的杂质(括号中为杂质),应选什么试剂?
①NaCl[Na2CO3]
②KNO3[KCl]
③CaCl2[NH4Cl]
④NaCl[MgSO4]
HCl
AgNO3
Ca(OH)2
Ba(OH)2
KCl+AgNO3=AgCl↓+KNO3
2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O
MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓
2HCl+Na2CO3=2NaCl+CO2↑+H2O
盐化学性质应用五:除杂质
1、鱼胆弄破后会使鱼肉粘上难溶解于水的胆汁(一种酸)而变苦,要减少这种苦味,用来洗涤的最佳物质是( )。
A、水 B、食盐
C、纯碱 D、食醋
C
生活与化学
2、某医院来了一急救病人。
病因:昨天晚上该病人感觉胃部不适、反酸,于是他
服用了一种主要成分为NaHCO3胃药。
病症:胃出血
既往病史:患有胃溃疡。
如果你是该病人的主治医师,请你分析出该病人胃出血的原因:
写出化学方程式:________________________
NaHCO3与胃酸反应生成CO2,在溃疡处造成胃穿孔而出血
NaHCO3+HCl=NaCl+H2O+CO2↑
[环保与化学]
蓝色多“恼”河
丹阳市蓝色多“恼”河
新闻链接:
2012年10月19日上午,江苏丹阳城区许多市民发现,一向土黄色的京杭大运河丹阳城区段一夜之间变成了“蓝色大运河”。环境监察大队及环境监测站人员分组赶赴现场展开调查。当日下午,环保部门已查明,大运河河水发蓝是某化工公司非正常排污所致。
1. 你猜测变蓝的河水中可能有什么离子?
2. 你认为含有该离子的水对人体有危害吗?
3. 你打算如何处理该河段污染?
这节课你学到了什么?
谁来总结一下!!!!
本
课
小
结
初级目标:理解盐的化学性质,并能准确书写化学方程式;
中级目标:能解析有关盐的化学性质的相关中考题型;
高级目标:通过练习能提升自己逻辑思维能力,学会举一反三;
超级目标:学会知识总结归纳,能将酸碱盐性质形成知识网络,能将化学知识联系生活实际问题;
谢 谢
